微流控技術在病原微生物檢測中的應用*
郝良玉,曲 晗,李志萍,王習文,王宇田,孫 瑞,崔煜菲 綜述,夏志平,△,李乾學▲ 審校
(1.吉林農業大學動物科學技術學院,吉林長春 130118;2.軍事獸醫研究所,吉林長春 130062)
隨著當今社會經濟的飛速發展,傳統的病原微生物檢測方法已經不能滿足現代的需求。傳統的菌落培養和血清學檢測方法不僅費時、費力,而且只能局限在實驗室中操作,而基于抗原抗體的酶聯免疫吸附試驗(ELISA法),因其容易出現假陽性檢測結果,盡管方法簡便但并不適用于精準分析。目前實驗室常見的聚合酶鏈式反應(PCR法),因其具有檢測范圍廣、明暗度較高、特異性強等特點受到歡迎,但實驗所需設備沉重,并不適用于現場快速檢測。因此,需要探尋一種新型技術,以達到適應現場、精準檢測、快速研判的目的。
1 芯片實驗室研究進展
微流控技術是一種交叉學科技術,在微尺度管道(5~500 μm)內操控微小體系流體(10-9~10-18L)的新型科學研究平臺,經過數余年的發展,現已成為生化分析中的一個獨立領域。在微流控平臺上,可以針對液體或氣體、流體進行微升、納升甚至皮升級的生物化學反應,能極大降低試劑的消耗量(至少2~3 個數量級)[1]。微流控芯片,簡單來講就是指待檢測樣品在一個小的實驗室裝置中連續完成樣品核酸的提取、純化、PCR、跑膠等過程而不需要人為的外在干預。微流控芯片作為當今生物醫學領域研究的前沿和熱點可以集中地將實驗室功能轉移到芯片上,把原有大型檢驗儀器微型化制成可完成生化等分析的便攜式儀器。
微流控芯片技術是在芯片毛細管電泳基礎上發展起來的,通過微加工手段在金屬、硅、玻璃、高分子聚合物等材質的基片上,加工出微米級別的流體通道、檢測室等微結構單元,從20世紀90年代起,微流控技術被多數人定義為一種分析化學平臺進而逐步快速發展。我國微流控研究起步較晚,但經過十多年的發展,微流控技術也已走向成熟。2000年以后,隨著微流控芯片的深入研究,這種技術逐漸得到學術界和產業界更高層次和更大范圍的認可。同時,這項技術作為微量流體亞毫米級別尺寸上的一種精確操控技術,將生物學與化學上所需的基本操作單位結合在小型芯片上。這種芯片多由儲液池和微通道構成,微通道包括有入口、主通道、輔助通道(側流通道)和出口。根據不同需要設計的入口和出口可以滿足不同流體的導入與導出。流體性質的樣品從入口進入,在主通道發生分離、混合和反應[2]。作為實現微流控功能的主要部分,主通道需要根據具體功能設計結構和尺寸。結構最簡單的通道是平面型通道,見圖1[3],圖1A為雙T形微流控芯片結構簡圖,圖1B為常見的微通道布局包括了直線形、多邊形、蛇形、螺旋形、線圈形、折疊形,需要混合不同流體時則常常采用二維或三維結構。相比而言三維結構需要通過提供更強的動力來完成混合,制作工藝也更為復雜。微通道可由石英、硅、玻璃等材料制作,不同材料的利弊及適用場所也有所不同。玻璃是一種成本低、透光性強、絕緣性和強度好的材料[4],可以及時觀察微通道內流體狀態,適合通常的樣品分析。晶體硅制作的微流控器件有著散熱性強,與其他電子元件交互性好的優勢,但硅的絕緣性和透光性較差、硅片間黏合率低等缺點影響了硅的應用。目前,高分子聚合材料因其成本低、易于加工和批量生產,制作過程簡單而多用于較復雜通道的制備,其中以聚甲基丙烯酸甲酯(PMMA)和環狀烯烴共聚高分子(COC)最受歡迎。
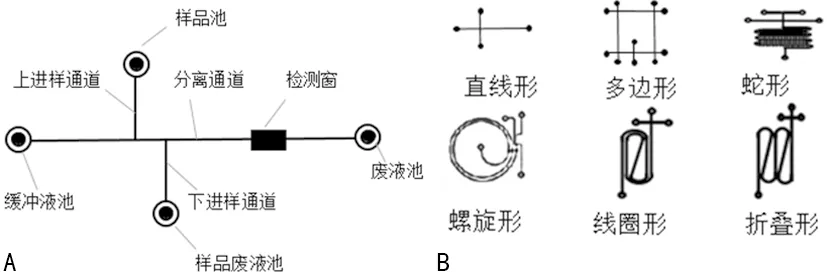
注:A為雙T形微流控芯片結構簡圖;B為常見的微通道
圖1雙T型微流控芯片結構簡圖及常見微通道布局
現階段越來越多的研究者嘗試通過3D打印技術加工微流控芯片,這項技術的發展使微流控芯片制作過程更為簡便,成本低廉。目前已有研究利用微流控芯片實現DNA的快速分離[5]。利用微流控芯片上搭載各化學反應,可以發展藥物方面的合成篩選。我國體外診斷主要集中在生化分析和免疫診斷上[6],而國外歐美國家微流控片在體外診斷方面已經取得明顯突破,通過實現全自動PCR分子診斷,微流控展現出巨大潛能[7-8]。器官芯片也是當今的熱門研究方向,利用微流控芯片的集成功能制備器官芯片,這一技術在2016年的達沃斯論壇上入選年度十大新興技術之一。國內已有團隊研發出一種使多種細胞及組織在體外共存的類器官多功能微流控芯片[9]。何佳芮等[10]設計出可以聯合檢測大腸埃希菌菌體抗原及藥敏分析的微流控芯片,這種方式證實了微流控芯片制備向產業化發展的可行性。WANG等[11]利用聚二甲基硅氧烷(PDMS)作為結構材料制備微流體結構,通過磁性納米顆粒對樣品溶液進行磁性捕獲,以熒光分子標記的抗性IgG作為信號觀測,提高分析分辨率并降低了可能出現因表面吸附而產生的堵塞現象,整個樣品的檢測和分析都集合在一個微流體平臺上使檢測過程高效、準確。JAMIE等[12]通過在一個蛋白質芯片上集成反應單元,可以實現酶促反應、產物電泳分離、組分標記和信號檢測等連續進行。
2 微流控技術在病原檢測中的應用
傳統病原微生物檢測主要包括涂片檢查、分離培養、血清學鑒定和分子生物學鑒定,相對于微流控芯片技術,這些傳統檢測方法冗時費力,而新型微流控技術現已在核酸分離和定量分析、DNA測序及各類病原體的檢測等方面廣泛應用,在蛋白、氨基酸、PCR產物等領域也有了成熟的檢測技術,其基于免疫分析原理,主要以抗原、抗體和熒光靶標為新型標記物。在傳統檢測方法上發展出來的芯片大致分為兩類,電化學芯片和基因芯片[13]。電阻抗技術結合微通道制作而成的電化學微流控芯片,是通過在芯片上自動集成化操作,可以高效準確地收集數據,由于電化學傳感器在結構設計和性能與微流控芯片相匹配,這種電化學微流控芯片更適用于即時檢測。基因芯片的構建,融入了微流控平臺和PCR技術,這項技術手段可以很好地解決在實際環境中面臨的問題,比如,分流協同檢測提高了樣品檢測效率并保證了檢測過程不受干擾。通過基因芯片分離擴增基因片段,可以建立全自動微生物分型,實現基因芯片產業化,提高檢測效率。利用熒光標記單鏈DNA來制作微流控芯片,芯片經物理吸附待檢測樣品與單鏈DNA相結合,避免了表面處理和探針固定等繁瑣步驟,這種方式可以多通路同時檢測多種病原體,但需要通過毛細管道進入反應區域,所以該種芯片以濾紙作為制作材料檢測效果更為良好。
2.1細菌病原體檢測 病原微生物具有傳播性、感染性和毒力,針對各種病原微生物的特點,應用在病原微生物上的微流控技術可以結合不同方法產生更好檢測效果。針對某種病原體在多通道微流控芯片上采用定位捕獲富集,通過熒光檢測后定量分析,這種新的試驗方法在實際檢測中有著極大的潛在優勢。對紙基芯片進行等離子體處理后,紙表面上產生了功能性基團醛基,以實現抗體的固定化。這種運用夾心法化學發光免疫分析的固定化蛋白方式,建立了在紙上進行熒光免疫測量球蛋白的新方法,相比于傳統方法操作更為簡便。而通過PCR檢測復雜樣品中的細菌病原體不受限于通道尺寸和形狀,對其進行有效的DNA提取時效果顯著、結果明確,同時PCR芯片可以實現DNA的單分子擴增及核酸的定量實驗[13]。通過大量探針與不同標記物的樣品雜交后檢出的信號強度,可以分析出樣本序列可實現病原體的檢測。鑒定細菌通常采用兩種方式,一種是傳統方法培養細菌后進行藥敏實驗,將待測細菌放入不同生化發酵管中,觀察各發酵管的反應確定細菌種類;另一種是病原體核酸檢測技術,多采用基于PCR的分子診斷。而新型基于微通道毛細阻力的藥敏檢測技術,通過改變流體毛細阻力通道的長度來控制液體的流速,以驅使不同種類的菌體分流向不同通道,不僅能夠對細菌進行分選、培養和分離,同時可以對其進行高敏度的檢測。由于芯片的簡便性及多樣性,微通道可根據病原種類的不同特點進行針對性設計,XIA等[14]設計出含20個微通道芯片對多種病原菌同時檢測,部分細菌檢測的準確性高達100%。如圖2A中1~8分別為加熱開關、磁球開關、通道、插頭、磁球、4個獨立反應池、mini-Luer連接器、溫度開關,圖2B為排列成條紋粒子的微磁球芯片,圖2C為混合磁粉的芯片,JULICH等[15]利用磁珠的磁性對捕獲的目標DNA高效洗滌后,可檢測出水體表面的蘇云金桿菌和土拉熱桿菌。通過運用液滴及介電泳技術實現高通量顆粒檢測與分選,陶冶[16]在單個液滴中實現一步法反轉錄的PCR擴增,由此構建高通量液滴的熒光信號檢測平臺,實現通過液滴微流控技術來準確分析低拷貝數下的重組病毒。這種技術對病原體基因的特征片段進行針對性設計和選擇,檢測其PCR產物,可以得到后續實驗所需的多種信息,芯片中每孔可供多個不同的PCR同時進行,具有廣泛的實用性。集毛細管電泳、熒光標記和PCR技術于一體的微流體技術,在基因測序及表達、病原體檢測等領域正在高速發展,在單細胞分析方面也有著廣泛的應用。

注:A為微流控芯片;①為加熱開關;②為磁球開關;③為通道;④為插頭;⑤為磁球;⑥為4個獨立反應池;⑦為mini-Luer連接器;⑧為溫度開關;B圖為微磁球芯片;C為混合磁球芯片
圖2純化DNA的微流控芯片系統
2.2核酸檢測 核酸作為生物體基本的遺傳物質,對核酸進行精準檢測也就是對這種病原體的分析。微流控技術對病原體核酸進行檢測時,微通道內施加電場產生能量變化,所需的試樣量少,可使分子擴散程度低,分離效果極好,因此微流控CE分析在核酸診斷分離中的分辨能力要遠遠好于平板凝膠電泳。將核酸提取、PCR擴增、分子雜交、電泳分離及檢測有機地結合在一張微芯片上,這張微芯片其快速、高質量的分離效能在寡核苷酸、DNA、RNA片段分析及基因表型和測序應用中可以得到充分反映。TSUKAKOSHI等[17]對特異性結合的DNA適配體進行篩選,對得到序列的二級結構進行分析后,將序列長度進行了優化,通過設計芯片結構對兩端引物序列進行封閉,有效避免了該段序列對目標結合時產生的影響。PETRALIA等[18]研制了基于硅微柱微流體裝置的生物過濾器,見圖3,微芯片從一側進樣經過中間層硅柱由另一側輸出,芯片由不同規格的高分子聚碳酸酯、PDMS、硅層、玻璃層構成,用于提取乙型肝炎病毒的全基因組DNA。微流控芯片與PCR技術相結合,制作成基于磁珠提取核酸方法的微流控芯片,是將親水性陰離子交換劑預先固定在磁珠表面,利用二氧化硅顆粒來吸附帶負電荷的核酸,達到從樣品中最大程度提取和純化核酸,在引物約束下特異性地PCR擴增。富集與蛋白質特異性相結合的核酸,是進一步檢測的前提及關鍵。現階段微流控芯片結合分子診斷技術,待檢樣品體積只需幾微升,加熱器直接集成在芯片上,可以較傳統PCR方法效率提高2~10倍。

圖3 硅微柱生物濾池提取核酸示意
2.3蛋白質及其他檢測 蛋白質是生命的物質基礎,對蛋白質結構和功能進行準確分析可以檢測出機體的生理或病理變化。傳統蛋白檢測需要提取蛋白質,對凝膠電泳分離后的蛋白區帶進行切割、酶降解,然后用質譜等方法檢測分析。這種傳統方法無法滿足現代科學的精準、高效等需求。而隨著RNA標記物的研究深入,檢測核糖核蛋白中的mRNA等物質,通過流體蛋白質的大小在時間和空間上分離病原體蛋白,是一種低成本快速檢測蛋白的方法[19-20]。將電滲流分離和紫外分光光譜檢測等技術集合在一塊小芯片上,將待檢樣品加入后,芯片自動按照設定好的檢測程序完成檢測,這種檢測手段快速,且成本低。基于微流控芯片的蛋白質免疫分析方法的微反應空間大于表面積,分子擴散的距離減小[21-22],使整體反應效率大大提高。GIUFFRIDA等[23]在不同入口處加入各反應物,在T形連接點形成液滴后在混合反應區完成檢測,見圖4,通過金納米粒子增強出的生物發光信號與適配體相互作用結合,可將樣品體積低至1 μL并將檢測時間控制在10 min內,其極低的檢測限也可供臨床根據所需選擇。

圖4 微流控原理圖
3 微流控技術在病原檢測領域的優勢
相對于傳統的免疫診斷方式和病原的鑒定培養而言,微流控技術在病原檢測尤其是現場檢測方面有著獨特的優勢[24-25]。(1)自動化、污染小、更安全,樣品檢測的多個步驟集成在一張芯片上。根據實驗設計采取不同微通道,使繁瑣的實驗流程變得簡易。封閉式自動化的結構可以保證檢測期間樣品不受污染,同時也減少對實驗室等外在環境造成的影響,保證了后續實驗操作不受中間產物的影響。(2)高通量性。因為微通道可以根據所需設計成三維-多通道,這種立體多元結構可以將待檢測樣品完美分流,各通道不受其他通道影響。同一時間同一樣品可做不同項目檢測,與傳統生化檢測方法相比,極大地提高了檢測效率的同時,也保證了檢測結果的準確性,符合高通量操作快速、靈敏、準確等特點。(3)檢測成本低。由于系列操作集中在一塊小芯片上,各個結構單元微小,所需的檢測試劑和待檢樣品消耗量自然隨之減少。盡管檢測試劑濃度可能增大,但實際使用量要遠小于常規檢測方法,節約了實驗成本也避免造成浪費。因為自動化集中操作,所需被檢測的樣本量只需要微升甚至納升級別。隨著微流控技術的進步,產業化商業化的發展,一塊微芯片的成本控制在可接受范圍將逐步實現。
正因為微流控具有以上幾個重要的優勢和優點,使其成為了即時檢驗(POCT)的首選,并在臨床檢測中逐漸推行開來。
4 存在的問題和發展趨勢
微流控技術可極大地縮短樣品處理時間,通過精密控制液體流動,最大化地利用試劑耗材,把整個化驗室的功能集成在微芯片上,為病原微生物檢測等領域提供了無限的前景。盡管微流控可以大幅度降低試樣和試劑的消耗,但因其昂貴的制作成本和復雜的制作工藝使這項技術并不能很好地應用在臨床實際檢測中,同時制作微芯片的方法和基底材質受限過大,對于操作人員的技術要求較高。現階段隨著各項學科研究的深入,生物芯片將得到更為廣泛的應用,新興的數字微流控技術(DMF)在行業內引起廣泛關注,這種可實現離散液滴精準自動化操縱的新型液滴操縱技術對于檢測樣品具有十分重要的意義。同時,微機電系統(MEMS)是指尺寸在幾毫米甚至更小的高科技裝置,因其融合了精密機械加工、薄膜和硅加工等多項技術,期待微機電系統在微流控芯片小型化中帶來的新研究思路。

