馬鈴薯種質資源塊莖晚疫病抗性鑒定
敖 翔,閔凡祥,白雅梅,呂文河*
(1.東北農業大學農學院,黑龍江 哈爾濱 150030;2.黑龍江省農業科學院植物脫毒苗木研究所,黑龍江 哈爾濱 150086;3.東北農業大學資源與環境學院,黑龍江 哈爾濱 150030)
由致病疫霉菌(Phytophthora infestans)引起的晚疫病是馬鈴薯生產中一種極具毀滅性的病害。其最初起源于墨西哥,首次發現在德國[1]。1845年,愛爾蘭發生了惡名昭彰的“愛爾蘭大饑荒”,數年間病害造成了愛爾蘭數百萬人的死亡和遷移,此次饑荒的罪魁禍首就是致病疫霉[2]。隨后,晚疫病迅速傳遍整個歐洲,并在世界其他馬鈴薯主產區開始發病和流行,對全球馬鈴薯的產量造成了嚴重的損失[3]。2012年,中國大面積爆發馬鈴薯晚疫病,北方地區全面流行,南方地區偏重流行,全國發病面積達265.2萬hm2,造成產量損失近300萬t[4]。
晚疫病可發生于馬鈴薯整株,不僅可以侵染植株地上部分,還可使塊莖發病。馬鈴薯抗晚疫病的鑒定方法有田間抗性鑒定和實驗室抗性鑒定。在實驗室抗性鑒定中,目前多數學者利用離體葉片法來篩選抗病品種或材料[5-7]。但有時馬鈴薯地上植株與地下塊莖對晚疫病的抗病性表現并不一致[8-11]。馬鈴薯晚疫病抗病性可分為植株抗性和塊莖抗性。植株抗性表現為地上植株有較強抗病性,但地下塊莖卻表現為感病,易腐爛;塊莖抗性表現為地上植株容易發病,而地下塊莖則抗病,不易受病菌侵染。長久以來,育種家們將育種目標主要放在對馬鈴薯地上葉片抗性的篩選鑒定上,而對地下塊莖抗性的研究卻較少。感病塊莖無論在田間還是貯藏期,一旦被侵染極易腐爛,就會造成嚴重損失,若作為種薯播種,還會成為晚疫病初侵染源進一步擴散[12]。本研究的目的是通過室內塊莖抗性鑒定方法,對利用國外種質資源創造的農藝性狀表現優良且產量較高的馬鈴薯高世代無性系進行塊莖晚疫病抗性評價,進而篩選塊莖抗晚疫病的材料,以期為馬鈴薯抗晚疫病育種提供新材料。
1 材料與方法
1.1 試驗材料
1.1.1 供試菌株
塊莖晚疫病抗性鑒定所用菌株為KS12-20(1.2.3.4.5.6.7.8.9.10.11)、 SH13-7(1.3.4.7.10.11)、MZ14-20(1.2.3.4.5.6.7.8.9.10.11)、 MZ15-30(1.3.4.7.9.10)和NH12-9(1.4.6.7)共5個。菌株選擇依據實驗室前期試驗結果,前4個為2012~2015年黑龍江省當年的優勢小種菌株,第5個為毒力基因數目相對較少的菌株,其中KS12-20和MZ14-20為“超級毒力小種”。
1.1.2 供試馬鈴薯種質資源
用于塊莖晚疫病抗性鑒定的馬鈴薯材料共15份,包括1個感病對照品種(‘荷蘭15號’),1個抗病對照品種(‘克新18號’),13個馬鈴薯高世代無性系(H17-44049、 H17-44056、 H17-44057、 H17-44107、H17-44114、 H17-44121、 H17-54374、 H17-54316、H17-54071、H17-54113、H17-54229、H17-54280和K17-193)。在這13個馬鈴薯高世代無性系中,除 H17-54229(‘中薯 3 號’בNorland’)外,其他無性系中至少一個親本是荷蘭品種或利用荷蘭種質資源選育的品種或無性系。無性系H17-54229父本‘Norland’是一個美國品種。高世代無性系選擇的標準是農藝性狀表現優良,產量特別是商品薯(≥75 g)產量高。
1.2 試驗方法
1.2.1 接種前準備
用于接種的馬鈴薯塊莖為收獲后存貯在8~9℃下2個月的無病無傷塊莖。將塊莖清洗干凈,用1%次氯酸鈉溶液浸泡30 min進行表面消毒,再用滅菌水清洗3遍,將殘留次氯酸鈉溶液消除。每個塊莖橫向切下2片厚11 mm的塊莖片,用滅過菌的濾紙吸干表面水分,將薄片放在有濾紙的培養皿中,置于20℃光周期培養箱(16 h光照,8 h黑暗)中愈傷24 h[13]。
1.2.2 接種培養
孢子懸浮液制備:將待測菌株預培養10 d,在培養皿中加入適量滅菌水,用涂布棒將孢子囊充分洗出,過濾吸出液體即為孢子囊懸浮液,4℃環境下2~3 h待其釋放游動孢子即為游動孢子懸浮液,利用血球計數板將其濃度調至5×104個/mL備用。
將用于接種的晚疫病菌株制成孢子懸浮液,取1滴滴在塊莖片的中心,置于保濕保鮮盒中,18℃光周期培養箱高濕黑暗培養7 d后開始調查。每個品種8次重復(4塊莖×2片/塊莖)。設置陰性對照,將同等體積滅菌水滴在薯片中心,放置在相同環境中。
1.2.3 抗性評分
將單片塊莖翻過來進行評分。將薯片下表面切掉薄薄一層,以除去被空氣氧化的褐色,進而調查統計組織發病情況。使用DPS 7.31軟件對數據進行方差分析,最后用度量感染面積的方法來確定抗病等級,抗病等級參照唐洪明[14]和王騰[15]的標準(表1)。
2 結果與分析
2.1 不同晚疫病菌株對馬鈴薯塊莖抗性鑒定
利用5個菌株對13個馬鈴薯無性系及2個馬鈴薯品種(對照)進行抗性鑒定,所有陰性對照均未發病,說明培養環境沒有晚疫病菌和其他對試驗結果產生影響的菌。7 d后對接種塊莖進行侵染面積調查,結果顯示不同菌株對不同馬鈴薯種質資源侵染狀況均不同,且差異明顯(表2)。綜合來說,H17-54374侵染面積最小(4.97%),H17-54071侵染面積最大(75.15%)。圖1為SH13-7菌株對部分馬鈴薯塊莖侵染癥狀。
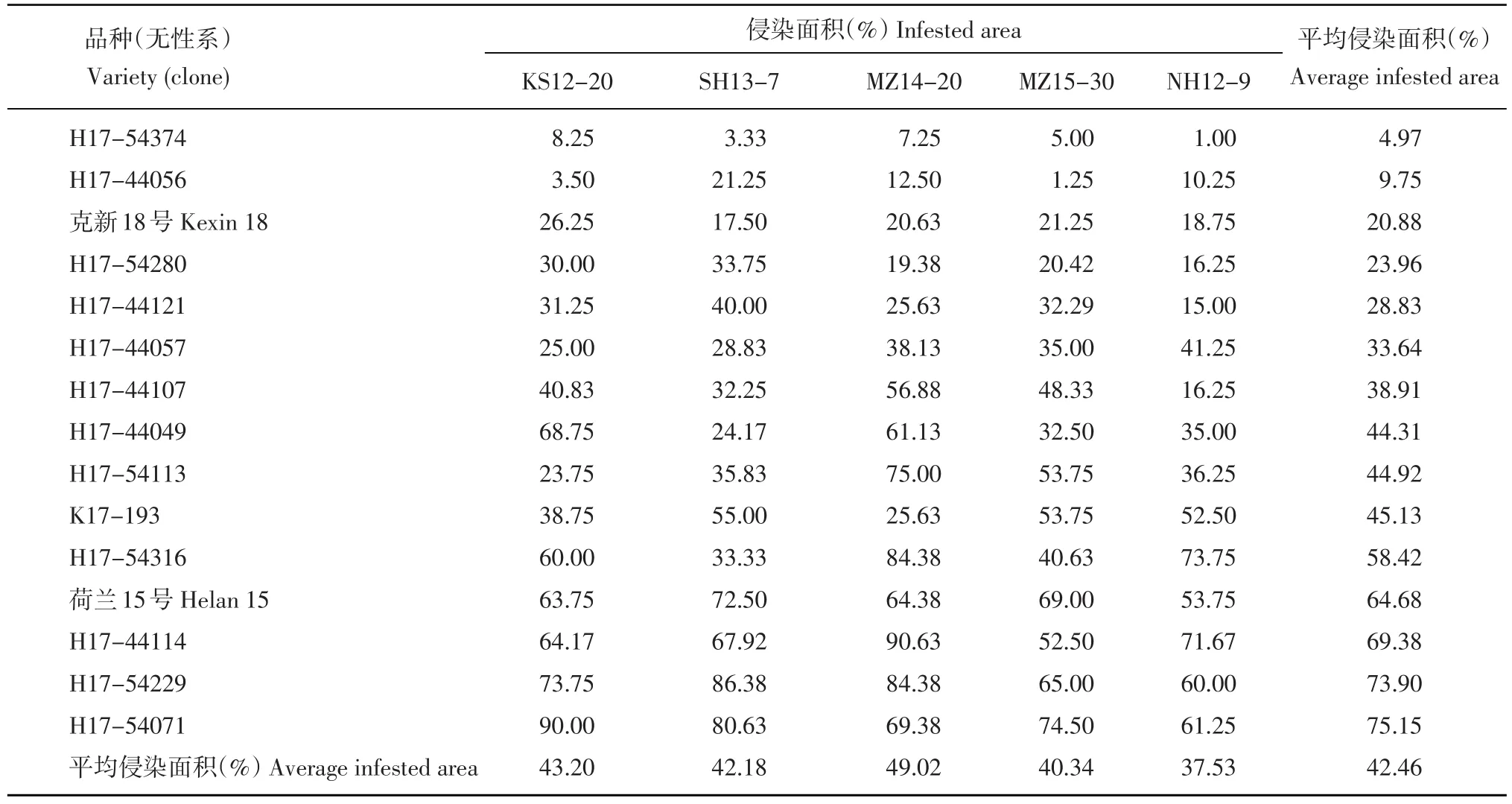
表2 不同晚疫病菌株對馬鈴薯塊莖抗性鑒定結果Table 2 Identification of late blight resistance of potato tubers inoculated with different Phytophthora infestans isolates

圖1 部分馬鈴薯薯片接種菌株SH13-7的癥狀Figure 1 Symptoms of some potato chips inoculated with isolate SH13-7
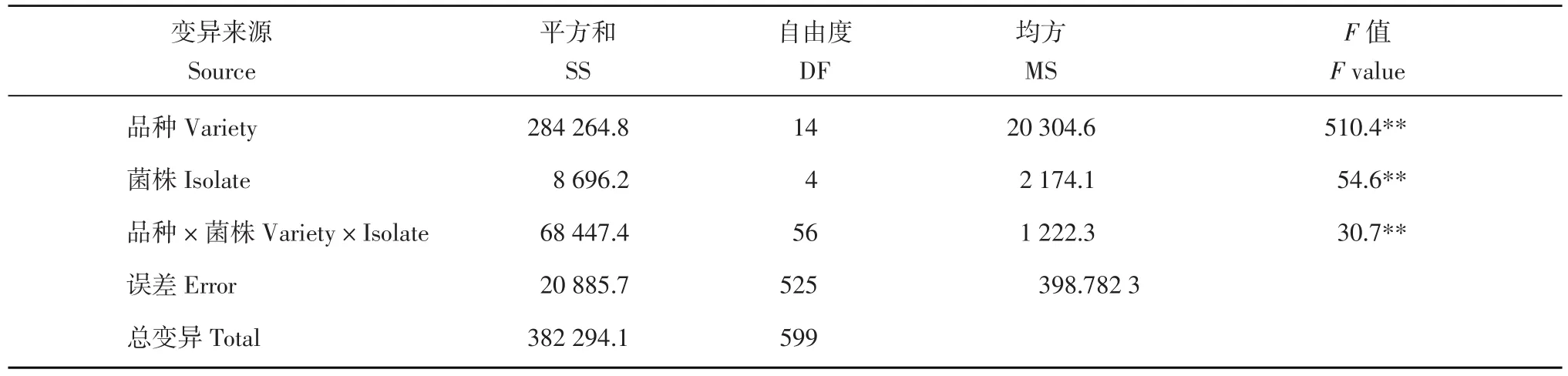
表3 品種和菌株對晚疫病菌塊莖侵染面積影響方差分析Table 3 Analysis of variance for effects of potato variety and isolate on infected area of potato chips inoculated with Phytophthora infestans
抗性鑒定結果方差分析顯示,品種間、菌株間、品種與菌株間的互作效應均極顯著(表3),說明塊莖侵染面積情況受薯塊品種、侵染菌株以及薯塊品種與侵染菌株互作效應影響。
用菌株KS12-20對塊莖進行抗性鑒定,塊莖侵染面積為3.50%~90.00%,其中H17-54374、H17-44056、H17-54113和H17-44057受侵染面積低于抗病對照‘克新18號’,但只有H17-54374和H17-44056與抗病對照差異顯著;H17-54071、H17-54229、H17-44049和H17-44114受侵染面積高于感病對照‘荷蘭15號’,但只有H17-54071和H17-54229與‘荷蘭15號’差異顯著(圖2a)。用菌株SH13-7對塊莖進行抗性鑒定,塊莖侵染面積為3.33%~86.38%,只有H17-54374受侵染面積低于抗病對照,并差異顯著;H17-54229和H17-54071受侵染面積高于感病對照,且差異顯著(圖2b)。用菌株MZ14-20對塊莖進行抗性鑒定,塊莖侵染面積為7.25%~90.63%,其中H17-54374、H17-44056和H17-54280受侵染面積低于抗病對照,但只有H17-54374和H17-44056與抗病對照差異顯著;H17-44114、H17-54316、H17-54229、H17-54113和H17-54071受侵染面積高于感病對照,其中除H17-54071外均與‘荷蘭15號’差異顯著(圖2c)。用菌株MZ15-30對塊莖進行抗性鑒定,塊莖侵染面積為1.25%~74.50%,H17-44056、H17-54374和H17-54280受侵染面積低于抗病對照,但只有H17-44056和H17-54374與抗病對照差異顯著;H17-54071受侵染面積高于感病對照,但差異不顯著(圖2d)。用菌株NH12-9對塊莖進行抗性鑒定,塊莖侵染面積為1.00%~73.75%,其中 H17-54374、H17-44056、H17-44121、H17-44107和H17-44280受侵染面積低于抗病對照,但只有H17-54374和H17-44056與抗病對照差異顯著;H17-54316、H17-44114、H17-54071和H17-54229受侵染面積高于感病對照,且均與‘荷蘭15號’差異顯著(圖2e)。雖然品種和菌株互作效應極顯著,但仔細考察圖2中的數據可發現,不同品種對被測株系反應總的趨勢還是一致的,特別是無性系H17-54374和H17-44056對接種5個株系的反應均較抗病。


圖2 不同菌株對馬鈴薯塊莖的侵染面積Figure 2 Infested area of potato tubers inoculated with different isolates
5個菌株中,MZ14-20和KS12-20致病力最強,但KS12-20和SH13-7差異不顯著。NH12-9致病力最弱(圖3a)。13個無性系間,H17-54374和H17-44056受侵染面積低于抗病對照,且與其差異顯著;H17-54071、H17-54229和H17-44114受侵染面積高于感病對照,且與其差異顯著(圖3b)。
2.2 馬鈴薯種質資源的抗性類型劃分

圖3 不同菌株和不同品種(無性系)的平均侵染面積Figure 3 Average infested area of different isolates and different varieties(clones)

表4 馬鈴薯種質資源的抗性類型劃分Table 4 Classification of resistance type of potato germplasm resources
對13份馬鈴薯高世代無性系進行薯片抗性鑒定,未發現0級材料,發現1級材料1份、2級材料1份、3級材料1份、4級材料6份、5級材料4份(表4)。其中抗病對照品種‘克新18號’抗病等級為3級,感病對照品種‘荷蘭15號’抗病等級為5級。對照抗性類型進行劃分,發現高抗材料1份(H17-54374), 中抗 材 料 2份(H17-44056和H17-54280),抗性材料占所有無性系的23.08%;感 病 材 料 6 份(H17-44121、 H17-44057、H17-44107、H17-44049、H17-54113和K17-193),占所有無性系的46.15%;高感材料4份(H17-54316、H17-44114、H17-54229和H17-54071),占所有無性系的30.77%。
3討 論
培育抗晚疫病品種是防治晚疫病最經濟有效的方法,而篩選馬鈴薯種質資源是培育抗晚疫病品種的關鍵步驟。目前多數抗晚疫病種質資源篩選的研究均采取田間自然抗性或者室內離體葉片的方法進行鑒定,對塊莖抗性鑒定的報道較少。由于受不同基因控制,有時馬鈴薯地上植株與地下塊莖對晚疫病的抗病性經常表現不一致[16],如果馬鈴薯葉片對晚疫病表現抗性不一定就說明塊莖也表現抗性。地下塊莖是馬鈴薯的主要經濟產量,在植株葉片抗病的前提下,利用塊莖抗性鑒定方法來篩選種質資源更為直接、可靠。Dorrance和Inglis[13]利用田間整薯抗性鑒定、室內整薯塊莖鑒定和室內塊莖薄片鑒定3種方法對不同馬鈴薯品種進行了抗性鑒定。有些學者利用室內塊莖薄片鑒定方法鑒定塊莖的抗病性,部分原因是該方法可以忽視掉薯皮對致病疫霉的抗性活動,這樣可以更清晰的明確薯塊抗性[17,18]。
本研究采用的5個菌株中有4個為4年的優勢小種,且2年的優勢小種為超級毒力小種,另,也包括了含有致病基因最少的小種。MZ14-20和KS12-20均是超級毒力小種,兩者的致病力均較強,但MZ14-20致病力顯著高于KS12-20的致病力,說明不同的遺傳背景可能會影響病原菌的致病力,具體原因需進一步研究,所以菌株的選擇多樣性會對抗性鑒定結果產生一定影響。
荷蘭是馬鈴薯育種大國,亦是種薯出口大國。荷蘭馬鈴薯塊莖均勻、芽眼淺,多為橢圓形、卵圓形。例如‘Favorita’,具有高產、優質等特點,但抗病性,如晚疫病抗性較差。本研究試驗材料除一個無性系外,其余材料雙親中至少有1個是荷蘭馬鈴薯品種或用荷蘭馬鈴薯種質資源選出的無性系,但并沒有對其塊莖進行晚疫病抗性鑒定。本研究對2個馬鈴薯品種(‘克新18號’和‘荷蘭15號’)和13個馬鈴薯高世代無性系進行塊莖抗性鑒定,其中2個馬鈴薯品種的鑒定結果與王騰[15]的報道結果一致,從13個馬鈴薯高世代無性系篩選出了3個作為抗晚疫病種質資源進行進一步的育種工作,同時為挖掘新的抗晚疫病基因研究提供原材料。

