核酸檢測聯合酶聯免疫吸附試驗在獻血者血液感染性指標篩查中的應用
孫春玲
(周口市中心血站檢驗科,河南 周口466000)
為保障臨床輸血安全,多年來我國采供血機構采用兩種不同廠家酶聯免疫吸附試驗(ELISA)試劑對獻血者血液標本進行乙型肝炎表面抗原(HBs Ag)、丙型肝炎抗體(抗-HCV)、人類免疫缺陷病毒抗體(抗-HIV)等血清學項目檢測,但由于窗口期感染、病毒核酸變異以及隱匿性感染等因素,使得部分獻血者血液雖經血清學檢測合格后仍然存在感染乙型肝炎、丙型肝炎和艾滋病的風險[1]。依據《血站技術操作規程(2015)》(國家衛生計生委關于印發血站技術操作規程(2015版)的通知.國衛醫發〔2015〕95號)要求,自2016年3月1日始我國采供血機構對獻血者血液標本全面實施ELISA和核酸檢測(NAT)兩種方法聯合檢測,以降低經輸血傳播乙型肝炎、丙型肝炎和艾滋病的風險。本文回顧分析64 420例獻血者的實驗室篩查資料,為提高血液質量及確保輸血安全提供依據。
1 材料與方法
1.1 研究對象
選擇周口市中心血站2016年3月至2017年4月采集的無償獻血者血液標本64 420例為研究對象,其中男30 790例,女33 630例,年齡18~60歲,中位年齡32歲;初次獻血39 940例,重復獻血24 480例。所有獻血者均符合獻血者健康檢查要求[2],均簽署自愿獻血協議書。
1.2 檢測試劑與儀器
檢測試劑:初檢HBs Ag、抗-HCV、梅毒螺旋體抗體(抗-TP)、抗-HIV ELISA試劑由珠海麗珠生物技術有限公司提供,復檢 HBs Ag、抗-HCV、抗-TP、抗-HIV ELISA試劑由廈門新創生物技術有限公司提供;初檢、復檢丙氨酸氨基轉移酶(ALT)檢測試劑盒分別由貝克曼庫爾特實驗系統(蘇州)有限公司和上海科華生物工程股份有限公司提供;HBV/HCV/HIV三聯合核酸提取試劑和檢測試劑由上海浩源生物科技有限公司提供。ELISA法和NAT質控品均由北京萬泰生物科技有限公司提供。試劑和質控品均批批檢合格并在有效期內使用。主要血清學檢測儀器:初檢儀器主要是瑞士RSP 150加樣系統和德國BEPⅢ第三代全自動酶免系統,復檢儀器主要是MF-FA ME24/30全自動酶免系統,ALT檢測設備為貝克曼AU480型全自動生化分析儀。NAT檢測儀器:Chi TaS BSS1200系統、HAMILTON-EZbead系統和ABI7500全自動PCR擴增分析儀。所有檢測設備均經過廠家校驗,且均可良好運行。
1.3 ELISA和NAT檢測方法
1.3.1 標本留取
采集獻血者靜脈血于兩支試管(每管5 mL血樣),1支為EDTAK2抗凝管,用于 HBs Ag、抗-HCV、抗-TP、抗-HIV和ALT血清學檢測;另1支為含分離膠、無菌、無RNA酶和無DNA酶的真空采血管,用于HBV-DNA、HCV-RNA和HIV-RNA檢測。標本留取后在2~8℃環境保存,核酸試管采集血樣后4 h內完成離心、分離出血漿并在72 h內完成HBV-DNA、HCV-RNA和HIV-RNA檢測。
1.3.2 ELISA 檢測
64 420例無償獻血者標本均使用兩種不同廠家的試劑檢測,每批實驗設空白對照孔、陰性對照孔、陽性對照孔、室內質控孔,完成HBs Ag初、復檢檢測,初檢和復檢由不同人員操作。結果判定標準:S/CO(樣本吸光度值/臨界值)≥1.0判為陽性,0.7<S/CO<1.0判為灰區,S/CO≤0.7判為陰性。抗-HIV檢測為陽性標本送至周口市疾病預防控制中心HIV確認實驗室進行確認。
1.3.3 NAT 檢測
將ELISA檢測為陰性的無償獻血者標本,每8個標本混為一個混樣池,且均設定內標對照。混樣測定無反應判為陰性,混樣測定有反應時予以拆分檢測,拆分后無反應者判為陰性,拆分后有反應者判為陽性。
1.4 統計學方法
采用SPSS20.0統計軟件包分析數據,比較采用χ2檢驗,檢驗水準a=0.05,以P<0.05表示差異有統計學意義。
2 結果
2.1 血清學指標檢測結果
在64 420例獻血者中ALT、HBs Ag、抗-HCV、抗-HIV和抗-TP血清學檢測共1362項不合格,其中ALT不合格220項,在以上1362項不合格中,21例存在兩項指標重疊感染,因而共計1341例獻血者血清學檢測不合格,63 079例獻血者血清學檢測結果合格。64 420 例獻血者 HBs Ag、抗-HCV、抗-HIV和抗-TP檢測結果見表1。
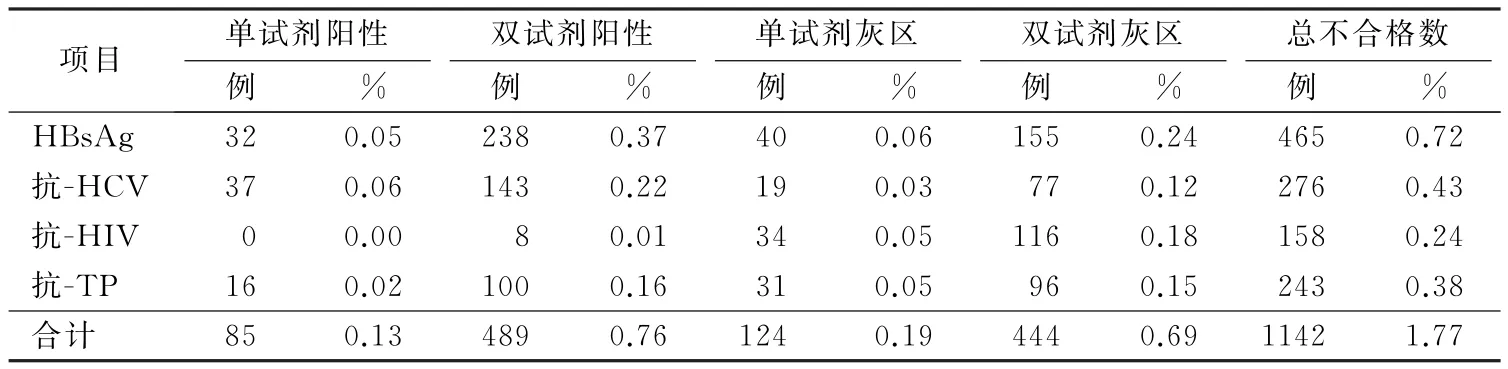
表1 64 420例獻血者HBs Ag、抗-HCV、抗-HIV和抗-TP檢測結果
2.2 血清學檢測結果合格獻血者NAT檢測情況
在血清學檢測均合格的63 079例獻血者中,檢出HBV-DNA陽性57例(0.09%),HIV-RNA陽性1例,未檢出HCV-RNA陽性獻血者。
2.3 HBs Ag(-)/HBV-DNA(+)獻血員分布情況
在血清學檢測均合格的63 079例獻血者中,HBV-DNA陽性檢出率男性和女性比較差異無統計學意義(P>0.05);初次獻血與重復獻血者比較及不同年齡段獻血者比較差異均有統計學意義(P<0.05,P<0.01)。見表2。
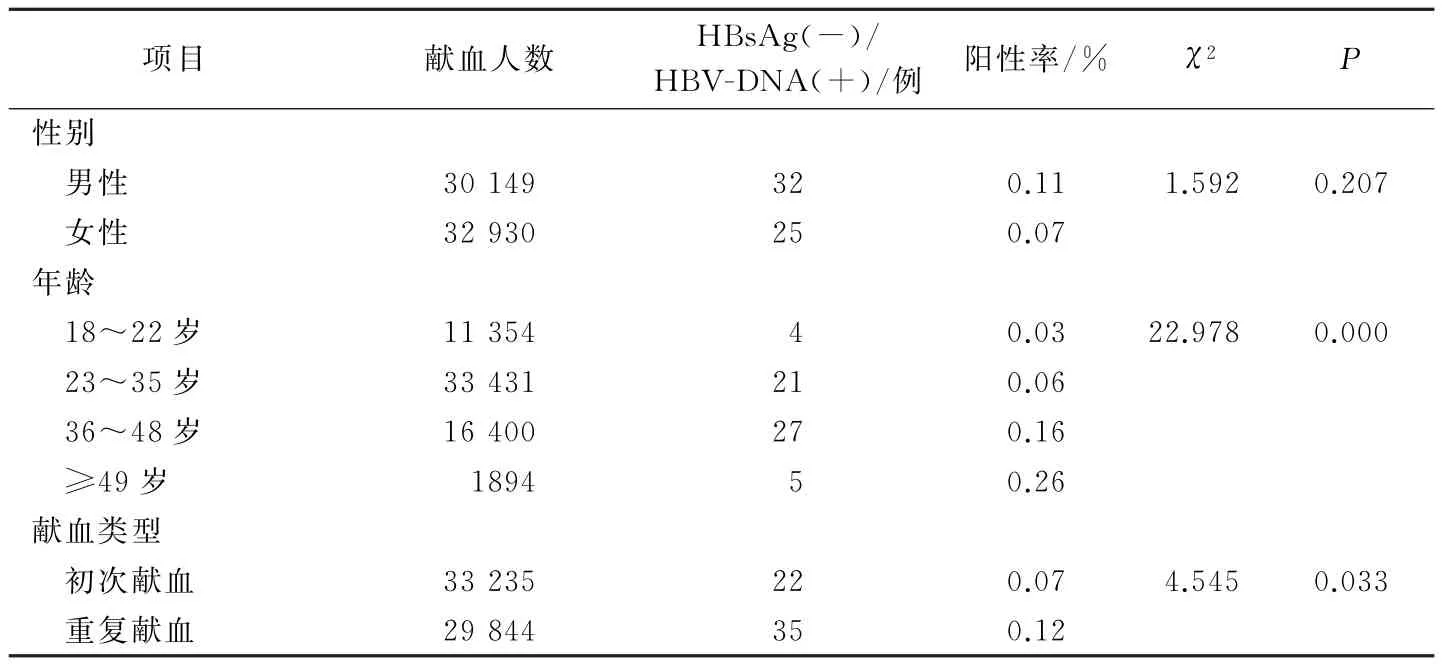
表2 63 079例獻血者中HBV-DNA檢測陽性/HBs Ag陰性獻血員分布情況
3 討論
目前輸血及血液制品是臨床疾病治療不可替代的重要措施,多年來,采供血機構一直采用血清學技術檢測輸血相關病毒標志物的抗原或抗體,極大地降低了經輸血傳播乙型肝炎、丙型肝炎等感染性疾病,但由于試劑靈敏度、窗口期感染、病毒基因變異、免疫靜默、隱匿性感染等諸多因素存在[3],有極少部分獻血者血液雖經ELISA法檢測合格,輸注患者后仍然可引起乙型肝炎、丙型肝炎、艾滋病等感染性疾病的傳播。雖然ELISA檢測試劑盒的靈敏度、特異性在不斷提高,但仍相繼有不同文獻報道經輸血傳播肝炎、HIV的案例[4-6],給患者的健康造成極大危害。
ELISA法檢測是以抗原、抗體作為檢測對象,曾勁峰等[7]研究顯示,約70%的HCV和90%的HIV、HBV ELISA法漏檢是由窗口期感染引起,此時ELISA法常檢測不出來而造成漏檢,而NAT檢測可將HCV、HBV和HIV的窗口期分別縮短82%(59 d)、20%(9 d)和50%(11 d)。NAT 是一種具有較高特異性和敏感性的免疫學檢測方法,其通過核酸擴增技術捕獲獻血者血液標本中較早出現的病毒核酸,可檢出因病毒變異、窗口期感染ELISA法漏檢的標本[8],并且具有操作過程簡便、易于自動化、核酸標本回收率高等優勢,適于采供血機構對獻血者標本進行大規模篩查。
本研究中,63 079例經血清學檢測HBs Ag、抗-HCV、抗-HIV呈陰性獻血者中,應用上海浩源Chi Tas 1200核酸檢測篩查出57份(0.09%)HBV-DNA陽性,高于林紅等[9]報道的0.06%陽性率,這可能與本地區是乙型肝炎的高流行病區域,自然人群中乙型肝炎的感染率較高有關。HBV血清轉換前窗口期與隱匿性乙肝病毒感染(OBI)獻血者是導致HBs Ag篩查后輸血傳播感染HBV殘余風險的主要原因[10]。HBV窗口期感染與隱匿性乙肝病毒感染的獻血者均為血清HBs Ag陰性、HBV-DNA陽性,HBV窗口期感染獻血者HBs Ag會隨著時間推移由陰性轉換為陽性,而OBI獻血者其HBs Ag一般不會轉換為陽性,通常伴隨抗-HBc陽性,但部分低滴度抗-HBs獻血者中也會存在[11]。河南省是HCV高發地區,1~75歲自然人群中HCV陽性率高于全國平均水平[12],但本文并未檢出HCV-RNA,這可能與HCV主要感染肝細胞,當肝細胞壞死后方可釋放HCV進入血液中有關。抗體產生通常伴隨HCV感染且抗-HCV比較穩定,而HCV-RNA在4℃或室溫易被環境中RNA酶降解,其只有在-20℃以下環境保存時比較穩定,因此HCV-RNA檢測并不能完全代替以往的ELISA篩查,兩種方法互補檢測才能更好地提高血液質量。
此外,本研究結果顯示,在63 079例血清學檢測合格獻血者中,不同性別獻血者HBV-DNA陽性率比較差異無統計學意義(P>0.05),而在不同年齡段分組比較差異有統計學意義(P<0.01),≥49歲年齡段獻血者HBV-DNA陽性率最高(0.26%),18~22歲年齡段獻血者陽性率最低(0.03%),這可能與隨獻血者年齡增長其機體免疫功能逐漸下降相關[11];我國自20世紀90年代開始將乙型肝炎疫苗納入新生兒計劃免疫,因而18~22歲年齡段獻血者乙肝疫苗接種率較高,此年齡段獻血者HBV-DNA陽性率較低。重復獻血人群HBV-DNA陽性率高于初次獻血人群,這可能與低病毒載量的重復獻血者經過多次NAT檢測,增加了HBV-DNA檢出的概率;另外,由于重復獻血人群長期堅持獻血,這部分獻血者年齡普遍較初次獻血者大,這也與表2中獻血者HBV-DNA陽性檢出率與年齡相關相映襯。
綜上所述,ELISA篩查獻血者血液標本存在一定的漏檢現象,NAT檢測可有效降低經輸血傳播乙型肝炎、丙型肝炎、艾滋病的風險,從而提高血液質量和臨床輸血安全。

