實時超聲造影在局灶性前列腺癌靶向冷凍消融治療后隨訪中的應用價值
謝少偉,董柏君,王艷青,夏建國,李紅麗,張時君,楊文琪,薛 蔚,李鳳華
1.上海交通大學醫(yī)學院附屬仁濟醫(yī)院超聲醫(yī)學科,上海 200127;2.上海交通大學醫(yī)學院附屬仁濟醫(yī)院泌尿外科,上海 200127
我國前列腺癌發(fā)病率呈逐年上升趨勢[1]。對局灶性前列腺癌的治療,目前臨床上以根治術為主。但根治術的創(chuàng)傷較大,并發(fā)癥較多,明顯影響患者生活質(zhì)量;且部分前列腺癌患者年齡較大,合并其他老年性疾病機會較多,無法耐受根治術。近年來,前列腺冷凍消融術因其微創(chuàng)、并發(fā)癥少,越來越多地應用于前列腺癌治療并取得了良好療效,成為前列腺癌治療的有效選擇[2-3]。但對于局部不規(guī)則的腫瘤,冰球邊緣可能殘留小塊癌組織,導致局部消融不徹底,存在局部復發(fā)的可能。因此,采用有效的影像學方法對前列腺癌靶向冷凍消融術后的消融范圍進行隨訪具有重要臨床意義。經(jīng)直腸超聲造影(contrast-enhanced transrectal ultrasound,CETRUS)技術可以提供組織血流灌注的情況,是評估腫瘤局部治療后療效的理想影像學方法。本研究回顧性分析15例接受前列腺癌靶向冷凍治療患者的CETRUS資料,探討CETRUS在局灶性前列腺癌靶向冷凍消融治療后隨訪中的臨床應用價值。
1 資料和方法
1.1 研究對象
2014年6月—2015年3月,共15例患者經(jīng)穿刺病理確診為局灶性前列腺癌后行靶向冷凍消融治療。入組標準:前列腺特異性抗原(prostate-specific antigen,PSA)<20 ng/mL;Gleason評分≤7;臨床分期cTlc~cT2b期;穿刺針數(shù)≥10針,陽性率<50%;腫瘤位于前列腺一側(cè);盆腔多參數(shù)MRI或CT檢查和骨掃描檢查確認腫瘤位于前列腺內(nèi),未突破包膜,并排除淋巴結、骨和其他部位轉(zhuǎn)移;之前未接受其他相關治療。入組患者年齡75~82歲,平均78.3歲。術前PSA 7.3~19.6 ng/mL,平均11.7 ng/mL。臨床分期:cTlc期2例,cT2a期7例,cT2b期6例。活檢病理Gleason評分:6分10例,7分5例。
1.2 手術方法
均采用CryoCare氬氦刀系統(tǒng)(美國Endocare公司)進行治療。術前對患者超聲、MRI影像資料及穿刺活檢結果進行評估,如影像學檢查無明顯異常,以穿刺病理為準,確定腫塊的位置和范圍、冷凍針的數(shù)量及進針路徑。患者全身麻醉,取截石位暴露會陰部。在經(jīng)直腸超聲探頭引導下,于腫瘤附近經(jīng)會陰置入1~3根冷凍針。然后放置4根測溫針,1根位于尿道旁,1根位于直腸前或迪氏筋膜,1根位于同側(cè)前列腺頂部,1根位于同側(cè)神經(jīng)血管束。插入尿道保護器,尿道保護器內(nèi)循環(huán)水保持恒溫42 ℃。接通高壓氬氣,最低溫度為-135~-145 ℃,冷凍10 min。接通高壓氦氣升溫至15~20 ℃,復溫5 min。繼續(xù)重復冷凍-復溫1個循環(huán)。術中實時監(jiān)測冷凍針及測溫針的溫度,同時采用超聲實時監(jiān)控冰球形成范圍,監(jiān)測冰球距膀胱、直腸壁的距離,使冰球完全覆蓋腫瘤的同時避免損傷周圍臟器。
1.3 超聲造影檢查儀器與方法
所有患者于術前,術后第1天、6個月、1年及之后每年和生化復發(fā)時行經(jīng)直腸超聲檢查,包括灰階、彩色多普勒成像及CETRUS掃查。使用飛利浦iU22超聲診斷儀,C10-3v經(jīng)直腸探頭,成像機械指數(shù)為0.06。超聲造影劑SonoVue購自意大利Bracco公司,劑量為2.4 mL,經(jīng)肘部淺靜脈團注。在注射造影劑的同時行超聲造影成像,造影劑到達前列腺后,開始進行前列腺橫斷面從底部到尖部連續(xù)掃查,并同步存儲圖像。掃查時間約90 s。隨訪中,若消融灶內(nèi)出現(xiàn)明顯造影劑增強為CETRUS異常。
1.4 PSA檢查
術后1個月、3個月及之后每3個月行PSA檢測。生化進展以Pheonix標準定義,即生化復發(fā)的標準為術后PSA降到最低點后升高2 ng/mL。生化有效率定義為生化無進展人數(shù)所占比例。
2 結 果
15例均順利完成手術。術后隨訪27.8~35.1個月,中位時間為31.0個月。15例患者均存活,無新發(fā)轉(zhuǎn)移病灶。冷凍術后所有患者PSA下降(圖1),PSA最低值為0.9~14.8 ng/mL,平均4.2 ng/mL。PSA降至最低值的時間為1~9個月,平均5.7個月,73.3%(11/15)的患者隨訪無生化復發(fā),CETRUS隨訪亦未發(fā)現(xiàn)異常。
冷凍手術術前超聲或MRI檢查陽性10例,陰性5例。術后第1天常規(guī)灰階超聲示前列腺體積增大,冷凍消融灶呈水腫性改變,消融灶與周圍正常組織分界不清,無法清晰區(qū)分,彩色多普勒成像未見明顯血流信號;CETRUS示冷凍消融灶內(nèi)造影劑增強缺損區(qū),或僅見個別造影劑微泡進入,邊界不清,周圍神經(jīng)血管束增強不明顯。術后6個月常規(guī)灰階超聲示冷凍側(cè)前列腺體積縮小明顯,與周圍組織分界不清,內(nèi)部回聲不均勻,部分可出現(xiàn)多發(fā)鈣化灶,彩色多普勒成像未見明顯血流信號;CETRUS示冷凍消融灶造影邊界清晰,內(nèi)未見造影劑微泡進入,可見包膜及周圍神經(jīng)血管束增強。術后1年CETRUS示冷凍消融范圍穩(wěn)定(圖2)。
在出現(xiàn)生化復發(fā)的4例患者中,2例CETRUS檢查發(fā)現(xiàn)冷凍消融灶內(nèi)出現(xiàn)造影劑明顯增強,予間歇性內(nèi)分泌治療后PSA下降;2例CETRUS檢查示冷凍消融灶內(nèi)未見明顯造影劑增強,予主動監(jiān)測,PSA穩(wěn)定。
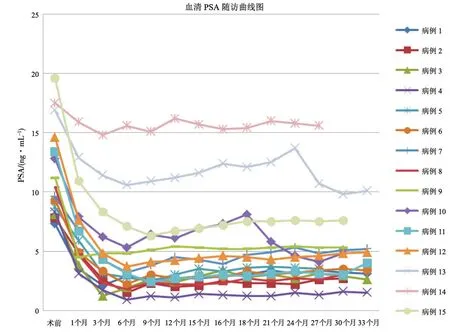
圖1 前列腺癌靶向冷凍消融治療后血清PSA隨訪曲線圖

圖2 患者男性,73歲,術前PSA 11.2 ng/mL,經(jīng)會陰前列腺穿刺病理證實右側(cè)外腺3針為Gleason評分7分的前列腺癌
3 討 論
前列腺癌冷凍消融術是將直腸腔內(nèi)超聲、經(jīng)皮穿刺介入技術和現(xiàn)代冷凍技術三者結合使用的微創(chuàng)治療方法,具有操作簡單、痛苦小及創(chuàng)傷小等優(yōu)點,適用于無法行根治性切除患者。其利用低溫冷凍腫瘤組織,使組織細胞功能受損后產(chǎn)生結構破壞,冷凍腺體組織和腫瘤組織壞死、脫落,毛細血管和小血管痙攣,造成局部血液循環(huán)障礙。冷凍還可直接損傷微血管壁,導致血栓形成,局部組織缺血缺氧,引起組織壞死[4]。局部冷凍消融術后嚴密隨訪必不可少,目前大多數(shù)研究仍以PSA水平來定義前列腺癌復發(fā),即生化復發(fā)。但生化復發(fā)并不等同于原位復發(fā),前列腺增生、炎癥及新腫瘤病灶出現(xiàn)等同樣可以導致術后PSA升高。國外學者經(jīng)大樣本研究發(fā)現(xiàn),術后PSA最低值與腫瘤特異性生存率及腫瘤無遠處轉(zhuǎn)移生存率沒有明顯相關性[5]。因此,能精確評估冷凍消融范圍,檢出前列腺癌復發(fā)病灶并引導穿刺的影像學技術至關重要。
經(jīng)直腸超聲安全、有效、實時、方便,是目前引導前列腺穿刺及微創(chuàng)治療中使用最多的影像學技術及評價手段之一。但常規(guī)二維超聲不能反映冷凍消融灶的范圍,彩色能量多普勒超聲不能顯示微血管層面的信息,并不能準確描繪治療區(qū)域的范圍。超聲造影利用造影劑微氣泡較強的背向散射信號,使含有血管的組織回聲明顯增強,這樣冷凍后壞死組織與周圍正常組織之間的增強差異可清晰呈現(xiàn)出兩者的分界,能很好地評估局部治療病灶的壞死范圍。有關動物前列腺射頻消融的研究顯示,超聲造影評估局部治療病灶范圍大小與病理大小有很好的相關性[6],已在肝癌局部介入治療效果的評價中體現(xiàn)出重要價值,被認為能與增強CT或MRI相媲美[7-8]。此外,由于前列腺癌患者年齡多較大,合并心腦血管疾病機率較大,相當一部分接受過支架放置手術的患者不能接受MRI檢查,超聲造影在這方面具有優(yōu)勢。
本研究中,常規(guī)灰階及彩色多普勒超聲不能準確評估冷凍消融灶范圍,僅能反映局部回聲或血流信號的改變。而CETRUS能夠更加直觀地顯示冷凍治療術后血流缺失的消融灶,與周圍殘存前列腺組織分界清楚,能很好地描繪出消融灶的范圍,具有獨特的優(yōu)勢。同時,對前列腺行實時CETRUS掃查不受切面選擇的限制,注射1次造影劑即能獲取整個前列腺血流灌注的信息,更有利于準確反映消融灶的范圍。對于冷凍消融灶的CETRUS圖像轉(zhuǎn)歸,發(fā)現(xiàn)術后第1天即出現(xiàn)造影劑增強缺損區(qū),但與周圍的邊界不清,消融灶范圍不穩(wěn)定,部分病例消融灶內(nèi)可見個別造影劑進入,這可能與手術時間較短,消融效果還未穩(wěn)定有關;6個月后CETRUS檢查發(fā)現(xiàn)消融灶與周圍組織邊界清楚,范圍穩(wěn)定,在此基礎上進行定期觀察隨訪有利于復發(fā)病灶的檢出。
冷凍消融術后定期復查超聲造影及生化復發(fā)后予超聲造影檢查,可以更早期、更準確地檢出消融灶內(nèi)造影劑異常增強區(qū),發(fā)現(xiàn)復發(fā)或殘留灶。本研究4例生化復發(fā)患者中,CETRUS發(fā)現(xiàn)2例消融灶內(nèi)造影劑異常增強,予間歇內(nèi)分泌治療后PSA下降;另2例CETRUS檢查無異常增強,予主動監(jiān)測,PSA穩(wěn)定,證實了CETRUS在前列腺癌隨訪中的準確性。但本研究未對復發(fā)患者行穿刺活檢證實,存在不足。
總之,實時CETRUS是臨床上局灶性前列腺癌靶向冷凍消融術后隨訪的有效影像學方法,能準確顯示消融灶的范圍,可以早期發(fā)現(xiàn)術后復發(fā)或殘留病灶。

