1例COPD患者藥物性肝損傷的病例分析及用藥監護
李雪靜 李書誼 王思箭
藥物性肝損傷是指由各類處方或非處方的化學藥物、生物制劑、傳統中藥、天然藥、保健品、膳食補充劑及其代謝產物乃至輔料所誘發的肝損傷[1]。近年來, 我國藥物性肝損傷住院診治人數有升高趨勢, 目前發現的可能導致肝損傷的藥物中以抗結核藥物和中草藥居多, 其他可導致肝損傷的藥物有抗生素、抗腫瘤藥物和抗甲狀腺藥物等[2], 這也是很多新藥臨床試驗失敗或撤市的主要原因之一。本文對1例COPD患者在治療過程中發生藥物性肝損傷的癥狀、原因進行分析討論, 并提出相應的臨床及藥學監護建議。
1 病歷資料
患者, 男, 57歲, 身高173 cm, 體重66 kg。因“反復咳嗽、咳痰20余年, 活動后喘憋9年, 加重3 d”于2017年10月28日入院。患者7年前曾行右上肺切除術, 無基礎疾病, 否認肝炎病史及食物藥物過敏史。
輔助檢查:血常規:白細胞計數(WBC)18.8×109/L, 中性粒細胞百分率(N%)84.8%, 血沉(ESR) 8 mm/h;血生化:肌酐 92.6 μmol/L, 谷丙轉氨酶(ALT)30.7 IU/L, 谷草轉氨酶(AST) 22.6 IU/L, 堿性磷酸酶(ALP)71 IU/L, γ-谷氨酰轉肽酶(γ-GGT)12.9 IU/L, 總膽紅素 (TBIL) 4.8 μmol/L ;C 反應蛋白(CRP) 157 mg/L;肺部CT示雙肺氣腫并肺大泡、雙肺支氣管擴張并感染。
入院診斷:COPD急性加重期;支氣管擴張并感染;慢性肺源性心臟病(失代償期)Ⅱ型呼吸衰竭;④肺大泡;⑤右上肺切除術。
2 方法
患者入院第1天給予哌拉西林他唑巴坦4.5 g, i.v.gtt.,q.8h., 抗感染治療;同時給予氨溴索30 mg, i.v.gtt., q.12 h., 祛痰;沙丁胺醇2.5 mg霧化吸入, b.i.d., 與多索茶堿0.3 g, i.v.gtt.,q.d., 擴張支氣管;甲潑尼龍琥珀酸鈉40 mg, i.v.gtt., q.d., 與布地奈德1 mg霧化吸入, t.i.d., 抗炎;托拉塞米10 mg, i.v.gtt.,b.i.d., 利尿;鹽酸川芎嗪240 mg, i.v.gtt., q.d., 與環磷腺苷葡胺180 mg, i.v.gtt., q.d., 改善微循環;泮托拉唑鈉40 mg, i.v.gtt., q.d.,保護胃黏膜等對癥治療。
第5天患者咳嗽、咳痰、憋喘癥狀未得到明顯改善, 加用左氧氟沙星0.5 g, i.v.gtt., q.d., 同時將甲潑尼龍琥珀酸鈉減量20 mg, i.v.gtt., q.d., 停用改善微循環藥物。
第9天痰培養結果示嗜麥芽寡養單胞菌, 遂將抗感染方案改為左氧氟沙星0.5 g, i.v.gtt., q.d., 聯合米諾環素100 mg,p.o., b.i.d.。患者霧化吸入沙丁胺醇后, 右下肢出現抽搐震顫的癥狀, 停用沙丁胺醇。
第11天患者在滴注泮托拉唑鈉時出現惡心、干嘔等胃腸道不適, 醫囑停用泮托拉唑。
第13天患者血生化全項結果示AST、ALT異常增高,肝功出現異常, 停用原有藥物治療方案, 給予還原型谷胱甘肽1.2 g, i.m., q.d.和甘草酸二銨腸溶膠囊150 mg, p.o., t.i.d.保肝治療, 同時給予醋酸潑尼松片15 mg, p.o., q.d.和沙美特羅替卡松粉吸入劑(250/50 μg) 1吸/d。
保肝治療3 d后患者感染癥狀仍未緩解, 患者應用左氧氟沙星和米諾環素后出現肝功異常, 考慮依替米星對肝臟的影響較小, 且患者腎功良好, 故給予依替米星300 mg, i.v.gtt.,q.d.繼續抗感染治療。6 d后患者感染癥狀得到控制, 病情穩定, 復查肝功轉氨酶較前趨于正常, 準予出院。
治療過程中, 患者肝功各項指標出現異常變化, 引起臨床藥師的高度重視, 患者入院時肝功能檢查各項指標均正常,否認肝炎病史。結合患者治療過程及病情變化, 藥物導致的肝功能損傷不能排除, 因此, 藥師建議密切監測肝功, 加強保肝治療。治療后患者肝功能各項指標有所好轉, 具體轉歸見表1。
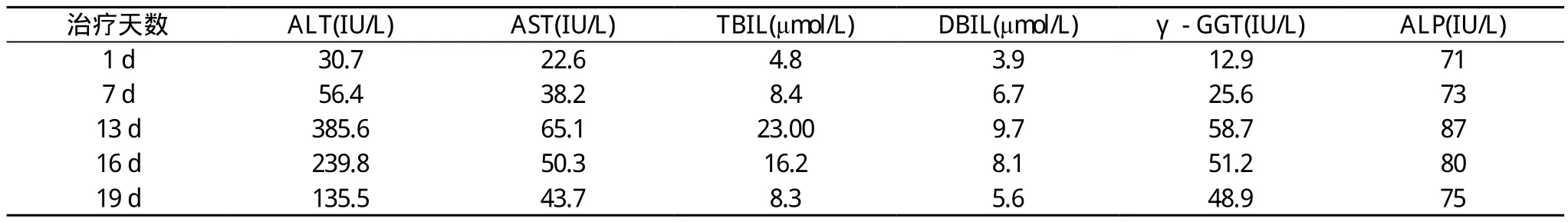
表1 藥物治療過程中的肝功能指標
3 討論
3.1 藥物性肝損傷的評定 目前的研究認為[3], 國際共識的藥物性肝損傷因果評價表(RUCAM)對于確診藥物性肝損害可控性和認可度較高, 根據RUCAM量化評分系統9條評判參數逐一打分, 患者從初次服用可疑藥物至出現肝功能異常, 時間為7~13 d(+2分);停藥后7 d內ALP下降≥50% 最大正常值上限(ULN)(+2分);年齡≥55歲(得1分);有合并用藥且時間具有提示性(-1分);完全排除甲型肝炎、乙型肝炎、急性丙型肝炎、膽道梗阻、酗酒、新近發生過低血壓以及排除巨細胞病毒EB病毒、皰疹病毒感染(+2分);總分為6分, 故認為該病例很可能為藥物性肝損傷。
3.2 藥物性肝損傷與患者用藥的關聯性評價 患者入院后給予抗感染及祛痰、擴張支氣管、消炎、利尿、改善微循環、保護胃黏膜等對癥治療。除擴張支氣管藥物多索茶堿、抗菌藥左氧氟沙星、米諾環素外, 其他藥物應用時間較短, 均未見明顯肝損傷的相關報道。
多索茶堿甲基黃嘌呤的衍生物, 其導致肝損傷的機制可能是由于黃嘌呤氧化酶(XOD)是體內核酸代謝中一種重要的酶, 因甲基黃嘌呤的蓄積, XOD的大量釋放, 其氧化反應的持續, 自由基的大量產生, 在機體缺血缺氧的基礎上加重了肝細胞的損害。曾有報道[4], 多索茶堿0.3 g, i.v.gtt., q.d., 連用7 d后, 患者出現納差、腹脹, 肝功能損傷。停藥后予保肝對癥治療, 7 d后復查肝功能恢復正常。
米諾環素(二甲胺四環素)是一種長效、高效的半合成四環素類廣譜抗生素。由于臨床應用限制, 關于米諾環素引起的不良反應的報道不多, 曾有報道長期大劑量服用米諾環素會造成肝損害, 表現為肝功能異常, 谷丙轉氨酶升高[5],但短時間常規劑量使用米諾環素致嚴重肝功能異常的情況報道較少。
左氧氟沙星是臨床應用較為廣泛的第3代氟喹諾酮類抗菌藥, 自從2001年Karim等[6]報道首例由左氧氟沙星引起的肝損傷以來, 以后陸續有類似的病例報道。其發生機制有兩種:藥物的直接肝毒性和免疫機制, 此病例均不能排除。
在藥物的相互作用方面, 患者曾聯合使用左氧氟沙星和米諾環素, 二者均有肝毒性, 加大了發生肝損傷的幾率。而左氧氟沙星的說明書則明確指出其與茶堿類藥物的相互作用, 通過對肝藥酶的抑制作用而影響茶堿類藥物在肝臟的代謝, 使其在體內蓄積, 易導致中毒[7]。其他同期應用的藥物中,尚未出現藥物相互作用致不良反應的報道。
3.3 保肝治療 發現患者肝功異常后藥師建議立即停用之前使用的所有藥物, 阻止其進一步惡化。據國際醫學科學組織理事會(CIOMS)確立的標準[8], 患者ALT≥3ULN, 且ALT活動度/ALP活動度≥5, 屬于肝細胞損傷型。藥師建議根據患者肝功能受損分型, 選擇適宜的保肝藥物輔助治療, 當出現嚴重的免疫介導反應時, 應短期給予大劑量激素治療。還原型谷胱甘肽可激活巰基酶, 促進易代謝低毒化合物的形成,調節細胞膜代謝;甘草酸二銨可保護肝細胞膜, 調節免疫、抗炎、解毒、抗氧化, 均有利于患者病情的恢復。6 d后, 患者肝功各項指標逐漸下降, 趨于正常。
在整個治療過程中, 患者使用多種藥物產生較為明顯的不良反應, 如沙丁胺醇、泮托拉唑鈉, 這兩種藥物均經由肝臟代謝。藥物在肝內主要依靠藥物代謝酶代謝, 由于基因的遺傳多態性[9], 不同個體對于藥物的耐受性和敏感度差異較大, 不同種族人群則表現出對藥物代謝的不同表現類型, 通常分為快代謝型和慢代謝型。由于遺傳多態性的存在, 部分個體在代謝過程中會積蓄更多的有毒或致癌的物質, 進一步造成肝損傷, 或原本不具抗原性的藥物, 在肝內轉化后形成具有抗原性的代謝產物, 引起免疫性肝損傷[10]。患者使用沙丁胺醇、泮托拉唑鈉在正常劑量下發生的不良反應通常是藥物劑量過大才會出現的, 可能與藥物積聚有關。誘發患者藥物性肝損傷的具體機制尚不能明確, 隨著科學研究的進展,明確某藥引起的藥物性肝損與其代謝酶的基因多態性相關,可在臨床用藥時, 通過測定患者肝藥酶的基因型, 初步判斷用藥個體的表型, 從而科學指導確定個體的用藥量或確定合適的聯合用藥方案, 以減少藥物性肝損傷的發生率。
綜上所述, 臨床藥師參與藥學監護可有效地避免藥物性肝損傷的發生發展, 對合理、安全使用藥物起到了應有的作用, 并對藥物性肝損傷的診治有進一步的體會。如鑒于藥物性肝損傷的診斷相對比較主觀, 可推廣使用相對客觀的RUCAM輔助診斷;而藥物性肝損傷的處理, 關鍵是及時停用可疑藥物和合理使用護肝藥物。

