靜脈化療聯合腹腔熱灌注化療對胃癌患者術后免疫功能及生存質量的影響
劉 冬,劉 冠,湯忠祝,吳 列
(浙江省腫瘤醫院腹部放療科,杭州 310022)
胃癌患者早期多無明顯臨床癥狀,或者部分患者僅表現出非特異性消化道癥狀,因此胃癌發現并就診時多數患者已處于中晚期[1-2]。胃癌根治術是治療該病最主要的方法,但切除率僅為40%左右,治療效果不理想,而行全身性化療對患者的毒副作用較大,嚴重影響患者的生活質量[3-4]。目前,胃癌的治療仍是臨床醫師面臨的一項嚴峻挑戰。腹腔灌注化療是將化療藥物稀釋后,直接灌注于腹腔內的區域性給藥途徑。其中腹腔熱灌注化療是一種腹腔惡性腫瘤輔助治療手段,已在胃腸道腫瘤的治療中發揮了很好的療效,通過對腫瘤局部加溫,使其達到一定溫度持續一定時間,既能殺滅腫瘤細胞,又不損害正常組織,達到治療腫瘤的目的,近年來在臨床上應用廣泛[5-6]。本研究旨在探討靜脈化療聯合腹腔熱灌注化療對胃癌患者術后免疫功能及生存質量的影響。
1 對象與方法
1.1 研究對象
選取2016年1月至2017年6月在浙江省腫瘤醫院行胃癌根治術后的患者80例,均經胃鏡、病理學相關檢查確診為胃癌,術前均未接受放化療,心、肺、肝、腎等功能均正常。排除合并其他惡性腫瘤和免疫性疾病、冠心病、高血壓等疾病,不接受本研究的治療方案及對治療方案中相關藥物過敏的患者。將80例患者按治療方法的不同分為2組:對照組40例,男19例,女21例,年齡(51.6±5.1)歲,病程(0.5±0.3)年。病理類型:高分化腺癌14例,中分化腺癌13例,低分化癌7例,黏液腺癌6例;腫瘤TNM分期:Ⅱ期15例,Ⅲ期14例,Ⅴ期11例。觀察組40例,男20例,女20例,年齡(52.1±4.9)歲,病程(0.6±0.2)年。病理類型:高分化腺癌13例,中分化腺癌15例,低分化癌6例,黏液腺癌6例;腫瘤TNM分期:Ⅱ期14例,Ⅲ期15例,Ⅴ期11例。2組基線資料比較差異無統計學意義(P>0.05),具有可比性。
1.2 治療方法
觀察組采用腹腔熱灌注化療聯合靜脈化療,即在胃癌根治術結束、未關閉腹腔前,將灌注管置于患者的腹腔左右兩側。根據患者的術后恢復情況,于術后1~2 d時采用腹腔熱灌注化療。在治療前,用0.9%氯化鈉注射液沖洗腹腔灌注管內的血塊。然后,連接熱灌注化療機,將3000 mL化療液(順鉑注射液50 mg加入0.9%氯化鈉注射液中配制成化療液)加熱至38 ℃后,以100 mL·min-1的速度開始灌注,視患者耐受情況和生命體征繼續加熱至43 ℃,并逐步提高灌注流速(最大流速<300 mL·min-1),持續1~1.5 h,調節熱灌注化療機使腹腔內化療液維持2000 mL以上。治療后,腹腔內留存1000 mL左右的化療液,外接引流袋于灌注管上,使化療液緩慢流出,7 d后取出灌注管。在術后2周采用常規靜脈化療,即采用注射用奧沙利鉑200 mg加入5%葡萄糖注射液500mL中靜脈滴注3 h,第1天;氟尿嘧啶500 mg·d-1,以微量泵持續靜脈滴注120 h,第1—5天;注射用亞葉酸鈣300 mg·m-2加入5%葡萄糖注射液250 mL中靜脈滴注2 h,第1—5天。對照組在術后2周采用常規靜脈化療,治療方法同觀察組。2組均5 d為1個療程,化療結束2周后進行下一周期化療,共治療6個周期。
1.3 觀察指標與生存質量評定方法
觀察2組治療前、治療后免疫功能相關指標(CD3+、CD4+、CD8+值,CD4+/CD8+比值)及治療后生存質量的情況。
生存質量評定方法:依據卡氏功能狀態評分標準(KPS)。提高:治療后較治療前KPS評分增加≥10分;穩定:治療后較治療前KPS評分增加或減少<10分;下降:治療后較治療前KPS評分減少≥10分。提高率=提高例數/總例數×100%。
1.4 統計學方法
2 結果
2.1 2組治療前后免疫功能相關指標的比較
2組治療前CD3+、CD4+、CD8+值,CD4+/CD8+比值比較差異無統計學意義(P>0.05)。與同組治療前比較,2組治療后CD3+、CD4+值均升高,CD4+/CD8+比值均降低(均P<0.05);與對照組比較,觀察組治療后CD3+、CD4+值均升高更明顯,CD4+/CD8+比值降低更明顯(均P<0.05)。見表1。
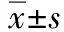

組別n時間CD3+/%CD4+/%CD8+/%CD4+/CD8+比值對照組40治療前43.29±3.2733.61±2.9537.26±3.311.17±0.21治療后52.56±5.87?37.89±3.43?31.57±3.18?0.98±0.08?觀察組40治療前43.31±3.2933.98±2.9737.52±3.291.39±0.29治療后56.91±6.01?#44.86±3.98?#26.81±3.25?#0.99±0.07?#
*P<0.05與同組治療前比較,#P<0.05與對照組比較。
2.2 2組治療后生存質量提高率的比較
治療后生存質量,觀察組提高26例,穩定9例,下降5例,提高率為65.00%;對照組提高11例,穩定16例,下降13例,提高率為27.50%。觀察組治療后生存質量提高率高于對照組(65.00%比27.50%,P<0.05)。
3 討論
胃癌是起源于胃黏膜上皮的惡性腫瘤,在我國各種惡性腫瘤中發病率居首位[7],50歲以上人群為胃癌的高發人群。近年來,由于生活方式的改變及工作壓力的增大,胃癌的發病也呈現年輕化的趨勢[8]。另外,胃癌早期沒有特異性臨床癥狀,或是出現噯氣、上腹不適等非特異性癥狀,常被認為是胃潰瘍、胃炎等慢性胃病,未引起患者的重視[9]。
目前,臨床上治療胃癌常用的方式主要有手術、放化療、支持治療、靶向治療等[10]。胃癌患者經上述方法治療后復發率較高,有研究[11]表明這是由于腹腔內術后殘留病灶及游離的癌細胞發生轉移,導致腫瘤復發,進而胃癌術后治療失敗。腹腔內熱灌注化療是近年來興起的一種胃癌治療技術,是將熱療與化療結合的一種治療手段。有研究[12]表明,相對正常組織,腫瘤組織對熱更為敏感。熱療可通過增加癌細胞的通透性來促進化療藥物進入細胞,抑制DNA的修復與合成,從而發揮抗腫瘤效應。另外,化療藥物經腹腔熱灌注后,能在腹腔內維持較高的藥物濃度,藥物作用于癌細胞的時間也進一步延長,使藥物治療達到最佳效果[13]。鐘勇偉等[14]研究證實,腹腔熱灌注化療有助于改善患者的術后免疫功能,進一步提高患者的生存質量。本研究結果顯示,與對照組比較,觀察組治療后CD3+、CD4+值和生存質量提高率均升高更明顯,CD4+/CD8+比值降低更明顯(均P<0.05),其與劉紅波等[15]研究的結果相符,分析其原因可能是由于腹腔熱灌注熱療過程中高溫有助于增加癌細胞的抗原性,激活細胞抗腫瘤免疫應答,改善免疫功能。此外,該治療方法能使腹腔內抗癌藥物的濃度高于體循環的濃度,可達數倍甚至上百倍,并能夠最大程度殺滅腹腔內的癌細胞和殘留病灶。

