微生物直接種間電子傳遞:機制及應用*
黃玲艷 劉 星 周順桂
(福建農林大學資源與環境學院,福州 350002)
微生物種間電子傳遞(Interspecies electron transfer,IET)是指電子供體微生物與電子受體微生物之間通過直接或間接方式傳遞電子形成互營生長關系,從而共同完成單一微生物不能完成的代謝過程的現象[1-3]。例如,在以乙醇為電子供體、富馬酸為電子受體的地桿菌共培養體系中,金屬還原地桿菌Geobacter metallireducens不能以富馬酸為電子受體氧化乙醇,硫還原地桿菌G. sulfurreducens無法以乙醇為電子供體還原富馬酸,但當兩微生物同時存在時,G. metallireducens可將乙醇氧化產生的電子傳給G. sulfurreducens,G. sulfurreducens再將電子傳至富馬酸,實現G. metallireducens與G. sulfurreducens的電子互營[4]。微生物IET分為間接種間電子傳遞(Mediated IET,MIET)和直接種間電子傳遞(Direct IET,DIET)。其中,MIET是指微生物間通過氧化還原性內源(細菌自身產生的)小分子物質如氫/甲酸、核黃素等或外源(天然存在或人工合成)小分子物質如腐殖質等實現電子傳遞的方式,是一種經典的互營生長機制[5]。DIET是指微生物間通過自身導電結構如導電菌毛和細胞色素c等實現電子交換的過程[6]。此外,外源導電物質如活性炭[7]和磁鐵礦[8]也能介導微生物間的IET。由于它們介導的IET不需要能量載體的協助,而是直接依靠介體的導電性實現電子傳遞,因此將這類IET歸為DIET。
微生物IET起源最早可追溯至20世紀初。1906年Omelianski[9]分離得到的乙醇氧化產甲烷奧氏桿菌(Methanobacillus omelianskii)。之后,Bryant等[10]發現M. omelianskii其實是產乙酸菌與產甲烷菌的共培養物,產乙酸菌與產甲烷菌間以氫氣為電子載體實現電子互營。除氫氣外,1988年Thiele和Zeikus[11]發現甲酸也能協助微生物間的電子傳遞,并且在互營產甲烷消化器中甲酸對IET的貢獻遠大于氫氣的貢獻。在很長一段時間內,微生物間以氫/甲酸為電子載體進行電子傳遞被認為是微生物間電子互營的主要方式,直至2010年Summers等[4]在地桿菌G. metallireducens與G. sulfurreducens的共培養體系中發現細胞色素c和菌毛介導的DIET,才打破了微生物互營代謝的傳統認識,為微生物IET研究打開了新視角。
微生物IET普遍存在且方式多樣。產甲烷反應器、厭氧沉積物中廣泛存在的產甲烷菌Methanosaeta與地桿菌Geobacter之間既能借助氫/甲酸[12]和氧化還原性小分子物質[13-15]等實現電子轉移,也能利用自身導電菌毛和氧化還原蛋白進行IET。目前微生物間利用氫/甲酸實現共培養的研究已比較成熟,但DIET研究仍處于初級階段。為進一步理解厭氧微生物間的電子互營,本文在論述MIET機制的同時,重點闡述了DIET機制及研究現狀,列舉了代表性IET微生物,介紹了IET在環境修復、溫室氣體減排等過程中的作用,并就IET未來研究方向提出了展望。
1 微生物IET機制
微生物IET方式分為MIET和DIET。其中,MIET包括:種間氫/甲酸轉移(即微生物間以氫/甲酸為電子載體實現IET的方式,圖1a)和電子穿梭機制(即微生物利用具有氧化還原特性的小分子物質如吩嗪、核黃素、腐殖質等實現電子轉移的過程,圖1b);DIET包括:納米導線機制(微生物間利用自身導電菌毛實現電子互營,圖1c)、氧化還原蛋白機制(主要以細胞色素c為電子載體進行電子傳遞,圖1d)和導電物質介導機制(利用外源導電顆粒如活性炭、磁鐵礦等進行電子傳遞,圖1e)。此外,近年來在海洋沉積物中發現的電纜細菌(Cable bacteria)與硫氧化菌間的長距離氧化還原耦合也被認為是微生物IET的一種(圖1f):電纜細菌利用自身的長纖毛將硫氧化菌傳來的電子傳至沉積表面的含氧層,將氧氣還原生成水,與硫氧化菌實現電子互營[16]。
1.1 MIET機制及研究現狀
1967年Bryant等[10]在研究乙醇氧化產甲烷奧氏桿菌(M. omelianskii)時首次發現以氫氣為電子載體的IET。該奧氏桿菌是產乙酸菌S菌株與產甲烷菌Methanobacterium ruminantium的共培養物。在該共培養體系中,S菌株氧化乙醇產氫氣,M. ruminantium利用氫氣還原CO2產甲烷。前者屬于吸能反應,不能自發發生,必須依賴后者不斷消耗氫氣降低氫分壓(理論上需小于0.1kPa),才能持續反應[19]。除氫外,Thiele和Zeikus[11]在互營產甲烷消化器中發現甲酸也能促進微生物IET,并且甲酸對IET的貢獻(大于90%)遠高于氫氣對IET的貢獻(小于10%)。1989年Boone等[20]在互營菌(Syntrophomonas wolfei)與產甲烷菌(M. formicicum)的共培養體系中,采用擴散模型進一步證實了種間甲酸轉移的存在,并且發現種間甲酸轉移速率是種間氫轉移的100倍。2002年Plugge等[21]發現丙酸鹽氧化菌與產甲烷菌共培養體系在甲酸和氫氣同時存在的情況下生長更好,表明種間氫和甲酸轉移可同時發生。此外,對于既可消耗氫氣又可產生氫氣的互營體系,微生物IET甚至存在電子反向傳遞的可能。例如在Desulfovibrio vulgaris和Methanosarcina barkeri的共培養體系中,D. vulgaris降解乳酸生成乙酸、二氧化碳和氫氣,電子經由氫氣傳遞至M. barkeri將二氧化碳還原成甲烷[22]。但當氫氣濃度較低時,M. barkeri自身會釋放出氫氣,氫氣能被D. vulgaris利用,因此D. vulgaris和M.barkeri之間存在電子反向傳遞(電子由M. barkeri傳至D. vulgaris)的可能[23]。此外,2008年Kosaka等[24]研究發現在以氫氣為電子載體的互營體系中,甲酸脫氫酶會表達生成甲酸,推測甲酸是微生物種間氫轉移的臨時電子載體。De Bok等[25]根據費克擴散定律,對比氫氣和甲酸的擴散速率和溶解度,提出氫氣主要參與近距離的電子傳遞,而甲酸參與遠距離的電子轉移的理論。2013年Felchner-Zwirello等[26]研究認為微生物間可以通過縮短距離來達到增加種間氫轉移通量的目的。
在種間氫/甲酸轉移體系中,微生物氧化有機物產氫通常與NAD+/NADH、FAD/FADH2或輔酶F420/F420-H2以及Fd(ox)/Fd(red)(Fd,鐵氧化還原蛋白)等氧化還原中間體的相互轉化相耦聯[27]。這些耦聯反應在標準狀態下的吉布斯自由能通常為正值,反應無法自發發生。當氫氣分壓小于某值時,吉布斯自由能由正值變為負值,反應可自發發生,方便電子供體微生物傳出電子(表1)。
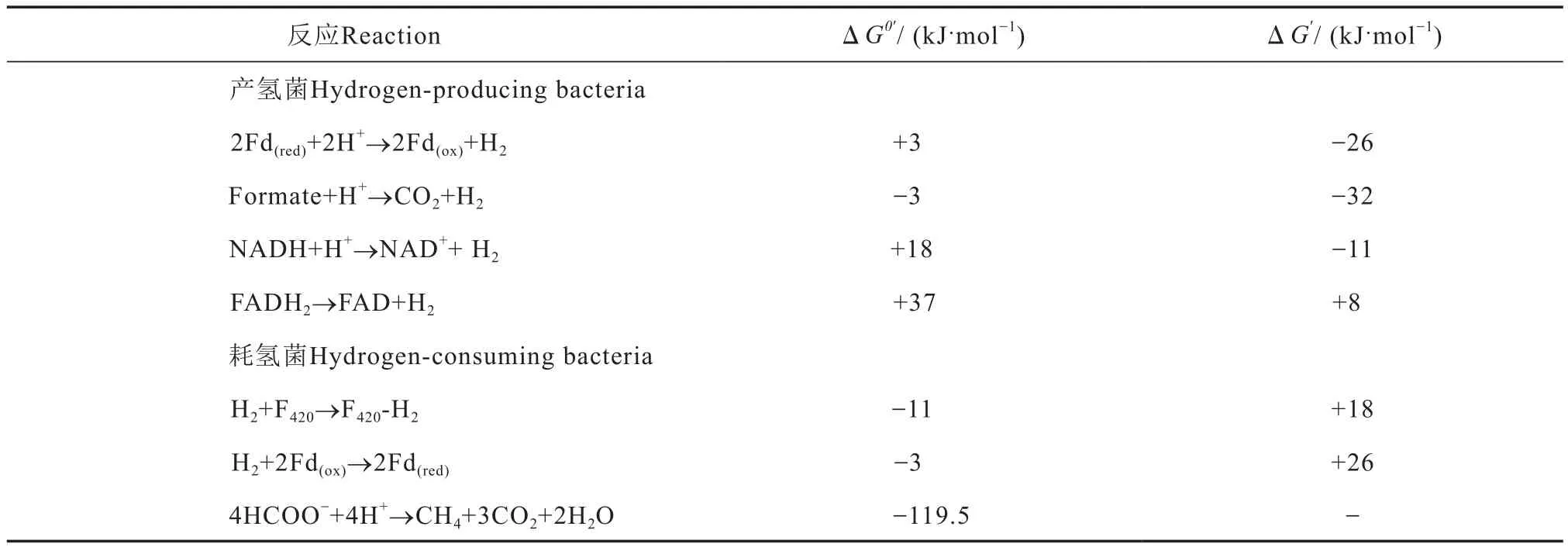
表1 種間氫/甲酸轉移中氫/甲酸相關反應能量變化[5]Table 1 Energy variation of hydrogen/formate-related reactions in interspecies hydrogen/formate transfer[5]
電子穿梭機制是指微生物間借助自身分泌、天然存在或人工合成的具有氧化還原活性的小分子物質(電子穿梭體)進行電子傳遞的方式[28]。1978年Biebl和Pfennig[29]在脫硫單胞桿菌Desulfuromonas acatoxidans和突柄綠菌Prosthecochloris aestuarii的共培養體系中發現硫化物能夠介導微生物IET。其中,D. acatoxidans以乙醇為電子供體將硫單質還原成硫化物,P.aestuarii通過光合作用固定CO2并將硫化物氧化生成硫單質,如此循環往復實現IET。2002年Kaden等[30]在以乙酸為電子供體、硝酸鹽為電子受體的地桿菌G. sulfurreducens與沃林氏菌Wolinella succinogenes共培養體系中發現了L-胱氨酸/半胱氨酸介導的IET。G. sulfurreducens在氧化乙酸的同時將L-胱氨酸還原成L-半胱氨酸,W.succinogenes利用L-半胱氨酸將硝酸鹽還原,而L-半胱氨酸被氧化成L-胱氨酸再次參與乙酸氧化。2015年Smith等[15]發現在外源添加腐殖質類似物AQDS的情況下,G. sulfurreducens與G. metallireducens的互營代謝速率得到促進,并且突變株共培養實驗證明AQDS協助的IET能為受體微生物G. sulfurreducen提供足夠能量用于生長。
1.2 DIET機制及研究現狀
2010年Summers等[4]在以乙醇為電子供體、富馬酸為電子受體的G. metallireducens與G.sulfurreducens共培養體系中發現了細胞色素c和菌毛介導的DIET。DIET的發現打破了對微生物IET的傳統認知,是微生物IET研究的一大里程碑。目前地桿菌參與的DIET研究最為透徹,本節將主要總結地桿菌參與的DIET機制研究。
地桿菌參與的DIET體系如G. metallireducens與G. sulfurreducens的共培養中,通常能看到大量菌毛形成的纏繞結構[4]。在菌毛的作用下,互營微生物雙方形成緊密的團聚體,以縮短電子傳遞距離,減少能量損耗。而對于無導電菌毛介導的互營體系通常無法實現DIET。如G. metallireducens在缺失菌毛表達能力的情況無法與產甲烷菌Methanosaeta或Methanosarcina實現IET[31]。并且G. metallireducens與G. sulfurreducens中無論哪一方被敲除菌毛表達基因均無法與對方進行電子互營[4,6],表明了菌毛在DIET中的重要地位。
菌毛是從細胞表面延伸出來的絲狀蛋白,不僅能幫助細菌附著,促進細胞運動,也能將電子傳出至胞外電子受體。2005年Reguera等[32]利用改造的原子力顯微鏡發現G. sulfurreducens菌毛具有導電歐姆響應。Lovley等[33]純化菌毛檢測發現G. sulfurreducens菌毛電導率能達到188Ms·cm-1,類似于金屬導電性,并提出了菌毛的類金屬導電模型[34](見圖2a):電子通過菌毛芳香環π-π軌道折疊形成的電子云進行傳遞,而細胞色素c在菌毛電子傳遞過程中只是充當中間體或電子儲容器。2011年Strycharz等[35]在G. sulfurreducens傳遞電子至電極的過程中,通過基因敲除等手段提出了不同于類金屬導電模型的電子躍遷理論(見圖2b):電子沿著菌毛上毗鄰的氧化還原蛋白(細胞色素c)逐步躍遷至電子受體實現電子轉移,其中菌毛起著電子傳遞支架的作用。2013年Bonanni等[36]結合類金屬導電模型和電子躍遷模型,提出了Stepping stone理論(見圖2c):電子沿著菌毛上的芳香環簇進行傳導,當芳香環簇距離大于電子可直接傳遞距離時,電子依靠菌毛上的細胞色素c進行傳遞。
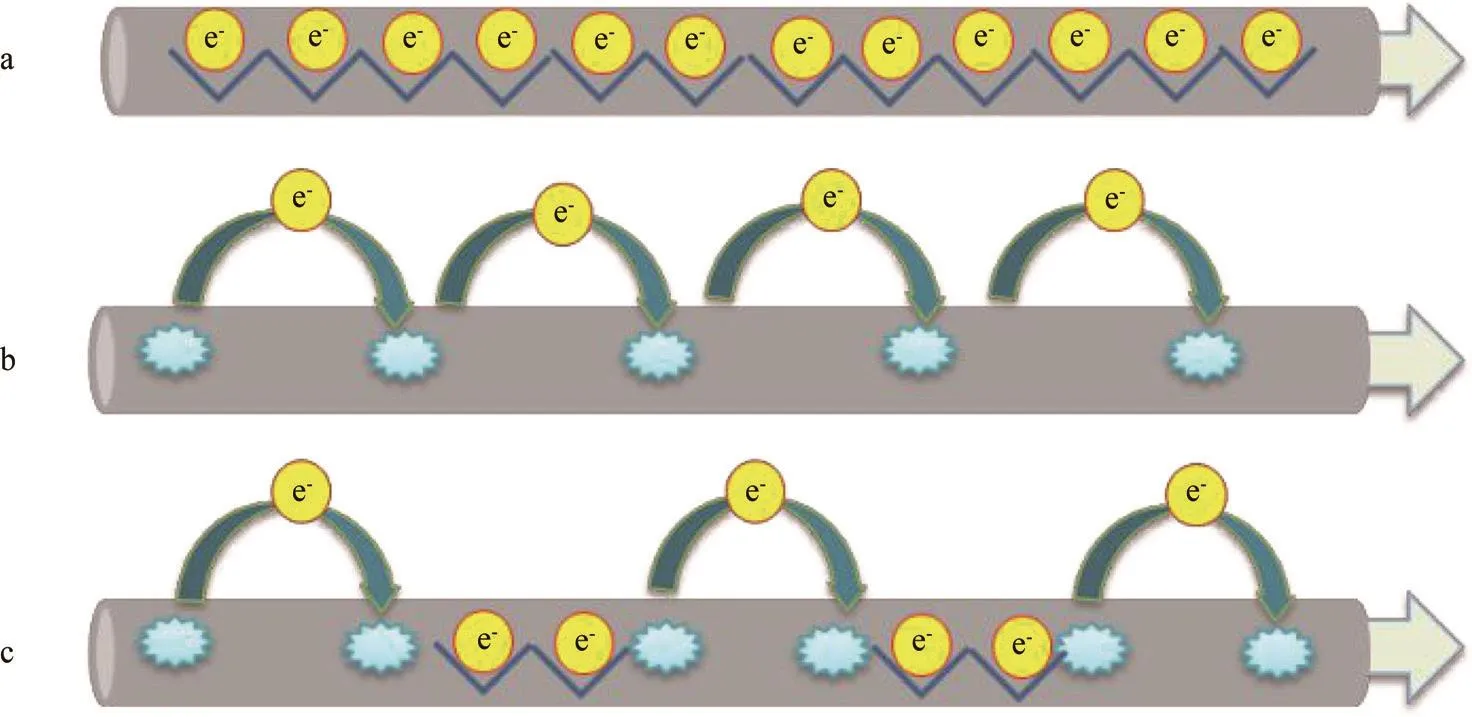
圖2 納米導線導電模型Fig. 2 Models of electron flow via nanowires
微生物周質和膜上通常分布有多種氧化還原蛋白,且在不同胞外電子傳遞模式下參與的細胞色素c種類存在差異[37]。根據2016年Shi等[38]提出的地桿菌G. sulfurreducens電子由內膜向外膜傳遞的模型(圖3):胞內電子通過氫醌的氧化反應將電子傳遞給內膜上的ImcH(高電位)或CbcL(低電位)蛋白,ImcH或CbcL上的電子經周質蛋白PpcA家族蛋白的介導傳遞至外膜蛋白如OmaB、OmcB、OmaC、OmcC。其中OmaB、OmcB與OmbB以及OmaC、OmcC與OmbC形成跨膜蛋白復合體介導電子傳遞,在胞外電子傳遞過程中起著重要作用。在以Fe3+為電子受體的胞外電子傳遞過程中,細胞色素OmcS是電子由細胞表面傳遞至胞外電子受體的重要介體蛋白[39]而參與較薄的陽極生物膜胞外電子傳遞的蛋白主要是OmcS和OmcE[40],當陽極生物膜變厚時,參與胞外電子傳遞過程的細胞色素主要是菌毛蛋白PilA和細胞色素OmcZ[41]。
在地桿菌參與的DIET過程中,發揮重要作用的氧化還原蛋白是外膜細胞色素OmcS。2010年Summers等[4]在G. metallireducens與G. sulfurreducens的互營體系中發現一種與G.sulfurreducens導電菌毛相結合的氧化還原蛋白—細胞色素OmcS得到了大量表達,并且G.sulfurreducens在敲除掉OmcS的表達基因后無法與G. metallireducens實現共培養,表明OmcS在DIET中擔當著重要角色。此外,跨膜蛋白在IET也發揮了一定的作用。2017年Phuc等[42]在突柄綠菌P. aestaurii與地桿菌G. sulfurreducens的互營厭氧光合成體系中發現,兩者外膜緊密接觸,且G. sulfurreducens在缺失跨膜孔蛋白與細胞色素復合體(ombB-omaB-omcB-orfS-ombC-omaC-omcC)的情況下無法與P. aestaurii達成共培養關系,表明外膜蛋白影響了微生物間的DIET過程。2015年Benomar等[43]通過蛋白熒光標記發現,脫硫弧菌Desulfovibrio vulgaris和梭菌Clostridium acetobutylicum共培養時進行了蛋白交換,表明微生物間存在通過交換蛋白實現IET的可能。
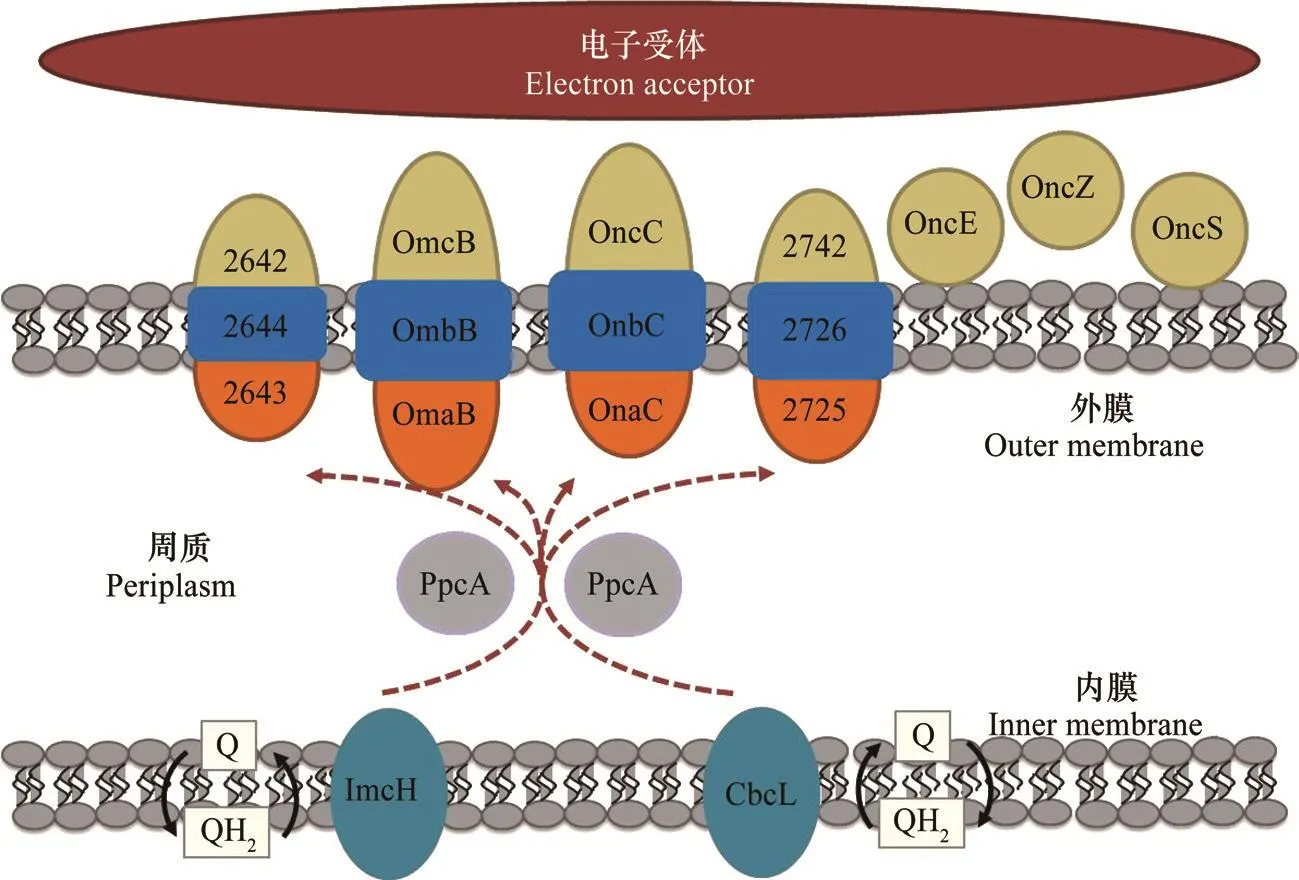
圖3 地桿菌電子由內膜向外膜的轉移[38-41]Fig. 3 Electron transfer from inner membrane to outer membrane in Geobacter[38-41]
除依靠自身導電結構進行DIET之外,微生物也能借助外源的非生物導電材料如磁鐵礦、顆粒活性炭或生物炭等實現DIET。2012年Kato等[44]在水稻土中添加(半)導體鐵氧化物如磁鐵礦和赤鐵礦發現Geobacter與Methanosarcina間的電子傳遞得到了促進,而添加非導電性鐵氧化物對Geobacter與Methanosarcina間的電子傳遞不具備促進作用。2015年Li等[45]在水稻土中分別加入二氧化硅包裹的磁鐵礦和裸露的磁鐵礦發現,二氧化硅包裹的磁鐵礦不能像裸露磁鐵礦一樣促進微生物DIET,表明磁鐵礦對DIET的促進作用與導電性相關。同年,Liu等[46]發現原本無法實現電子互營的G. sulfurreducens的細胞色素OmcS缺陷株與G.metallireducens在外源添加磁鐵礦的作用下能夠形成共培養,但G. sulfurreducens的菌毛PilA突變株與G. metallireducens不能恢復電子互營,表明磁鐵礦可以彌補細胞色素OmcS的缺失,但不能替代菌毛的功能。導電碳材料如顆粒活性炭、生物炭和碳布等也可以介導微生物IET[47]。2012年Liu等[7]發現,在顆粒活性炭的介導下,G. sulfurreducens細胞色素OmcS缺陷株或菌毛蛋白PilA缺陷株能夠與G. metallireducens實現電子互營,證明顆粒活性炭具有介導DIET的能力,且顆粒活性炭介導下的DIET無需菌毛和細胞色素c參與。此外,Chen等[48-49]發現導電性生物炭和碳布能促進G.metallireducens與G. sulfurreducens及M. barkeri間的DIET,但對D. vulgaris與G. sulfurreducens的種間氫轉移無促進作用。
1.3 IET微生物
MIET常見形式有種間氫/甲酸轉移和電子穿梭體介導的IET,其中,種間氫/甲酸轉移常見于產甲烷微生物群落,如產甲烷菌與產乙酸菌[10]、產甲烷菌與脫硫弧菌[22]、地桿菌與甲醇降解菌[50]。此外,電子穿梭體如硫化物、L-半胱氨酸、AQDS等也能協助微生物MIET,如脫硫菌與光合菌[29]、地桿菌與沃林氏菌[30]等之間的電子傳遞。
DIET由于需要微生物導電菌毛和細胞色素c的介導,常見于地桿菌參與的共培養體系,如地桿菌與地桿菌[46]、地桿菌與產甲烷菌[31,48,51]、地桿菌與光合菌[42]、地桿菌與脫氮菌[52]等。外源添加的(半)導電材料如磁鐵礦、活性炭等也能協助微生物DIET(表2)。此外,脫氯菌與互營菌[53]、厭氧甲烷氧化菌與硫酸鹽還原菌[54]間也能以DIET形式進行電子傳遞。在厭氧甲烷氧化古菌ANME-1與硫酸鹽還原菌HotSeep-1的互營代謝過程中,ANME-1與 HotSeep-1的胞外細胞色素c和菌毛相關基因得到了高度表達,表明菌毛和細胞色素c在兩者互營過程中扮演著重要角色[54]。

表2 部分參與IET微生物及其IET方式Table 2 Microorganisms participating in IET and their IET patterns

續表
2 微生物IET應用
2.1 厭氧消化產甲烷
厭氧消化技術是指厭氧環境中,微生物分工合作將大分子有機廢物水解并最終生成可再生生物質能源氫氣和甲烷的過程[55]。常規厭氧消化系統具有啟動緩慢、處理能效低、反應時間長等缺點,提高產甲烷菌的代謝活性和產甲烷速率是提高厭氧消化效能的關鍵所在。2014年Cruz等[8]發現磁鐵礦顆粒能夠更快速地引發丙酸降解產甲烷,表明磁鐵礦對微生物有機物氧化產甲烷具有促進作用。2016年Dang等[56]發現往厭氧消化池添加導電碳材料如碳布、碳氈和活性炭等可促進厭氧消化池中有機物的降解。Zhao等[57]通過往厭氧消化池添加導電碳布發現微生物IET方式由IHT轉變為DIET,緩解了消化池中酸對種間氫轉移的抑制作用。Yang等[58]發現厭氧消化池中的微生物量與有機物降解速率密切相關,因此外源添加產甲烷微生物,可加快微生物厭氧消化產甲烷過程。
2.2 甲烷厭氧氧化
甲烷是一種重要的能源物質,也是引起地球溫室效應的重要氣體。微生物主導的甲烷厭氧氧化能夠有效地減少甲烷的排放[59]。目前為止發現的甲烷厭氧氧化類型主要有硫酸鹽還原型甲烷氧化和反硝化型甲烷氧化,并且認為是微生物進行IET的結果[60]。2015年McGlynn等[54]發現增強菌毛和細胞色素c的表達可促進甲烷厭氧氧化。此外,Egger[61]和Ettwig[62]等發現在鐵氧化物如磁鐵礦納米顆粒等協助下,微生物甲烷厭氧氧化得到促進,表明外源添加(半)導體材料是提高甲烷厭氧氧化速率的重要手段。
2.3 微生物脫氯
含氯污染物通常具有持久性,對環境及人類的健康威脅大。微生物厭氧脫氯是自然環境下含氯污染物的主要分解方法,但脫氯微生物在總微生物群中占的比重較低,對含氯污染物的降解有限。2015年Mao等[53]發現微生物IET能夠促使污染物脫氯。并且添加磁鐵礦納米顆粒可以促進微生物IET脫氯反應[63],表明導電材料如磁鐵礦納米顆粒等能夠加快含氯污染物的降解。
3 展 望
微生物IET研究不僅有助于深入理解厭氧微生物互營代謝,也可為生物能源生產、溫室氣體減排以及環境修復提供技術支撐。微生物IET的核心是電子在微生物之間的傳遞,研究IET的微觀機制,發掘高效IET微生物,尋找提高微生物IET效率的方法,是將微生物IET用于實踐的重點研究方向。目前微生物IET微觀機制的研究仍處于初級階段,電子究竟如何進行傳遞、自然界中是否存在更高效的IET微生物以及是否存在更為經濟高效的方法加速微生物IET等這些問題尚待進一步明晰。地桿菌作為土壤中廣泛存在的電活性菌已有大量研究報道其胞外電子傳遞機制[64]:1)以Fe3+為電子受體的胞外電子傳遞過程中,G. sulfurreducens的細胞色素OmcS是參與胞外電子傳遞的主要蛋白[39];2)在以電極為電子受體的情況下,參與胞外電子傳遞的主要蛋白是OmcS、OmcE[40]以及OmcZ[41];3)在DIET過程中,外膜細胞色素OmcS是參與胞外電子傳遞的主要氧化還原蛋白[4]。受限于生物手段及技術水平,目前尚無法對微生物IET的電子傳遞路徑進行全程追蹤,無法明確參與IET的所有蛋白及結構。研究微生物IET微觀機制,確定參與IET的蛋白及結構,通過基因改造等手段,可提高微生物IET。2013年Leang等[65]發現,改造G.sulfurreducens的基因使其表達更多的導電菌毛,能夠提高G. sulfurreducens的產電能力。2016年Tan等[66]發現改造菌毛上的氨基酸能夠使菌毛的導電性能增強,提高胞外電子傳遞效率。此外,往IET體系中添加導電材料如活性炭等物質能夠有效的促進胞外電子傳遞。本課題組2017年Chen等[67]通過外源添加信號分子發現能夠促進微生物產電,增強生物膜電化學活性。Ye等[68]發現赤泥能夠增加混菌培養體系的導電性,促進微生物產甲烷。由于外源添加這些物質增強微生物胞外電子傳遞能力的成本較高,尋找廉價高效的微生物IET介導材料是將IET用于實際的可行方向。

