迷走神經阻滯對非氣管插管胸腔鏡手術患者咳嗽反射的影響
曹存禮,岳修勤,黃守印
(1.濮陽市人民醫院,河南 濮陽 457000;2.新鄉醫學院第一附屬醫院,河南 新鄉 453100)
胸腔鏡手術需要肺隔離術為鏡下操作提供良好視野,手術主要采用雙腔支氣管插管全麻。為減輕氣管插管以及全身麻醉并發癥,保留自主呼吸,非氣管插管麻醉(non-intubated anesthesia, NIA)開始用于胸腔鏡手術[1]。但是手術操作會誘發咳嗽反射限制了NIA的應用。目前臨床常用胸段硬膜外鎮痛、靜脈鎮靜、超聲引導下迷走神經阻滯以抑制咳嗽反射[2]。本研究擬探討超聲引導下迷走神經阻滯抑制咳嗽反射NIA胸腔鏡手術的安全性和可行性。
1 資料與方法
1.1 一般資料
選擇2016年8月—2017年12月擬在我院行胸腔鏡手術患者80例,ASA分級I~Ⅱ級,無嚴重心肺功能障礙、高血壓病、精神病史、肺結核病史,無凝血功能障礙、胃食管反流病等合并癥,體質量指數(BMI)≤24 kg/m2,手術種類有肺大泡切除術、縱膈腫瘤切除術、肺葉楔形切除術等,術前1天按隨機數字表法分為對照組(double-lumen endobronchial tube group,DLT組)和觀察組(non-intubated group,NI組)。5人退組,原因為術晨體溫>37℃、術后外科原因出血、月經來潮等,最終NI組36人,DLT組39人完成研究。本研究經本院倫理委員會審查并批準。
1.2 麻醉方法
兩組術前禁食8小時,禁飲4小時,術前30 min肌注阿托品0.01 mg/kg(最大劑量≤0.5 mg),入室后及術中監測血壓、脈搏、血氧飽和度(SPO2)、呼氣末二氧化碳分壓(end tidal carbon dioxide partial pressure,PETCO2)和腦電雙頻指數(bispectralindex,BIS),建立靜脈通道。
1.2.1 NI組患者頭偏向健側,于頸部以S-NERVE索諾聲便攜式彩超線陣高頻探頭(8~14 MHz)橫斷掃描頸動脈鞘,頸總(內)動脈和頸內靜脈間后方可見一周邊強回聲、中心低回聲圓形結構影像即迷走神經,在頸7橫突水平以2 %利多卡因3 mL行迷走神經阻滯,5 min后出現聲音嘶啞可判斷阻滯成功。側臥位后靶控輸注丙泊酚(血漿濃度1~3 μg/mL)和瑞芬太尼(血漿濃度0.5~2 ng/mL),調節瑞芬太尼速度使呼吸頻率于12~20次/min,BIS值40~60時根據手術區域在脊柱旁橫突外側約2 cm處平面內法逐根阻滯肋間神經,每次0.5 %鹽酸羅哌卡因3 mL,鹽酸羅哌卡因總劑量不超過2 mg/kg,阻滯范圍為手術切口及切口上下各一肋間。于胸壁做小切口,置入Trocar并造成醫源性氣胸,使術側肺自然塌陷。如果患者自主呼吸頻率過快則增加瑞芬太尼靶控血漿濃度,使呼吸頻率維持12~20次/min。術中患者嗆咳嚴重或SPO2低于90 %超過5 min,則改為氣管插管全身麻醉。
1.2.2 DLT組以丙泊酚2~2.5 mg/kg、舒芬太尼0.3 μg/kg、羅庫溴銨0.6 mg/kg快速麻醉誘導,可視喉鏡下插入可視雙腔支氣管導管并視頻定位,靶控輸注丙泊酚(血漿濃度3~6 μg/mL)和瑞芬太尼(血漿濃度1~4 ng/mL),使BIS值維持于40~60,血壓維持于術前±20 %,根據手術需要間斷注射羅庫溴銨。手術開始后單肺通氣,調節呼吸及參數使PETCO2維持于35~45 mmHg。
1.3 觀察指標
①術中評價指標包括滯留手術室時間、手術時間、手術開始20 min 二氧化碳分壓(PaCO2)、NI組基礎心率(HRb)和迷走神經阻滯后心率(HRvb);術后評價指標:進食時間、胸腔引流管引流量、惡心嘔吐發生率、嗎啡注射次數、住院日及麻醉滿意率。②手術開始后10 min及20 min肺塌陷分級及肺塌陷滿意率。肺塌陷滿意度分級標準見表1。
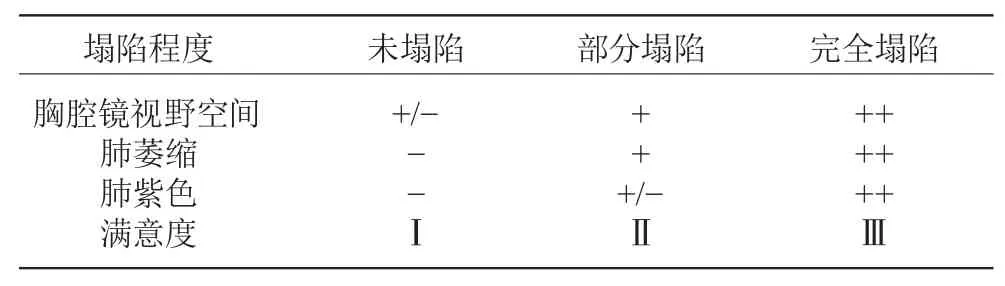
表1 肺塌陷滿意度分級
麻醉滿意評分標準[2]:1:術后無惡心嘔吐,靜息狀態和咳嗽時均不感覺疼痛;2分:術后有輕度惡心嘔吐,但不影響進食,靜息狀態不感覺疼痛,咳嗽有輕度疼痛,但可耐受;3分:術后有中度惡心嘔吐,給予止吐藥物后惡心嘔吐消失,食欲差;靜息狀態輕度疼痛,咳嗽時中度疼痛,可能需要給予鎮痛藥物;4分:術后即使給予止吐藥物仍有惡心嘔吐,無法進食;靜息狀態和咳嗽時均感疼痛,需要給予鎮痛藥物。2分及以下為麻醉滿意。
1.4 統計學方法
2 結果
2.1 一般資料
兩組年齡、性別等一般資料比較,差異無統計學意義(P>0.05),具有可比性。見表2。
2.2 術中及術后評價指標
兩組順利完成麻醉和手術,術中無低氧血癥等并發癥,NI組術中無嗆咳體動,無更改麻醉方式病例。兩組手術室滯留時間、手術時間、胸管引流量和術后住院日比較,差異無統計學意義(P>0.05);NI組基礎心率和迷走神經阻滯后心率比較,差異無統計學意義(P>0.05);NI組手術開始20 min PaCO2、麻醉滿意率顯著高于DLT組,術后惡心嘔吐發生率、嗎啡鎮痛次數顯著低于DLT組,差異有統計學意義(P<0.05)。見表3。
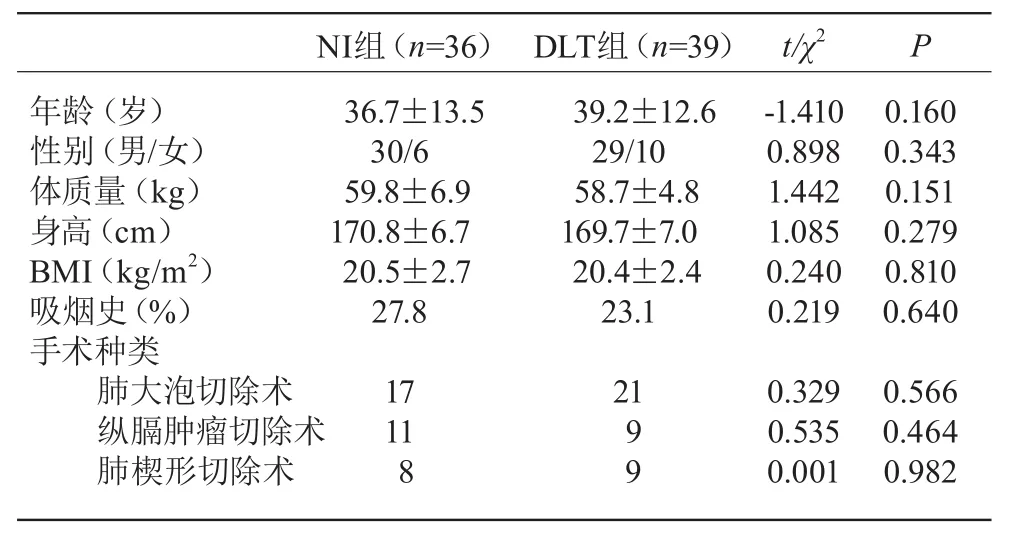
表2 兩組一般資料比較
2.3 肺塌陷分級及肺塌陷滿意率
兩組肺塌陷均能滿足手術需求,DLT組手術開始10 min及20 min肺塌陷滿意率高于NI組,差異有統計學意義(P<0.05)。見表4。
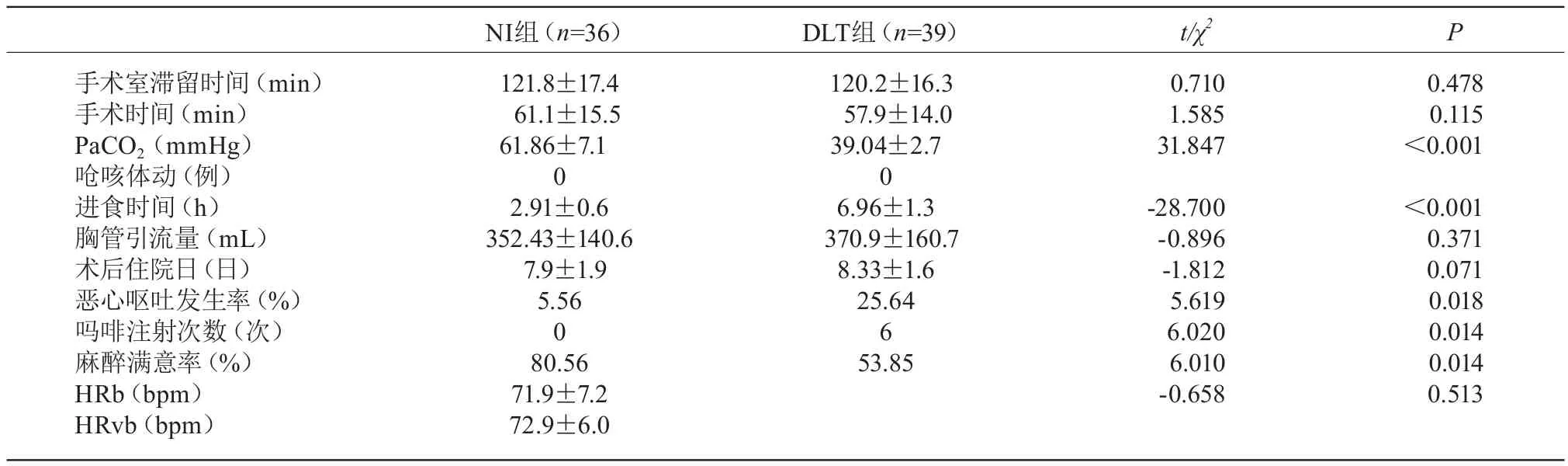
表3 兩組術中及術后結果比較
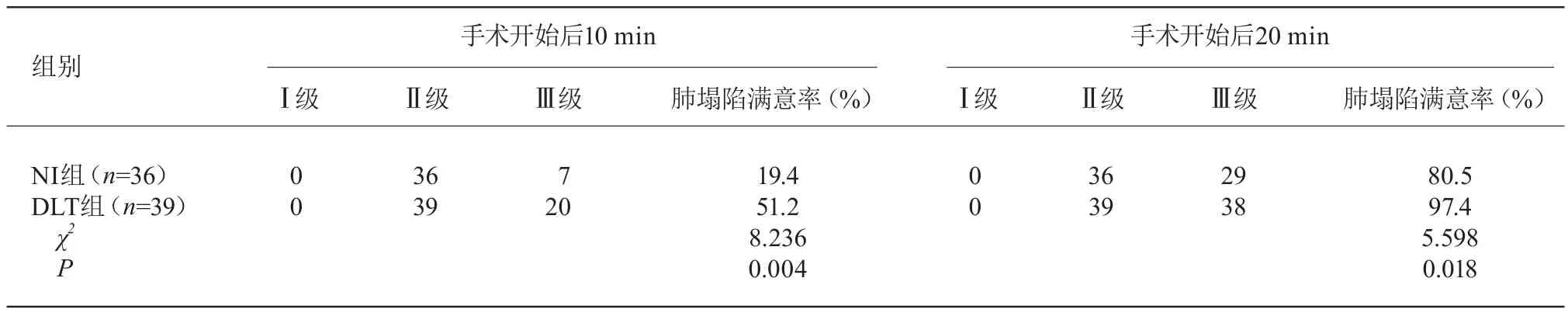
表4 肺塌陷分級及肺塌陷滿意率
3 討論
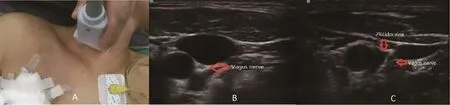
圖1 超聲引導下頸部迷走神經阻滯
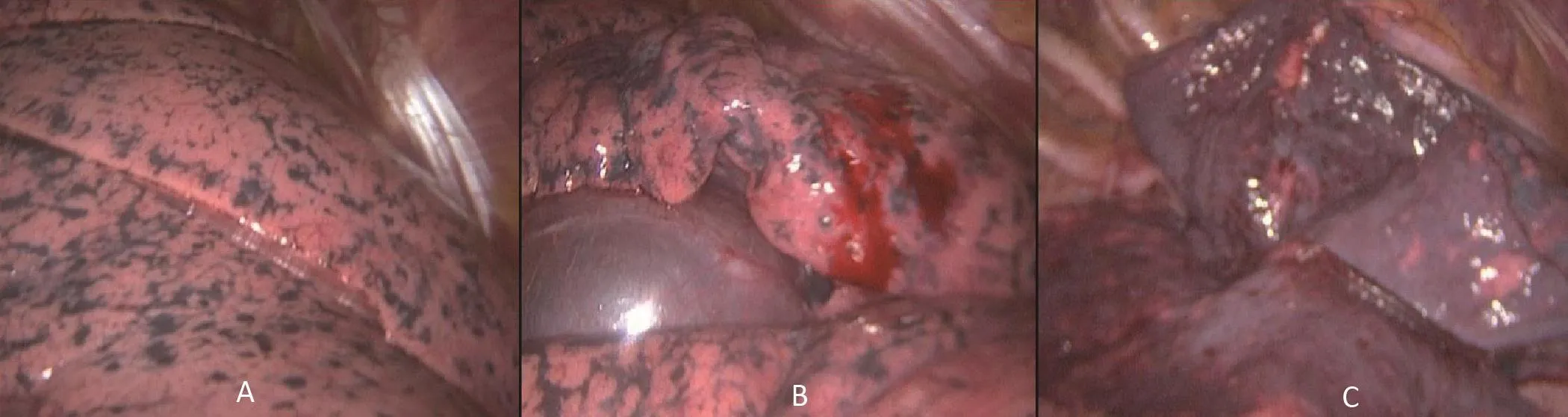
圖2 非氣管插管組患者肺塌陷情況
支氣管插管全身麻醉肺隔離通氣可使術側肺塌陷,為胸腔鏡手術提供良好鏡下視野,是此類手術廣泛應用的麻醉方式。然而支氣管插管全麻及機械通氣并發癥如術后咽痛、譫妄、認知功能障礙、肌松藥殘留、肺不張、呼吸機相關性肺損傷、惡心嘔吐、氣管支氣管損傷等較常見[3-5]。麻醉誘導期和蘇醒期患者血流動力學變化大,應激反應強,會降低自身免疫力,尤其是對于老年體弱和惡性腫瘤患者[6]。為避免以上并發癥,加速術后康復,臨床開始探索非氣管插管麻醉用于胸腔鏡手術,但是操作過程中容易引起咳嗽反射,臨床應用受到限制[7]。
自主咳嗽反射有完整的咳嗽反射弧參與完成[8],迷走神經阻滯可以阻斷咳嗽反射弧,防止嗆咳體動。頸動脈鞘起自顱底,向下延續至縱隔,迷走神經位于頸內(總)動脈與頸內靜脈間靠后,超聲圖像呈周邊高回聲、中心圓形低回聲結構,位置表淺,成像清晰[9],阻滯易于實施。阻滯后由于同時阻滯同側喉返神經而表現為聲音嘶啞,可作為阻滯成功的標志。本研究中,NI組術中未出現嗆咳體動,咳嗽反射抑制效果較好,持續時間達3~6 h,能滿足一般手術需求。與王淑珍等[10]研究不同,本研究中NI組實施迷走神經阻滯后心率未出現明顯變化,推測原因可能為阻滯位置位于頸7橫突水平,低于王淑珍等甲狀舌骨水平,從而避免阻滯迷走神經頸部心支,且可避免阻滯副神經、舌咽神經、舌下神經等及相關并發癥。
與胸段硬膜外阻滯、椎旁阻滯、豎脊肌阻滯等比較,超聲引導下肋間神經阻滯麻醉平面可控性強,持續時間長,能更好控制術后疼痛,避免導管移位、硬膜外血腫、脊髓損傷、全脊髓麻醉等并發癥[11-13],也可避免阻滯胸交感神經鏈而影響循環,使氣道反應性增加。
醫源性氣胸后,術側胸腔壓力升高,肺自然回縮力使肺逐漸塌陷,有效通氣面積減少,肺內分流增加,血氧含量下降,動脈血氧分壓降低,激活頸動脈體化學感受器,使呼吸加深加快,加劇縱隔擺動,不利于胸腔鏡下手術操作,可通過調節瑞芬太尼靶控輸注速度使呼吸頻率保持12~20次/min。然而,此措施可能加劇CO2潴留和低氧血癥,雖然允許性高碳酸血癥(PaCO2≤80 mmHg)已被證實具有肺保護作用,但也應注意監測,避免呼吸頻率過慢而過度CO2潴留,對于顱內壓升高、肺循環阻力增加和心功能不全者應謹慎[14]。
本研究中,兩組手術室滯留時間、手術時間、胸管引流量和術后住院日比較,差異無統計學意義,說明迷走神經阻滯非氣管插管麻醉能滿足胸腔鏡手術需求,雖然肺塌陷滿意率低于對照組,但均達Ⅱ級以上,能滿足手術需求。觀察組術后惡心嘔吐等并發癥少,胃腸功能恢復較快,麻醉滿意率高于對照組。
超聲引導下迷走神經阻滯可抑制非氣管插管胸腔鏡手術患者咳嗽反射,避免嗆咳體動,且可減少術后并發癥,提高麻醉滿意率,促進快速康復。

