氧空位依賴的氯氧化鉍光催化反應
楊金龍
中國科學技術大學化學與材料科學學院,合肥 230026
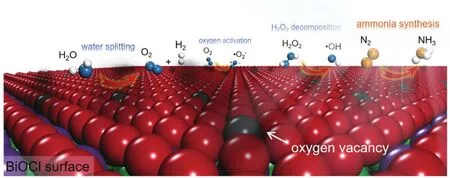
常見的小分子(O2,H2O,H2O2,N2)在BiOCl氧空位上的吸附、活化和光催化反應
隨著現代材料表征技術與理論模擬計算的協同發展,人們逐漸認識到對于實際的催化劑,其表面少量缺陷相比于其體相結構和化學組成起著更重要的作用1。鑒于此,深刻地理解表面氧空位與光催化中動力學、熱力學以及反應路徑之間的關系非常重要。其中氧空位是最常見并且研究最多的一種陰離子缺陷2。最近,華中師范大學化學學院張禮知教授研究團隊結合氧空位依賴的光催化表面化學的研究現狀及其團隊在該領域的最新研究進展,在Angewandte Chemie International Edition上撰寫了題為“Oxygen Vacancy-Mediated Photocatalysis of BiOCl: Reactivity, Selectivity and Perspective”的綜述3。
作為三元氧化物的代表物之一,BiOCl具有獨特的各向異性層狀結構。不同于其他半導體材料,BiOCl的表面結構(如特定晶面暴露和表面氧空位)不僅易于調控,還呈現出新穎的晶面相關物理化學性質和氧空位介導光催化反應過程。在分子氧活化方面,BiOCl(001)面氧空位可以通過單電子還原路徑活化氧分子到超氧負離子,并進一步通過的途徑產生其它活性氧物種;BiOCl(010)面氧空位則通過雙電子還原路徑直接活化氧分子到雙氧水。這些活性氧物種賦予了BiOCl優良的污染物氧化去除和選擇性氧化能力4–6。水分子在不同晶面的 BiOCl氧空位上會表現出不同地吸附構型,其中在 BiOCl(001)面氧空位上,水分子以分子態吸附;而在(010)面氧空位上水分子則以解離態吸附7。由于解離態吸附的水分子克服了水氧化中第一質子轉移反應H+)的能壘,進而表現出較高的活化狀態,其相比于分子態吸附的水分子更容易在熱力學和動力學上捕獲空穴。氧空位還被第一次證實為雙氧水解離吸附的活性位點,能直接誘發雙氧水中O―O鍵的異裂,產生一個占據在氧空位處的 OH-以及一個羥基自由基,而羥基自由基的存在形式與氧空位的結構息息相關8。BiOCl(001)面上的氧空位還能誘導產生游離的羥基自由基,而(010)面上的氧空位則選擇性地產生表面羥基自由基。不同存在形式的羥基自由基表現出不同的有機污染物去除特性。由于其富電子的特性,氧空位還可以有效地活化氮氣中N≡N三鍵,從而增大在其動力學上被還原的速率9。不僅如此,在BiOCl(001)面產生的氧空位上,氮分子是以“terminal end-on”模式吸附,并以“asymmetric distal,N2→ N-NH3→2NH3”的路徑被固定,產生NH3為主要產物;而在(010)面的氧空位上,氮分子則是以“side-on bridging”模式吸附,并且表現出更高的活化狀態,以“symmetric alternating,N2→ N2H2→ N2H4”的路徑被固定,產生N2H4為重要的中間產物10。
這些研究結果從表面分子層面闡述了氧空位與光催化反應的一些構效關系,鞏固并加深了半導體表面光催化的基本理論,為高效光催化劑的設計提供了新思路。
- 物理化學學報的其它文章
- Tree-Like NiS-Ni3S2/NF Heterostructure Array and Its Application in Oxygen Evolution Reaction
- CO Induced Single and Multiple Au Adatoms Trapped by Melem Self-Assembly
- Morphologies and Electronic Structures of Calcium-Doped Ceria Model Catalysts and Their Interaction with CO2
- Growth of Ordered ZnO Structures on Au(111) and Cu(111)
- In-situ APXPS and STM Study of the Activation of H2 on ZnO(1010)Surface
- Adsorption and Activation of O2 and CO on the Ni(111) Surface

