當前食品藥品復(fù)合質(zhì)量體系的特點、難點與對策
李秀梅,羅 萍,楊 帆,董曉蓉
(重慶市食品藥品檢驗檢測研究院,重慶 401121)
近年來,隨著職能的不斷擴充,藥檢機構(gòu)已由單一的藥品檢驗業(yè)務(wù)變?yōu)槎鄬W科、多領(lǐng)域檢驗。我院目前的檢驗業(yè)務(wù)有食品、藥品、化妝品、保健食品、生物制品、藥品包裝材料等,質(zhì)量管理體系也隨之不斷得到補充和完善,以適應(yīng)管理需要[1-2]。承擔食品檢驗業(yè)務(wù)尤其是接受食品職能劃轉(zhuǎn)后,由于食品檢驗和藥品檢驗在標準體系、檢驗?zāi)J健z驗量、樣品運轉(zhuǎn)流程、報告書審核流轉(zhuǎn)流程等方面存在較大差異[3-4],我院的質(zhì)量體系在運行中不斷地出現(xiàn)一些新問題[5]。現(xiàn)就我院的食品藥品復(fù)合質(zhì)量體系的特點、難點和對策進行探討。為方便表述,將我院業(yè)務(wù)范圍簡單分為食品和藥品兩大類,藥品類是指除食品之外的所有檢驗業(yè)務(wù)。
1 現(xiàn)狀及特點
1.1 食品藥品檢驗體系呈現(xiàn)新格局
資質(zhì)和檢驗量:目前,我院有資質(zhì)檢驗的相關(guān)項目為 3 553 項,其中食品 2 741 項(77.15% ),非食品(藥品、生物制品、包裝材料、化妝品、潔凈環(huán)境檢測)812項(22.85%)。我院2014年至2017年檢驗業(yè)務(wù)量中,食品檢驗量占比超過2/3。詳見表1。
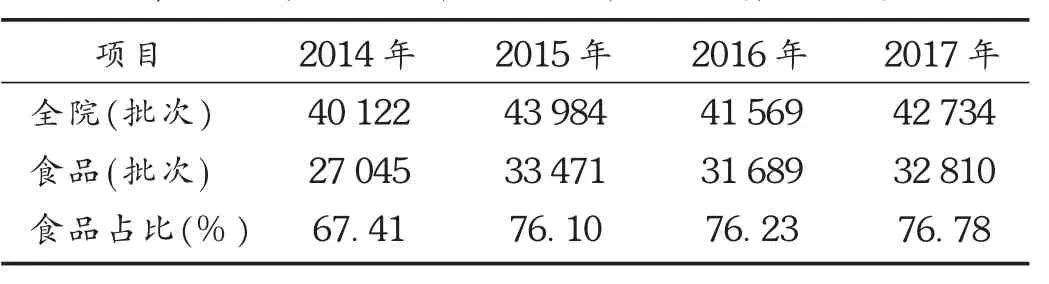
表1 我院2014年至2017年檢驗業(yè)務(wù)量組成
人員結(jié)構(gòu)特點:1)食品專用人員比例高。我院人員共325人,包括食品類檢驗專用人員133人(40.92%),藥品類檢驗專用人員129人(39.69%),共用管理人員63人(19.38%),其中食品類檢驗專用人員包括食品實驗室人員與食品業(yè)務(wù)部人員,藥品類專用人員僅指藥品類實驗室人員。2)食品實驗室人員及其中臨時聘用人員比例高。全院實驗室人員共233人,其中食品類實驗室人員 104 人(44.64%),含臨時聘用人員 59 人(56.73%)。
內(nèi)設(shè)管理機構(gòu):因食品和藥品的業(yè)務(wù)流程差異大,管理特點不同,在業(yè)務(wù)部分設(shè)食品類業(yè)務(wù)部和藥品類業(yè)務(wù)部。其中食品類業(yè)務(wù)部共29人,藥品類業(yè)務(wù)部14人,而其他管理部門(含質(zhì)管部)均共用。
1.2 食品藥品檢驗程序比較
軟件:我院目前有2個檢驗流程,一個是適用于藥品、保健食品、化妝品、藥包材等的Notes系統(tǒng),另一個是用于食品檢驗的Kingslims系統(tǒng),源自原質(zhì)檢院食品中心,增加了條碼標識,采取掃碼識別。優(yōu)點為效率較高,適用于食品業(yè)務(wù)量大的特點。
流轉(zhuǎn)記錄:藥品為電子流轉(zhuǎn)、紙質(zhì)流轉(zhuǎn)記錄2種方式并行。食品檢驗僅采取電子流轉(zhuǎn)記錄,無紙質(zhì)流轉(zhuǎn)記錄。其優(yōu)勢一是系統(tǒng)自動記錄,效率高;二是采用電子簽名的形式,每步都有痕跡,利于追溯問題源頭。
檢驗?zāi)J剑核幤吠ǔS?名主檢人承擔檢驗標準的大部分檢項,僅協(xié)檢微生物、藥理等項目。食品則采取分組、分環(huán)節(jié)方式檢驗,由報告組成員作為主檢人,將各檢項按微生物、理化、元素、氣相、液相分給各檢驗小組,各檢驗小組負責各自檢驗領(lǐng)域的項目,完成記錄,交報告組合成最終報告[3]。
審核方式:藥品原來采用檢驗人、復(fù)核、科室主任、業(yè)務(wù)部、院長5級審核,2015年起我院取消業(yè)務(wù)部審核,采取檢驗人、復(fù)核、科室審核、授權(quán)簽字人4級審核方式;授權(quán)簽字人為科室主任或院長,科室主任僅簽發(fā)合格的委托檢驗報告,其余各類報告均需院長最后簽發(fā)。食品采用檢驗人、復(fù)核、授權(quán)簽字人3級審簽?zāi)J剑瑑?yōu)點是效率高,但由于科室主任和院長可能不參與審核,存在風險隱患。
報告書打印:藥品為每份報告均打印紙質(zhì)報告。食品保存電子報告,客戶需要時才打印紙質(zhì)報告。
1.3 食品藥品標準管理體系差異[4]
藥品:院標準管理員負責標準的索取、確認、查新、錄入、歸檔,并將紙質(zhì)質(zhì)量標準掃描、編輯成PDF文檔并放局域網(wǎng)共享。電子文本定期備份并制成光盤歸檔。
食品:我院與重慶市標準化研究院簽有合同,食品類標準應(yīng)來源于其標準數(shù)據(jù)庫系統(tǒng)軟件平臺。科室標準管理員每月進行查新,院標準管理員負責與該院及科室對接。當急需使用的標準在該平臺未收錄時,檢驗科室可臨時從國家衛(wèi)生計生委、國家食品藥品監(jiān)督管理總局及國家標準委員會等機構(gòu)的官方網(wǎng)站下載。為保證標準的可控,規(guī)定了從官方網(wǎng)站下載的標準須由科室負責人、科室標準管理員、報告組組長或各專業(yè)組組長對標準的有效性進行審核確認,并加蓋“受控標準”印章。
1.4 食品標準變更頻繁
食品標準更新頻繁[4],尤其是國家衛(wèi)生計生委近期發(fā)布了大量的食品安全國家標準。根據(jù)《檢驗檢測機構(gòu)資質(zhì)認定管理辦法》對標準變更的要求,我院及時進行標準查新,并依據(jù)標準變更的性質(zhì),申請擴項評審或變更報備。僅2017年就變更報備2次,共333項。
1.5 食品擴項多
因業(yè)務(wù)發(fā)展需要或標準的實質(zhì)性變更,我院2015年至2017年先后6次共擴項730項。
2 難點[3-4]
2.1 人員文化差異大
由于我院食品檢驗及業(yè)務(wù)人員大部分是從質(zhì)檢整體劃轉(zhuǎn)的人員,文化理念有差異,缺乏歸屬感,對我院體系文件的理解和掌握不足、認同度不夠,執(zhí)行不理想。人員之間合作協(xié)調(diào)欠佳,管理難度較大。
2.2 食品參數(shù)多
由于食品參數(shù)和藥品參數(shù)的申報方式不同,造成了參數(shù)數(shù)量的很大差異。藥品類參數(shù)是按檢驗方法類別申報,故參數(shù)少,目前我院藥品參數(shù)僅146項,生物制品72項,藥包材127項。而食品參數(shù)是以一種具體的檢驗方法和檢驗標準為準,參數(shù)繁多,目前已達2 741項。食品參數(shù)數(shù)目的龐大,造成了在進行參數(shù)清理、管理、維持時,工作量很大,同時,在正確、準確選擇和使用食品參數(shù)資質(zhì)時,難度也很大。
2.3 儀器設(shè)備記錄較差
我院食品樣品量很大,食品一線的104人每年承擔3萬余批,給日常質(zhì)量管理造成了很大困難。最突出的問題是儀器設(shè)備的部分維護、使用記錄信息不完整,不利于追溯所有樣品。
2.4 標準偏離較普遍
藥品檢驗標準都是針對特定廠家的產(chǎn)品,通過嚴格的方法學驗證而制訂,產(chǎn)品標準與產(chǎn)品之間是一一對應(yīng)的關(guān)系,質(zhì)量標準較完善,基本無偏離[4]。而食品的產(chǎn)品標準是針對同類品種而制訂,不一定對每個樣品適用,因此,食品標準的適用性較差,偏離較普遍。主要偏離類型有方法使用范圍(樣品類型)及方法重復(fù)性等[4]。
2.5 報告書更改較多
在近3年的評審管理工作中發(fā)現(xiàn),食品報告存在較多的更改,2016年更改多達100余份,主要是對一般信息的更改,非結(jié)論更改。
2.6 食品復(fù)檢結(jié)論不一致較多
由于食品業(yè)務(wù)量大、不合格比例高,所受理的復(fù)驗數(shù)目較多,復(fù)驗結(jié)論不一致的情況也時有出現(xiàn)。食品管理法規(guī)定以復(fù)檢結(jié)果為最終結(jié)果,因食品復(fù)檢單位的行業(yè)分布廣,分布在食品藥品、質(zhì)檢、出入境、質(zhì)監(jiān)站等不同系統(tǒng),各機構(gòu)間的理解差異大,不易溝通協(xié)調(diào),不利于客觀、公正地探討和解決技術(shù)問題。
2.7 投訴舉報多
因全社會對食品的關(guān)注度很高,職業(yè)打假人盛行,食品檢驗遇到的投訴舉報相對較多,投訴舉報內(nèi)容主要是對資質(zhì)、標準更新、標準適用范圍等的疑問。
3 對策
3.1 加強文件制度建設(shè)
為使質(zhì)量體系能有效保證各項檢驗業(yè)務(wù)工作的規(guī)范開展,我院不斷地對質(zhì)量體系文件進行了相應(yīng)的補充、修訂和完善,共增修訂體系文件40余份。我院從管理細節(jié)上區(qū)別對待不同的檢驗領(lǐng)域,使其滿足準則要求的同時,更契合不同檢驗領(lǐng)域的特點[6-8]。
3.2 加強培訓(xùn)
為提高全院員工熟悉、掌握實驗室管理的相關(guān)規(guī)定及我院質(zhì)量管理體系知識的能力,保障我院的各項檢驗工作符合質(zhì)量管理規(guī)范,確保檢驗結(jié)果和數(shù)據(jù)的科學性與準確性,我院近年加強了質(zhì)量體系知識的培訓(xùn)。2016年對全院集中開展質(zhì)量體系知識宣傳貫徹培訓(xùn)。2017年組織開展了全院質(zhì)量體系知識競賽,競賽分筆試和現(xiàn)場搶答2種形式,均采取閉卷方式,參賽對象是質(zhì)量體系相關(guān)所有科室和人員,參賽人員比例高達90%。獲獎的59人中,質(zhì)檢劃轉(zhuǎn)人員24人,占40.68%。通過持續(xù)培訓(xùn),提高了全院人員對質(zhì)量體系及實驗室相關(guān)管理規(guī)定的掌握程度。
3.3 加強食品質(zhì)控工作
我院針對檢驗?zāi)芰Υ嬖诘谋∪醐h(huán)節(jié)和關(guān)鍵環(huán)節(jié),制訂有針對性的質(zhì)量控制計劃。要求科室強化檢驗中的隨行質(zhì)控,遇到可疑結(jié)果尤其開展新擴參數(shù)的檢驗工作時,要與外機構(gòu)進行比對;近幾年加強了參加能力驗證等外部質(zhì)控的力度,2014年至2017年參加國內(nèi)食品能力驗證80次,涉及106個參數(shù)。從2016年起開始參加了國際能力驗證,目前已取得滿意結(jié)果15次。所參加的能力驗證活動覆蓋了食品理化分析、重金屬、農(nóng)藥殘留、獸藥殘留、食品添加劑、生物毒素、營養(yǎng)成分、微生物等子領(lǐng)域。領(lǐng)域覆蓋范圍和頻次均符合國家認可委《CNAS能力驗證領(lǐng)域和頻次表》(CNAS-AL07:2015)的規(guī)定。通過加強多種形式的質(zhì)控活動,進一步鍛煉和提高了檢驗?zāi)芰Γ_保了檢驗結(jié)果的準確性。
3.4 加強日常監(jiān)督
我院針對食品實驗室日常質(zhì)量管理中存在的突出問題[5,7],針對性地加強監(jiān)督工作。加強了對儀器設(shè)備的維護,使用記錄的監(jiān)督;加強了對原始記錄的監(jiān)督等;另針對食品實驗室臨時聘用人員比例高、在培人員、實習生多的特點,加強人員監(jiān)督工作。通過強化多種形式的監(jiān)督,體系運行更加健康、良好。
3.5 及時召開專題會解決問題
針對食品藥品檢驗領(lǐng)域增多,新情況、新問題復(fù)雜性愈加凸顯等情況[6],我院及時查找原因、完善程序、制訂對策,及時召開了復(fù)驗、偏離、非標方法確認及補充檢驗方法管理等專題研討會,分析了各類問題的現(xiàn)狀和原因,明確了相應(yīng)控制程序,強調(diào)了控制難點和要點,以提高檢驗數(shù)據(jù)結(jié)果的可靠性及檢驗?zāi)芰凸芾碣|(zhì)量。
3.6 加強食品的風險管控
因食品參數(shù)多,標準變更頻繁,為避免超范圍出報告的風險,我院編制計算機軟件對參數(shù)資質(zhì)進行管理,在業(yè)務(wù)受理和實驗室出報告時,可對參數(shù)資質(zhì)進行自動識別、標注,防范風險。
食品采取的主要為電子流程和電子報告,我院加強了對其規(guī)范性管理,增加了電子簽名的授權(quán)管理、報告更改的電子庫歸檔管理,以防風險。
食品不合格率較高(3% ~4%),原有的3級審核模式僅授權(quán)簽字人審簽報告,往往科室主任、分管領(lǐng)導(dǎo)、技術(shù)負責人不知曉,風險隱患大。為確保食品報告檢驗結(jié)果的準確性、科學性,以提高復(fù)驗結(jié)論的一致性,我院規(guī)定了對食品不合格報告實行“會簽制度”。
3.7 規(guī)范控制報告更改
因食品報告更改較多,為規(guī)范食品報告更改的管理,我院修訂了報告書更改程序,對報告書更改的審批流程進行了明確要求:一般信息的更改最后必須經(jīng)檢驗室分管院長審批同意;涉及結(jié)論和數(shù)據(jù)的更改必須經(jīng)檢驗室分管院長、技術(shù)負責人及院長皆審批同意。要求對報告書更改的審批應(yīng)嚴格把關(guān),并進行重點監(jiān)督。
因我院的實驗室信息管理系統(tǒng)正在建設(shè)中,現(xiàn)有管理手段還不夠先進,制約了質(zhì)量體系管理的水平和效率。對食品藥品質(zhì)量體系管理中不斷發(fā)現(xiàn)的新問題,我們將不懈思考和研究,不斷積累經(jīng)驗和教訓(xùn),探索新思路,努力在實驗室信息管理建設(shè)中積極探索解決手段[9-10],真正做到優(yōu)質(zhì)、規(guī)范、高效。

