吡格列酮對肥胖哮喘大鼠氣道重塑的影響及與瘦素的關系
陳治宇,鄧 俊,梁宇佳,劉春鳳,王宋平△
(1.四川省自貢市第四人民醫院呼吸內科 643000;2.西南醫科大學附屬醫院呼吸內一科,四川瀘州 646000)
隨著經濟水平提高,肥胖哮喘患病人數明顯增加。ULRIK[1]研究發現,肥胖是哮喘的獨立危險因素,肥胖哮喘治療效果不佳,可進展為重癥哮喘。肥胖對哮喘的影響除了胸腹脂肪堆積引起的機械效應導致呼吸肌功能紊亂,同時也可以通過內分泌途徑分泌大量促炎因子,如瘦素、腫瘤壞死因子-α(TNF-α)、白細胞介素(IL)-6。研究顯示,瘦素可加重哮喘氣道炎癥[2],但其具體機制不明。吡格列酮是一種胰島素增敏劑,對肥胖哮喘的氣道炎癥及重構有一定抑制作用,但機制亦不明確[3]。本研究利用吡格列酮作用于內源性及外源性瘦素干預的大鼠,探討吡格列酮是否可以通過降低肺組織中瘦素水平從而抑制哮喘的氣道重構及炎癥病變,為肥胖哮喘的治療提供一種新的思路。
1 材料與方法
1.1 材料
1.1.1 實驗動物 取3~4周齡雌性SD大鼠40只,體質量(80±5) g,清潔級,由西南醫科大學中心實驗室提供,飼養于西南醫科大學動物房,恒溫25 ℃,標準無卵清蛋白飼料,自由攝食和飲水,12 h黑暗交替,實驗大鼠適應性喂養1周,1周后采用成組設計方法,將其分為空白組(A組)、肥胖哮喘組(B組)、瘦素+肥胖哮喘組(C組)、吡格列酮+瘦素+肥胖哮喘組(D組),每組10只。
1.1.2 主要實驗藥物及器材 卵清蛋白(OVA)、氫氧化鋁(美國Sigma公司),鹽酸吡格列酮片(天津武田藥品有限公司),大鼠重組瘦素(美國Prospec公司),60% kcal高脂飲食(美國Research Diets 公司),StepOneTMReal-Time PCR儀(美國Life Technologies公司),大鼠轉化生長因子-β1(TGF-β1)酶聯免疫吸附試驗(ELISA)試劑盒、大鼠基質金屬蛋白酶-9(MMP-9)及其組織抑制劑(TIMP-1)ELISA試劑盒(蘇州卡文生物科學有限公司),光學顯微鏡(日本Olympus公司)等。
1.2 方法
1.2.1 肥胖哮喘氣道模型建立 參考文獻[4]報道的方法,并加以改進制作慢性肥胖哮喘模型。B、C、D組均給予60% kcal高脂飲食喂養8周,共計19周。A組給予普通飼料喂養,自由攝水,人為控制大鼠飲食量,每周稱重,B、C、D組大鼠以體質量超過A組大鼠體質量1/3為肥胖標準,第9周起B、C、D組在0、7、14 d腹腔注射0.5 mL生理鹽水致敏液[OVA 1 mg和氫氧化鋁25 μg]致敏,第21天對B、C、D組大鼠經腹腔注射50 mg/kg戊巴比妥鈉麻醉后,經鼻滴入0.2% OVA激發,3次/周,持續8周,實驗時間共19周,A組給予相同容積生理鹽水致敏和激發,21 d起C、D組每次激發前1 h腹腔注射大鼠重組瘦素1.75 μg·g-1·d-1,溶解于0.5 mL生理鹽水中,A、B組給予相同劑量生理鹽水注射,D組每次激發前30 min給予吡格列酮10 mg·kg-1·d-1灌胃,A、B、C組給予相同容積生理鹽水灌胃。
1.2.2 標本處理和采集 實驗大鼠末次激發后24 h,戊巴比妥鈉麻醉大鼠,心臟取血3 mL,靜置離心后使用生化分析儀測定血糖,打開胸腔,分離氣管,結扎左肺門,用冷生理鹽水3 mL灌洗右肺,連續3次,每次停留30 s,收集肺泡灌洗液(BALF,回收率大于80%視為成功),以計數白細胞、中性粒細胞、嗜酸性粒細胞數量,離心后取上清液用ELISA測定干擾素γ(IFN-γ)、IL-13、8-異前列腺素F2α(8-iso-PGF2α)、TGF-β1、MMP-9、TIMP-1,取新鮮左肺上葉放入-80 ℃冰箱保存,用于實時熒光定量PCR檢測,左肺下葉用4%多聚甲醛固定、常規制備病理石蠟切片,蘇木素-伊紅(HE)、Masson染色后鏡下觀察各組肺組織上皮細胞損傷程度及膠原沉積情況,并使用Image-Pro Plus圖像分析軟件分析并測量氣道重塑(氣道壁厚度、平滑肌厚度)相關指標。
1.2.3 肺組織中瘦素、脂聯素受體、過氧化物酶體增殖物激活受體-γ(PPAR-γ)mRNA的表達 提取大鼠肺組織總RNA,采用PrimeScriptTMRT reagent Kit with gDNA Eraser合成cDNA,在StepOneTMReal-Time PCR儀上使用SYBR?Premix Ex TaqTM試劑盒完成實時熒光定量PCR,反應程序:95 ℃,1 min預變性;95 ℃ 15 s,58 ℃ 20 s,72 ℃ 45 s,40個循環,每個樣品均作3個復孔,引物均由武漢金開瑞生物工程有限公司合成。實驗后觀察PCR熔解曲線確定擴增產物的特異性,引物序列見表1。

表1 實時免疫熒光檢測引物序列

2 結 果
2.1 各組大鼠體質量及血糖的變化 實驗開始時各組大鼠體質量相當,高脂飲食喂養9周后,B、C、D組較A組小鼠體質量增加,差異有統計學意義(P<0.01),隨著喂養時間延長體質量亦增加,造模結束時B、C、D組體質量均較A組增加約1/3,肥胖大鼠造模成功。4組小鼠血糖水平比較,差異有統計學意義(P<0.01),D組血糖(Glu)較C組降低,差異有統計學意義(P<0.01),見表2。
2.2 支氣管BALF中細胞計數及肺組織病理改變 C組BALF中白細胞、中性粒細胞計數較A、B組明顯升高,差異有統計學意義(P<0.05),見表3。HE染色A組鏡檢示氣道上皮排列較整齊,管腔光滑,未見炎性細胞浸潤,B、C、D組氣道上皮均可見炎性細胞浸潤及氣道上皮腫脹、斷裂,管腔可見明顯黏液分泌,其中C組較B組明顯,D組上皮細胞破壞情況較C組有所改善(圖1)。Masson染色鏡檢氣道上皮可見A組氣管腔光滑,氣道上皮有少許膠原沉積,B、C、D組均可見較多膠原沉積,其中C組沉積量最多,D組較C組沉積量有所減少(圖2)。

表2 不同組大鼠體質量及Glu水平比較
*:P<0.01,與A組比較;#:P<0.01,與B組比較;△:P<0.01,與C組比較

表3 不同組大鼠支氣管BALF中細胞計數
*:P<0.05,與A組比較;#:P<0.05,與B組比較;△:P<0.05,與C組比較

A:A組;B:B組;C:C組;D:D組
圖1各組大鼠肺組織HE染色(×100)
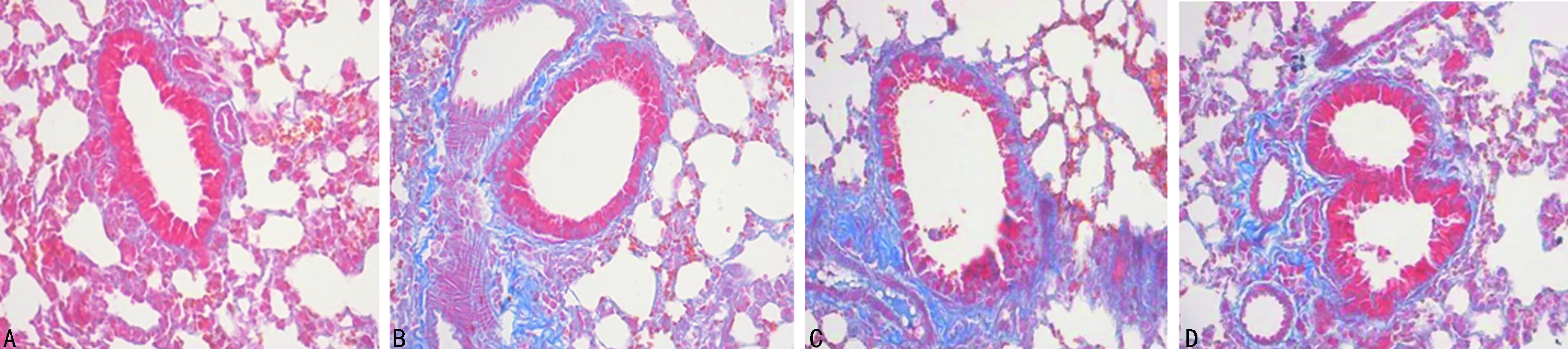
A:A組;B:B組;C:C組;D:D組
圖2各組大鼠肺組織Masson染色(×100)
2.3 氣道的形態學改變 在大鼠的支氣管壁厚度測量中,B、C、D組較A組明顯增厚,且C組較B組亦明顯增厚,D組經吡格列酮干預后氣道壁厚度較C組減小,差異有統計學意義(P<0.05);氣管平滑肌厚度變化趨勢與支氣管壁厚度變化趨勢大致相同(P<0.05),見表4。

表4 不同組大鼠氣道壁厚度及平滑肌厚度比較
*:P<0.05,與A組比較;#:P<0.05,與B組比較;△:P<0.05,與C組比較
2.4 各組大鼠BALF中IFN-γ、IL-13、8-iso-PGF2α、TGF-β1、MMP-9及TIMP-1水平比較 在BALF中,C組IFN-γ、8-iso-PGF2水平較A、B組升高,D組較C組降低,差異均有統計學意義(P<0.05);C組IL-13水平較B組降低,D組經吡格列酮干預IL-13水平升高,差異有統計學意義(P<0.05),見表5。B、C、D組TGF-β1、MMP-9及TIMP-1水平較A組明顯升高,C組TGF-β1、MMP-9及TIMP-1水平較B組升高,D組TGF-β1、MMP-9及TIMP-1水平較C組降低,差異有統計學意義(P<0.05),見表6。

表5 各組大鼠BALF中IFN-γ、IL-13及8-iso-PGF2
*:P<0.05,與A組比較;#:P<0.05,與B組比較;△:P<0.05,與C組比較
2.5 肺組織中瘦素、脂聯素受體及PPAR-γ mRNA表達水平比較 瘦素mRNA在C組表達水平最高,明顯高于A、B組,D組瘦素mRNA表達水平較C組降低,差異均有統計學意義(P<0.05)。C組脂聯素受體1、2的mRNA表達水平均低于B、D組,差異均有統計學意義(P<0.05)。D組PPAR-γ mRNA表達水平較C組升高,差異有統計學意義(P<0.05),見表7。

表6 各組大鼠BALF中TGF-β1 、MMP-9及TIMP-1
*:P<0.05,與A組比較;#:P<0.05,與B組比較;△:P<0.05,與C組比較

表7 各組大鼠肺組織瘦素、脂聯素受體及PPAR-γ mRNA
*:P<0.05,與A組比較;#:P<0.05,與B組比較;△:P<0.05,與C組比較
3 討 論
肥胖引起哮喘加重的原因除了胸腹脂肪堆積引起呼吸肌功能障礙的機械性因素,還存在內分泌因素的參與,脂肪組織具有內分泌功能,可分泌瘦素、TNF-α等促炎因子,也可分泌脂聯素、PPAR-γ等抗炎因子[5-6]。研究顯示,肥胖哮喘急性發作時血清瘦素水平明顯升高[7],可以推測肥胖哮喘與體內瘦素水平之間存在一定聯系[8]。肥胖哮喘主要以氣道黏液分泌過多、氣道重塑病變為主,易導致氣道受限進行加重,激素治療不佳。
吡格列酮是PPAR-γ受體激動劑,是胰島素增敏劑,主要機制是與脂肪細胞PPAR-γ受體結合增加體內組織對胰島素的敏感性。研究發現PPAR-γ廣泛表達于氣道上皮細胞、巨噬細胞、T淋巴細胞等,PPAR-γ受體激動劑對哮喘的氣道炎癥有一定的抑制作用,已知的機制可能參與調解脂聯素/絲裂原活化蛋白激酶(Adipo/MAPK)通路,以及與上調Adipo水平及抑制核因子-κB(NF-κB)等因子相關[9-10]。此外,研究發現吡格列酮在血管平滑肌中可抑制瘦素表達,從而抑制血管平滑肌增殖達到抗動脈粥樣硬化的作用[11-12]。TGF-β1是一種促纖維化因子,主要促進細胞外基質的產生及抑制其降解,基質金屬蛋白酶類(MMPs)是一類可降解細胞外基質的蛋白酶,作用于肺組織中Ⅳ型膠原纖維,而TIMP-1可以抑制MMP-9產生,促進細胞外基質的膠原沉積,促進氣道重塑進展,氣道中MMP-9、TIMP-1水平升高可提示氣道重塑的發生[11]。
本實驗利用高脂飲食、OVA建立肥胖哮喘模型,并加用PPAR-γ激動劑吡格列酮干預,實驗結果顯示,肥胖哮喘組Glu水平明顯升高,符合BOLINDER等[12]關于肥胖可引起Glu升高的研究,吡格列酮干預組大鼠Glu有所降低,其中機制可能是吡格列酮通過增加機體對胰島素的敏感性降低血糖[13],內外源性瘦素共同作用的C組支氣管壁及平滑肌厚度,TGF-β1、MMP-9、TIMP-1水平明顯高于A、B組,說明肥胖哮喘引起氣道重塑可能與瘦素相關,瘦素水平越高,氣道重塑程度越嚴重,與SINGH等[14]研究結果一致;經吡格列酮干預后D組氣道上皮破壞程度、氣道重塑程度、TGF-β1、MMP-9 、TIMP-1水平較C組降低,且肺組織中PPAR-γ、脂聯素受體1、2 mRNA表達水平較C組明顯升高,而D組瘦素mRNA表達水平較C組降低,提示吡格列酮可以通過抑制肺組織中瘦素表達及上調脂聯素的表達,進而降低肥胖哮喘大鼠氣道相關促纖維化及促炎因子水平,達到抑制肥胖哮喘氣道重塑及炎癥病變的作用。
瘦素是白色脂肪組織分泌的蛋白,被發現廣泛表達于氣道上皮細胞、Ⅱ型肺泡上皮細胞、巨噬細胞。研究中發現,肥胖哮喘模型中瘦素水平較單純肥胖組高,單純肥胖組較空白組瘦素水平升高,表明肥胖促進體內瘦素水平升高,哮喘炎癥使肥胖模型組瘦素水平更高[15]。本實驗發現,B組中氣道重塑及炎癥程度較A組明顯升高,且瘦素mRNA表達水平升高,說明肥胖哮喘氣道重塑和炎癥加重與瘦素水平上調相關,與ZHENG等[16]研究結果一致;而在SUTHERLAND[17]的研究中發現,單純肥胖小鼠體內瘦素水平升高,但氣道炎性病變較正常組無明顯變化,考慮瘦素不是哮喘的始發因素,而是與哮喘氣道炎癥相互促進。本研究結果顯示,C、B組BALF中炎性細胞以中性粒細胞計數升高為主,可以推測瘦素升高可促進氣道內中性粒細胞增加,與普通型哮喘氣道內嗜酸性粒細胞為主不同,解釋了肥胖哮喘對激素的抵抗作用。IFN-γ由輔助性T淋巴細胞1(Th1)分泌,促使初始T淋巴細胞(Th0)向Th1分化,而IL-13由輔助性T淋巴細胞2(Th2)分泌,有募集氣道內嗜酸性粒細胞的作用。LEIRIA等[18]研究顯示,普通哮喘氣道內主要是Th1/Th2細胞因子調節失衡,以Th2偏移為主;而本次實驗中發現,肥胖哮喘大鼠氣道內IFN-γ水平明顯升高,IL-13水平降低,加用外源性瘦素后更加明顯,說明瘦素引起肥胖哮喘模型氣道重構與Th1優勢表達相關,而吡格列酮干預后可以同時降低IFN-γ、IL-13水平,以IFN-γ水平降低明顯,說明吡格列酮可以通過抑制Th1表達,促進Th1/Th2細胞因子平衡,抑制哮喘氣道重構及炎癥病變。8-iso-PGF2是氧化應激反應重要的細胞因子,本實驗發現經吡格列酮干預后,氣道內8-iso-PGF2水平和瘦素mRNA水平下降,提示吡格列酮抑制氣道內瘦素表達與降低氣道內氧化應激水平相關。
綜上所述,本實驗證實吡格列酮通過上調肥胖哮喘大鼠肺組織中PPAR-γ水平,抑制肺組織中瘦素表達,達到改善肥胖哮喘大鼠氣道重塑及氣道炎癥病變程度的作用,其機制可能是通過降低肥胖哮喘大鼠肺組織中氧化應激水平,改善Th1/Th2細胞因子偏移,降低促肺纖維化因子水平、上調氣道內脂聯素水平,為肥胖哮喘的藥物治療提供了新的方向。

