視網膜光凝對糖尿病視網膜病變患者神經纖維層厚度的影響
張 暢,賈洪強,楊棟梁
0引言
糖尿病視網膜病變(diabetic retinopathy,DR)是主要的不可逆盲眼病之一,2010年我國成年人糖尿病(diabetes mellitus,DM)患病率為9.7%(約9 240萬人),糖尿病前期患病率為15.5%(約1.5億人)[1]。研究證實DR不僅僅是視網膜微血管病變,也是一種神經退行性病變[2]。全視網膜激光光凝術(panretinal photocoagulation,PRP)是控制DR進展、阻止視力進一步喪失的常用治療方法,但PRP可導致視網膜神經纖維層(retinal nerve fiber layer,RNFL)厚度的降低[3]。文獻報道大多是PRP術后1~6mo觀察的RNFL厚度變化[4-5],對于PRP術后1a的RNFL厚度變化未見報道。本研究通過OCT測量DR患者PRP術前和術后1a的RNFL厚度,探討分析PRP治療對視盤周圍RNFL厚度的影響,現將結果報告如下。


時間上方下方鼻側顳側全周平均厚度術前124.54±18.03121.77±18.5274.86±16.7174.71±18.5896.48±12.43術后1wk125.98±15.43131.23±15.9675.33±18.6282.39±18.46103.16±9.98術后4wk131.40±10.68140.58±16.1576.46±18.4393.09±18.92110.33±11.08術后6mo118.80±17.36103.32±19.9362.40±13.2469.75±12.9286.54±21.44術后12mo106.67±17.34105.28±23.2762.38±12.9965.22±15.2787.57±18.09F35.22567.78420.75835.72540.497P<0.001<0.001<0.001<0.001<0.001
1對象和方法
1.1對象選取2014-05/2017-06在我院行PRP治療的92例92眼DR患者,其中男46例46眼,女46例46眼,年齡54~73歲,糖尿病病程1~19a。納入標準:血糖均控制穩定,眼壓<21mmHg,眼部未接受過其他手術或激光治療。考慮到RNFL厚度的性別、年齡差異變化,本研究中患者男女例數相同、年齡相當;患者眼底符合DR國際臨床分類法標準且需行PRP治療。排除標準:嚴重白內障、病理性近視、玻璃體積血、彌漫性黃斑水腫、視盤或周圍新生血管及其他視網膜病變。本研究經醫院倫理委員會批準同意,PRP治療前均告知患者或其家屬研究方法和目的,自愿接受治療檢查并簽署知情同意書。所有患者依從性好,均觀察單眼的RNFL厚度變化,且均行視力、眼壓、裂隙燈和眼底檢查。
1.2方法
2.3.1 經常通風。長期靜止封閉狀態下,車內的各種有害物質含量比較高,若為新車,則含量更高,汽車剛啟動時打開車窗通風會比較好,汽車行駛時選擇空調外循環則比較好。特別是剛購買的新車更應該經常通風,即使不使用也需要經常通風換氣。
1.2.1PRP治療方法應用Nidek MC500多波長激光機,波長532nm,能量250~350mW,黃斑血管弓附近后極部光斑直徑200μm,中周邊部300μm,曝光時間0.2s,光斑強度Ⅲ級。每位患者分4次完成PRP,首先光凝范圍為后極部視網膜,其余中周部均分3次完成,每次治療光斑數400~500點,根據眼底病變嚴重程度,光凝范圍為距視盤周圍1~1.5PD以外區域,顳側上、下血管弓及黃斑中心凹顳側2PD以外區域,2個光斑間隔為0.5~1個光斑直徑。局限性黃斑水腫行“C”形光凝,光斑直徑50μm,曝光時間0.1s,淺Ⅱ級光斑。7d后檢查裸眼和最佳矯正視力并進行下一次治療。所有患者PRP全部完成后1、4wk,3、6、12mo隨訪視力、眼壓和眼底檢查,PRP后3mo行FFA檢查,適時補充光凝,PRP治療均由同一位操作熟練且經驗豐富的醫師完成。
1.2.2OCT檢查方法采用RS-3000型OCT的DISC CIRCLE程序,測量分析以視盤為中心、直徑3.45mm范圍DR患者光凝術前和術后1a(采用Follow-Up程序自動追蹤模式)視盤周圍RNFL厚度,按上方(S)、下方(I)、鼻側(N)、顳側(T)4個象限掃描顯示并分析。每位患者均重復掃描5次,選擇其中最高信號強度的三幅圖像保存并進行數據處理。獲取各個象限和全周RNFL平均厚度值。所有患者檢查前均充分散大瞳孔,OCT均由同一位經驗豐富的技術員完成。
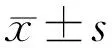
2結果
DR患者PRP術后視盤各象限RNFL厚度變化結果:(1)上方:手術前后不同時間點的RNFL厚度比較,差異有統計學意義(P<0.001)。與術前比較,術后1wk時RNFL厚度未見明顯變化,差異無統計學意義(P>0.05);術后4wk時RNFL厚度增厚,差異有統計學意義(P<0.05),而術后6、12mo厚度呈逐漸變薄趨勢,差異有統計學意義(均P<0.05);(2)下方:手術前后不同時間點的RNFL厚度比較,差異有統計學意義(P<0.001)。與術前比較,術后1、4wk時RNFL厚度增厚,術后4wk時厚度最厚,差異有統計學意義(P<0.05);術后6、12mo厚度明顯變薄,差異有統計學意義(均P<0.05);術后6mo和12mo厚度變薄趨勢比較,差異無統計學意義(P>0.05);(3)鼻側:手術前后不同時間點的RNFL厚度比較,差異有統計學意義(P<0.001)。與術前比較,術后1、4wk時RNFL厚度無明顯變化,差異無統計學意義(均P>0.05),而術后6、12mo厚度明顯變薄,差異有統計學意義(均P<0.05);術后6mo和12mo厚度變薄趨勢比較,差異無統計學意義(P>0.05);(4)顳側:手術前后不同時間點的RNFL厚度比較,差異有統計學意義(P<0.001)。與術前比較,術后1、4wk時RNFL厚度增厚,4wk時厚度最厚,差異有統計學意義(P<0.05);而術后6、12mo厚度明顯變薄,差異有統計學意義(均P<0.05);術后6mo和12mo厚度變薄趨勢比較,差異無統計學意義(P>0.05)。(5)全周平均RNFL厚度:手術前后不同時間點的RNFL厚度比較,差異有統計學意義(P<0.001)。與術前比較,術后1、4wk時RNFL厚度增厚,4wk時厚度最厚,差異有統計學意義(P<0.05);術后6、12mo厚度明顯變薄,差異有統計學意義(均P<0.05);術后6mo和12mo厚度變薄趨勢比較,差異無統計學意義(P>0.05),見表1。
3討論
近年來我國糖尿病患者呈逐年上升趨勢,DR是糖尿病在眼科最常見的以微血管改變為主要特征的致盲性并發癥。PRP是目前阻止DR進展、防止失明的最為有效和重要的手段,可使視力喪失的風險降低50%[6],其主要機制是破壞視網膜色素上皮細胞和光感受器復合體,降低細胞的高耗氧量,使組織發生瘢痕化,脈絡膜微血管的氧和營養物質便于擴散到視網膜,使視網膜缺血、缺氧狀態得以改善,減少VEGF因子的產生,抑制新生血管形成,從而減少DR的并發癥,達到阻止病變進展的目的。研究中我們選用的多波長532nm激光、Ⅲ級光斑,治療作用部位在視網膜色素上皮層和脈絡膜毛細血管淺層,主要由該層黑色素細胞吸收,葉黃素吸收少。光凝后視網膜脈絡膜廣泛形成粘連瘢痕,改善了視網膜供氧,有效地阻止了視網膜微血管病變的進展。但PRP治療在有效阻止DR進展的同時亦具有一定的損傷性,RNFL可發生損害出現厚度變化。有作者報道[7],PRP治療后4wk內,RNFL厚度較治療前增厚,治療6mo后RNFL厚度較治療前降低,但目前未見更長期的報道,由此我們可以看出,PRP治療不可避免地對視網膜組織造成一定的損傷,在阻止DR微血管病變進展的同時,如何減輕和保護視網膜神經細胞的功能,術后RNFL厚度監測有著同樣重要的臨床意義。
隨著OCT技術的發展,其分辨率和掃描速度進一步提高,使視盤周圍RNFL測量更為精確。視覺傳導功能依賴于視網膜神經纖維的多少,RNFL的組成主要是神經節細胞的軸突,其數量又決定了RNFL厚度[8],是反映視細胞和視覺傳導功能的重要指標,各種致病因素導致的神經細胞機能障礙或軸突軸漿流改變均可造成RNFL厚度改變。
本研究中DR患者PRP術后與術前比較,術后4wk時視盤上方、下方、顳側和全周RNFL 平均厚度增加,術后6、12mo與術前比較,視盤各象限和全周RNFL平均厚度均變薄,且變薄趨勢無明顯變化,差異均有統計學意義(P<0.05),這些改變可能與視盤周圍神經纖維走形密集、損傷后容易發生改變有關。我們考慮視盤周圍RNFL的損傷可能與兩個方面有關:(1)光凝術中的熱損傷:激光斑區域溫度可以達到40℃~60℃,這種熱能可損傷視網膜全層[9-10],神經節細胞軸突在PRP后亦可產生損傷,最終造成視網膜神經節細胞的永久損害。另外532nm波長激光主要被視網膜色素上皮層和脈絡膜的黑色素細胞吸收,Ⅲ級光斑主要作用于視網膜內核層,光凝所產生的熱損傷造成光斑周圍組織溫度亦升高,導致其非選擇性的損害。視網膜毛細血管中血紅蛋白吸收熱能后,局部組織微循環血管受損阻塞,從而加重了視網膜組織的缺血、缺氧狀態,進一步促使神經節細胞和Müller細胞等的凋亡增加,最終出現視盤周圍RNFL厚度變薄。(2)糖尿病患者發生的神經退行性病變:文獻報道糖尿病患者在患病早期甚至眼底未發生血管改變之前RNFL厚度已降低[11]。隨著病程的延長和血糖波動,視網膜神經退行性病變加重,視網膜神經細胞凋亡更加顯著。各種致病因素導致的神經細胞機能障礙或神經節細胞軸突萎縮,進而造成RNFL厚度呈逐漸下降的趨勢。另外視網膜神經細胞分泌的多種生長因子(如胰島素、VEGF、PEDF、神經生長因子等)具有一定的神經保護作用[12],使視網膜神經細胞的凋亡減少。光凝造成的視網膜神經細胞損傷,使生長因子分泌減少,進一步導致神經退行性病變加重。有研究表明PDR患者PRP前后VEGF等因子降低[13]。在本研究中可以看出,PRP術后4wk時RNFL厚度增加明顯與光凝術中的熱損傷相關,而在術后6~12mo后由于各種因素的作用最終導致RNFL厚度呈現變薄的趨勢。但本研究中未觀察比較DR作為一種神經退行性病變而造成的RNFL厚度變化對激光治療的干擾,今后仍需進一步大樣本以相應年齡、病程、分期等因素分組觀察行激光治療與未行激光治療的DR患者,在相同時間點測量視盤周圍RNFL厚度變化規律。
因此DR發生的視網膜神經細胞病變和PRP對RNFL的損傷應得到充分重視,如何能夠更好地保護視網膜神經細胞的機能對DR治療具有重要意義。對于糖尿病患者,在嚴格控制血糖、血壓、血脂等全身狀況穩定的前提下,定期檢查眼底,按DR的不同分期,在光凝治療過程(尤其是PRP)中應充分考慮RNFL的損傷,避免光凝過度導致視網膜神經組織發生不必要的損傷。選擇適當的光凝能量、光斑大小和曝光時間,適當延長每次治療間隔,以利于減輕視網膜的慢性炎癥反應和視網膜神經細胞損傷的修復,在有效的治療和控制DR的同時,最大程度地減少PRP對RNFL的損傷,降低DR患者視覺功能喪失的發生率。

