靜電紡絲制備聚乙烯醇/納米纖維素復(fù)合纖維及以其作載體的釋藥性能
,,,,
(1. 福建工程學(xué)院 材料科學(xué)與工程學(xué)院,福建 福州 350118; 2.高分子材料及制品福建省高校重點(diǎn)實(shí)驗(yàn)室,福建 福州 350118)
1 前 言
藥物釋放體系使用過(guò)程中藥物釋放的高效性和安全性等問(wèn)題已成為研究者關(guān)注的熱點(diǎn)。其中高分子聚合物或脂質(zhì)體作為藥物釋放體系在臨床試驗(yàn)上已被廣泛使用[1]。高分子材料在藥物釋放體系中具有重要地位,這是由于脂質(zhì)體藥物釋放體系結(jié)構(gòu)不穩(wěn)定,而高分子藥物釋放體系具有結(jié)構(gòu)可控性?xún)?yōu)點(diǎn)。根據(jù)劑型結(jié)構(gòu)的不同, 高分子藥物釋放體系可分為微膠囊、微粒或納米粒、電紡納米纖維以及水凝膠等。由于靜電紡絲技術(shù)設(shè)備操作方便,可利用的材料種類(lèi)繁多,易制備復(fù)合纖維支架,且能夠通過(guò)簡(jiǎn)單的改變其工藝參數(shù)、材料組成等方法達(dá)到控制藥物釋放速率和藥物釋放量的目的,使靜電紡絲技術(shù)作為一種簡(jiǎn)單制備納米纖維藥物釋放體系的方法而被研究者們廣泛關(guān)注[2-6]。
纖維素是一種含量豐富的可再生天然高分子材料,可以從植物和動(dòng)物中獲取,同時(shí)采用纖維素在酸中水解可以獲得NC。由于NC具有較高的比表面積和結(jié)晶度,較低的成本,優(yōu)良的機(jī)械性能,良好的生物降解性和生物相容性等優(yōu)點(diǎn),使其已經(jīng)廣泛應(yīng)用于生物、醫(yī)學(xué)、食品等領(lǐng)域[7-8]。但由于NC分子中氫鍵的大量存在,使得NC較難溶于普通溶劑,不能單獨(dú)采用靜電紡絲技術(shù)制備纖維。PVA是一種無(wú)味,無(wú)毒且具有良好成纖能力的水溶性高分子材料[9]。但由于其具有較高的親水性能,使制備獲得的PVA藥物載體具有較快的藥物釋放速率。為了在提高NC可紡性的同時(shí),降低PVA的親水性能,達(dá)到降低藥物載體的藥物釋放速率的目的,本文采用靜電紡絲技術(shù)制備PVA/NC、PVA/NC/氨芐西林鈉復(fù)合纖維, 研究藥物含量、材料配比對(duì)復(fù)合纖維形態(tài)、親水性能和藥物釋放速率的影響。
2 實(shí) 驗(yàn)
2.1 原料
PVA粉末(型號(hào)2488,醇解度88%);NC(型號(hào)LY100),其直徑為100~200nm,長(zhǎng)度為100~500nm。磷酸緩沖鹽(PBS)粉末;氨芐西林鈉粉末。
2.2 靜電紡絲溶液的配制
首先,將0.06g NC放入30mL去離子水,超聲震蕩30min后獲得0.2%(w/v,g/mL)NC均勻懸浮溶液;其次,稱(chēng)取2g PVA溶于20mL去離子水,在80℃恒溫水浴中攪拌6h,得到10%(w/v)的PVA均勻紡絲液;最后,將10% PVA與0.2% NC溶液分別以體積比為9/1、8/2、7/3的配比振蕩混合,得到不同材料配比的PVA/NC均勻混合紡絲液;另外,稱(chēng)取不同量的氨芐西林鈉加入體積比為8/2的PVA/NC混合紡絲液振蕩2h,分別制得藥物質(zhì)量分?jǐn)?shù)為0.5%、1%和2%(w藥物/wPVA/NC)的載藥混合溶液。
2.3 復(fù)合纖維的制備
首先,將5mL均勻紡絲溶液裝入注射器內(nèi),將其安裝在SN-50微量注射泵上,注射器出口連接內(nèi)徑為0.8mm的針頭;其次,采用聚四氟乙烯管將注射器內(nèi)的紡絲液連接到紡絲針頭,且其連接高壓發(fā)生裝置;最后采用鋁箔紙覆蓋的接地平板電極作為纖維的接收裝置。注射器的進(jìn)給速度為0.3mL/h。為了研究紡絲電壓和收集距離對(duì)PVA/NC復(fù)合纖維形態(tài)的影響,本文電壓分別取10、14和18kV,收集距離分別取10、13和15cm。紡絲針頭為23G(外徑=0.6mm、內(nèi)徑=0.3mm),紡絲溫度控制為50℃。相對(duì)濕度為40%左右。
2.4 復(fù)合纖維的微觀(guān)形貌分析
利用S-3400N型SEM觀(guān)察復(fù)合纖維表面形態(tài),電子束電壓為5kV,觀(guān)察前樣品噴金處理40s。采用Nano Measure圖片處理軟件統(tǒng)計(jì)復(fù)合纖維直徑分布和平均直徑。
2.5 復(fù)合纖維親水性測(cè)試
采用SL200B型接觸角測(cè)試儀測(cè)定PVA/NC復(fù)合纖維表面潤(rùn)濕性能(親水性)。利用30μL去離子水液滴進(jìn)行測(cè)量,當(dāng)液滴滴落到復(fù)合纖維表面并穩(wěn)定后采用高速攝像機(jī)進(jìn)行拍攝,并通過(guò)軟件計(jì)算出其接觸角數(shù)值。每個(gè)樣品測(cè)試5次,求其平均值。
2.6 藥物釋放實(shí)驗(yàn)
利用一定量的去離子水溶解PBS粉末,將其配制為濃度0.1mol/L,PH 7.4的緩沖溶液;分別稱(chēng)量一定量的氨芐西林鈉溶于上述PBS溶液,分別配制藥物含量為1.6、3.2、6.4、8.0、12.8μg/mL的氨芐西林鈉標(biāo)定溶液,在氨芐西林鈉最大吸收波長(zhǎng)209nm處測(cè)定其吸光度,繪制標(biāo)準(zhǔn)曲線(xiàn)。
取不同藥物含量的PVA/NC/氨芐西林鈉復(fù)合纖維,裁剪成1×1cm試樣,并測(cè)量其質(zhì)量W0,分別置于裝有10mL PBS溶液的玻璃瓶?jī)?nèi),將其放于37℃恒溫培養(yǎng)箱內(nèi),在規(guī)定的時(shí)間內(nèi)取出10mL釋放液,并加入等量的PBS緩沖液繼續(xù)釋放藥物,用紫外分光光度計(jì)在209nm波長(zhǎng)處測(cè)試釋放液的吸光度。利用藥物標(biāo)準(zhǔn)曲線(xiàn)方程計(jì)算藥物釋放濃度及釋藥量,并計(jì)算累計(jì)釋藥百分率并作累計(jì)釋藥曲線(xiàn)。同時(shí),通過(guò)復(fù)合纖維累計(jì)釋放的總藥量W藥和復(fù)合纖維質(zhì)量W0,計(jì)算復(fù)合纖維實(shí)際載藥量。
3 結(jié)果與分析
3.1 材料配比對(duì)復(fù)合纖維形態(tài)的影響
圖1是不同材料配比下PVA/NC復(fù)合纖維的SEM形貌圖和直徑分布圖。由圖可知,三種配比下均獲得了形態(tài)良好的復(fù)合纖維,其直徑分布范圍為100~400nm,均勻性良好。隨著NC含量降低,復(fù)合纖維直徑分布的均勻性降低,且平均直徑增加。這是由于隨著NC含量的降低,混合溶液黏度增加,使溶液射流在電場(chǎng)中的分化能力降低,導(dǎo)致其在電場(chǎng)力的作用下較難被完全拉伸,從而復(fù)合纖維平均直徑增加,直徑分布均勻性降低[10]。本文采用NDJ數(shù)顯黏度計(jì)分別測(cè)得10% PVA及PVA/NC為9∶1、8∶2、7∶3的混合溶液黏度為245、221、213和196mPa·S。
3.2 紡絲電壓對(duì)復(fù)合纖維形態(tài)的影響
圖2給出了不同電壓下制備的PVA/NC復(fù)合纖維SEM圖和直徑分布圖。由圖可知,隨著紡絲電壓的升高,PVA/NC復(fù)合纖維直徑分布的均勻性提高,且平均直徑降低。這主要是由于紡絲電壓的升高導(dǎo)致高分子溶液射流表面的電荷密度增大,同時(shí)電荷之間的相互排斥力增強(qiáng)使纖維易于分化,從而使復(fù)合纖維直徑降低[11]。
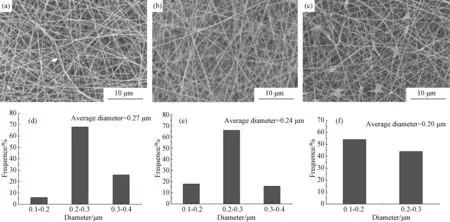
圖1 不同材料配比下PVA/NC復(fù)合纖維SEM形貌圖(a,b,c)和相應(yīng)的直徑分布圖(d,e,f)[PVA/NC=9/1(a,d), 8/2(b,e), 7/3(c,f),紡絲電壓14kV,收集距離13cm]Fig.1 SEM images (a,b,c) and diameter distribution (d,e,f) of PVA/NC composite fiber under different material proportion: PVA/NC=9/1(a,d), 8/2(b,e), 7/3(c,f), voltage=14kV, collected distance=13cm
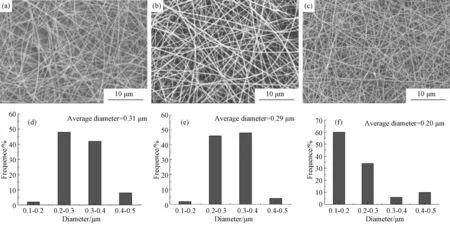
圖2 不同紡絲電壓下制得的PVA/NC復(fù)合纖維SEM形貌圖(a,b,c)和相應(yīng)的直徑分布圖(d,e,f)[紡絲電壓=10kV (a, d), 14kV (b,e), 18kV (c, f), PVA/NC體積比8/2,收集距離15cm]Fig.2 SEM images (a, b, c) and diameter distribution (d, e, f) of PVA/NC composite fiber under different electrospinning voltage of 10kV (a, d), 14kV (b,e), 18kV (c, f) [PVA/NC=8/2, collected distance=15cm]
3.3 收集距離對(duì)復(fù)合纖維形態(tài)的影響
圖3給出了不同收集距離下制備的PVA/NC復(fù)合纖維SEM圖和直徑分布圖。由圖可知,當(dāng)收集距離較小(如10cm)時(shí),PVA/NC復(fù)合纖維之間出現(xiàn)較嚴(yán)重的粘結(jié)現(xiàn)象,且纖維直徑分布均勻性較差,這是由于當(dāng)收集距離較小時(shí),制備獲得的復(fù)合纖維在電場(chǎng)中被拉伸的時(shí)間較短,紡絲溶劑沒(méi)有足夠的時(shí)間揮發(fā),從而導(dǎo)致纖維之間的粘結(jié)現(xiàn)象。隨著收集距離的增大,復(fù)合纖維粘結(jié)現(xiàn)象消失,這是因?yàn)殡S著收集距離增大,復(fù)合纖維被拉伸和溶劑揮發(fā)的時(shí)間增加,使復(fù)合纖維得到了充分拉伸,且溶劑得到了充分揮發(fā),從而使粘結(jié)現(xiàn)象消失[10]。值得注意的是,隨著收集距離的增加,復(fù)合纖維平均直徑先降低后增大,直徑分布均勻性先增加后降低。例如,收集距離從10cm增大至13cm時(shí),復(fù)合纖維平均直徑減小,這是因?yàn)殡S收集距離增加,溶劑揮發(fā)路徑和揮發(fā)時(shí)間增大,使纖維分化環(huán)境變優(yōu),且高分子射流體在電場(chǎng)中被拉伸的時(shí)間增大,從而導(dǎo)致復(fù)合纖維平均直徑減小。相反,當(dāng)收集距離從13cm增大至15cm時(shí),復(fù)合纖維平均直徑由0.24μm增大至0.29μm,這是由于溶劑在合適的路徑內(nèi)得到充分揮發(fā)后,獲得凝固定型的復(fù)合纖維,再增加纖維拉伸和溶劑揮發(fā)時(shí)間對(duì)復(fù)合纖維的直徑不再產(chǎn)生明顯的影響。同時(shí),由電場(chǎng)強(qiáng)度=電壓/距離可以看出,當(dāng)電壓恒定時(shí),增加紡絲距離將使電場(chǎng)強(qiáng)度降低,使纖維分化能力降低。因此,收集距離的進(jìn)一步增加反而會(huì)使纖維平均直徑增加,直徑分布均勻性降低[12]。

圖3 不同收集距離下制備的PVA/NC復(fù)合纖維SEM形貌圖(a,b,c)和相應(yīng)的直徑分布圖(d,e,f)[收集距離=10cm (a, d), 13cm (b, e), 15cm (c, f), PVA/NC體積比8/2,紡絲電壓14kV]Fig.3 SEM images (a, b, c) and diameter distribution (d, e, f) of PVA/NC composite fiber under different collected distance of 10cm (a, d), 13cm (b, e), 15cm (c, f). [ PVA/NC=8/2, voltage=14kV]
3.4 PVA/NC復(fù)合纖維的親水性能
圖4給出了不同材料配比下PVA/NC復(fù)合纖維膜的水接觸角值。由圖可知,隨NC含量增加,復(fù)合纖維膜水接觸角從25°增加至57°。這主要是由于PVA分子鏈中含有大量的羥基導(dǎo)致其為可溶于水的高分子材料,具有較好的親水性能,NC的加入,降低了復(fù)合纖維的親水性能[7],因此可以通過(guò)簡(jiǎn)單的調(diào)節(jié)PVA/NC材料配比來(lái)控制復(fù)合纖維的親水性能。
3.5 PVA/NC/氨芐西林鈉復(fù)合纖維形態(tài)及釋藥性能
圖5為不同藥物含量下PVA/NC/氨芐西林鈉復(fù)合纖維的SEM圖和直徑分布圖(PVA/NC體積比8/2,紡絲電壓14kV,收集距離13cm)。由圖可知,隨氨芐西林鈉含量增加,復(fù)合纖維平均直徑增大,直徑分布均勻性降低且表面出現(xiàn)粘結(jié)現(xiàn)象。這是因?yàn)樗幬锖吭黾樱箯?fù)合纖維內(nèi)部包裹的氨芐西林鈉藥物增多,從而復(fù)合纖維平均直徑增大,比表面積降低,復(fù)合纖維表面溶劑揮發(fā)速率變慢,溶劑揮發(fā)不完全,導(dǎo)致復(fù)合纖維表面出現(xiàn)部分粘結(jié)現(xiàn)象。

圖4 不同材料配比下制備的PVA/NC 復(fù)合材料水接觸角Fig.4 Water contact angles of the PVA/NC composite fiber under different material proportion
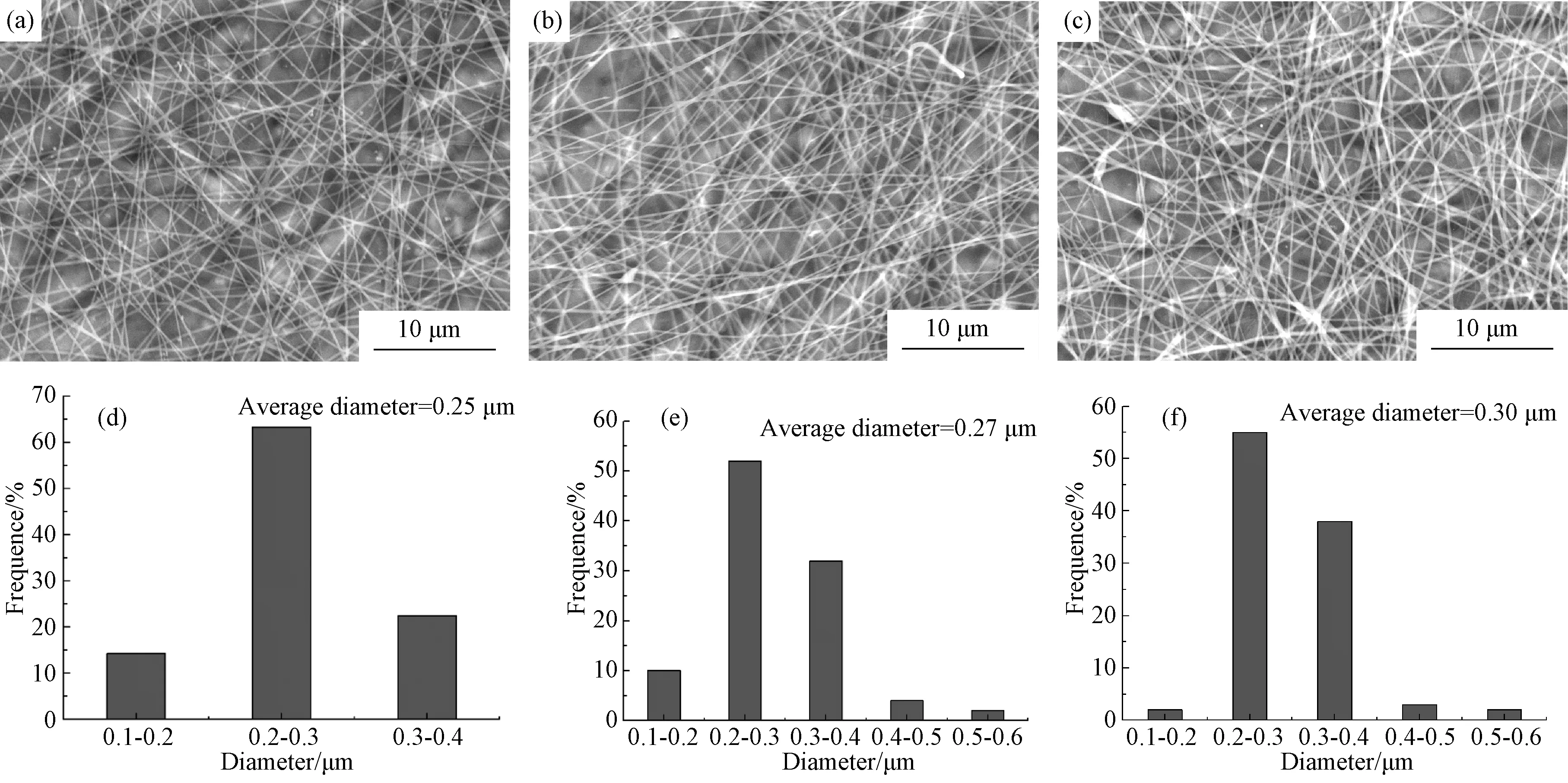
圖5 不同藥物含量PVA/NC/氨芐西林鈉復(fù)合纖維的SEM圖(a,b,c)和相應(yīng)的直徑分布圖(d,e,f)[藥物含量=0.5%(a, d), 1% (b, e), 2% (c, f)]Fig.5 SEM images (a, b, c) and diameter distribution (d, e, f) of PVA/NC/ampicillin sodium composite fiber under different drug content of 0.5% (a, d), 1%(b, e), 2% (c, f)
圖6為不同藥物含量下PVA/NC/氨芐西林鈉復(fù)合纖維的藥物釋放曲線(xiàn)。

圖6 不同藥物含量下PVA/NC/氨芐西林鈉復(fù)合纖維的藥物釋放曲線(xiàn)Fig.6 Drug release curves of PVA/NC/ampicillin sodium composite fiber under different drug contents.
由圖6可見(jiàn),在藥物釋放初期,載藥復(fù)合纖維膜體出現(xiàn)較快的藥物釋放速率,處于藥物突釋階段,這是因?yàn)橛H水性藥物具有較高的離子能,在靜電紡絲過(guò)程中較易吸附于復(fù)合纖維表面,因此,釋藥初期產(chǎn)生較快的藥物釋放速率。隨著藥物釋放時(shí)間的增加,復(fù)合纖維表面的藥物釋放完畢后,復(fù)合纖維內(nèi)部藥物逐漸被釋放,但緩沖溶液浸入纖維內(nèi)部和藥物向外擴(kuò)散的時(shí)間較長(zhǎng),導(dǎo)致藥物釋放后期具有較慢的釋放速率。通過(guò)計(jì)算獲得不同藥物含量即投藥量為0.5%,1%,2%下,復(fù)合纖維的實(shí)際載藥量分別為0.36%,0.52%和0.98%。由圖6可知,隨載藥量降低,復(fù)合纖維藥物釋放速率增大,這是因?yàn)楫?dāng)載藥量較低時(shí),由SEM圖可知復(fù)合纖維平均直徑較小,比表面積較大,使緩沖溶液較易浸入復(fù)合纖維內(nèi)部,且表面藥物含量較多,因此使其藥物釋放速率增大[13]。
4 結(jié) 論
采用靜電紡絲技術(shù)制備了PVA/NC載藥復(fù)合纖維,研究了材料配比、紡絲電壓和收集距離對(duì)PVA/NC復(fù)合纖維形態(tài)、直徑分布和平均直徑的影響。探討了材料配比對(duì)復(fù)合纖維親水性能影響,并分析了氨芐西林鈉含量對(duì)PVA/NC載藥復(fù)合纖維膜形態(tài)和藥物釋放速率的影響。結(jié)果表明:隨著NC含量增加,PVA/NC復(fù)合纖維直徑降低,直徑分布均勻性增加,親水性降低;PVA/NC/氨芐西林鈉載藥復(fù)合纖維膜在藥物釋放初期具有較快的釋放速率,且藥物含量越少,其復(fù)合纖維直徑越小,比表面積越大,表面藥物含量越多,導(dǎo)致其藥物釋放速率越大。

