以患者為中心:新血糖管理時代的胰島素選擇
梁琳瑯
沈陽軍區總醫院內分泌科,遼寧 沈陽 110000
2012年美國糖尿病學會(American Diabetes Association,ADA)和歐洲糖尿病研究協會(European Association for the Study of Diabetes,EASD)聯合聲明提出,對2型糖尿病(type 2 diabetes mellitus,T2DM)患者的血糖管理應采用個體化血糖控制目標和個體化治療方案,糖尿病治療進入以患者為中心的新血糖管理時代。以患者為中心的治療定義為:根據個體患者的偏好、需要和價值,提供有效的治療,并保證以患者價值指導所有臨床決策。此外,該聲明還指出,種族也是一個重要因素[1]。中國T2DM患者血糖特征不同于西方患者,加之社會文化和醫療保健制度的差異,胰島素治療方案應依據患者特點制定。本文將分析中國T2DM血糖特點、控制現狀,并剖析其背后的機制,溯本追源地探究真正適合中國患者的胰島素起始治療方案。
1 以患者為中心管理的血糖管理時代,首先要分析患者特點
在以患者為中心的臨床治療策略中,需根據患者的血糖譜特征、胰島功能、飲食特點、現有治療方案、控制情況、年齡、病程、預期壽命、并發癥或合并癥病情嚴重程度等因素進行綜合考慮,選擇個體化治療方案。中國T2DM患者患病機制、血糖水平及飲食習慣有以下特點:β細胞早相分泌減退更為明顯,餐后血糖升高比例更多,主食以精制米面制品為主,對血糖符合較大。
1.1 中國T2DM患者的血糖特點:普遍存在餐后血糖升高中國糖尿病人群餐后血糖(postprandial plasma glucose,PPG)升高的比例高于歐洲人群。DECODE研究的13個歐洲糖尿病隊列中有65%的患者餐后2h PPG>11.1mmol/L[2],而在與之對應的DECODA研究的11個亞洲糖尿病隊列中,餐后2h PPG>11.1mmol/L的患者比例高達82%[3]。楊文英教授在2010年發表于《新英格蘭醫學雜志》的流行病學調查顯示,80%以上的中國新診斷T2DM患者存在餐后高血糖,其中男性單純空腹高血糖型糖尿病(isolated fasting hyperglycemia,IFH)、單純負荷后高血糖型糖尿病(isolated postprandial hyperglycemia,IPH)、負荷后高血糖/空腹高血糖型糖尿病(postprandial hyperglycemia/fasting hyperglycemia,PH/FH)的比例分別占20%、44%、36%,女性分別占15%、50%、35%[4]。針對中國T2DM患者普遍存在PPG升高的血糖特點,治療策略應強調對PPG的控制。
1.2 中國T2DM的患病機制:β細胞功能受損,且以早相分泌缺陷為主目前認為,T2DM的發病機制主要包括胰島分泌功能缺陷和胰島素抵抗兩大因素。發病之初可以通過胰島β細胞代償性分泌以維持血糖水平,但隨著β細胞負擔的不斷加重,引起功能受損失代償衰竭,從而表現為血糖升高[5]。
一項對糖耐量正常、糖尿病前期和T2DM中國老年群體隨訪3年的研究[6]顯示,老年人在由基線的糖耐量正常(normal glucose tolerance,NGT)或糖尿病前期進展為糖尿病后,β細胞功能分別較基線降低11.6%和26.1%。另一項對1016例盎格魯-凱爾特和1514例中國新發糖尿病患者(病程不足2年)評估12年的研究[7]發現,盎格魯-凱爾特人的T2DM促發因素為肥胖、胰島素抵抗、血脂異常等代謝綜合征因素,而中國早期T2DM患者并未表現上述代謝綜合征因素患病率增加。提示在中國T2DM發病中,早發β細胞缺陷是更重要的促發因素。可見,在中國人群T2DM的發生發展過程中,胰島素β細胞功能的變化起著重要作用。
β細胞的胰島素分泌可分為早相(第一時相)和晚相(第二時相)分泌兩個部分,早相分泌的是β細胞內貯存的胰島素顆粒,在血糖急性升高后10min內分泌;晚相分泌的是β細胞新產生的胰島素,在血糖升高后2~3h達到平臺期[8]。Lin的研究[8]探討了胰島素早相分泌、晚相分泌和胰島素抵抗在T2DM發病中的變化,結果發現,在T2DM發生過程中,胰島素抵抗未見加重,但隨著空腹血糖(fasting plasma glucose,FPG)升高,早相胰島素分泌顯著降低,提示早相胰島素分泌缺陷是T2DM發生的關鍵觸發因素。另一項在中國人群中進行的研究[9]證實,早在糖尿病前期,早相胰島素分泌指數已下降至最大值的一半,當進展到顯性糖尿病階段時,進一步降至最大值的四分之一。
由此可見,中國T2DM患者的發病機制與胰島β細胞早相分泌不足有關。針對這一特點,治療策略應重視餐后血糖的控制。
1.3 中國T2DM的飲食特點:以升糖指數較高的精制米面制品為主升糖指數(glycaemic index,GI)是量化攝入不同含碳水化合物食物后PPG反應的一個指標[10]。
具有高升糖指數的白米飯是大部分中國人的主食,已有研究顯示米飯攝入量與T2DM的發病風險相關[11]。陶利等[12]對T2DM患者飲食攝入的調查分析顯示,中國T2DM患者主食有82.15%來源于高GI的精制米面及其制品。對多種族參與的SWAN研究的分析[13]也發現,大米對中國和白種人的膳食升糖負荷的貢獻分別占40.2%和8.75%。Kataoka等[14]對不同種族進食葡萄糖、泰國香米、糙米、印度香米、蒸谷米和澳洲長米后的血糖反應的研究顯示,中國人群進食相同數量5種大米后的血糖反應(血糖曲線下面積的增加)較歐洲人群高出60%(P<0.001),進食葡萄糖后的血糖反應較歐洲人群高出39%(P<0.004)。
由此可見,中國2型糖尿病患者在疾病早期已存在β細胞功能受損和普遍存在PPG水平升高,且中國人群的飲食和患病機制的特點使得PPG水平升高較歐洲人群更為明顯。鑒于此,中國2型糖尿病患者應采取能夠覆蓋PPG的胰島素補充治療方案。
2 中國2型糖尿病的胰島素治療現狀
鑒于中國T2DM患者較早出現β細胞功能缺陷和普遍存在PPG升高的特點以及社會醫療背景,胰島素治療面臨更大挑戰。
首先,我國T2DM患者起始胰島素治療較晚。INTENSE、PRESENT、A1chieve、IMPROVE、ORBIT等[15-19]真實世界臨床研究中中國人群數據顯示,中國T2DM患者起始胰島素治療時已處于疾病中晚期階段,病程通常已達6~8年,平均糖化血紅蛋白(Hemoglobin A1c,HbA1c)已超過9%,且起始胰島素治療時已有1/3以上患者發生并發癥,隨疾病進展,各種并發癥發生率逐漸增高[20]。
其次,起始基礎胰島素治療者的血糖達標率仍很不理想,且血糖控制維持時間較短。一項全國性調查研究顯示,三甲醫院門診和住院部T2DM患者使用起始基礎胰島素HbA1c達標率為38%~42%[21],基層醫院起始基礎胰島素治療者的HbA1c達標率更低,只有23%[22]。由于達標率低等原因,患者需轉換為其他胰島素治療方案,起始基礎胰島素治療者在6個月后僅有45.47%維持原方案[21]。
鑒于我國T2DM患者普遍存在的PPG升高和起始基礎胰島素治療達標率低、無法長期維持血糖控制的現狀,需要遵循以患者為中心的原則,尋求更適合中國T2DM人群的起始胰島素治療方案。
3 選擇預混胰島素,實現以患者為中心的血糖管理
基于中國T2DM患者以上血糖、發病機制和血糖控制現狀,我們需要采取兼顧空腹和餐后血糖的胰島素治療方案。
3.1 預混胰島素在改善β細胞早相分泌方面更具優勢中國T2DM人群早期即存在胰島β細胞的早相分泌缺陷,且隨著疾病進展,早相分泌缺陷不斷加重[7]。預混胰島素制劑中同時含有補充早相分泌的短效成分和覆蓋基礎胰島素需要的中長效成分,兼顧空腹血糖和餐后血糖水平。
預混胰島素類似物制劑中的速效胰島素類似物對人胰島素分子進行了修飾,使六聚體在高濃度下快速解離,具有吸收快、起效快、作用峰值高和作用時間短的特點,可以更好地模擬早相胰島素分泌。一項對新診斷T2DM患者的研究[23]發現,餐前15~30min皮下注射預混胰島素類似物可較好地模擬生理性早相胰島素分泌,并使PPG水平顯著降低。
3.2 預混胰島素在兼顧空腹和餐后血糖方面更具優勢預混胰島素制劑可兼顧餐后和空腹血糖的控制。藥代動力學和藥效學研究[24,25]顯示,預混胰島素(類似物)可通過補充餐時和基礎胰島素分泌,有效控制PPG和FPG水平。與基礎胰島素相比,起始預混胰島素治療治療可獲得更全面的血糖控制效果。Meta分析[26]顯示,在控制FPG水平方面,預混胰島素類似物與基礎胰島素的效果相似[95%CI(-15.76~-29.94),P=0.543],但預混胰島素類似物控制PPG水平更佳[95%CI(-20.09~-9.31),P<0.0001],HbA1c降幅較基礎胰島素治療更優[95%CI(-0.60~-0.04),P=0.002],且不增加重度低血糖風險(0.98%vs1.12%,P=0.841)。中國人群的大樣本觀察性研究[15-18,27]也一致證實,起始預混胰島素類似物治療12~26周后,可顯著降低FPG、PPG和HbA1c水平,且低血糖風險較低(表1)。
由此可見,預混胰島素方案可針對中國T2DM患者胰島素早相分泌缺陷和普遍存在PPG升高的特點,提供更全面控制血糖、更適合中國患者的起始胰島素治療選擇。
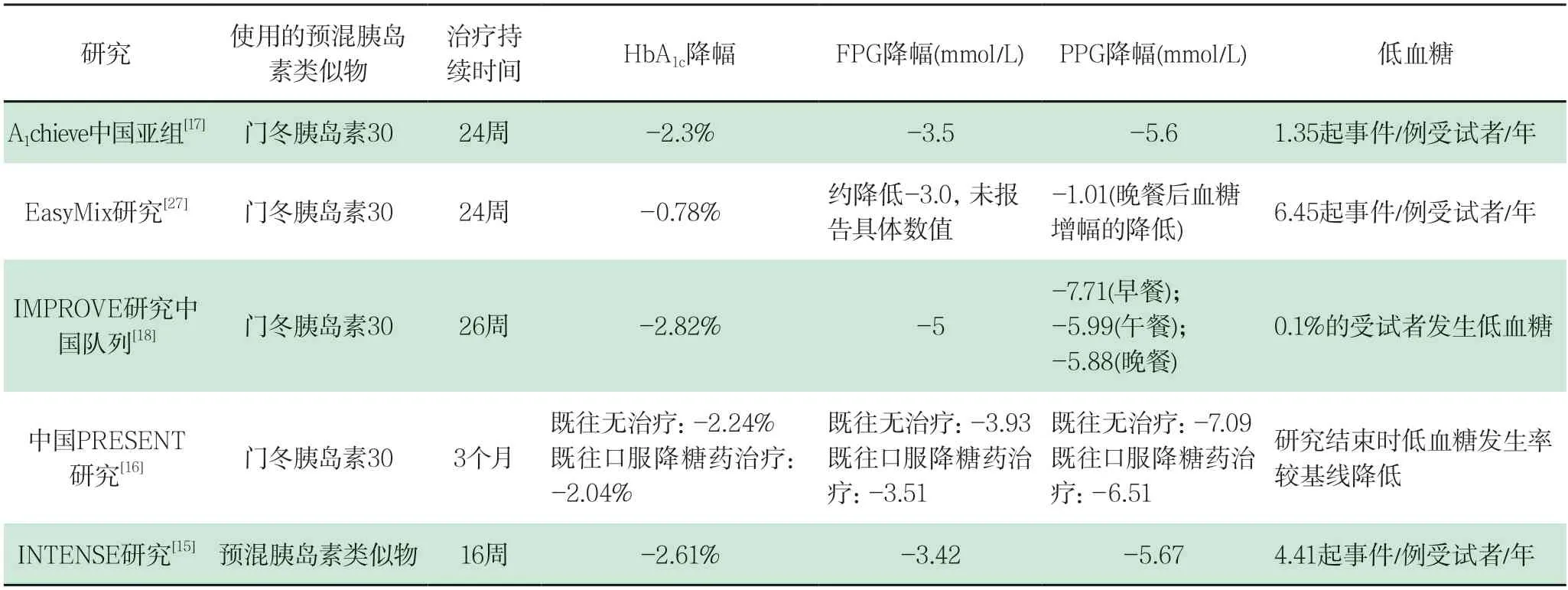
表1 中國人群大樣本觀察性研究中預混胰島素類似物治療的有效性和安全性
4 結語
中國T2DM患者普遍存在PPG升高、早期已有胰島素早相分泌缺陷,且多以升糖指數較高的精制米面為主食,對中國T2DM患者的起始胰島素治療必須強調對PPG的控制。預混胰島素類似物方案可補充早相胰島素分泌的不足,更好地模擬生理性胰島素分泌,有效兼顧空腹和餐后血糖控制。相對基礎胰島素而言,預混胰島素是更適合中國T2DM人群的起始胰島素治療選擇。

