水芹中芹菜素的提取純化與抗氧化活性研究
黃志強,吳娜梅,唐明明,孫漢巨,李延紅,何述棟,劉和平,郜四羊
(1.合肥工業大學食品與生物工程學院,安徽合肥 230009;2.安徽四平食品開發有限責任公司,安徽銅陵 244000)
芹菜素,又叫芹黃素,是天然存在的一種黃酮類化合物,有“植物雌激素”之稱,廣泛存在于多種水果、蔬菜、豆類和茶葉中,其中芹菜含量最高。芹菜素的化學名稱為5,7,4'-三羥基黃酮(5,7,4'-trihydroxyflavone),其4',5,7位置的3個羥基和C2,C3之間的雙鍵決定了其獨特的生理學效應和生物學特性。芹菜素的分子式為C15H10O6,分子量為270,不溶于水,易溶于乙醇、二甲基亞砜(DMSO)。純品呈淺黃或黃綠色,是天然的抗氧化劑,有降血壓和舒張血管、預防動脈粥樣硬化、抑制腫瘤等作用[1]。
水芹(Oenanthe javanica),為傘形科草本植物,又名水英、野芹菜等[2]。其營養豐富,含有多種人體不可缺少的營養物質,如黃酮、多糖、礦物質及揮發油類,具有良好的食用價值[3]。同時,水芹在臨床對高血壓病、高脂血癥、心腦血管疾病、乙型肝炎具有防治作用。有研究報道,水芹中黃酮含量很高,但有關水芹中芹菜素的報道較少。試驗對水芹黃酮的提取進行了優化研究,并對芹菜素的提取純化、鑒定及其抗氧化性進行了初步研究,旨在為水芹功能成分分析和深加工提供理論依據。
1 材料與方法
1.1 原料與試劑
水芹,桐城市牯牛背農業開發有限公司提供;無水乙醇(分析純)、硝酸鋁、亞硝酸鈉、氫氧化鈉(粉狀)、蘆丁標準品、X-5型大孔吸附樹脂、AB-8型大孔吸附樹脂、HP-20型大孔吸附樹脂、磷酸(優級純)、甲醇(色譜純);芹菜素標準品,上海源葉生物科技有限公司提供;濃鹽酸、去離子水。
1.2 儀器及設備
722E型分光光度計,上海光譜儀器有限公司產品;HH-2型數顯恒溫水浴鍋,江蘇金壇市榮華儀器制造有限公司產品;FA2004型電子分析天平,上海精科天平有限公司產品;BT-100型恒流泵,上海滬西分析儀器廠有限公司產品;85-2型恒溫磁力攪拌器,金壇市城東新瑞儀器廠產品;DHG-9070A型電熱恒溫干燥箱,上海躍進醫療儀器廠產品;SHZ-D型循環水式真空泵,鞏義市予華儀器有限責任公司產品;RE-52AA型旋轉蒸發器,上海亞榮生化儀器廠產品;LGJ-12型冷凍干燥機,北京松源華興科技發展有限公司產品;SQW-40DⅡ型超微粉碎機,山東三清易辰有限公司產品;層析柱,上海廈美生化科技發展有限公司產品;E2695型制備液相色譜儀,美國WATERS有限公司產品;質譜儀,美國WATERS有限公司產品。
1.3 芹菜素的提取及純化
1.3.1 工藝流程
水芹→清洗→切碎→冷凍干燥→超微粉碎→水浴提取→樹脂吸附→乙醇洗脫→旋蒸→冷凍干燥→制備液相分離。
1.3.2 操作要點
(1)清洗。用蒸餾水清洗水芹的葉和莖,除去水芹葉、莖中肉眼可見的雜質。
(2)切碎。用潔凈的刀將水芹葉、莖切成指甲大小的碎片。
(3) 冷凍干燥。在-60℃,3~10 Pa條件下,將水芹葉、莖碎片進行冷凍干燥,使水分含量≤0.5%。
(4)超微粉碎。采用偏振式超微粉碎機對干燥后的水芹進行超微粉碎,粉碎時間15 min。
(5)水浴提取。用乙醇溶液浸提,選用不同梯度的料液比、乙醇體積分數、提取溫度和提取時間進行浸提。
(6)樹脂吸附。按吸附及洗脫操作條件,將提取液加入層析柱中,吸附流速2.5 mL/min,平衡時間3 h。因黃酮被AB-8型大孔樹脂吸附,而其他糖類、蛋白等成分不被樹脂吸附,采用去離子水洗脫樹脂,至流出液完全透明為止。
(7)乙醇洗脫。用90%乙醇溶液洗脫大孔樹脂,至流出液為無色為止,收集洗脫液。
(8) 旋轉蒸發。在溫度40℃,真空度≥4 kPa條件下,采用旋轉蒸發器,將洗脫液進行真空濃縮,至液體至原體積的1/3為止。
(9) 冷凍干燥。在-60℃,3~10 MPa條件下,將濃縮液進一步冷凍干燥,使水分含量≤0.5%,得到黃酮粉末。
1.4 試驗方法
1.4.1 水芹中粗黃酮含量標準曲線的確定及其含量測定
粗黃酮含量的測定采用硝酸鋁-亞硝酸鈉比色法,以蘆丁為標準品在510.0 nm處進行比色測定,然后,以吸光度為縱坐標,蘆丁質量濃度為橫坐標,繪制標準曲線,回歸方程為[4-5]:
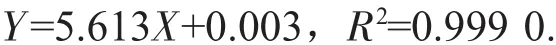
式中:X——蘆丁質量濃度,mg/mL;
Y——吸光度A。
水芹粗黃酮的提取采用水浴法提取[6]。利用標準曲線計算樣品粗黃酮總量,根據公式(1)計算提取物粗黃酮得率。
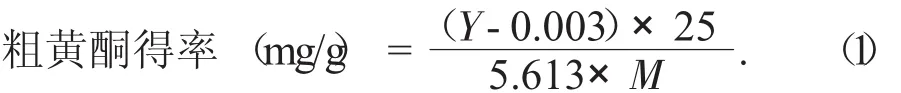
式中:Y——標準曲線上對應的吸光度;
M——所用原料的質量,g。
1.4.2 水芹中粗黃酮提取的單因素研究[7-9]
(1) 乙醇體積分數對水芹中粗黃酮提取的影響。稱取0.5 g水芹粉于置5個20 mL燒杯內,分別加入15 mL體積分數為60%,70%,80%,90%,100%的乙醇為提取劑,在70℃條件下回流提取4 h,計算粗黃酮得率,確定較適宜的乙醇體積分數。
(2)提取溫度對水芹中粗黃酮提取的影響。稱取0.5 g水芹粉置于5個20 mL燒杯內,加入80%乙醇15 mL為提取劑,在提取溫度分別為50,60,70,80,90℃條件下回流提取4 h,計算粗黃酮得率,確定較適宜的提取溫度。
(3)提取時間對水芹中粗黃酮提取的影響。稱取0.5 g水芹粉于5個20 mL燒杯內,加入80%乙醇15 mL作為提取劑,在70℃條件下回流提取2,3,4,5,6 h,計算粗黃酮得率,確定較適宜的提取時間。
(4)料液比對水芹中粗黃酮提取的影響。稱取0.5 g水芹粉置于7個50 mL燒杯內,以80%的乙醇為提取劑,其料液比為1∶10,1∶15,1∶20,1∶25, 1∶30,1∶35,1∶40,在70℃條件下回流4 h,計算粗黃酮得率,確定較適宜的料液比。
1.4.3 水芹中粗黃酮的提取工藝優化
考慮到不同提取因素間的相互作用,在單因素試驗基礎上,以乙醇體積分數、提取溫度、提取時間和料液比為4個主要因素,進行四因素三水平L9(34)正交試驗,確定水芹中粗黃酮的最佳提取工藝。
1.4.4 大孔吸附樹脂純化水芹粗黃酮[10-12]
(1) 大孔樹脂的預處理。將 AB-8,X-5和HP-20型這3種大孔吸附樹脂分別用90%乙醇浸泡24 h,同時不停攪拌,使大孔吸附樹脂和乙醇充分接觸,完成后用蒸餾水洗至無醇味;然后再用5%的鹽酸溶液浸泡4 h,用蒸餾水洗至pH值為中性;最后,用5%的氫氧化鈉溶液浸泡4 h,用蒸餾水洗至pH值為中性,備用[13]。
(2)大孔吸附樹脂的靜態吸附和靜態解析試驗[14]。準確稱取預處理過的大孔吸附樹脂(AB-8,X-5和HP-20型) 各3 g,置于250 mL錐形瓶中,加入黃酮提取液60 mL,恒溫(25℃) 下振蕩24 h至吸附平衡,取出后再次過濾,在波長510 nm處測定吸光度,根據公式(1)計算黃酮得率。用蒸餾水將吸附飽和的大孔吸附樹脂洗至洗脫液無色,再次過濾,并且吸干表面水分,加入90%乙醇30 mL,于室溫下振蕩12 h,將樹脂濾出,于波長510 nm處測定吸光度,根據公式(1)計算黃酮得率,并根據公式(2)計算吸附率,公式(3)計算解析率。
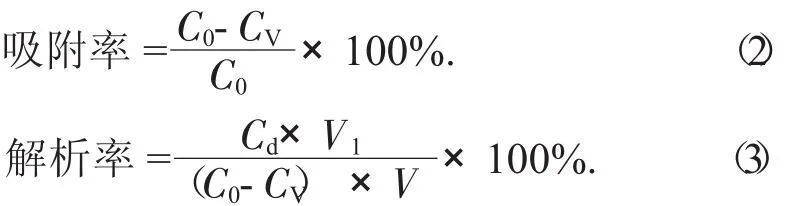
式中:C0——初始質量濃度,mg/mL;
CV——剩余質量濃度,mg/mL;
Cd——解析液質量濃度,mg/mL;
V1——解析液體積,mL;
V——溶液體積,mL。
(3) 大孔吸附樹脂對粗黃酮純化[15-18]。采用濕法裝柱,用3 BV去離子水將柱子壓實,然后將粗黃酮提取液以2 mL/min的流速上柱吸附,富集15 min后,再用去離子水洗至上層液呈無色,再用90%的乙醇洗脫,收集洗脫液直至洗脫液為無色。將收集到的液體進行濃縮,再用冷凍干燥機進行干燥,制得粗黃酮備用。
1.4.5 制備型液相色譜制備芹菜素
精確稱量20 mg粗黃酮樣品于20 mL小燒杯中,再加入10 mL甲醇,超聲溶解10 min,取出后將溶液過0.22μm膜,備用。其中,制備型液相色譜條件設置為:Galaksil EP-C18M型色譜柱(20 mm×250 mm,平均粒徑10μm);流動相:乙腈-0.2%磷酸水溶液(35∶65,V∶V),流動相流速5 mL/min,檢測波長345 nm,柱溫25℃,進樣量5 mL[19-20]。
1.4.6 分析型高效液相色譜驗證芹菜素
樣品制備方法同上,高效液相色譜條件設置為:SepaxGP-C18型色譜柱(250 mm×4.6 mm,平均粒徑5μm);流動相:乙腈-0.2%磷酸水溶液(35∶65,V∶V),流動相流速1.0 mL/min,檢測波長345 nm,柱溫30℃,進樣量20 L[21]。
1.4.7 質譜分析
采用四級桿飛行時間質譜儀對利用制備型液相色譜儀制得的芹菜素單體進行MS/MS分析,且MS/MS條件為:ESI離子源、電噴霧離子化正離子采集模式,掃描范圍50~500 m/z,毛細管電壓3 500 V,霧化氣壓40.0 psi,干燥溫度310℃,干燥氣流速度9 mL/min[22]。
1.4.8 抗氧化活性研究
(1) 清除DPPH自由基(DPPH·) 的能力。精確吸取芹菜素粗提物及單體樣品溶液(質量濃度梯度為20,30,40,50,60 g/mL) 各 2 mL,分別與2 mL濃度為2×10-4mol/L的DPPH無水乙醇溶液混合,充分搖勻后放置30 min。以2 mL蒸餾水與無水乙醇的混合溶液為參比,于波長517 nm處測定吸光度,記為A1;精確吸取樣品溶液各2 mL分別與2 mL蒸餾水混合均勻,以蒸餾水為參比,于波長517 nm處測定吸光度,記為A2;精確吸取2 mL濃度為2×10-4mol/L DPPH無水乙醇溶液與2 mL蒸餾水混合均勻后,以2 mL蒸餾水與2 mL無水乙醇的混合溶液為參比,于波長517 nm處測定吸光度,記為A0。以上吸光度均各測3次[23]。以VC為陽性對照,根據公式(4) 計算清除率:
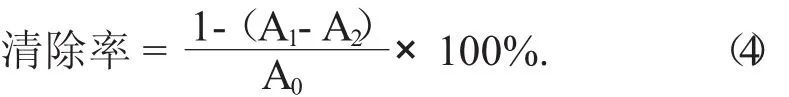
(2) 清除羥基自由基(·OH) 的能力。精確吸取芹菜素粗提物及單體樣品溶液(質量濃度梯度為2,4,6,8,10 g/mL) 各1 mL,依次加入1 mL 9 mmol/L FeSO4溶液、1 mL 9 mmol/L水楊酸乙醇溶液和1 mL 9 mmol/LH2O2,充分搖勻,于37℃水浴下反應30 min,對同樣濃度的VC作同樣處理作為陽性對照,以蒸餾水為參比,于波長510 nm處測定吸光度,記為A1;以蒸餾水代替樣品作為待測溶液,于波長510 nm處測定吸光度,記為A0;以蒸餾水代替FeSO4,1 mL 9mmol/L水楊酸和1 mL 9 mmol/L H2O2溶液,于波長510 nm處測定吸光度,記為A2。以上吸光度均各測3次[24]。根據公式(5) 計算清除率:
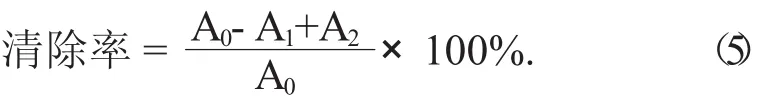
(3) 清除超氧陰離子(O2-·) 的能力。取25℃下預熱過pH值8.2,濃度50 mmol/L Tris-HCl緩沖溶液2.25 mL,置于10 mL試管中,加入芹菜素粗提物及單體樣品溶液(質量濃度梯度為1,2,4,6,8 g/mL)2 mL,再加入25℃下預熱過的45 mmol/L鄰苯三酚溶液75 L,迅速混勻,反應4 min后加入20 L濃度為10 mol/L HCl溶液終止反應,對同樣濃度的VC作同樣處理并作為陽性對照,以蒸餾水為參比,于波長320 nm處測定吸光度,記為A1;按上述方法,以2 mL蒸餾水代替樣品,于波長320 nm處測定吸光度,記為A2;以蒸餾水代替鄰苯三酚溶液,于波長320 nm處測定吸光度,記為A0。以上吸光度均各測3次[25]。根據公式(6) 計算清除率:
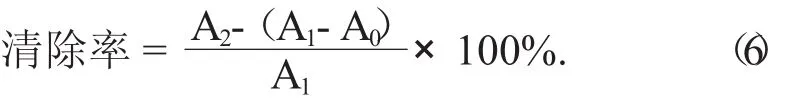
2 結果與分析
2.1 水芹中粗黃酮的提取工藝優化
2.1.1 水芹中粗黃酮提取的單因素試驗結果
水芹中粗黃酮提取的單因素試驗結果見圖1。
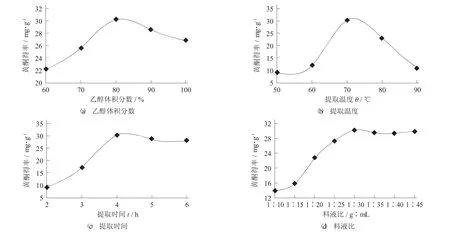
圖1 水芹中粗黃酮提取的單因素試驗結果
乙醇體積分數對水芹中粗黃酮提取的影響如圖1(a)所示。很顯然,隨著乙醇體積分數的提高,黃酮得率明顯上升,且乙醇體積分數達到80%時,黃酮得率最高(30.24 mg/g)。乙醇體積分數進一步提高后黃酮提取量有所下降。由于黃酮類化合物結構各異,其溶解特性因極性不同而有所差異。水芹黃酮中含多種成分,既有黃酮苷類又有苷元類,所以選用一定比例的乙醇溶液能夠最大程度地提取出來。
提取溫度對水芹中粗黃酮提取的影響如圖1(b)所示。可以看出,當提取溫度從50℃上升到70℃時,黃酮得率顯著上升,從9.11 mg/g上升至30.24 mg/g,這是由于提取溫度升高可加快分子擴散速率,從而促進黃酮類物質的析出。但提取溫度進一步上升時,黃酮得率明顯下降,這可能因為提取溫度較高,破壞了黃酮類化合物的結構,并增加了其他非黃酮物質的析出。
提取時間對黃酮得率的影響如圖1(c) 所示。顯而易見,提取時間從2 h上升至4 h時,黃酮得率提高到最高值(30.24 mg/g),隨著提取時間的延長,黃酮得率無明顯變化。這可能是因為黃酮成分的溶出需要一個過程,隨著提取時間的延長,而達到飽和狀態,使得黃酮得率無明顯變化。
料液比對黃酮得率的影響如圖1(d)所示。很明顯,當料液比從1∶10上升至1∶30時,黃酮得率快速上升到最大值(30.24 mg/g)。然而,隨著料液比的進一步提高,黃酮得率不僅沒有增大,甚至還出現了略微的下降,這可能是因為黃酮成分的溶出已經達到飽和。
2.1.2 水芹中粗黃酮的最佳提取工藝的確定
考慮到不同提取因素間的相互作用,在單因素試驗的基礎上,選擇L9(34)正交試驗進行最佳提取工藝的確定。
正交試驗因素與水平設計見表1,正交試驗結果見表2。
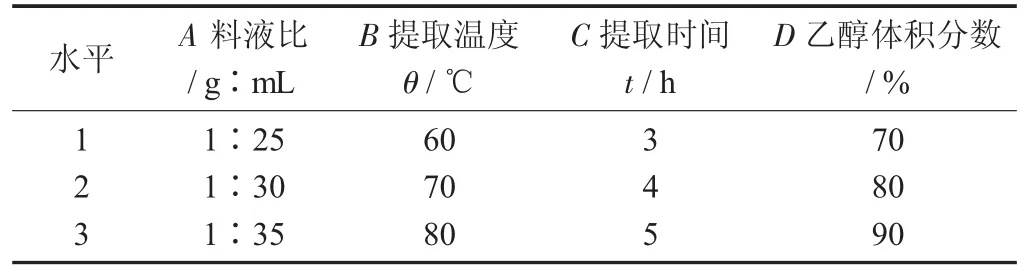
表1 正交試驗因素與水平設計
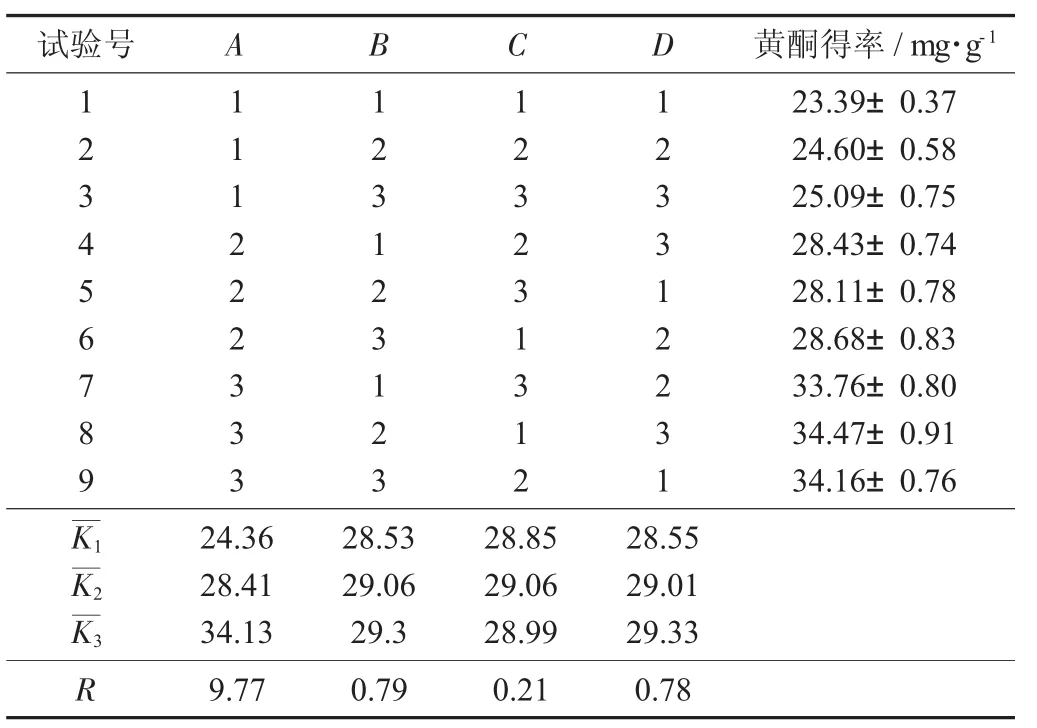
表2 正交試驗結果
由表2可知,影響從水芹中提取粗黃酮的主次因素排列次序為料液比>提取溫度>乙醇體積分數>提取時間。根據結果觀察,8號試驗的黃酮得率最高,提取工藝為料液比1∶35,提取溫度70℃,提取時間3 h,乙醇體積分數90%。然而從極差分析的結果看,最佳組合為A3B3C2D3。所以,對A3B2C1D3和A3B3C2D3進行驗證試驗,結果分別為33.76,36.75 mg/g,最終確定A3B3C2D3為水芹中粗黃酮的最佳提取工藝,即料液比1∶35,提取溫度80℃,提取時間4 h,乙醇體積分數90%。
2.2 大孔吸附樹脂的篩選
評定大孔吸附樹脂性能,不僅需要有較大的吸附量,還需要較大的解析率,所以可以通過測定大孔吸附樹脂AB-8,HP-20和X-5型這3種的吸附率和解析率來進行篩選。
3種大孔樹脂對水芹黃酮的吸附率和解析率見表3。
由表3可知,弱極性的AB-8型大孔樹脂對水芹黃酮的吸附率和解析率最大,分別為69.87%和72.57%,故選擇AB-8型大孔樹脂對水芹黃酮進行純化。分析其原因,可能是水芹黃酮中非極性物質相對比較少。
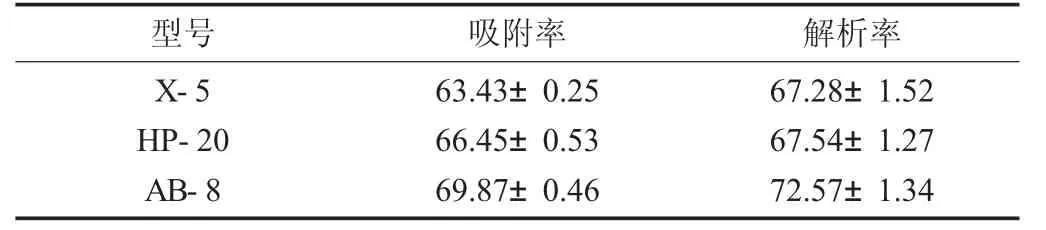
表3 3種大孔樹脂對水芹黃酮的吸附率和解析率/%
2.3 制備型液相色譜分析結果
芹菜素粗提物的制備液相色譜圖見圖2。
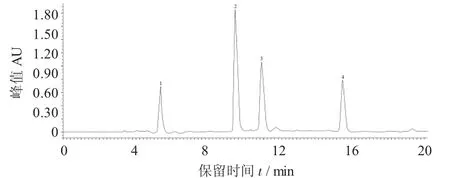
圖2 芹菜素粗提物的制備液相色譜圖
由圖2可以看出,黃酮化合物得到了較好的分離,分離出的單體有4種,出峰時間分別為5.35,9.45,11.01,15.38 min,其相對含量分別為12.23%,46.32%,23.34%,18.26%[19]。
芹菜素分析型高效液相色譜圖見圖3。
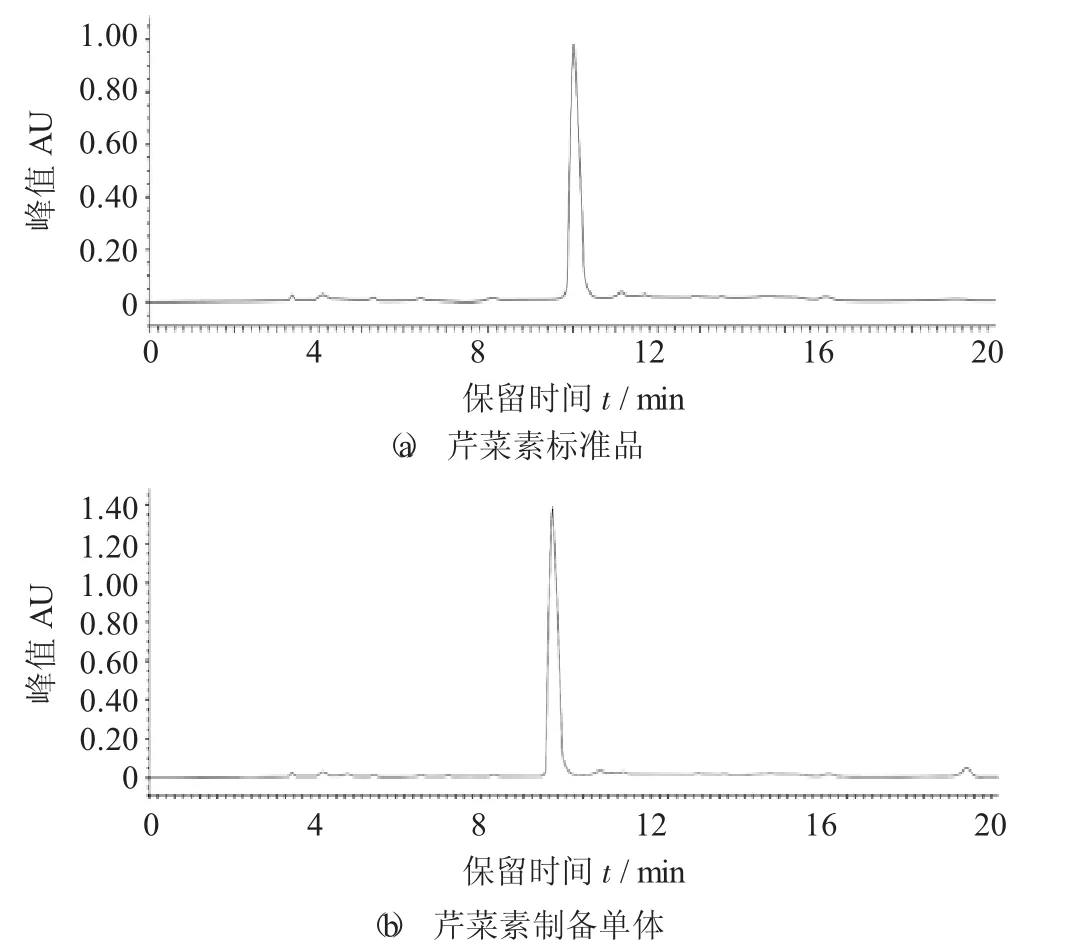
圖3 芹菜素分析型高效液相色譜圖
相同的色譜條件下,芹菜素標準品的高效液相色譜圖如圖3(a)所示,得出其出峰時間為10.06 min。通過制備液相收集出2號峰的液體。將收集的單體進一步進行高效液相分析,結果如圖3(b) 所示,其出峰時間為9.52 min,為單一色譜峰,制備效果較好。
2.4 質譜分析結果
芹菜素單體質譜圖見圖4。
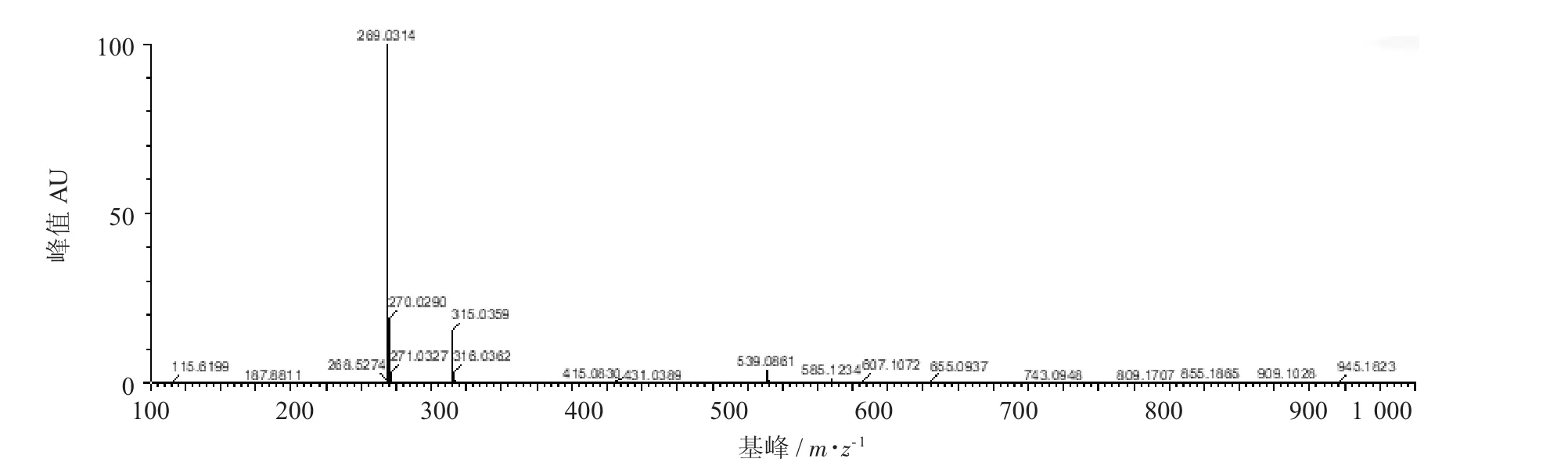
圖4 芹菜素單體質譜圖
由圖4可知,基峰269 m/z是芹菜素去質子化后形成的準分子離子峰,說明芹菜素具有較強的酸性,容易失去氫質子形成負離子而被檢測。質譜峰187 m/z和268 m/z等可能是269 m/z的碎片離子,另一些相對豐度較低的峰則可能來自溶液中電噴霧溶劑和樣品溶劑或芹菜素標準品所含的少許雜質[23]。
2.5 抗氧化活性研究結果
2.5.1 清除DPPH自由基能力
芹菜素對DPPH自由基清除能力見圖5。
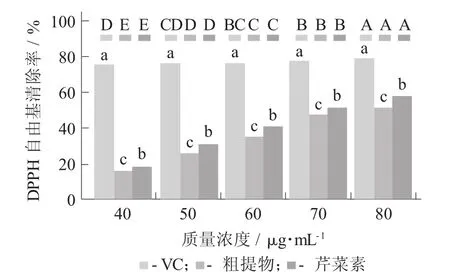
圖5 芹菜素對DPPH自由基清除能力
顯然,DPPH自由基清除能力與芹菜素單體的質量濃度呈正相關的關系,同一質量濃度下,芹菜素單體、粗提物和VC的清除能力大小為VC>芹菜素單體>粗提物。在質量濃度為60 g/mL時,VC的清除率高達94.83%。芹菜素能直接作用于DPPH自由基,其原因可能是其直接提供H+給DPPH自由基,也可能是其轉移電子到DPPH自由基。
2.5.2 清除羥基自由基(·OH)能力
芹菜素對羥基自由基清除能力見圖6。
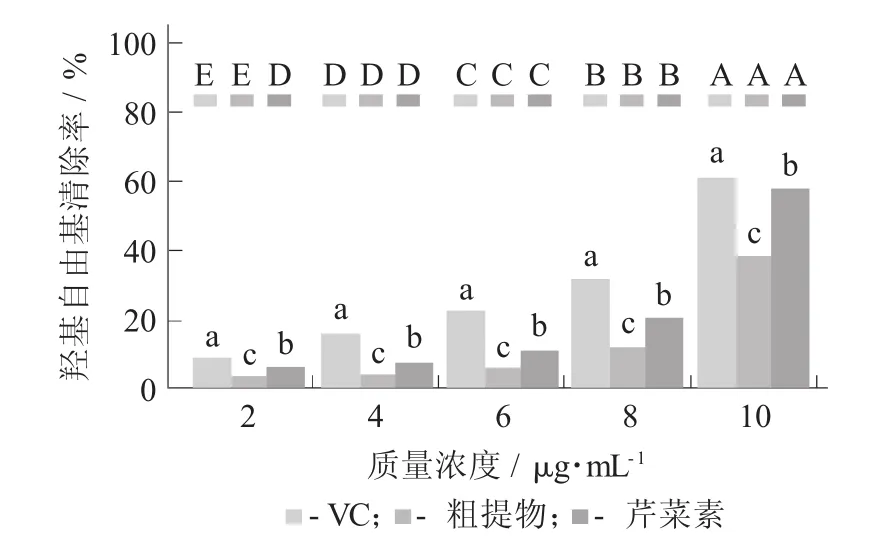
圖6 芹菜素對羥基自由基清除能力
由圖6可知,和清除DPPH自由基類似,VC的清除效果最好,芹菜素單體對羥基自由基的清除能力弱于VC,且羥基自由基清除能力與芹菜素單體的質量濃度呈正相關關系,同一質量濃度下,芹菜素單體、粗提物和VC的清除能力大小為VC>芹菜素單體>粗提物。在質量濃度為10 g/mL時,芹菜素單體和VC的清除能力接近,VC的清除率達到了60.82%,芹菜素單體的清除率為57.49%。這可能是因為芹菜素提供H+與·OH結合,使其還原成惰性化合物或穩定的自由基。
2.5.3 清除超氧陰離子(O2-·) 能力
芹菜素對超氧陰離子自由基清除能力見圖7。
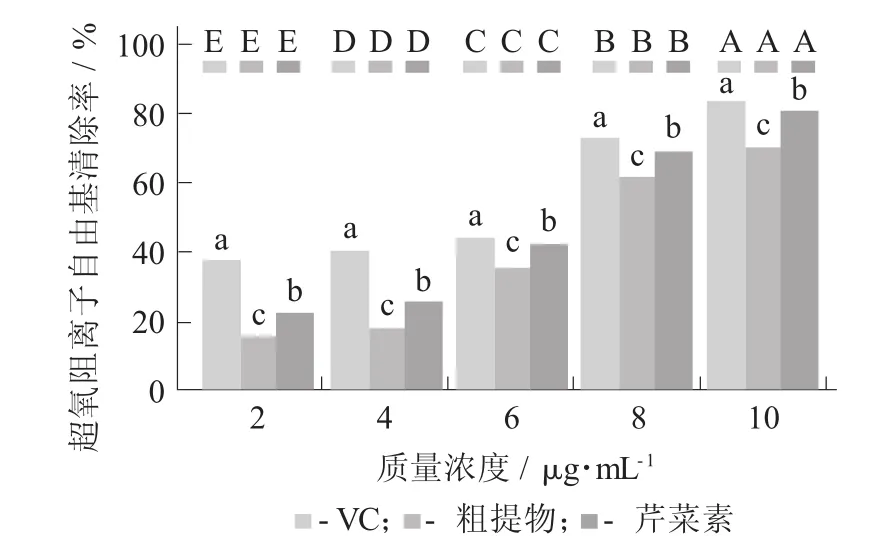
圖7 芹菜素對超氧陰離子自由基清除能力
很明顯,相同質量濃度下,芹菜素單體、粗提物和VC的清除能力大小為VC>芹菜素單體>粗提物。但在質量濃度為4 g/mL以上時,芹菜素單體和VC的清除能力相差不大;質量濃度為8 g/mL時,VC的清除率達到了82.64%,芹菜素單體的清除率為79.78%。關于清除O2-·的機理相關研究較少,猜測其原理與清除DPPH自由基和羥基自由基的原理相似,均提供不穩定的自由基。
3 結論
以水芹為原料,首先通過單因素試驗和四因素三水平正交試驗優化了水芹中黃酮的提取工藝,最佳提取工藝為料液比1∶35,提取溫度80℃,提取時間4 h,乙醇體積分數90%。通過大孔吸附樹脂對粗黃酮進行分離與純化,確定了AB-8型大孔吸附樹脂對粗黃酮的純化效果最好。通過制備液相色譜對粗黃酮進行分離純化,經高效液相色譜分析(HPLC) 和質譜進行驗證出分離的該物質為芹菜素單體,且純度較高。同時,芹菜素粗提物及單體對DPPH自由基、羥基自由基和超氧陰離子自由基都具有一定的清除能力,其中芹菜素單體的抗氧化性要大于粗提物,且芹菜素單體對超氧陰離子自由基的清除能力較強。

