主動脈夾層中層P53、MDM2及TRIM25的表達變化和VSMC表型轉化
任 偉 王志維 李博文 昌金星 王嘉慧
主動脈夾層(aortic dissection,AD)是心血管外科的常見的災難性疾病之一,其發生率呈逐年上升趨勢,目前認為主動脈中層平滑肌的退行性病變、炎癥、力學沖擊三者參與夾層的發生,平滑肌收縮對血流力學沖擊的拮抗是血管的穩態之一,一旦損傷容易誘發夾層。血管平滑肌細胞(vascular smooth muscle cells,VSMC)的表型轉化是主動脈中層退行性變的主要特征,但是其轉化的具體機制仍未闡明[1~3]。三基序蛋白25(tripartite-motif protein25, TRIM25)能夠通過泛素化參與多種細胞功能的調節,包括細胞周期調控和轉錄,主要在子宮、胚胎及主動脈組織中表達[4,5]。本研究通過對正常主動脈組織和夾層主動脈中層中TRIM25、P53、MDM2表達量變化和VSMC表型變化的研究,探討其在AD形成過程的作用及可能機制。
材料與方法
1.一般資料:選取2015年1月~2016年1月在武漢大學人民醫院行全弓替換手術患者12例作為AD組。納入標準:主動脈CTA明確診斷為A型主動脈夾層,發病1周以內;排除標準:馬方綜合征和特納綜合征等結締組織疾病,合并二葉式主動脈瓣畸形或胸部損傷,再次心臟手術者和CTA或術中發現嚴重的主動脈壁粥樣硬化。正常對照組的患者來自于心臟死亡捐獻者,無主動脈疾病史,其他排除標準同上。術前資料總結發現兩組患者年齡性別和體重無明顯差異,AD組合并高血壓者明顯高于正常組,詳見表1。術前簽署知情同意書,并獲得武漢大學人民醫院倫理委員會的批準。
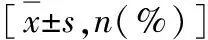
表1 AD組和正常對照組的基本特征
主要試劑骨橋蛋白(OPN)和(平滑肌肌動蛋白(α-SMA)兔單克隆抗體購于北京博奧森公司,P53和p-P53(Ser15) 鼠抗人單克隆抗體購于美國Santa Cruz公司,MDM2兔抗人單克隆抗體購于英國Abcam公司,TRIM25兔抗人單克隆抗體購于武漢三鷹公司,抗鼠/兔二抗購于美國Licor公司。
2.免疫組化染色:獲取升主動脈組織后去除主動脈外膜和內膜,保留中層組織,固定后石蠟包埋,4μm厚切片。石蠟切片二甲苯脫蠟 2 次,梯度乙醇水化,微波修復抗原10min,3%雙氧水孵育15min 以阻斷內源性過氧化物酶,PBS沖洗后5%山羊血清封閉,分別加入鼠抗人α-SMA、OPN、P53、TRIM25、MDM2一抗,稀釋比例為1∶100,HRP標記的抗鼠二抗37℃孵育30min;各步驟用PBS洗3min×3次,DAB顯色劑,蘇木素輕度復染,脫水透明后封片。在顯微鏡下觀察陽性染色區域為棕黃色或棕褐色顆粒;采用Image-Pro Plus 6圖像分析軟件(美國Media Cybernetics公司)對免疫組織化學染色進行計量分析。從每張切片中連續手動隨機取5個高倍視野(×200倍)。分別對切片免疫組織化學染色的陽性區域、陽性細胞數進行定量分析,計算每視野陽性染色的積分吸光度(IOD)值,并取積分吸光度之和。
3.Western blot法實驗:將取得的組織在1~2ml勻漿皿中于4℃ 生理鹽水中洗凈、稱量、研磨,加用400μl單去污劑裂解液PMSF,裂解30min后在4℃下12000r/min離心5min,取上清于0.5ml EP管,取少量蛋白提取液,使用PerkinElmer酶標儀測定蛋白含量(波長560nm),標本儲存于-80℃備用。將蛋白質樣品液與上樣緩沖液混合,煮沸5min,SDS-PAGE凝膠電泳分離蛋白,半干轉法(北京六一公司)將蛋白質轉至PVDF膜,室溫下用5%脫脂奶粉封閉2h,加入一抗GAPDH(1∶1000),α-SMA、OPN、P53、MDM2、TRIM25、p-P53(1∶500)。4℃過夜,加帶顯色劑的抗鼠二抗,室溫震動下孵育2h,TBST避光洗滌(5min×3次)后直接奧德賽掃膜儀(美國Licor公司)上掃膜,再對條帶進行背景調節和灰度值測定并分析。
4.RT-PCR檢測:稱取200mg超低溫凍存的主動脈中層組織使用液氮碾磨法碾磨成粉末,加入1ml Trizol溶液充分勻漿,將勻漿液轉移至EP管中,室溫靜置5min,向上述勻漿裂解液中加入1/5體積氯仿,充分混合至乳白色,室溫靜置5min,12000×g離心力 4℃離心15min,取上層無色上清液至另一EP管中,向上清液中加入0.5~1.0倍體積的異丙醇,上下顛倒充分混勻后室溫靜置10min,12000×g離心力 4℃離心10min,棄上清,加入與Trizol等體積的75%乙醇,輕輕顛倒洗滌,7500×g離心力 4℃離心5min后棄去上清,倒扣EP管干燥沉淀后,加入適量的RNase-free水溶解沉淀,紫外分光光度計檢測RNA的 純度和濃度。按照日本TaKaRa公司反轉錄試劑盒說明書(RR047A),反應分兩步,步驟一:取一PCR管,分別加入5×gDNA Eraser Buffer 2μl、gDNA Eraser 1μl、Total RNA 1μg,然后用RNase Free dH2O補足至10μl,于PCR儀上42℃保溫2min,迅速置冰上冷卻;步驟二:提前配制Master Mix,將步驟一的10μl反應液與Master Mix 10μl混勻后于PCR儀上按照37℃ 15min→85℃ 5s→4℃∞設定程序進行反應,上述所有反轉錄程序均為1個循環。反轉錄完成后按照TaKaRa公司RT-PCR試劑盒(RR820A)進行PCR,反應體系如下(總體積20μl):SYBR Premix Ex Taq 10μl+PCR Forward Primer (10μmol/L) 0.8μl+PCR Reverse Primer (10μmol/L) 0.8μl + ROX Reference Dye Ⅱ0.4μl+DNA模板2μl+dH2O 6μl;擴增程序如下:Stage 1(1 Reps): 95℃ 30s→Stage 2 (40 Reps): 95℃ 5s→60℃ 34s→Dissociation。所有引物均在上海生物工程股份有限公司合成,各基因引物序列如下:P53上游引物:5′-AGGTTGGCTCTGACTGTACC-3′,下游引物:5′-GATTCTCTTCCTCTGTGCGC-3′;MDM2上游引物:5′-CAGGCAGGGGAGAGTGATA-3′,下游引物:5′-GTGATGGAAGGGGGGGATT-3′;TRIM25上游引物:5′-AATACACGGAAATGAAGGCT-3′,下游引物:5′-AACTCATCCCTCTTGGTCAG-3′;β-actin 上游引物:5′-AGCGAGCATCCCCCAAAGTT-3′,下游引物:5′-GGGCACGAAGGCTCATCATT-3′。

結 果
1.免疫組化檢測主動脈中層平滑肌細胞變化:主動脈中層的主要細胞成分就是平滑肌細胞,免疫組化證實獲取組織主要細胞成分是α-SMA陽性的平滑肌細胞。已有研究表明VSMC由分化型轉變成未分化型會導致SMC收縮功能減弱,而這有可能導致主動脈中層組織薄弱。在本實驗中,分別檢測主動脈中層分化型VSMC表型標志物α-SMA和未分化型表型標志物OPN。通過免疫組化染色實驗發現,與正常對照組比較,在AD組血管中層的α-SMA含量顯著降低而OPN含量顯著升高,差異有統計學意義(P<0.01,圖1,表2)。

圖1 兩組主動脈α-SMA和OPN表達免疫組化(×200)與正常對照組比較,*P<0.01

表2 主動脈α-SMA和OPN免疫組化IOD值
2.免疫組化檢測主動脈中層P53、MDM2和TRIM25含量變化:通過免疫組化檢測發現AD組中層的P53、MDM2和TRIM25含量與正常對照組比較顯著增多,而p-P53蛋白表達量下降比較差異有統計學意義(P<0.01,圖2,表3)。

圖2 AD組和正常對照組主動脈中層(免疫組化,×200)與正常對照組比較,*P<0.01

表3 P53、MDM2、TRIM25和p-P53 IOD值
3.Western blot法檢測主動脈中層蛋白表達:與正常對照組比較,α-SMA和p-P53在AD患者主動脈組織內表達顯著降低(P<0.01),而在AD患者主動脈組織中OPN、P53、MDM2、TRIM25蛋白水平卻顯著增高,差異有統計學意義(P<0.01,表4,圖3)。
4.RT-PCR檢測結果:進一步通過RT-PCR檢測了P53、MDM2和TRIM25的mRNA表達,發現夾層組中P53、MDM2和TRIM25的mRNA表達量也增加(P<0.01,表5,圖4)。

表4 AD組和正常對照組相關蛋白表達水平

圖3 Western blot法檢測結果A.MDM2;B.TRIM25和P53;C.α-SMA、OPN和p-P53;與正常對照組比較,*P<0.01

mRNA正常對照組(n=12)AD組(n=12)P531.000±0.0002.235±0.203?MDM21.000±0.0001.697±0.203?TRIM251.000±0.0001.794±0.191?
與正常對照組比較,*P<0.01
討 論
AD的典型組織學特征是中層退行性變,目前對主動脈中層退行性變的分子機制正被廣泛研究,但尚未闡明[6]。大量研究顯示微纖維、膠原、蛋白聚糖和黏多糖、血管VSMC等主動脈壁的組成結構和功能異常是AD發生的病理基礎。而VSMC的表型轉化和凋亡在AD發生、發展中扮演重要角色,其受多種信號通路調節包括MAPK、PI3K和cAMP等[7,8]。最近發現P53 是 VSMC 分化的強誘導因子,P53 導致VSMC由去分化型向分化型轉化,分化型VSMC可以維持血管彈性和收縮血管,不易導致主動脈中層退行性變[9]。Leeper等也發現,CDKN2B缺失的情況下,P53 表達上調,動物模型主動脈瘤形成。在本實驗中也證實AD組中P53含量明顯增多,α-SMA含量減少,說明AD中VSMC由分化型向去分化型轉變。但這違背了 P53 作為VSMC 分化誘導因子的功能。

圖4 兩組P53、MDM2、TRIM25 mRNA表達水平與正常對照組比較,*P<0.01
P53下游轉錄激活產物之一是MDM2,它可以通過與P53結合形成復合物,維持低水平的P53蛋白表達進而抑制P53介導的轉錄活性,這個P53/MDM2反饋回路也是保持機體生理功能的重要機制之一。 如果出現了各種刺激因素包括低氧、DNA損傷和核苷酸缺失等情況會導致P53蛋白表達和轉錄活性迅速增加,從而激活下游的靶基因MDM2。當DNA修復后,負調節因子MDM2開始反饋抑制P53,從而防止P53的進一步作用[10,11]。而在本研究中發現AD組的MDM2含量較正常組顯著增加。在AD組主動脈中層組織中,Western blot法檢測MDM2的蛋白含量增加,并且通過 RT-PCR檢測筆者發現MDM2的mRNA含量較對照組增加數倍。所以,筆者推測在AD發病過程中,MDM2和P53的負反饋平衡被打亂:增加的P53促進MDM2的mRNA表達量增加,使 MDM2的mRNA表達量增多進而增加MDM2的蛋白含量,但是增加的MDM2蛋白不能降解P53蛋白,導致P53蛋白的穩定性增加并致使P53在AD中層組織中聚集。
MDM2可通過多種分子機制參與對P53的反饋抑制,包括:①P53的活性由多種因素決定,激活的P53在細胞核內激活其靶基因的轉錄,其降解在胞質中進行。核輸出序列(NES)和核定位序列(NLS)是MDM2具有核質穿梭能力的重要標志,亞細胞定位對于其抑制P53轉錄活性非常重要。如果P53在高表達狀態,細胞核中的P53可以被MDM2直接降解。如果P53在低表達狀態時,其轉錄激活位點可以被具有MDM2突變的NES結合,從而抑制P53活性; ②MDM2的N端具有疏水和芳香氨基酸形成的深溝,P53作為轉錄因子TFIID的組成部分與MDM2結合后抑制了其轉錄激活靶基因的能力; ③P53蛋白的特異性E3連接酶就是MDM2,其可以使P53蛋白和泛素相連接后泛素化P53,再被蛋白酶在細胞質中降解[12,13]。
而TRIM25作為一種泛素化E3連接酶,主要表達在胚胎、子宮、甲狀腺、主動脈和脾臟中表達,很少在其他組織中表達。有研究報道,在經雌激素治療過的乳腺癌患者中可檢測到高水平的TRIM25、P53和MDM2的表達[14]。而本研究發現夾層組的TRIM-25蛋白和mRNA水平的表達量均顯著增加。因而筆者推測可能由于夾層中TRIM-25的表達量增加競爭性抑制MDM2與P53的泛素化降解從而增加P53含量。但是P53的活性受到抑制,從而不能誘導VSMC分化,通過Western blot法檢測也發現夾層組P53的磷酸化水平降低。
綜上所述,AD主動脈中層中P53、MDM2及TRIM 25表達量均顯著增加,主動脈中層中VSMC表型向去分化型轉變,可能是由于P53/MDM2反饋環平衡被TRIM25打亂所致。但是P53、MDM2及TRIM25在主動脈中層組織中的增多究竟是AD發病之前的誘因或者是其發病之后的結果,同時高血壓對血管平滑肌細胞的影響如何?這需要進一步在體外細胞和動物實驗來驗證TRIM-25的過表達是否會導致MDM2和P53結合障礙從而引起其含量增加,導致VSMC表型和功能發生變化。

