脂蛋白a和超敏C反應蛋白聯合檢測對糖尿病腎病早期診斷的臨床價值
孫文早 李紅玲 范麗娜 鄒 毅 黃 晶 秦前安 崔梅芳
2010年,全球成年糖尿病患者約為2.85億,預計到2030年糖尿病患者將增加1倍以上,高達4.39億[1]。但國際糖尿病聯盟最新公布數據顯示在2017年全球糖尿病患者已達4.25億,估計到2045年糖尿病患者將達到6.29億。我國糖尿病發生率也急劇增加,目前成為僅次于心血管和腫瘤之后的第3大疾病[2]。2型糖尿病為一種胰島素抵抗、脂代謝、高血壓、高血糖和肥胖等聯合構成的代謝紊亂綜合征,是一種自身免疫性和慢性炎癥所引起的血糖升高的慢性疾病,常伴其他并發癥存在[3]。糖尿病腎病(diabetic nephropathy,DN)是糖尿病的慢性并發癥之一,在我國DN的發生率每年呈遞增趨勢,也是糖尿病并發癥中致殘、致死的重要原因[4]。目前,2型糖尿病腎病的發病機制尚不明確,患者尿蛋白的檢測常作為臨床診斷糖尿病腎病的重要證據[5, 6]。由于DN呈進行性發展,并且這種改變是不可逆的,所以對患者的預后和生命質量造成了嚴重影響,并且治療難度較大,無特效藥物能改變這種變化。因此早期對DN進行診斷,并進行相應治療,將對提高患者生存質量,延長患者生命具有重要意義。本研究通過探討2型糖尿病患者血清中Lp(a)及 hs-CRP 的含量及兩者聯合檢測對糖尿病腎病病情發展的相關性,旨在為DN患者的早期診斷、臨床轉歸、以及終末期發展方向提供新思路。
材料與方法
1.一般資料:選取2016年9月~2017年6月來筆者醫院住院就診治療的2型糖尿病患者120例,糖尿病的診斷根據1999年WHO糖尿病診斷標準確診。其中男性65例,女性55例,患者年齡45~70歲,病程2~21年。根據24h尿蛋白排泄率(UAER)將其分為兩組,其中單純糖尿病組73例,UAER<30mg/24h;糖尿病腎病組47例,UAER>30mg/24h。另選筆者醫院同期健康體檢者50例作為本研究的健康對照組,其中男性34例,女性16例,年齡35~81歲,均無器質性病變,血糖、血脂、UAER 均在正常范圍,尿糖均為陰性。該實驗方案經醫院醫學倫理委員會批準并經患者知情同意。
2.血清Lp(a)和 hs-CRP的檢測:所有研究對象均空腹8~12h,于次日清晨空腹抽靜脈血3ml,分離血清檢測血清Lp(a)及 hs-CRP,同時留取24h尿(晨起8:00時~次日8:00時)。免疫比濁法測定UAER。 UAER計算公式:UAER=尿白蛋白(mg/ml)×24h 尿量(ml)。筆者醫院檢驗科檢測各組Lp(a)、hs-CRP水平。脂蛋白a和hs-CRP試劑由北京利德曼公司提供,采用德國Roche公司COBAS6000全自動生化分析儀分別檢測,使用與試劑配套的校準品及質控品。

結 果
1.一般臨床資料比較:各組性別、年齡、體重、身高等比較,差異無統計學意義(P> 0.05),詳見表1。
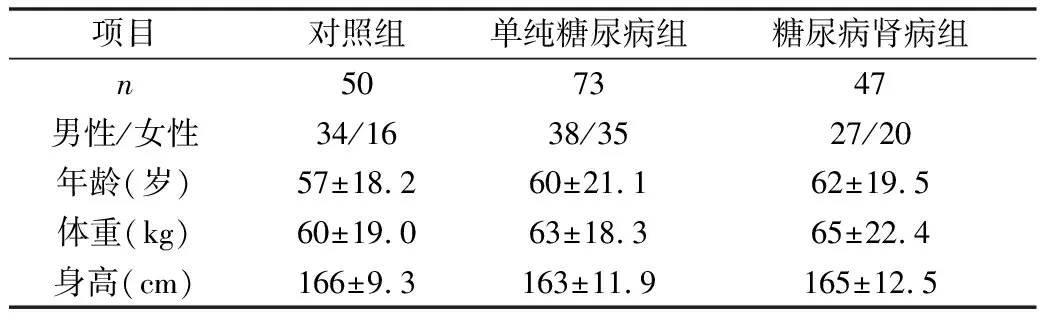
表1 一般臨床資料比較
2.3組Lp (a)、hs-CRP及UAER的比較:與對照組比較,單純糖尿病組與糖尿病腎病組UAER增加,Lp (a)、hs-CRP水平增高,差異有統計學意義(P<0.01)。同時,隨著2型糖尿病發展,即隨著UAER逐步升高,與單純糖尿病組比較,糖尿病腎病組Lp (a)、hs-CRP均顯著升高,差異有統計學意義(P<0.05),詳見表2。
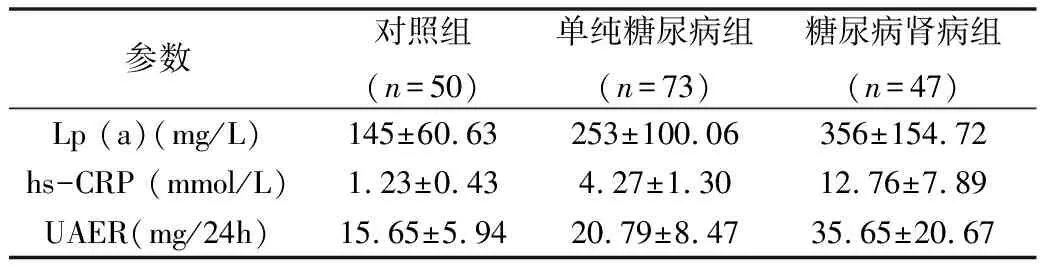
表2 3組中Lp(a)、hs-CRP及UAER的比較
3.Lp (a)、hs-CRP與UAER相關性分析:多因素線性相關分析顯示,Lp (a)、hs-CRP與UAER均呈顯著正相關(r=0.387,P<0.05;r=0.782,P<0.01), Lp(a)與 hs-CRP 變量間呈顯著正相關(r=0.793,P<0.05)。
討 論
研究表明,我國2 型糖尿病的發生率呈逐年上升的趨勢,且其嚴重并發癥DN患者也逐年增多,糖尿病腎病患者死亡的主要原因為長期的高血糖刺激導致腎臟嚴重受損,最終致腎衰竭,嚴重威脅患者的生命健康[7]。DN患者臨床表現可以分為5期,即腎小球高濾過和腎臟肥大期、正常白蛋白尿期、早期糖尿病腎病期(持續微量白蛋白尿期)、臨床糖尿病腎病期和終末期腎衰竭期。由于DN病情進展緩慢,起病較隱匿,糖尿病腎病早期僅表現為腎小球體積輕微增大,基膜輕微增厚,腎小球濾過率相對增加,但相關尿蛋白的監測則完全在正常范圍內,即便是糖尿病腎病Ⅲ期,其臨床表現也僅為微量蛋白尿,現有診斷方法很難發現,部分實驗室檢測指標特異性與敏感度仍處于探索階段,故急需尋求特異性與靈敏性較高的實驗室診斷指標,早期發現DN,早期進行相關治療[8~10]。
2型糖尿病作為一種慢性炎性疾病,高血糖導致患者的血清Lp(a)含量增加,對冠狀動脈粥樣硬化、腎動脈硬化以及其他部位的動脈硬化起著重要的作用。近年來隨著脂質學說和炎癥學說概念的提出,Lp(a)和重要的急性時相反應蛋白hs-CRP在糖尿病及DN的發生、發展中的作用逐漸引起人們的關注[11, 12]。因此本研究通過對正常健康對照者、糖尿病患者及DN患者血清中Lp(a)、hs-CRP與UAER的檢測,探究Lp (a)、hs-CRP與糖尿病患者及DN患者之間的關系,為DN患者的早期診斷提供重要的臨床依據。
研究顯示,Lp(a)常沉積于腎小球微血管中,經氧化或糖基化修飾后,導致腎小球肥大及其他相應的病變。當Lp(a)升高,糖尿病微血管病變程度增加[13, 14]。糖尿病所導致的微血管病變中,Lp(a)升高能導致纖溶酶原的活性受到抑制[15]。本研究通過對3組檢測對象血清中Lp(a)及hs-CRP的檢測,發現單純糖尿病組與DN組UAER增加,Lp(a)、hs-CRP水平明顯增高,同時隨著2型糖尿病發展,即隨著UAER逐步增加,與單純糖尿病組比較,DN組Lp (a)、hs-CRP也顯著升高,這表明Lp(a)在糖尿病及DN的發生發展過程具有重要作用,同時也顯示出Lp(a)在DN的早期診斷中的重要意義。
而作為慢性炎癥型疾病的2型糖尿病,由于糖尿病患者自身持續高血糖濃度,從而導致患者血流變的變化,繼發機體的炎性反應。同時由于患者早期脂質等在腎臟的沉積,導致腎小球毛細血管變性硬化,進一步加重腎臟本身的缺血缺氧性改變,形成惡性循環,導致糖尿病患者處于高hs-CRP狀態,導致DN的形成,這也是DN形成的一個重要原因[16]。因此,這種模式會形成一種遞增性的循環,導致血清Lp(a)、hs-CRP水平與腎臟的損害程度呈正相關。而本研究通過多因素線性相關分析也顯示, Lp(a)、hs-CRP與UAER均呈顯著正相關,Lp(a)與 hs-CRP 變量間呈顯著正相關。
綜上所述,通過當前對2型糖尿病及其發展致DN過程致病機制的認識,同時結合本研究,筆者提出2型糖尿病患者通過Lp(a)、hs-CRP的檢測能早期間接反映患者的腎臟損害程度,尤其當兩者聯合檢測時,更能及時預警患者腎功能的減退與損傷,起到早發現、早治療的理想效果。

