前體物和誘導子對內生真菌CH1產乙基長春胺的影響
任娜,劉佳佳,楊棟梁,徐士杰,欒明寶,趙娜娜,彭櫻子,吳義強,袁光明
?
前體物和誘導子對內生真菌CH1產乙基長春胺的影響
任娜1, 2,劉佳佳1,楊棟梁1,徐士杰1,欒明寶3,趙娜娜1,彭櫻子1,吳義強4,袁光明4
(1. 中南大學 化學化工學院,湖南 長沙,410083; 2. 湖南科技職業學院 藥學院,湖南 長沙,410118; 3. 中國農業科學院 麻類研究所,湖南 長沙,410205; 4. “木竹資源高效利用”湖南省高校2011協同創新中心,湖南 長沙,410004)
為了提高內生真菌CH1.次級代謝產物乙基長春胺的產量,首先采用單因素試驗法考查環氧合酶抑制劑萘普生、羥化酶誘導子過氧化氫、前體物色氨酸、色胺、馬錢子苷及裂環馬錢子苷對內生真菌CH1產乙基長春胺的影響;在單因素試驗的基礎上,采用SPSS(統計產品與服務解決方案)19.0設計L18(36)正交試驗,進一步優化各前體物和誘導子的質量濃度,并在最優條件下進行試驗驗證。研究結果表明:在內生真菌CH1發酵液中添加前體物和誘導子均對內生真產乙基長春胺有顯著影響(顯著性概率小于0.05);當萘普生、色氨酸、色胺、馬錢子苷和裂環馬錢子苷質量濃度分別為8,100,95,105和25 mg/L,過氧化氫質量濃度為20 μg/L時,能有效提高乙基長春胺的產量,在此條件下進行驗證試驗,乙基長春胺產量可達5.09 mg/L,與不加前體物質相比提高2.63倍。
前體;誘導子;內生真菌;乙基長春胺
長春胺(vincamine)是從小蔓長春花(L.)中分離得到的一種吲哚生物堿。長春胺類生物堿如長春胺、半合成的長春西汀、乙基長春胺等具有增加腦血流、促進腦部氧的利用及保護神經元等多種有益于腦、心血管、血液循環等系統的藥理作用[1?3],在臨床上常用于治療腦梗塞后遺癥、腦出血后遺癥、腦動脈硬化癥,已成為治療老年癡呆的重要藥物。隨著我國進入老齡化社會,具有治療老年癡呆功能的長春胺類藥物具有巨大市場潛力和社會效益。但由于小蔓長春花中長春胺含量低,長春胺的化學全合成法不具備應用價值;而半合成法所需的馬鈴果()種子供應不穩定,使得長春胺類生物堿的產量有限,限制了它們的廣泛應用[4?6],因此,尋求解決長春胺類藥物供應問題的新方法很有必要。1993年,STIERLE等[7]從短葉紅豆杉()中分離出1株產紫杉醇內生真菌(),促進了內生真菌合成藥物分子和藥物先導化合物的研究[8?11]。目前,從內生真菌中篩選產長春胺類生物堿菌株的研究已取得一些進展。YIN等[12]從小蔓長春花的莖、葉片和根中篩選得到1株具有產長春胺類生物堿能力的內生真菌,產率約為0.1 mg/L。楊顯志等[13]也進行了關于產長春新堿的長春花內生真菌的研究。REN等[14]從夾竹桃植物的根、莖、葉中分離得到11株內生真菌,經TLC,HPLC和LC-MS分析,發現其中1株內生真菌CH1()的代謝產物中含有長春胺、乙基長春胺、它波寧等多種長春胺類生物堿,其中它波寧和乙基長春胺從內生真菌中獲得,這成為獲得它波寧和乙基長春胺的新途徑。但由于其含量不高,產長春胺類生物堿內生真菌用于工業化生產還需進一步提高產量才能實現。在培養基中添加前體物質是一種提高長春胺類生物堿產量的有效方法[15?17]。MCCOY等[18]通過在長春花細胞培養體系中添加不同的色氨酸衍生物獲得了不同于原長春花中生物堿的新型吲哚生物堿。在長春花細胞培養體系中添加色胺、色氨酸,馬錢子苷等前體物質,對長春胺類生物堿的合成均有顯著影響[17, 19?23]。目前,還沒有在長春胺類生物堿內生真菌中生物堿合成前體調控的報道,為此,本文作者根據植物細胞培養體系中長春胺類生物堿合成的生物途徑相關報道,采用單因素和SPSS正交試驗設計,以乙基長春胺產量為優化目標,探究環氧合酶抑制劑萘普生、羥化酶誘導子過氧化氫、前體物質色胺、色氨酸、馬錢子苷、裂環馬錢子苷等對實驗室分離得到的內生真菌CH1.發酵生產乙基長春胺的影響,以便為進一步研究產乙基長春胺內生真菌的生物合成途徑提供參考,同時為工業化大規模生產提供技術基礎。
1 試驗
1.1 菌株與試劑
試驗用菌株為本課題組從夾竹桃科植物中分離得到的產乙基長春胺內生真菌CH1(.)[14],其菌株保存號為CCTCCM 2014676。試驗用色氨酸和萘普生為生化試劑、過氧化氫、色胺、馬錢子苷、裂環馬錢子苷,均為分析純。
1.2 培養基
固體培養基(potato dextrose agar,PDA):土豆,質量分數為20%(去皮切塊,煮沸20 min后,過濾取汁);葡萄糖質量分數為2%;瓊脂質量分數為2%。
發酵培養基:土豆,質量分數為20%;葡萄糖、蔗糖、牛肉膏、無水硫酸鎂質量分數分別為1%,1%,1%和0.05%;水;pH為7。
1.3 菌株發酵培養及代謝產物的提取
將實驗室保存的內生真菌菌種CH1接種到PDA培養基上,于27 ℃條件下活化3 d,然后接種到裝有100 mL發酵培養基的250 mL錐形瓶中,于溫度為 27 ℃、轉速為170 r/min條件下培養3 d后,移至潔凈工作臺上,根據實驗需求往其中添加相關的前體物質(孔徑為0.22 μm的微孔濾膜過濾),再置于27 ℃恒溫培養箱中靜置培養4~5 d。待發酵完成后,采用4層紗布將發酵液和菌絲體分離。將菌絲體置于60 ℃干燥后搗碎,用10倍體積的二氯甲烷浸泡過夜、抽濾,收集二氯甲烷,反復進行3次。將發酵液于旋轉蒸發儀(溫度為45 ℃)減壓濃縮至約100 mL,用等體積的二氯甲烷重復萃取3次,合并所有二氯甲烷,并在旋轉蒸發儀上于30 ℃時減壓濃縮至體積為10 mL,用直徑為0.22 μm的微孔濾膜過濾除菌,置于溫度為4 ℃的冰箱保存,備用。
1.4 乙基長春胺含量測定
采用高效液相色譜(high performance liquid chromatography,HPLC)法進行測定。色譜條件如下:色譜柱為C18柱(4.6 mm×250 mm,5 μm);流動相為乙腈、水(兩者體積比為2:1);流速為1 mL/min;檢測波長為240 nm;柱溫為室溫;進樣量為20 μL;以實驗室自制乙基長春胺為對照品。
1.5 試驗設計
為了提高乙基長春胺的含量,首先采用單因素試驗法考查不同配比的環氧合酶抑制劑萘普生(4,6,8,10和12 mg/L)、前體物質(色氨酸(40,60,80,100和120 mg/L)、色胺(40,60,80,100和120 mg/L)、馬錢子苷(40,60,80,100和120 mg/L)、裂環馬錢子苷(10,20,30,40和50 mg/L))和羥化酶誘導子過氧化氫(10,15,20,25和30 μg/L)對內生真菌CH1產乙基長春胺的影響。在單因素試驗的基礎上,采用SPSS 19.0設計L18(36)正交試驗進一步優化前體物質及誘導子。
1.6 數據分析
結果采用SPSS 19.0 進行數據統計和分析,作圖軟件為Origin 7.5。
2 結果與討論
2.1 環氧合酶抑制劑萘普生質量濃度對乙基長春胺產量的影響
圖1所示為萘普生質量濃度對內生真菌CH1產乙基長春胺產量的影響。由圖1可知:較低質量濃度的萘普生能快速促進乙基長春胺的累積;隨著萘普生質量濃度增大,乙基長春胺的產量也隨之提高,當萘普生質量濃度達到8 mg/L以后,乙基長春胺含量又逐漸趨于穩定,這可能與內生真菌體內環氧合酶的活性有關。在長春胺類生物堿的合成途徑中,環氧合酶為蛇根堿生物合成途徑中的關鍵酶,而萘普生為環氧合酶抑制劑,可特異性阻斷蛇根堿的生物合成路徑,使得流向長春胺支路的中間代謝物增多,從而使乙基長春胺的合成能力增強。VERMA等[17]發現萘普生的加入可促進長春胺類生物堿的合成,這與本試驗結果基本一致。
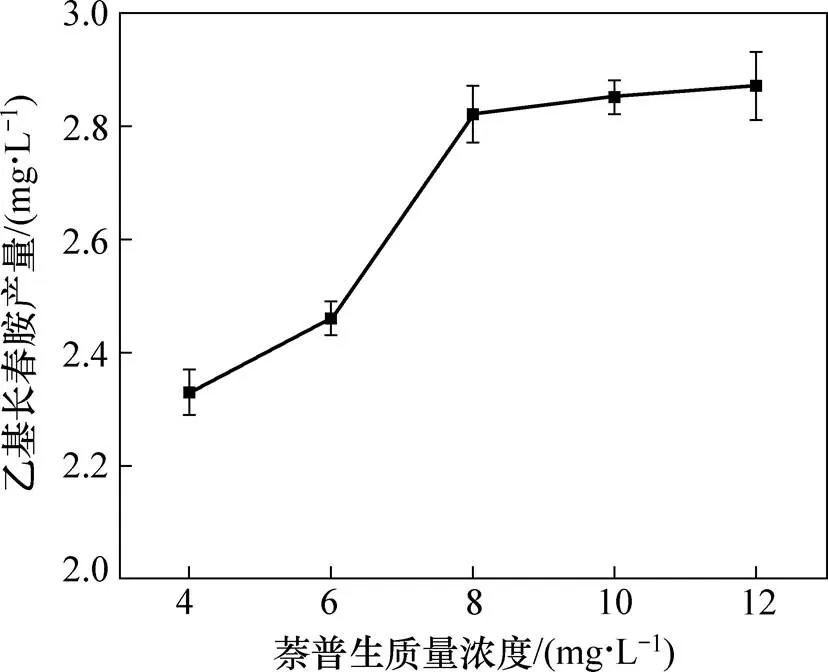
圖1 環氧合酶抑制劑萘普生質量濃度對內生真菌CH1乙基長春胺產量的影響
2.2 羥化酶誘導子過氧化氫質量濃度對乙基長春胺產量的影響
圖2所示為羥化酶誘導子過氧化氫質量濃度對乙基長春胺產量的影響。由圖2可知:首先增加過氧化氫質量濃度,乙基長春胺產量也隨之增加;而當過氧化氫質量濃度大于20 μg/L時,乙基長春胺產量呈下降趨勢,這可能是因為高質量濃度的過氧化氫對內生真菌CH1有毒害作用,從而使其乙基長春胺的產量下降,因此,可以認為乙基長春胺產量在過氧化氫質量濃度為20 μg/L達到最大值。過氧化氫為強氧化劑,可以增強還原型輔酶Ⅱ(NADPH)氧化酶、細胞氧化酶和羥化酶的活性。在長春胺類生物堿生物合成過程中,過氧化氫作為羥化酶誘導子,可以起到抑制長春質堿、使它波寧的合成量增加的作用。它波寧在生物體內將進一步轉化為乙基長春胺[17, 20],因此,為了提高羥化酶和過氧化酶的活性,可以通過向發酵液中加入羥化酶誘導子過氧化氫,進而達到提高乙基長春胺產量的目的。
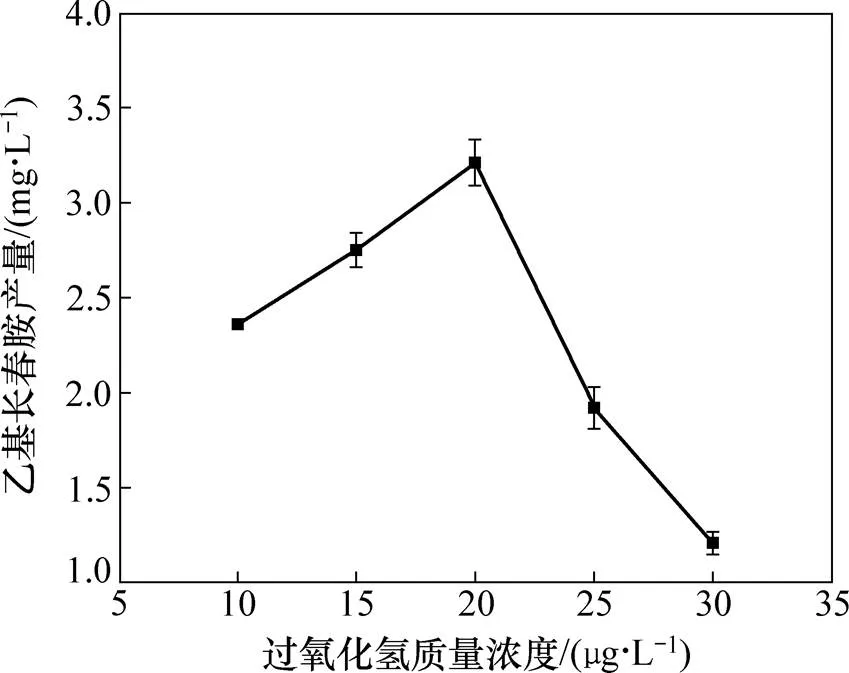
圖2 羥化酶誘導子過氧化氫質量濃度對內生真菌CH1乙基長春胺產量的影響
2.3 不同前體物對乙基長春胺產量的影響
圖3所示為不同前體物對乙基長春胺產量的影響。由圖3可知:當色氨酸、色胺、馬錢子苷和裂環馬錢子苷的質量濃度分別低于100,100,100和30 mg/L時,隨著前體物質量濃度的增大,乙基長春胺的產量也隨之提高。當色氨酸、色胺、馬錢子苷和裂環馬錢子苷的質量濃度分別超過100,100,100和30 mg/L時,乙基長春胺的產量呈下降趨勢,這可能是因為前體物過高的質量濃度不利于菌絲體的生長,進而影響次級代謝產物的累積。所以,當前體物質量濃度增加到一定程度時,乙基長春胺的產量呈下降趨勢。綜上可知:當色胺酸、色胺、馬錢子苷、裂環馬錢子苷質量濃度分別為100,100,100和30 mg/L時,可獲得較高產量的乙基長春胺。馬錢子苷為非甲羥戊酸途徑(MEP)途徑的中間產物,裂環馬錢子苷為MEP途徑的終產物,色胺和色氨酸為莽草酸途徑的中間產物,色氨酸在色氨酸脫羧酶(TDC)的作用下脫羧產生色胺。長春胺類生物堿的生物合成途徑起始于裂環馬錢子苷與色胺縮合形成的異胡豆苷[19, 23],因此,這4種物質均相當于長春胺類生物堿生物合成的前體物質。添加適當質量濃度的該類前體,可提高乙基長春胺的產量。
2.4 正交試驗設計及結果
為了考查各因素之間的關系,進一步優化各前體物及誘導子對內生真菌CH1產乙基長春胺的影響,應用SPSS 19.0軟件,設計萘普生、色氨酸、色胺、馬錢子苷、裂環馬錢子苷、過氧化氫這6種因素的3水平正交試驗L18(36)。表1所示為正交試驗結果及極差分析結果,根據極差分析法原理可知,極差越大,對乙基長春胺產量的影響程度越大。因此,由表1中判斷6個因素對乙基長春胺產量的影響程度從大至小依次為過氧化氫、裂環馬錢子苷、色胺、萘普生、馬錢子苷和色氨酸。表2所示為正交試驗方差分析結果。由表2可知,萘普生、色氨酸、色胺、馬錢子苷、裂環馬錢子苷、過氧化氫的分別為0.004,0.030,0.002,0.014,1.173×10?5和3.941×10?8,表明各前體物及誘導子對內生真菌CH1發酵產乙基長春胺的影響均顯著(顯著性概率<0.05),其中以過氧化氫的影響最為顯著,萘普生次之。綜合表1和表2中結果確定適合內生真菌CH1產乙基長春胺的最佳前體物及誘導子組合的質量濃度為:萘普生8 mg/L,色氨酸100 mg/L,色胺95 mg/L,馬錢子苷105 mg/L,裂環馬錢子苷25 mg/L,過氧化氫20 μg/L。可以推斷內生真菌CH1產長春胺類生物堿的前體物質與長春花植物細胞中的前體物質非常相似[17, 20]。在該試驗中,研究了1種羥化酶誘導子、1種環氧合酶抑制劑和4種前體物質對菌株CH1產乙基長春胺的影響,結果表明其產量有一定程度提高,但仍不能用于工業大規模生產,需對其進行進一步研究,如對內生真菌CH1菌株進行誘變育種和原生質體融合研究,以篩選出遺傳穩定的高產菌株;研究內生真菌CH1中乙基長春胺的生物合成途徑,通過其生物合成途徑,選擇有效的前體物及誘導子等,以提高乙基長春胺產量。
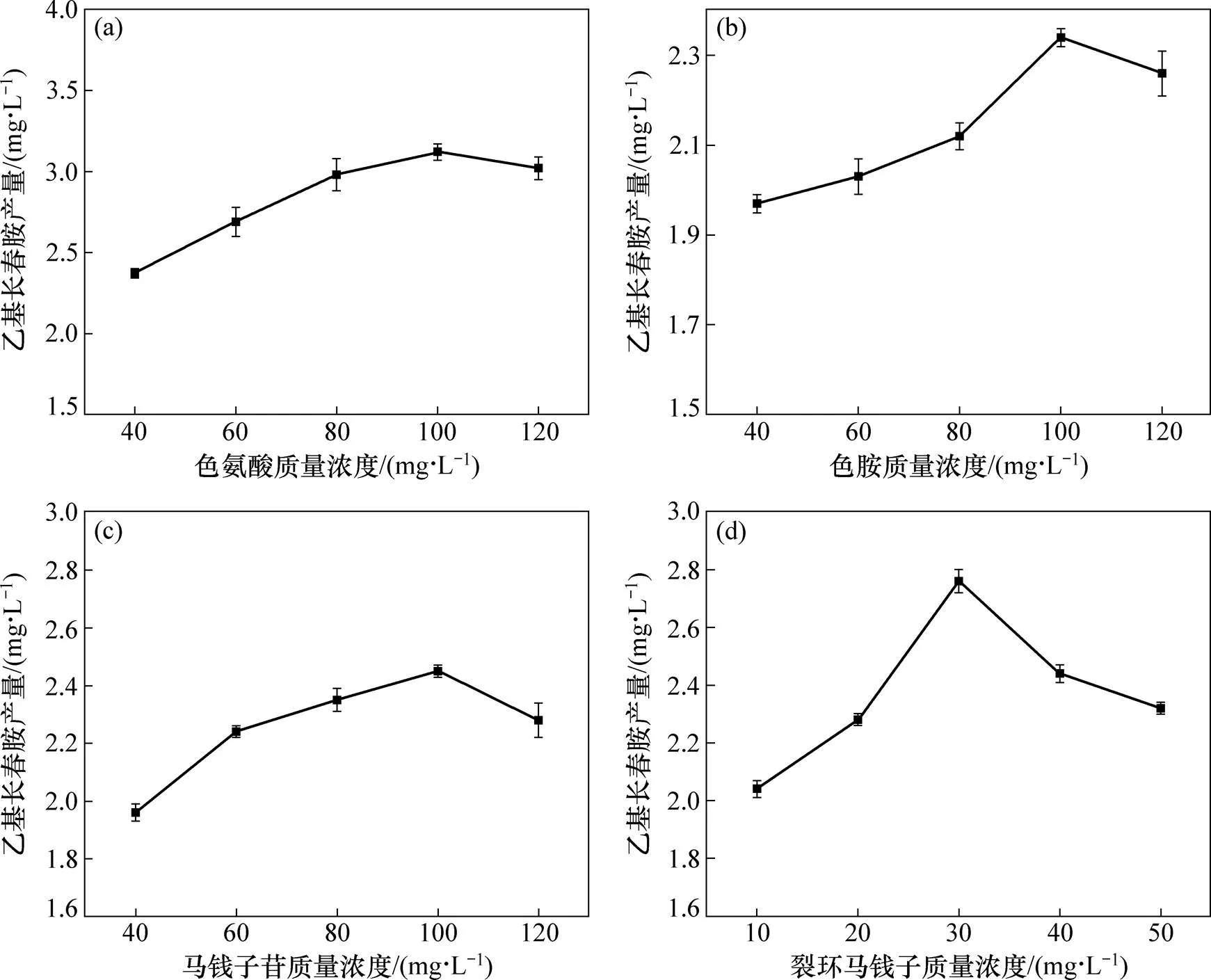
(a) 色氨酸;(b) 色胺;(c) 馬錢子苷;(d) 裂環馬錢子苷
注:1,2和3分別代表每個因素不同水平下的乙基長春胺產量的平均值;為極差。
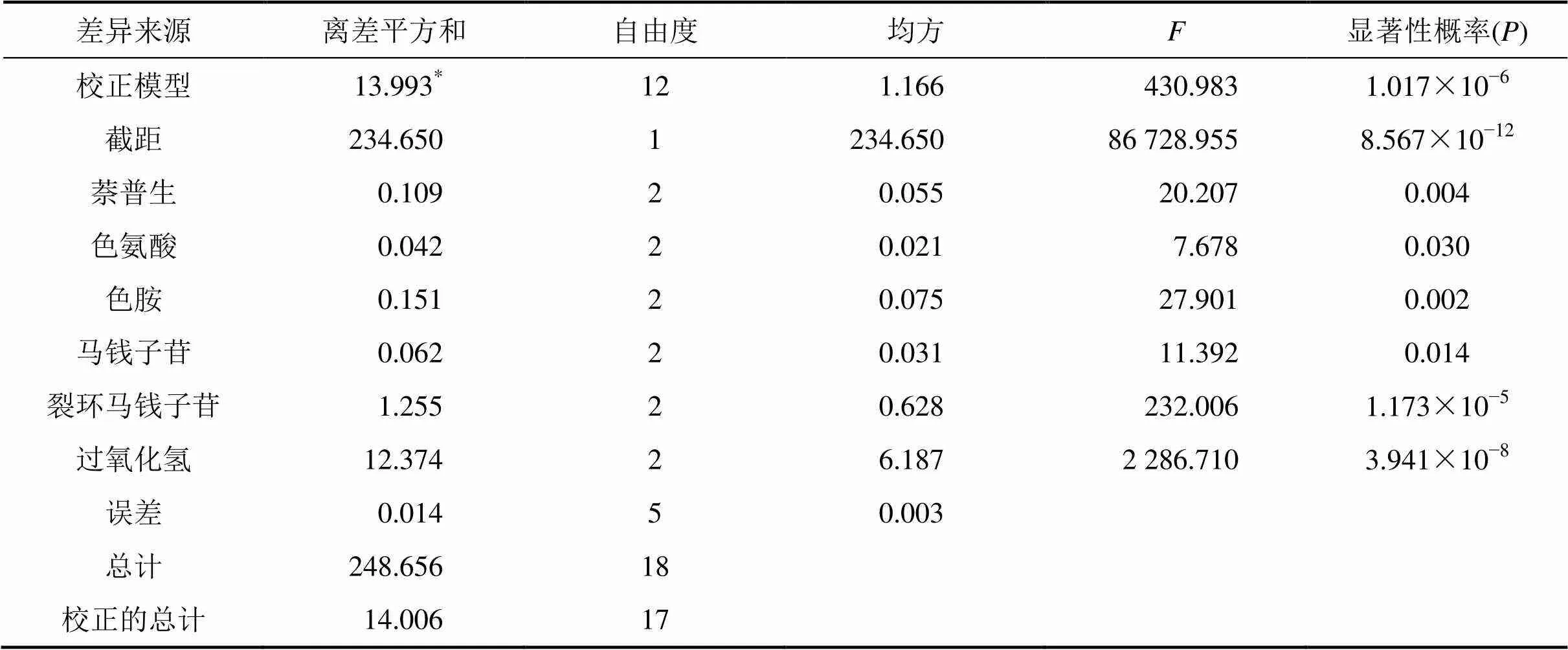
表2 正交試驗方差分析
*:2為判定系數,2=0.999(調整2=0.997);為各因素均方與隨機誤差均方的比值。
2.5 驗證試驗
在優化后的條件下,對內生真菌CH1進行發酵培養,其代謝產物中乙基長春胺的產量為5.090 mg/L,與不添加前體物時乙基長春胺產量(1.932 mg/L)[14]相比提高了2.63倍,表明優化后的前體物質及誘導子對內生真菌CH1中乙基長春胺的生物合成有促進作用。
3 結論
1) 在內生真菌CH1sp.發酵液中添加前體物和誘導子,有利于提高乙基長春胺的產量。
2) 在單因素試驗的基礎上進行SPSS L18(36)正交試驗設計,當環氧酶抑制劑萘普生、前體物質色氨酸、色胺、馬錢子苷和裂環馬錢子苷質量濃度分別為8,100,95,105和25 mg/L、誘導子過氧化氫質量濃度為20 μg/L時,可得到最大乙基長春胺產量5.12 mg/L,在此條件下進行驗證試驗,得到乙基長春胺產量為5.09 mg/L,較不加前體物和誘導子時提高2.63倍,乙基長春胺產量顯著提高。因此,尋找對內生真菌合成乙基長春胺具有重要影響的前體物質,對提高菌株CH1產乙基產春胺的能力具有重要意義,同時可為后續的發酵工藝研究提供參考。
[1] BAGOLY E, FEHéR G, SZAPáRY L. The role of vinpocetine in the treatment of cerebrovascular diseases based in human studies[J]. Orvosi Hetilap, 2007, 148(29): 1353?1358.
[2] SABRY S M, BELAL T S, BARARY M H, et al. A validated HPLC method for the simultaneous determination of vincamine and its potential degradant (metabolite), vincaminic acid:applications to pharmaceutical formulations and pharmacokinetic studies[J]. J Food Drug Ana, 2010, 18(6): 447?457.
[3] SAURABH C V, KISHOR N G. Vinpocetine:hype,hope and hurdles towards neuroprotection[J]. Asian J Pharm Res Dev, 2013, 1(4): 17?23.
[4] ALVES J C F, SIMAS A B C, COSTA P R R. Formal enantioselective synthesis of (+)-vincamine. The first enantioselective route to (+)-3, 14-epivincamine and its enantiomer[J]. Tetrahedron: Asymmetry, 1999, 10(2): 297?306.
[5] NEMES A, SZANTAY C J, CZIBULA L, et al. Synthesis of 18-hydroxyvincamines and epoxy-1,14-secovincamine: A new proof for the aspidospermane-eburnane rearrangement[J]. Heterocycles, 2007, 71(11): 2347?2362.
[6] ELES J, KALAUS G, LEVAI A, et al. Synthesis of vinca alkaloids and related compounds 98. oxidation with dimethyldioxirane of compounds containing the aspidospermane and quebrachamine ring system: a simple synthesis of (7S, 20S)-(+)-rhazidigenine and (2R, 7S, 20S)-(+)-rhazidine[J]. Journal of Heterocyclic Chemistry, 2002, 39(4): 767?771.
[7] STIERLE A, STROBLE G, STIERLE D. Taxol and taxane production by Taxomyces andreanae,an endophytic fungus of Pacific yew[J]. Science, 1993, 260(5105): 214?216.
[8] 陳建華, 劉佳佳, 臧鞏固, 等. 紫杉醇產生菌的篩選與發酵條件的調控[J]. 中南大學學報(自然科學版), 2004, 35(1): 65?69.CHEN Jianhua, LIU Jiajia, ZANG Gonggu, et al. Screening of taxol-producing endophytic fungi and regulation of fermentation conditions[J]. Journal of Central South University(Science and Technology), 2004, 35(1): 65?69.
[9] REN Na, LIU Jiajia, YANG Dongliang, et al. Sequence-related amplified polymorphism(SRAP) maker as a new method for identification of endophytic fungi from Taxus[J]. World Journal of Microbiology and Biotechnology, 2012, 28(1): 215?221.
[10] GARYALI S, KUMAR A, REDDY M S. Taxol production by an endophytic fungus, Fusarium redolens, isolated from Himalayan Yew[J]. J Microbiol Biotechnol, 2013, 23(10): 1372?1380.
[11] KUMAR V, RAI S, GAUR P, et al. Endophytic Fungi: Novel Sources of anticancer molecules[C]//VERMA V, GANGE A, eds. Advances in Endophytic Research. New Delhi: Springer, 2014: 389?422.
[12] YIN Hong, SUN Yuhong. Vincamine-producing endophytic fungus isolated from Vinca minor[J]. Phytomedicine, 2011, 18(8): 802?805.
[13] 楊顯志, 張玲琪, 郭波, 等. 一株產長春新堿內生真菌的初步研究[J]. 中草藥, 2004, 35(1): 79?81.et al[J]2004, 35(1): 79?81.
[14] REN Na, LIU Jiajia, YANG Dongliang, et al. Indentification of vincamine indole alkaloids producing endophyticfungi isolated from Nerium indicum, Apocynaceae[J]. Microbiological Research, 2016, 192: 114?121.
[15] 茍莉, 唐春強, 楊淑慎. 前體及誘導子和發酵條件對煙曲霉TMS-26產紫杉醇發酵體系優化[J]. 菌物學報, 2015, 34(6): 1165?1175. GOU Li, TANG Chunqiang, YANG Shushen. Optimization of Aspergillus fumigatus TMS-26 taxol production fermentation system by precursors, elicitors and fermentation conditions[J]. Mycosystema, 2015, 34(6): 1165?1175.
[16] 代文亮, 程龍, 陶文沂. 響應面法在紫杉醇產生菌發酵前體優化中的應用[J]. 中國生物工程雜志, 2007, 27(11): 66?72. DAI Wenliang, CHENG Long, TAO Wenyi. Application of response surface methodology in optimization of precursors for taxol production by Fusarium mairei K178[J]. China Biotechnology, 2007, 27(11): 66?72.
[17] VERMA P, KHAN S A, MATHUR A K, et al. Regulation of vincamine biosynthesis and associated growth promoting effects through abiotic elicitation, cyclooxygenase inhibition, and precursor feeding of bioreactor grown Vinca minor hairy roots[J]. Applied Biochemistry and Biotechnology, 2014, 173(3): 663?672.
[18] MCCOY E, O’CONNOR S E. Directed biosynthesis of alkaloid analogs in the medicinal plant Catharanthus roseus[J]. J Am Chem Soc, 2006, 128(44): 14276?14277.
[19] GUO Zhigang, LIU Yun, GONG Meizhen, et al. Regulation of vinblastine biosynthesis in cell suspension cultures of catharanthus roseus[J]. Plant Cell Tiss Organ Cult, 2013, 112(1): 43?54.
[20] 邢世海, 王荃, 潘琪芳, 等. 長春花萜類吲哚生物堿的生物合成途徑[J]. 西北植物學報, 2012, 32(9): 1917?1927.XING Shihai, WANG Quan, PAN Qifang, et al. Research progress of terpenoid indole alkaloids (TIAs) biosynthetic pathway of Catharanthus roseus[J]. Acta Botanica Boreali-Occidentalia Sinica, 2012, 32(9): 1917?1927.
[21] MOLCHAN O, ROMASHKO S, YURIN V. L-tryptophan decarboxylase activity and tryptamine accumulation in callus cultures of Vinca minor, L[J]. Plant Cell Tissue and Organ Culture, 2012, 108(3): 535?539.
[22] NIVISON-SMITH L, ACOSTA M L, MISRA S, et al. Vinpocetine regulates cation channel permeability of inner retinal neurons in the ischaemic retina[J]. Neurochemistry International, 2014, 66: 1?44.
[23] KUMAR K, KUMAR S R, DWIVEDI V, et al. Precursor feeding studies and molecular characterization of geraniolsynthase establish the limiting role of geraniol in monoterpene indolealkaloid biosynthesis in Catharanthus roseus leaves[J]. Plant Science, 2015, 239: 55?66.
Effects of precursors and elicitors on production of ethyl vincamine by endophytic fungus CH1
REN Na1, 2, LIU Jiajia1, YANG Dongliang1, XU Shijie1, LUAN Mingbao3, ZHAO Nana1, PENG Yinzi1, WU Yiqiang4, YUAN Guangming4
(1. School of Chemistry and Chemical Engineering, Central South University, Changsha 410083, China; 2. School of Pharmaceutical Sciences, Hunan Vocational College of Science and Technology, Changsha 410118, China; 3. Institute of Bast Fiber Crops, Chinese Academy of Agricultural Sciences, Changsha 410205, China; 4. Hunan Collaborative Innovation Center for Effective Utilization of Wood & Bamboo Resources, Changsha 410004, China)
In order to increase the yield of ethyl vincamine produced by endophytic fungus CH1, the effect of cyclooxygenase inhibitor and hydroxylase elicitor along with various precursors for the production of ethyl vincamine were researched. Firstly, the effects of naproxen, tryptophan, tryptamine, loganin, secologanin and hydrogen peroxide on ethyl vincamine production of endophytic fungus CH1 were investigated by single factor experiment. In addition, orthogonal experiment design was used to optimize the concentration by statistical software SPSS(statistical package for the social sciences) 19.0.The results show that the optimum mass concentrations for ethyl vincamine produced by endophytic fungus CH1 are as follows: naproxen 8 mg/L, tryptophan 100 mg/L,tryptamine 95 mg/L,loganin 105 mg/L, secologanin 25 mg/L, hydrogen peroxide 20 μg/L. Under the conditions, the highest ethyl vincamine production is up to 5.09 mg/L, which is 2.63 times higher than that before optimization. The addition of elicitors and precursors in the fermentation medium of endophytic fungus CH1 can significantly increase the production of ethyl vincamine (significance probability is less than 0.05), which lays foundation for the biosynthesis research of ethyl vincamine produced by endophytic fungus CH1.
precursor; elicitor; endophytic fungus; ethyl vincamine
10.11817/j.issn.1672?7207.2019.02.005
Q939.9
A
1672?7207(2019)02?0279?07
2018?06?10;
2018?08?08
國家自然科學基金資助項目(31671744);湖南省高校2011協同創新項目(422190011)(Project(31671744) supported by the National Natural Science Foundation of China; Project(422190011) supported by Collaborative Innovation Center Program for Effective Utilization of Wood & Bamboo Resources of Hunan Province)
劉佳佳,博士,教授,從事天然活性產物開發研究;E-mail:liujj0903@163.net
(編輯 陳燦華)

