RhoA蛋白及驅動蛋白KIF2A與卵巢癌臨床病理特征的相關性研究
管文華,項鋒鋼
(青島大學基礎醫學院 病理學系,山東 青島 266021)
卵巢癌是婦科常見的一種惡性腫瘤,卵巢癌的5年生存率較低,約在25%~30%[1],卵巢癌具有高的增殖及轉移潛力,但發病機制尚不完全清楚。研究卵巢癌的惡性生物學行為機制,尋找新的治療靶點,已經成為亟待解決的問題。
有研究提示,驅動蛋白KIF2A的表達與多種腫瘤的增殖和轉移密切相關[2]。Rho家族蛋白是Ras超家族中的一類小分子G蛋白,具有GTP酶活性,在細胞信號傳導中起著重要作用,與腫瘤新生血管生成、細胞凋亡、腫瘤轉移、腫瘤侵襲以及腫瘤生長增殖等有著十分密切的關聯。相關研究報道中明確提出,RhoA在許多腫瘤中表達增加[3]。但KIF2A和RhoA在卵巢癌中的研究尚少見報道。另外,同是促癌基因,兩者在卵巢癌中的表達有無相關性,兩者間是否存在調控關系,兩者可否作為卵巢癌靶向治療的新靶點,這些問題目前均無準確答案。
本研究通過檢測RhoA和KIF2A蛋白在正常卵巢、卵巢上皮良性腫瘤及卵巢癌組織中的表達情況,了解RhoA和KIF2A蛋白與卵巢癌臨床病理特征的關系及兩者間的相關性,為臨床治療卵巢癌提供實驗依據。
1 資料與方法
1.1 一般資料
選取2014年6月—2016年6月青島大學附屬醫院手術切除的卵巢癌患者45例、卵巢上皮良性腫瘤患者25例及正常卵巢組織患者20例。年齡26~69歲,平均(48.7±10.07)歲。所有患者在切除卵巢組織標本前均未進行化療或放療,正常卵巢組織取自子宮病變同時切除正常卵巢者,所有患者經手術后病理檢查確診。卵巢癌病理類型:漿液性21例,子宮內膜樣15例,黏液性9例;病理分級:低分化16例,高中分化29例;FIGO分期為Ⅰ、Ⅱ期26例,Ⅲ、Ⅳ期19例;術中清掃淋巴結發現有轉移者15例。
1.2 試劑
KIF2A小鼠單克隆抗體、RhoA小鼠單克隆抗體均購自英國Abcam公司,置入-20℃冰箱冷凍保存,工作濃度均為1∶100,鏈霉菌抗生物素蛋白——過氧化酶(SP)法試劑盒、DAB(3,3,-diaminobenzidine 3,3,-二氨基聯苯胺)酶底物顯色試劑盒均購自北京中杉金橋生物技術有限公司。
1.3 免疫組織化學染色
10%中性甲醛對實驗標本予以固定,常規石蠟包埋,連續切片,4 μm厚,每份標本留5張,其中1張進行HE染色,其余行免疫組織化學實驗。陽性對照物選取已知陽性組織切片,陰性對照物選取PBS代替一抗,采用SP法檢測,蠟塊切片經過脫蠟、水化后,滴加3%過氧化氫H2O2孵育10 min阻斷內源性過氧化物酶,滴加枸櫞酸鈉緩沖液(pH 6.0)進行抗原修復,切片上滴加封閉用正常山羊血清液(室溫下孵育20 min)。滴加一抗,4℃過夜,PBS洗滌,對生物素標記二抗(于37℃環境內予以孵育,孵育時間30 min)予以滴加,滴加1滴;PBS洗滌后,對辣根酶標記鏈霉卵白索工作液(37℃環境內予以孵育,孵育時間20 min)予以滴加,滴加1滴。PBS洗滌,對新鮮配制的DAB予以滴加顯色,顯色時間控制在6 min左右,于顯微鏡視野下觀察染色程度,充分水洗;水洗完成后選取蘇木精復染,二甲苯透明5 min,梯度乙醇脫水,中性樹脂封片,于顯微鏡視野下觀察。
1.4 免疫組織化學結果的判定
染色細胞漿中對KIF2A和RhoA予以染色處理,呈淺黃色—棕黃色,彌漫分布。判定主要依據陽性細胞百分比與染色強度[4],每張切片對典型腫瘤細胞視野予以隨機選取,共選取10個,每一個視野對100個腫瘤予以計數,并計算陽性細胞百分數。按照著色細胞陽性百分比予以評分:①4分為75%以上;②3分為51%~75%,彌散;③2分為26%~50%,局部;④1分為5%~25%,散發;⑤0分為5%以下,陰性。同時,按照染色強度予以評分,即:①強著色代表3分,中度著色代表2分,弱著色代表1分,不著色代表0分。將染色強度評分與著色細胞陽性百分比相乘,RhoA、KIF2A評分(0~12)分別對應4種表達強度,即:①強陽性(+++):9~12分;②中度陽性(++):5~8分;③弱陽性(+):2~4分;④陰性(-):0~1分。
1.5 統計學方法
數據分析采用SPSS 21.0統計軟件,計數資料采用例(%)表示,兩獨立樣本采用Mann-WhitneyU檢驗,多個獨立樣本的比較采用Kruskal-WallisH檢驗,在有統計學意義的基礎上,兩兩比較采用Nemenyi法,采用Spearman做相關性分析,P<0.05為差異有統計學意義。
2 結果
2.1 正常卵巢、卵巢上皮良性腫瘤及卵巢癌組織中KIF2A、RhoA的表達

圖1 KIF2A在卵巢癌中的高表達 (SP×400)
圖2 RhoA在卵巢癌中的高表達 (SP×400)
KIF2A和RhoA主要定位于細胞漿中(見圖1、2),免疫組織化學染色呈淺黃色—棕黃色(+)~(+++)。KIF2A在正常卵巢組織和卵巢上皮良性腫瘤組織中的陽性率分別為15.0%(3/20)和20.0%(5/25),在卵巢癌組織中陽性率為77.8%(35/45),3組比較差異有統計學意義(H=40.834,P=0.000);其中KIF2A在正常卵巢組織和卵巢上皮良性腫瘤組織中的陽性率比較差異無統計學意義(H=0.043,P=0.979);與卵巢上皮良性腫瘤組織、正常卵巢組織比較,卵巢癌組織中KIF2A的陽性率更高(H=27.931和26.397,均P=0.000)。見表1。
RhoA在正常卵巢組織和卵巢上皮良性腫瘤組織中的陽性率分別為10.0%(2/20)和16.0%(4/25),卵巢癌組織中陽性率為62.0%(28/45),3組比較差異有統計學意義(H=27.513,P=0.000);RhoA在卵巢正常組織和卵巢上皮良性腫瘤組織中的陽性率比較差異無統計學意義(H=0.090,P=0.960);與卵巢上皮良性腫瘤組織、正常卵巢組織比較,卵巢癌組織中RhoA的陽性表達更高(H=18.190和18.440,均P=0.000)。見表1。
2.2 卵巢癌組織中KIF2A、RhoA的表達與臨床病理特征的關系
Ⅰ、Ⅱ期卵巢癌KIF2A的表達較Ⅲ、Ⅳ期低,淋巴結轉移者KIF2A的表達較未轉移者高,差異均有統計學意義(P<0.05)。而不同年齡、不同組織學分級及不同病理類型KIF2A的表達差異無統計學意義(P>0.05)。見表2。
低分化卵巢癌較高分化者RhoA蛋白表達高,淋巴結轉移者RhoA蛋白較未轉移者表達高,差異有統計學意義(P<0.05)。而不同年齡、臨床分期及病理類型RhoA蛋白的表達差異無統計學意義(P>0.05)。見表3。
2.3 卵巢癌組織中KIF2A、RhoA表達的相關性
Spearman等級相關性分析結果表明,KIF2A、RhoA在卵巢癌中的表達呈正相關(rs=0.801,P =0.000)。見表4。

表1 KIF2A、RhoA蛋白在正常卵巢、良性上皮卵巢腫瘤及卵巢癌組織中的表達
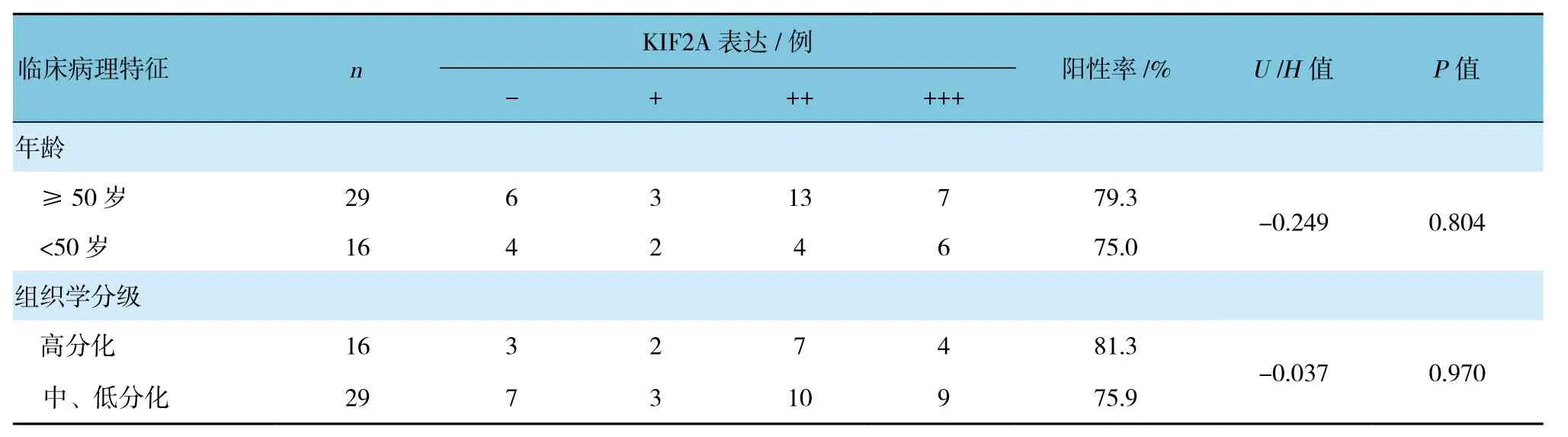
表2 KIF2A的表達與卵巢癌臨床病理特征的關系

續表2

表3 RhoA的表達與卵巢癌臨床病理特征的關系
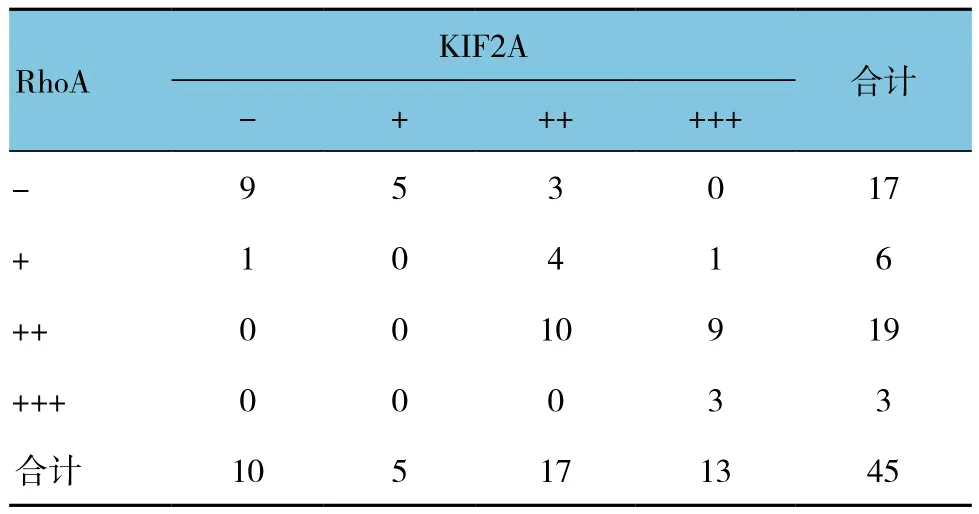
表4 卵巢癌組織中KIF2A與RhoA表達的相關性 例
3 討論
卵巢癌具有腫瘤細胞過度增殖、轉移和侵襲的特點,預后較差。近年來人們開始關注和研究微管驅動蛋白與腫瘤發生的關系,驅動蛋白在細胞有絲分裂中促進染色體移動的微管解聚過程中發揮重要作用[5],其功能異常可能引起基因組不均衡,造成子細胞中染色體異常,出現非整倍體、多倍體及腫瘤的發生[6-8]。KIF2A是驅動蛋白-13家族成員之一,具有催化解聚微管的作用,參與細胞有絲分裂,當KIF2A出現異常抑制或者異常激活狀況的時候,可對微管長度予以改變,導致中心染色體出現紊亂狀況,造成有絲分裂異常,最終對正常細胞增殖過程產生不良影響[9]。
本研究中,KIF2A在卵巢癌組織中表達增高,卵巢上皮良性腫瘤及正常卵巢組織中表達低,推測KIF2A異常高表達可能使微管發生動力學改變,微管解聚增強,加快促進細胞的分裂增殖,因此KIF2A可能參與卵巢癌細胞的增殖過程。另外本研究發現卵巢癌中KIF2A的高表達出現在臨床分期晚及有淋巴結轉移的癌組織中,推測可能因微管的減少和解聚與腫瘤周圍的局部浸潤和遠處轉移相關[10-12],驅動蛋白KIF2A高表達可能使微管解聚增加,細胞骨架不穩定,促進卵巢癌的局部浸潤和轉移過程。
近年來發現,RhoA蛋白與腫瘤的發生、發展存在重要關系。Rho活性在人類腫瘤中經常出現失調,可對腫瘤細胞浸潤、生長予以促進[13-14]。本研究發現在卵巢癌組織中RhoA高表達,而良性卵巢腫瘤及正常卵巢組織中為低表達,推測RhoA在卵巢癌的發生發展過程中可能通過對細胞骨架予以調節,對卵巢癌細胞增殖予以促進,使細胞間黏附作用下降,促進細胞外基質降解,促進卵巢癌的發生、發展。另外本研究顯示,RhoA在有淋巴結轉移的癌組織中表達高,在組織學分化低的癌組織中表達高,提示RhoA可能通過破壞腫瘤細胞間的黏附作用,促進細胞外基質降解,促進腫瘤血管形成參與了卵巢癌的浸潤和轉移。這與SHEPELEV等[3]的研究結果相一致。
KIF2A和RhoA在卵巢癌的侵襲和轉移過程中是否存在關聯機制尚不明確,尚無相關文獻報道。WANG等[15]在相關研究報道中明確提出,敲除KIF2A基因后,口腔鱗癌細胞內MMP-9基因水平會明顯下降,KIF2A不僅能夠通過對細胞骨架予以改變,對細胞運動能力產生影響,還可能與MMP-9有相互作用,進一步增強突變細胞的遷徙、入侵基膜能力,在此基礎上對腫瘤細胞轉移、侵襲予以合理調控。而RhoA和RhoC則同屬于Rho亞家族成員,可影響基質金屬蛋白酶活性。
本實驗結果表明,在卵巢組織中KIF2A和RhoA的表達呈正相關,且同是促癌基因,提示KIF2A和RhoA可能協同參與卵巢癌的發生、發展及轉移過程。實驗結果可能受實驗樣本、方法、條件的限制。兩者間的關系需要更多的理論和數據支持。探討兩者在卵巢癌發生、發展中的相互作用,有助于了解卵巢癌發生轉移的分子生物學機制,為臨床靶向治療提供新的實驗依據。

