葡萄糖在甘蔗制糖檢測中標定斐林試劑的研究
廖敏菊,韋佳秀,韋冬玲,曾月娥,韋海軍
(廣西糖業集團柳興制糖有限公司,廣西 柳州 545112)
0 前言
在甘蔗制糖過程中,具有還原性的糖主要為葡萄糖和果糖,總稱為還原糖。還原糖的產生或存在的多少,會直接影響到產品的生產過程和最終產品的產量和質量。對糖品中的還原糖分進行及時有效地檢測,就顯得極為重要。根據目前甘蔗制糖還原糖的檢測方法主要是《蘭艾農法》和《蘭艾農恒容法》,這兩種方法主要都是通過一定量的斐林試劑與糖品中具有還原性的糖進行化學反應,以確定糖品中還原性糖含量的高低。標定該試劑的標準溶液,甘蔗制糖檢測中一直以來都是根據《甘蔗制糖化學管理分析方法》中所述方法進行配制轉化糖標準溶液,其過程過于煩雜,時耗過長,在當前追求工作效率高度化的時代,已存在缺陷。為克服不利于提高工作效率的因素影響,文中以市售葡萄糖配制成標準溶液取代轉化糖標準溶液,對一定量的斐林試劑進行標定和檢測樣品還原糖分的研究。
1 實驗材料與方法
1.1 主要實驗儀器
錐形瓶:250ml;滴定管:50ml;加熱電爐:可調式電爐;分析天平:分度為萬分之一。
1.2 實驗主要試劑
還原糖測定所需甲液、乙液的混合試劑,即斐林試劑,是定量樣品中還原糖的主要物質。
1.2.2 轉化糖標準溶液
轉化糖標準溶液由純蔗糖經酸化水解轉化后進行配制。
1.2.3 葡萄糖標準溶液
以市售的葡萄糖分析純經烘至恒重后進行配制。
1.2.4 次甲基藍
還原糖檢測進行到反應終點的指示劑。
1.3 實驗操作
1.3.1 斐林試劑的規定量
企業投標報價,首先應根據招標文件、現場調查、施工組織設計、企業定額等估價依據,確定企業成本價,再加上預期利潤,得到企業的合理報價,而不是盲目追求低價,甚至低于企業成本。調研發現,企業經營部門編制投標書時,出現了現場調查不細,結合現場實際不夠,單價分析不合理,風險因素考慮不夠等問題,直接導致中標價低于企業成本,項目部成本壓力很大。如包西線某項目,標前調查時認為只有2~3公里的便道,實際施工時臨時便道修了20多公里,僅此一項虧損就達300多萬元。再如某鐵路項目2號隧道臨時便道需要通過一個既有線下的小通道橋,投標時忽略了這一因素引起的材料二次倒運費,造成中標單價偏低,實際施工時損失20多萬元。
檢測方法中用以檢測樣品中還原糖分的斐林試劑的規定用量是定量樣品中還原糖量的基礎,對某一定量的斐林試劑進行準確標定是關鍵。《蘭艾農法》的規定量是甲、乙各5mL等量混合為10mL的斐林試劑;《蘭艾農恒容法》的規定量是甲、乙各10mL等量混合為20mL的斐林試劑。
1.3.2 轉化糖標準溶液的配制
根據《甘蔗制糖化學管理分析方法》中所述,首先是將蔗糖進行純化處理,再將純蔗糖進行酸化水解處理,生成具有還原性的糖。其酸化處理過程,需在室溫20℃至25℃的條件下,經過8天的時間進行靜置轉化才能徹底水解完成。由于是經過酸化處理,其中的酸性比較強,在分取配制轉化糖標準溶液時,還需進行調節為中性或微堿性溶液,最后配制成《蘭艾農法》要求濃度為0.2%的轉化糖標準溶液或《蘭艾農恒容法》要求濃度為0.25%的轉化糖標準溶液。
1.3.3 葡萄糖標準溶液的配制
根據《蘭艾農法》或《蘭艾農恒容法》檢測還原糖分的要求配制標準溶液,將市場上可以直接購買的葡萄糖分析純于98~100℃條件下烘至恒重,利用分析天平準確稱取2.000克或2.500克葡萄糖分析純,以少量的蒸餾水將其溶解,并準確定容至1000mL,即獲濃度為0.2%或0.25%葡萄糖標準溶液。
1.3.4 斐林試劑的標定
還原糖檢測方法中所使用的斐林試劑是度量樣品中還原糖的主要物質,能否準確標定一定量的斐林試劑相當的還原糖量,是準確檢測樣品中還原糖分的關鍵。根據還原糖的檢測方法,利用配制的轉化糖標準溶液和葡萄糖標準溶液分別對同一定量的斐林試劑進行4次平行標定操作,結果如表1所示。
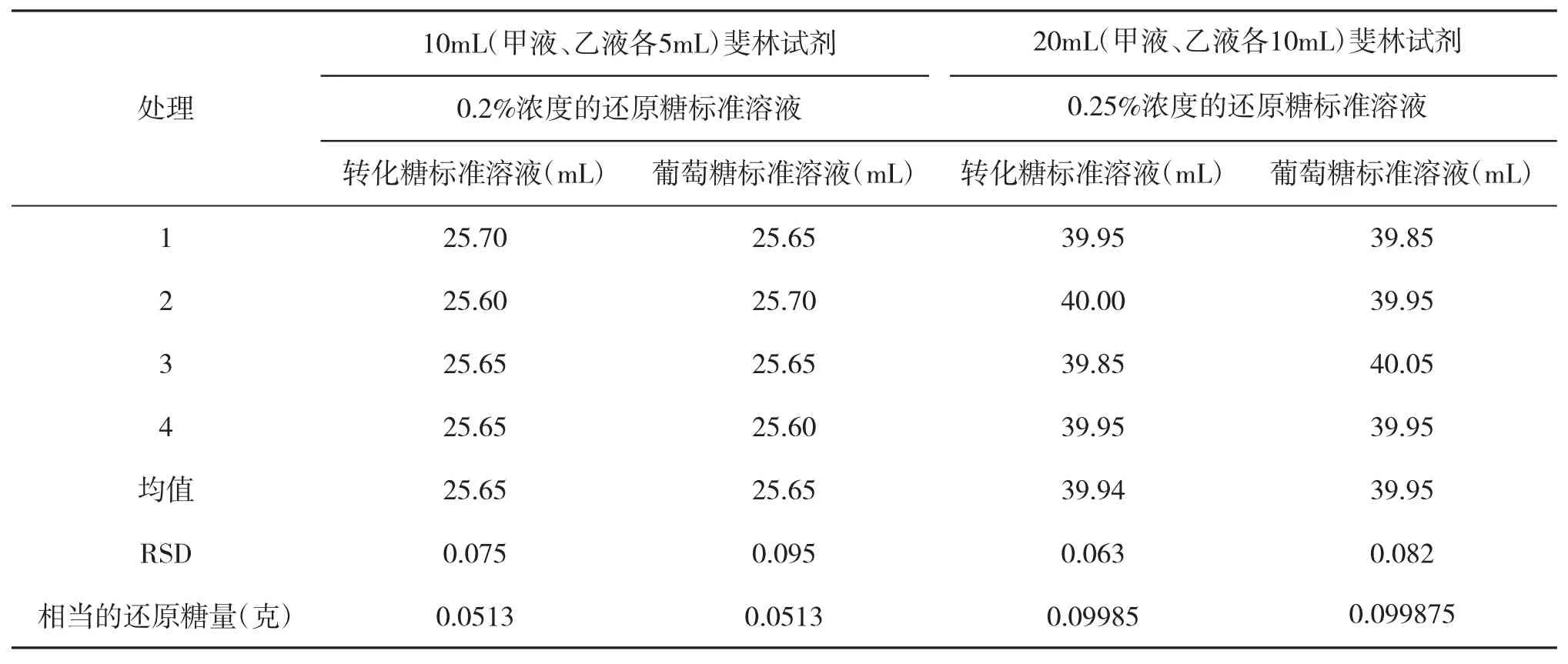
表1 兩種標準溶液對一定量斐林試劑進行標定的操作
1.3.5 經兩標準溶液標定的斐林試劑用于檢測樣品
以葡萄糖標準溶液標定的斐林試劑,對樣品的還原糖進行檢測,與以轉化糖標定的斐林試劑對同一樣品的還原糖分進行檢測比對,按標定方法以10ml(甲液、乙液各5ml)和20ml(甲液、乙液各10ml)分別對同一桔水樣品進行檢測其還原糖分,所得結果如表2所示。
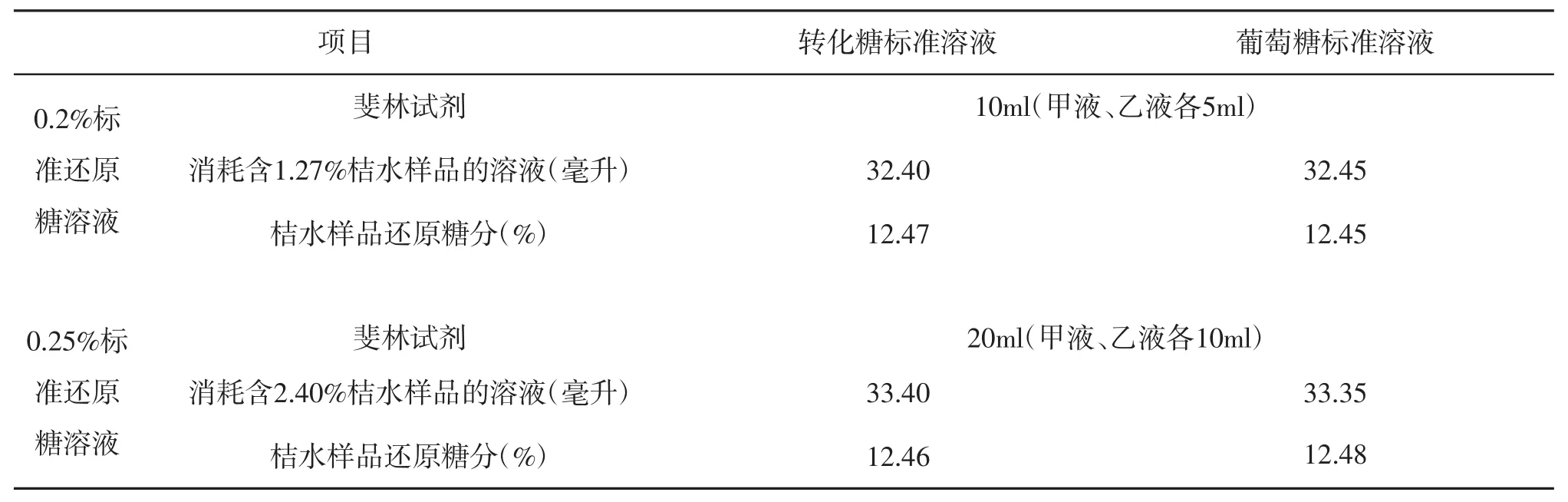
表2 斐林試劑經兩標準溶液標定后對同一桔水樣品的檢測
2 結果與討論
2.1 實驗概況
根據實驗結果表1中所示,由不同檢測方法,可知每種標準溶液只要是以相同的濃度對一定量的斐林試劑進行標定操作,其結果的標準偏差都很小,重現性很好,精密度較高。兩標準物質溶液分別進行四平行檢測,所獲結果平均值相近,說明由蔗糖轉化生成的轉化糖成份與葡萄糖相同。通常蔗糖在一定溫度和酸度條件作用,極易被轉化生成具有同分異構體的葡萄糖和果糖,并且這樣的轉化是不可逆的過程[1]。表2中顯示,利用兩標準溶液標定的斐林試劑用于檢測同一桔水樣品,其檢測還原糖分結果相近。進一步說明,一定量的斐林試劑只能與一定量的還原糖量反應,一定量的斐林試劑通過標準還原糖溶液的標定后,就可用于檢測、計算出樣品中的還原糖分。
2.2 兩標準物質具有的化學共性
表1中所列平均值相近,說明了轉化糖的主要成分是葡萄糖,實際上蔗糖經水解轉化的最終產物是葡萄糖與果糖,二者為同分異構體,與市售現成的葡萄糖化學性質相同,都具有還原性,能與具有氧化性的Cu2+起反應生成紅色的氧化亞銅沉淀。含有Cu2+離子的斐林試劑是將一定量的堿性酒石酸銅甲、乙液等量混合,立即生成藍色的氫氧化銅沉淀,這種沉淀很快與酒石酸鉀鈉反應,生成深藍色的可溶性酒石酸鉀鈉銅絡合物。在加熱條件下,用含有還原性糖的樣品溶液滴定此絡合物,其中的還原性糖(葡萄糖或果糖)與堿性酒石酸鉀鈉銅反應生成微紅色的氧化亞銅沉淀。在接近滴定終點時,以次甲基藍作指示,溶液又變藍色,繼續滴定,待二價銅全部被還原后,稍過量的還原性糖能將次甲基藍還原,溶液由藍色突然變為之前的紅色,即為滴定終點[2]。
2.3 物質參與反應的關系量
2.3.1 兩相同濃度的不同標準溶液與等量斐林試劑的反應量相等
由實驗結果可知,《蘭艾農法》所規定的斐林試劑量為10mL,利用轉化糖標準溶液進行標定,消耗濃度為0.2%的標準溶液體積均值為25.65mL,則其相當的還原糖量應為:0.2%×25.65=0.0513克,消耗相同濃度的葡萄糖標準溶液均值為25.65mL,則相當的還原糖量為:25.65×0.2%=0.0513克;在《蘭艾農恒容法》中,消耗濃度為0.25%的轉化糖標準溶液的均值為39.94mL,則其相當的還原糖量為0.25%×39.94=0.09985克;消耗同濃度的葡萄糖標準溶液均值為39.95mL,則其相當的還原糖量為0.25%×39.95=0.099875克。可見還原糖與斐林試劑進行反應能定量進行,這種定量是基于斐林試劑中能與之反應的Cu+量,配制斐林試劑的Cu+量一旦確定,就能度量樣品中的還原糖量。根據化學反應式,由1mol葡萄糖應該將6molCu2+還原為Cu+,但實際并不能根據化學反應式直接計算出樣品中的還原糖分,而是根據實驗結果驗證,1mol葡萄糖只能還原比5mol稍微多點的Cu2+,且隨反應條件而變化[3]。因此,只能先通過利用已知濃度的還原性糖標準溶液對一定量的斐林試劑進行標定,確定其所相當的還原糖量,再將欲測還原糖分的樣品,在同樣的條件下,以樣品溶液對一定量的斐林試劑進行滴定操作,根據所耗用樣品滴定量就可計算其中的還原糖。
2.3.2 兩標準溶液以不同濃度標定斐林試劑檢測樣品中的還原糖相等
表2中,依《蘭艾農法》的檢測要求是以10mL的斐林試劑進行,其相當的還原糖量為:0.2%×25.65×100%=0.0513克,則樣品桔水溶液與之反應的還原糖量為:桔水還原糖分×1.27%×桔水樣液滴定數=0.0513,由此可知:桔水還原糖分=0.0513÷(1.27%×桔水樣液滴定數)×100%=0.0513÷1.27%÷32.45×100%=12.45%,同理,依《蘭艾農恒容法》檢測的計算過程同此,桔水還原糖分=0.099875÷(2.40%×桔水樣液滴定數)×100%=0.099875÷(2.40%×33.35)×100%=12.48%。兩種標準物都可配制為不同濃度的溶液對一定量的斐林試劑進行標定,從而對需要檢測的樣品進行檢測,結果差不多。一定量的斐林試劑是標準物質定量樣品中還原糖分的“橋梁”。
3 結論
通過比對試驗可知,在甘蔗制糖檢測中轉化糖與市售葡萄糖都具有還原性,能與一定量的斐林試劑進行等量反應,不同的只是來源,轉化糖是以純蔗糖進行酸化水解處理最終生成葡萄糖和果糖,需要比較長的時間,而葡萄糖可以直接在市場上購買,省時省力。轉化糖中果糖與葡萄糖為同分異構體,化學性質相近,與市售葡萄糖化學性質相同,以市售葡萄糖作為標定斐林試劑的標準物質在甘蔗制糖檢測中的運用沒有任何問題,完全可以取代純蔗糖制作轉化糖標準溶液,對斐林試劑進行有效標定操作,這對進一步提高在甘蔗制糖中檢測還原糖分的工作效率有重要的意義。

