海藻多酚類化合物及其抗氧化活性研究進展
袁圣亮,段智紅,呂應年,馬曉鸝,歐陽佩佩
1(廣東醫科大學 海洋醫藥研究院,廣東 湛江,524023) 2(廣東醫科大學 附屬醫院,廣東 湛江,524001)
海洋的覆蓋率占地球表面的70%以上,是許多海洋生物的棲息地,其中海藻作為重要的生物資源有著極大的生物多樣性[1]。由于藻類生活在復雜和暴露的環境下,導致其結構的缺失和生理活性的損傷等。然而,海藻自身細胞具有很強的適應能力,主要是通過產生次級代謝產物,保護自身免受氧化應激的損傷[2]。與陸生植物相比,海藻產生的次級代謝物具有多種不同的結構和功能,是海洋資源的重要組成部分[3]。其中之一的海藻多酚類化合物已被證實具有較強的抗氧化活性,是很好的天然抗氧化劑[4]。
中國大型海藻物種數達到1 277種,主要有藍藻門(161種)、紅藻門(607種)、褐藻門(298種)和綠藻門(211種)4大類[5]。從不同海藻中分離得到的多酚類化合物主要包括:褐藻多酚類、黃酮類、酚酸類和鹵代酚類等[6]。這些化合物被認為具有抗氧化作用,可用于治療心血管疾病、糖尿病、癌癥、動脈粥樣硬化、老年癡呆以及其他一些退行性疾病等[7-8]。由于海藻多酚類化合物具有對人類健康有益的作用,可以作為天然的抗氧化劑廣泛應用于化妝品、食品和藥品等眾多領域[9]。因此,對海藻多酚類化合物抗氧化活性作用的研究顯得尤為重要。本文簡要綜述海藻多酚類化合物的分類及其抗氧化活性情況,并概述其抗氧化的相關機制和影響因素,旨在為海藻多酚的開發利用提供依據。
1 海藻多酚類化合物的基本結構
海藻多酚類化合物主要以間苯三酚為基本結構單元,通過不同的數量和不同的連接方式構成一類含有酚性羥基的次級代謝產物。按其酚性羥基的取代數目和結構的不同可將它們分為簡單酚類和復雜多酚類化合物[10]。簡單酚類根據其是否含有鹵素可分為鹵代酚類和非鹵代酚類。鹵代酚類主要是溴代單酚及其衍生物和溴代二酚化合物,極少含氯鹵素。非鹵代酚類主要來源于紅藻和褐藻,屬于簡單酚類衍生物和含有脂肪鏈的酚類,而且來源相對較少。現今研究主要集中在聚合的復雜多酚類化合物及其衍生物,這類海藻多酚根據其聚合形式的不同,可以分為6種結構類型[12-13](表1)。
2 海藻多酚類化合物的種類
從海藻中分離得到的一系列海藻多酚類化合物(表2),其來源豐富、種類多,且共同結構特征都是含有酚性羥基。根據酚性羥基的數目和位置的不同,可將他們分4種:褐藻多酚類、黃酮類、酚酸類和鹵代酚類,而且都具有一定的抗氧化活性。
2.1 褐藻多酚類
褐藻多酚是一類主要存在于褐藻的多酚類化合物,主要是通過醋酸-丙二酸途徑,以間苯三酚為單元進行生物合成得到的低聚物。褐藻多酚是水溶性很強的化合物,因為其羥基與水能形成氫鍵,且它們的分子質量在126~6 500 kDa之間[13]。與其他多酚類化合物相似,褐藻多酚也有多種生物活性,例如抗氧化、抗炎、抗癌、抗菌及血管緊張Ⅰ轉化酶抑制作用等,其中最顯著的活性為抗氧化活性[30]。
其中,空莖昆布(E.cava)作為褐藻中的一種,含有大量的褐藻多酚類化合物:phloroglucinol、eckol、fucodiphloroethol G、phlorofucofuroeckol A、dieckol、7-phloroeckol和6,6’-bieckol等[14]。CHANG等[31]通過由慶大霉素引起活性氧(ROS)增加誘導小鼠耳蝸損傷的體內實驗,發現二鵝掌菜酚對部分氧化損傷有保護作用,而且二鵝掌菜酚的濃度在大于67 μmol/L的情況下,具有顯著的自由基清除能力。另外,從黑藻(E.stolonifera)中分離出來的硫磺醇A、二鵝掌菜酚和二惡英被證明具有很強的DPPH自由基清除的活性,而且硫磺醇A和二鵝掌菜酚能夠抑制細胞內活性氧的生成[32]。MWANGI等[18]從極大昆布(E.maxima)中分離出4種褐藻多酚類化合物:酚葡糖醇、類褐藻多酚、7-間苯三酚基鵝掌菜酚和2-間苯三酚基鵝掌菜酚,且它們清除自由基的能力大小是7-phloroeckol>2-phloroeckol>eckol,都具有很好的抗氧化活性。
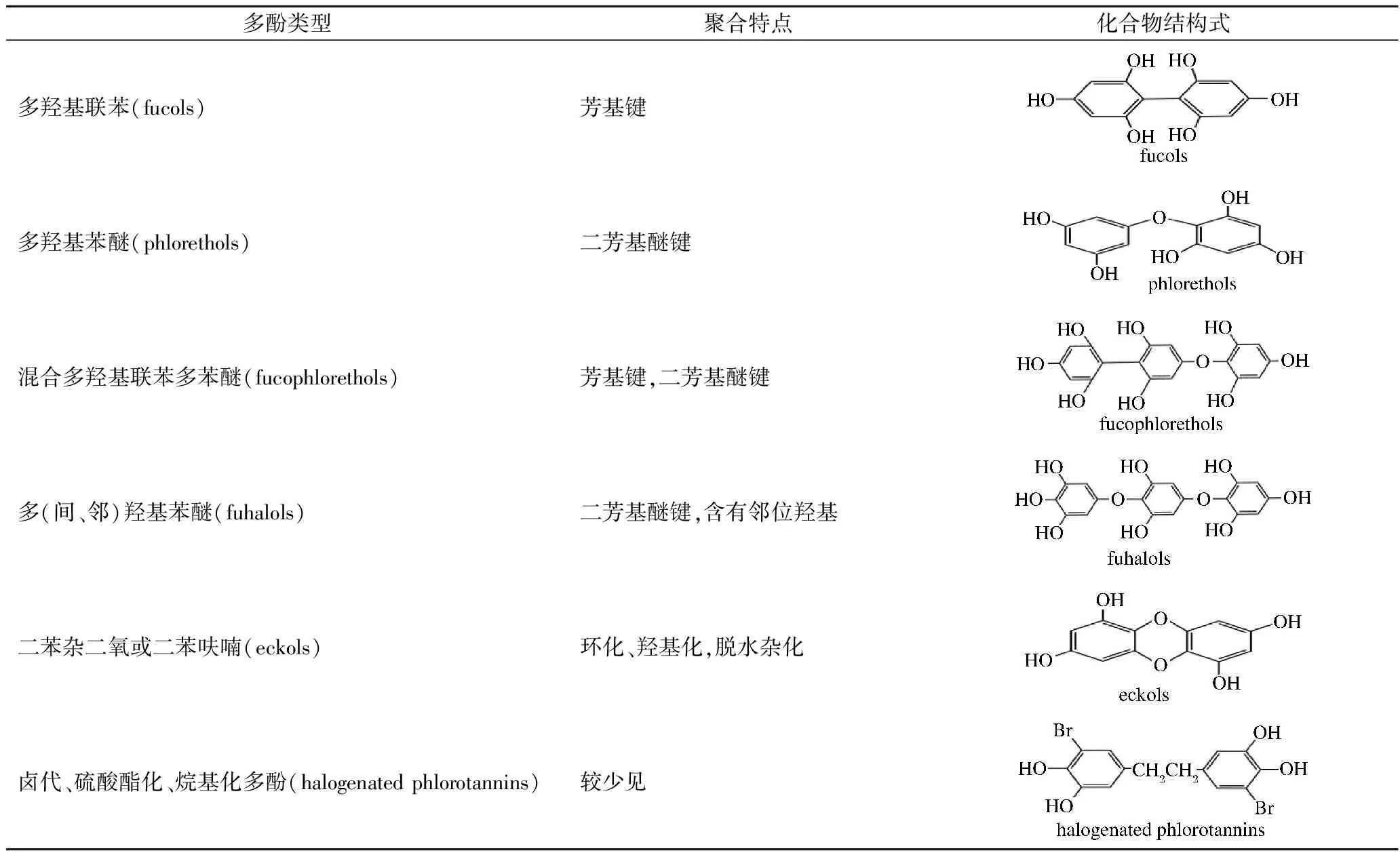
表1 海藻多酚類化合物的化學結構Table 1 Types of seaweed polyphenolic compounds

表2 不同種類的海藻多酚類化合物Table 2 Different species of seaweed polyphenolic compounds
續表2

多酚種類海藻種屬化合物名稱文獻酚酸類泡葉藻墨角藻quinic acid,hydroxybenzoic,rosmarinic acid,p-coumaric,ferulic acid[22]喇叭藻salicylic acid,gallic acid,quercetin,syringic acid[26]紫菜海帶科羊棲菜裙帶菜掌狀紅皮藻gallicacid,4-hydroxybenzoic acid[23]鹵代酚類多管藻urceolatol,7-bromo-9,10-dihydrophenanthrene-2,3,5,6-tetraol,4,7-dibromo-9,10-dihydrophenanthrene-2,3,5,6-tetraol,3-bromo-4,5-dihydroxybenzaldehyde,3,5-dibromo-4-hydroxybenzaldehyde[27]松節藻3-(2,3-dibromo-4,5-dihydroxybenzyl)-pyrrolidine-2,5-dione,4-(2,3-dibromo-4,5-dihydroxybenzylamino)-4-oxobutanoate,4-(2,3-dibromo-4,5-dihydroxybenzylamino)-4-oxobutanoic acid,3-bromo-5-hydroxy-4-methoxy-benzamide,2-(3-bromo-5-hydroxy-4-methoxyphenyl)acetamide[28]松節藻多管藻3-bromo-4,5-dihydroxybenzaldehyde,3-bromo-4,5-dihydroxy-benzyl methyl ether[29]
2.2 黃酮類
黃酮類化合物是以15個碳原子為基本骨架,并以C6-C3-C6為結構單元,由A,B,C 3個環組成,兩邊的是苯環,中間的是雜環,其生物合成途徑主要是通過苯丙烷代謝完成的。大部分的黃酮類化合物主要存在于陸生植物中,但最近有研究發現海藻中也存在著黃酮類化合物。
黃酮類化合物因其具有清除超氧陰離子和羥基自由基的能力而被人們熟知,主要是將氫原子供給那些自由基,穩定它們的結構并形成一個共振穩定的半醌基[33]。研究表明4種綠藻中總黃酮的含量與體外抗氧化活性,發現它們都具有很強自由基清除能力,且呈一定的劑量依賴性和極顯著的正相關性[36]。RAJAURIA等[20]從褐藻長海條藻(H.elongata)中,通過提取分離的方法得到黃酮類化合物山奈酚和薊黃素,而且純化后的亞組分比抗壞血酸具有更強的抗氧化能力(P<0.05)。MACHU等[23]分別從4種褐藻、2種紅藻和1種藍藻中分離得到6種黃酮類化合物,而且通過體外抗氧化活性實驗發現它們都具有很好的自由基清除能力。其中從來自褐藻的裙帶菜(U.pinnatifida)分離得到的黃酮類化合物表兒茶素沒食子酸酯的含量最高。此外,在生物系統中,黃酮類化合物能夠抑制多種氧化還原酶的活性如脂氧合酶和環氧合酶等,阻止細胞內一些活性氧的生成。除了具有自由基清除能力外,黃酮類化合物還因能螯合過渡的金屬離子而具有抗氧化性,因此能夠很好阻斷最易產生活性氧的芬頓反應。
2.3 酚酸類
酚酸類化合物是除了含酚性羥基外,芳環上還有羧基取代的一類化合物。酚酸類化合物被認為是莽草酸途徑的代謝產物,且具有很好的清除自由基能力,也能夠抑制鐵離子誘導脂質體的氧化作用。
人工養殖的魚腥藻(A.doliolum)和海綿藻(S.spongiosa)都含有兒茶酚酸、對羥基苯甲酸、綠原酸、丁香酸、咖啡酸、對香豆酸、水楊酸和肉桂酸等酚酸類化合物[24]。MEZGHANI等[25]第一次從綠藻孔石莼(U.rigida)分離鑒定得到酚酸類化合物香草酸、奎寧酸和丁香酸,并通過測定它們的DPPH自由基清除能力,表明酚酸類化合物是終止自由基的主要分子。AGREGAN等[22]在泡葉藻(A.nodosum)、二歧雙叉藻(B.bifurcata)和墨角藻(F.vesiculosus)中都發現含有酚酸類化合物。其中,3種海藻中都含有奎尼酸衍生物,泡葉藻中含有大量的羥基苯甲酸,泡葉藻和二歧雙叉藻中含有迷迭香酸衍生物以及墨角藻主要含有對香豆酸和阿魏酸衍生物。另外通過體外的抗氧化活性實驗,也表明來自3種海藻中的酚酸類化合物都具有清除自由基的能力,而且它們的抗氧化活性能力大小與其結構性質有關。這種特點在酚酸類化合物,如沒食子酸、兒茶酸、咖啡酸和綠原酸中已經得到證實。另外有研究發現,具有苯丙烯酸取代基的酚酸有很強的抗氧化活性,因為取代基能夠增強供氫原子能力而增強自由基清除能力。
2.4 鹵代酚類
鹵代酚類化合物主要存在于褐藻和紅藻,少有在綠藻,而且它們大部分都具有明顯的自由基清除活性[34]。目前,已從不同海藻中分離得到約上百種鹵代酚類化合物,主要是溴代酚類。LI等[27]從紅藻多管藻(P.urceolata)成功分離并鑒定到6種溴代酚(BPs),而且都具有很強的DPPH自由基清除活性。LI等[28]從紅藻松節藻(R.confervoides)中得到的5種含氮的溴代酚類化合物,都能夠清除DPPH自由基和ABTS自由基。另外,有研究從不同紅藻中都分離得到3-溴-4,5-二羥基苯甲醛(BDB),并且發現其對UVB誘導氧化損傷的人角質形成細胞具有保護作用[35]。
最近研究表明,溴代酚是最有潛力成為與自由基相關疾病的預防藥物之一,如糖尿病,癌癥,炎癥和神經退行性疾病等[36]。據Li等研究,溴代酚清除自由基的能力和抗氧化活性的強弱與其羥基的數目和結構有關,而且苯環上的溴取代會輕微減弱自由基清除的活性[27,37]。
3 海藻多酚類化合物的抗氧化作用機制
活性氧(reactive oxygen species, ROS)是一系列含氧化合物,對生物分子表現出很強的活性,而且對細胞的完整性構成威脅[38]。ROS主要包括含氧自由基和非自由基衍生物,而這些衍生物最終可以轉化為自由基或氧化劑[39]。過多的活性氧自由基會誘導過度氧化應激,從而造成基本生物分子的破壞,最終破壞DNA的結構而導致基因突變或細胞死亡[40]。來自海藻的多酚類化合物由于具有直接或間接清除自由基和活性氧的能力,被認為是預防或減少慢性疾病的天然抗氧化劑。
研究表明,自由基的直接清除是多酚類化合物抗氧化的一條最為重要的途徑[41]。根據量子化學計算的方法理論和實驗研究,這類化合物的自由基清除主要是通過氫原子轉移或電子轉移實現[42-43]。
氫原子轉移機制:酚性基團向(R·)提供氫原子,多酚類化合物(ArOH)破壞鏈式反應,阻止氧化進行。通過氫原子轉移機制,多酚類化合物轉化成苯氧基自由基(ArO·)。
R·+ArOH→RH+ArO·
氫原子轉移機制表明,多酚類化合物(ArOH)具有從酚羥基(-OH)中轉運氫原子的能力,而生成的苯氧自由基(ArO·)的穩定性決定了這類化合物清除自由基能力的強弱[18]。換言之,增加苯氧自由基穩定性能夠增強該類化合物的自由基清除能力。另外,多酚類化合物結構決定了酚羥基的解離度,解離度越大,則氫原子越易被轉移。因此,酚羥基的解離度是評價其清除自由基強弱的另一重要指標[44]。
電子轉移機制:多酚類化合物(ArOH)將電子轉移給(R·)從而生成陽離子自由基(ArOH+·)。
R·+ArOH→ArOH+·+ R-
因此,單電子轉移也可阻止自由基不斷的反應從而中斷氧化。從電子轉移的機制方面考慮,電勢或轉移電子的能力決定著酚類化合物的自由基清除能力。由此產生的陽離子自由基的穩定性取決于其電離電位值,而一個較低的值表示更好的穩定性[16]。
簡單來說,酚類化合物能與(R·)的自由基發生反應,它們通過共振穩定分子中未成對的電子,并在芳環內形成穩定的中間體,稱為“共振雜化”,簡單反應機理見圖1。多酚羥基在芳環中的鄰位排列增加了其羥基電子的穩定性,而且在芳環上的共軛雙鍵進一步穩固了電子的離域,增強了共軛體系,防止了其它基團的取代,從而增強了自由基清除能力[33]。因此,海藻多酚類化合物中的羥基是其清除自由基,具有抗氧化活性的重要基團。其中,由于不同的海藻多酚類化合物中羥基的數目和取代位置的差異,從而抗氧化作用不一樣。

圖1 多酚與自由基(R·)之間的共振穩定Fig.1 Resonance stability between polyphenols and free radicals (R·)注:彎曲的半箭頭表示單個電子的轉移
4 海藻多酚類化合物的抗氧化影響因素
4.1 結構的影響
目前,大部分研究集中在海藻多酚類化合物的提取工藝,較少有對其抗氧化活性的構-效關系研究。海藻多酚是含有1個或多個酚性羥基取代基的單體、低聚合或高聚合物的化合物,具有羥基的還原性,從而阻斷脂質體的氧化反應。此外,研究表明不同結構類型的海藻多酚類化合物之間,抗氧化活性作用有著很大差別。
研究表明[45],褐藻多酚具有多達8個相互連接的環結構,比來自陸生植物的其它多酚具有更有效的自由基清除活性。從這個意義上說,多羥基聯苯(fucols)和混合多羥基聯苯多苯醚(fucophlorethols)聚合類的褐藻多酚類化合物表現出比間苯三酚更強的抗氧化活性。HERMUND等[46]從墨角藻屬(F.vesiculosus)中分離了13個分子質量在374~870 Da之間的海藻多酚異構體化合物,并單獨測定各酚類化合物的抗氧化能力,表明低分子量酚類化合物具有較高的抗氧化能力。楊小青等[47]采用超濾膜截留法,從羊棲菜提取物中分段得到8組含多酚的不同組分,其中分子質量大于30 000的乙酸乙酯萃取組分的綜合抗氧化活性最好。然而,需要更進一步確定海藻多酚類化合物的分子量以及結構類型,才能明確其對抗氧化活性的影響。
4.2 含量的影響
在許多研究中,整個藻類以及它們的提取物或分級餾分的抗氧化活性大多歸因于酚類化合物。然而,它們的抗氧化活性可能是海藻提取物的復合組分共同作用。研究發現,低酚含量的幾種提取物顯示出比預期更高的活性[48]。這表明可能有其它提取化合物一起協同作用,例如:抗壞血酸、蛋白質或肽、甾醇、硫酸多糖和非極性色素等。
AIRANTHI等[49]在脂質體氧化測定結果中,發現5種不同褐藻的甲醇提取物的總多酚含量與其清除DPPH自由基能力大小之間并沒有相關性(P>0.05)。同樣,ZUBIA等[50]發現來自歐囊鏈藻(C.tamariscifolia)和墨角藻(F.ceranoides)的粗提取物雖然呈現較高的多酚含量,但是它們的DPPH自由基清除能力卻很低,也沒有相關性。但是也有相反的報道稱,海藻多酚含量與清除自由基能力之間存在正相關性。PINTEUS等[51]對27種海藻的二氯甲烷和甲醇提取物進行抗氧化能力篩選,通過比較多酚含量與DPPH自由基清除和氧自由基的吸收能力,結果表明海藻提取物的多酚含量與DPPH和過氧自由基的清除能力呈高度相關性。
在陸生植物提取物中酚類物質含量與抗氧化活性之間的相關性幾乎總是線性的。然而,由于藻類提取物的復雜性,海藻酚類化合物含量與其抗氧化活性之間的簡單相關性并不十分可靠,因此需要對活性組分和其他物質進行更詳細的表征,才能更好地確定其抗氧化能力。
4.3 提取工藝的影響
海藻多酚類化合物作為天然抗氧化劑,無論是粗提取物還是單一餾分,提取工藝是極為關鍵的過程。不同的提取工藝,會影響到海藻多酚類化合物的結構和含量,進而影響其抗氧化能力。在提取過程中,尤為關鍵的是提取溶劑和提取溫度的影響。
首先,提取溶劑會影響總多酚提取產率和抗氧化活性。LOPEZ等[52]研究發現,水提取比有機溶劑提取具有較高的多酚提取率和更好的自由基清除活性。LAMIA等[53]分別用3種不同的有機溶劑從囊葉藻(C.crinita)提取總多酚,并比較它們的產率(AcOEt>CHCl3>MeOH)和抗氧化活性的關系,結果表明海藻總多酚含量高的清除自由基效果更好。另外,有研究發現隨著溫度的升高,在100~300 ℃的高壓和亞臨界下,水提取促進細胞壁的降解,促使抗氧化劑的釋放和提取,從而提高提取率[54]。在85 ℃加熱時,裙帶菜(U.pinnatifida)的水提取物中總多酚含量減少;但在121 ℃加熱時,多酚含量更高和DPPH自由基清除活性更強[55]。這表明不同溫度提取到的海藻多酚類化合物,其抗氧化能力不同。
4.4 其他因素的影響
影響海藻多酚類化合物抗氧化活性的因素除了多酚自身結構、含量和提取工藝外,可能還會有一些其它自然因素,例如生長的自然環境。STENGEL等[56]認為有幾個方面影響海藻多酚的變化:(1)生長環境因素(日光,營養素,鹽度,溫度,海水pH和污染物等);(2)海洋生物的相互作用等;(3)時間和空間因素(季節、晝夜變化和遺傳變異造成空間和種群的差異)。其中,多酚類化合物往往積累在海藻表皮層,其含量隨著生長年齡和周期變化,而且不同部位之間的含量也有所不同[57]。這些客觀因素,最終又會影響海藻多酚類化合物的結構和含量,繼而影響其抗氧化作用。
5 展望
顯然,海藻多酚類化合物有著豐富的來源和廣闊的開發前景。作為天然抗氧化劑,關鍵是如何更高效、更環保和更可持續性地開發。從研究現狀看,海藻多酚類化合物的研究主要集中在提取分離純化及一些生物活性的探究,對其單一化合物的化學結構與生物活性之間的關系、活性作用機制等研究相對不足。從應用方面看,海藻多酚作為抗氧化劑在食品、藥品和保健品等方面的應用較多,但是缺乏科學依據和理論基礎。因此,海藻多酚類化合物研究不應局限于體外抗氧化的測試,應當深入到其在體內的作用機理、藥理活性和生物利用度等模型系統。最后,可以通過化學修飾對其結構進行改良,或者與其它物質結合形成具有協同作用的混合物,提高海藻多酚類化合物的有效利用率,從而促進藻類更進一步的開發應用。

