混菌發酵聯合分段控溫工藝提高柑橘皮渣可溶性膳食纖維含量
曹 艷,范 銘,童 創,陸勝民,*,楊 穎,邢建榮,鄭美瑜,唐偉敏,劉 哲
(1.浙江省農業科學院 食品科學研究所,農業農村部果品采后處理重點實驗室,浙江省果蔬保鮮與加工技術研究重點實驗室,浙江 杭州 310021; 2.浙江師范大學 化學與生命科學學院,浙江 金華 321004)
柑橘是世界上產量最大的水果之一。我國是世界第一大柑橘生產國,2016年,我國柑橘產量約3 500萬t。皮和渣等副產物約占柑橘鮮重的30%~50%[1],其中含有大量糖類、有機酸、維生素等營養物質,以及黃酮、精油等有益成分[2]。目前,國內只有小部分柑橘果皮用于提取果膠和香精油,以及入藥或加工成飼料,大部分皮渣被作為廢棄物直接丟棄,造成了極大的資源浪費。
膳食纖維是一類來源于植物的非淀粉多糖,分為可溶性膳食纖維(soluble dietary fiber, SDF)和不可溶性膳食纖維(insoluble dietary fiber, IDF)2類,具有調節腸道菌群、預防腸道疾病、輔助調節血糖血脂水平、預防心血管疾病等多種功效。SDF可溶于水,也可吸水膨脹,并能被腸道微生物酵解,主要包括果膠、植物膠、黏膠等。IDF不溶于水,也不能被腸道微生物酵解,主要包括纖維素、半纖維素、木質素等[3-5]。Schneeman等[6]提出,當膳食纖維中SDF的含量在30%~50%時,可達到平衡膳食的要求。目前市場上的膳食纖維主要來自谷物及豆渣、薯渣、甜菜渣等農產品加工副產物,但其中SDF所占比例都很小(占副產物原料干重的4%~10%)[7-10],不僅生理活性較低,而且口感粗糙,達不到平衡膳食的要求。Baker[11]和Grigelmo-Miguel等[12]研究表明,柑橘皮渣可以作為優質膳食纖維的制備原料,其SDF含量高于谷物來源的膳食纖維。因此,利用柑橘皮渣生產膳食纖維具有豐富的材料來源和良好的市場前景。
常規制備膳食纖維的方法有化學法、物理法、生物法等。化學法、物理法制備過程中會產生大量廢水,對產品產量及產物性能無明顯的改善作用;而利用微生物發酵法制備膳食纖維,條件溫和且綠色環保[13-16]。目前,已有以柑橘皮渣或其他水果皮渣為原料通過固態發酵法制備SDF的研究[1,17-18],但基本采用單一種類的發酵菌株和恒定發酵條件,總膳食纖維(total dietary fiber, TDF)和SDF比例提高有限。
本文在前期研究基礎上進一步優化發酵工藝,采用混菌發酵聯合分段控溫工藝,提高臍橙皮渣發酵產物中TDF和SDF含量,制備高品質柑橘膳食纖維。同時,研究了該工藝對浙江主栽柑橘品種皮渣發酵生產膳食纖維的適用性,旨在擴大柑橘皮渣原料范圍,提高資源利用率,減少環境污染。
1 材料與方法
1.1 主要原料
取贛南臍橙、溫州蜜柑和常山胡柚剝皮分瓣后榨汁,將殘留的皮和渣分別烘干至手抓成團、落地即散的程度(含水量約70%),冷凍保存。其中:贛南臍橙為本研究的主要原料,用于確定提高SDF含量的最佳發酵工藝;溫州蜜柑和常山胡柚作為代表性柑橘皮渣原料,用于對最佳發酵工藝的適用性進行驗證。
1.2 菌種
青霉菌Penicilliumsp. CIs14,實驗室自行篩選的可產高活性纖維素酶的菌株,適用于柑橘皮渣發酵生產膳食纖維,經口急性毒性實驗證明無毒[19]。菌種保存于-80 ℃冰箱,培養基上活化長出孢子后用于發酵種子培養。
植物乳桿菌Lactobacillusplantarum,實驗室自行篩選。菌種保存于-80 ℃冰箱,發酵之前經培養基活化。
1.3 培養基組成及培養條件
植物乳桿菌種子培養液:蛋白胨1.0%(質量分數,下同),牛肉膏1.0%,酵母提取液0.5%,葡萄糖2.0%,乙酸鈉 0.5%,檸檬酸氫二胺0.2%,吐溫-80 0.1%,K2HPO40.2%,MgSO4·7H2O 0.02%,MnSO4·7H2O 0.005%,110 ℃滅菌20 min。將活化后的植物乳桿菌接種于培養基中,28 ℃靜置培養2~3 d。
青霉菌柑橘皮渣種子培養基:柑橘皮和渣按2∶1(質量比)混合均勻,添加蛋白胨0.2%(質量分數,下同)、酵母粉0.1%、MgSO4·7H2O 0.1%,110 ℃滅菌20 min。將活化后的青霉菌孢子制成孢子懸浮液,接入培養基中,接種量10%(質量分數),在28 ℃、相對濕度60%~80%條件下培養3~4 d[19]。
柑橘皮渣發酵培養基:柑橘皮和渣按2∶1(質量比)混合均勻,添加蔗糖2%(質量分數,下同)、蛋白胨0.2%、酵母粉0.1%、KH2PO40.37%、K2HPO40.11%、(NH4)2SO40.3%、MgSO4·7H2O 0.22%,攪拌均勻,分裝于500 mL燒杯中,厚度3~5 cm,110 ℃滅菌20 min。
單一菌種發酵工藝(工藝1):柑橘皮渣發酵培養基接種10%(質量分數)植物乳桿菌或青霉菌,在28 ℃、相對濕度60%~80%條件下培養2或5 d。
青霉菌發酵聯合分段控溫工藝(工藝2):柑橘皮渣發酵培養基中接種10%(質量分數)青霉菌,在28 ℃、相對濕度60%~80%條件下培養5 d,向發酵結束的皮渣中添加100~200 mL無菌水,攪拌均勻,在45 ℃條件下100 r·min-1振蕩培養24 h。
混菌發酵工藝(工藝3):柑橘皮渣發酵培養基中先接種10%(質量分數,下同)植物乳桿菌,28 ℃培養2 d后,接種10%青霉菌種子培養基,在28℃、相對濕度60%~80%條件下培養5 d。
混菌發酵聯合分段控溫工藝(工藝4):柑橘皮渣發酵培養基中先接種10%(質量分數,下同)植物乳桿菌,28 ℃培養2 d后,接種10%青霉菌,繼續于28 ℃、相對濕度60%~80%條件下培養5 d。向發酵結束的皮渣中添加1.5倍體積無菌水,攪拌均勻,在45 ℃條件下100 r·min-1放置24 h。
1.4 發酵樣品后處理
將不同種類柑橘皮渣或發酵產物于80 ℃烘至恒重,粉碎,過50目篩。過篩后的粉末樣品用于測定TDF、SDF和IDF含量。
1.5 膳食纖維提取及含量測定
稱取烘干粉碎過篩后的樣品10 g置于燒杯中,各加入250 mL pH 6.8的PBS緩沖液,超聲30 min至樣品完全分散。加入1 mL木瓜蛋白酶溶液(25 kU·mL-1),用鋁箔蓋住,60 ℃超聲30 min,過濾。濾渣用蒸餾水洗滌3次,每次100 mL,收集合并洗滌液,轉移至燒杯中,加入4倍體積的95%(體積分數,下同)乙醇(預熱至60 ℃),用鋁箔蓋住燒杯,室溫沉淀1 h,過濾,殘渣分別用150 mL 78%乙醇、95%乙醇和丙酮各沖洗2次,50 ℃烘干并稱量,得到SDF含量。殘渣分別用150 mL 78%乙醇、95%乙醇和丙酮各沖洗2次,50 ℃烘干、稱量,得到IDF含量[20],計算得到TDF含量及SDF/TDF。
1.6 數據統計分析
所有數據均采用Excel 2010進行整理,并在SPSS 19.0軟件上進行方差分析。
2 結果與分析
2.1 單一菌種發酵柑橘皮渣產物中TDF和SDF的含量
從表1可以看出,單獨接種植物乳桿菌發酵后的臍橙皮渣中SDF和TDF含量分別為25.8%和81.7%,SDF/TDF為31.5%,比未發酵的臍橙皮渣分別提高150.5%、35.0%和85.3%。單獨接種青霉菌發酵后的臍橙皮渣中SDF和TDF含量分別為31.4%和88.6%,SDF/TDF為35.5%,比未發酵的臍橙皮渣分別提高204.9%、46.4%和108.8%。
表1不同發酵條件下臍橙皮渣中SDF、IDF和TDF的含量
Table1Contents of SDF, IDF and TDF in navel orange peel and pomace under different treatments

%
同列數據后無相同字母的表示差異顯著(P<0.05)。下同。
Data marked without the same letters in the same column indicated significant difference atP<0.05. The same as below.
2.2 不同發酵工藝下臍橙皮渣中TDF和SDF的含量
如表2所示,相較于青霉菌發酵(工藝1),青霉菌發酵聯合分段控溫工藝(工藝2)和混菌發酵工藝(工藝3)下,SDF含量和SDF/TDF顯著(P<0.05)提高,但工藝2和工藝3下各指標并無顯著差異。在混菌發酵聯合分段控溫工藝下,發酵產物中SDF含量和SDF/TDF比單獨接種青霉菌發酵下分別提高33.8%和30.1%,且較工藝2和工藝3條件下也有顯著(P<0.05)提高。
2.3 混菌發酵聯合分段控溫工藝的適用性
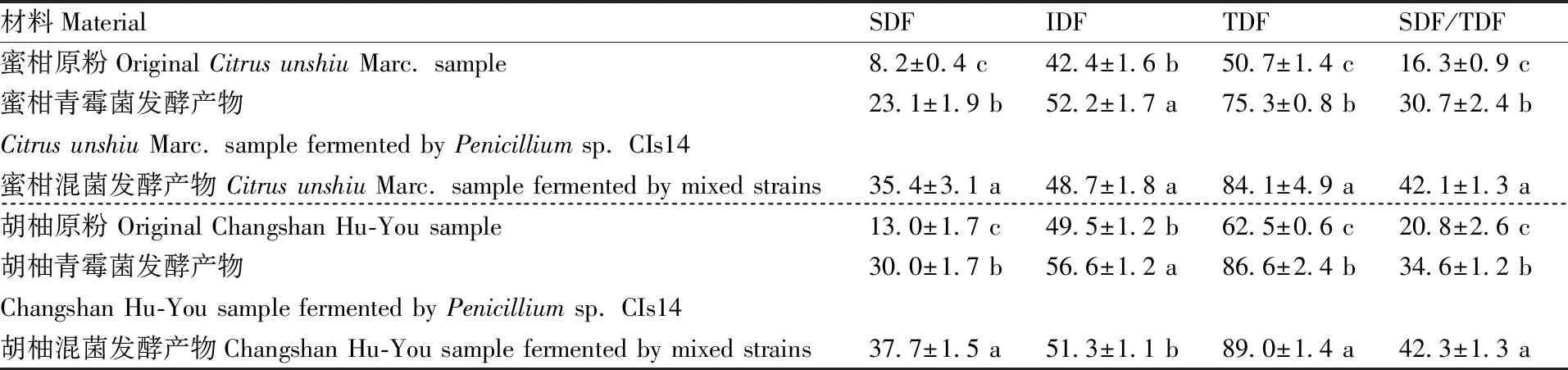
從表3可以看出,采用混菌發酵聯合分段控溫工藝的蜜柑和胡柚皮渣中SDF、TDF含量和SDF/TDF均比未發酵皮渣顯著(P<0.05)提高, SDF含量和SDF/TDF分別比單獨接種青霉菌發酵條件下提高25.6%和22.3%以上。
表2不同發酵工藝下發酵產物中膳食纖維各組分含量
Table2Contents of SDF, IDF and TDF under different fermentation technologies

%
表中工藝1僅采用青霉菌單獨發酵。
In the above table, technology 1 only appliedPenicilliumsp. Cis14 during the fermentation.
表3蜜柑和胡柚皮渣經發酵后膳食纖維中SDF、IDF、TDF含量及SDF/TDF
Table3Contents of SDF, IDF and TDF and SDF/TDF in peel and pomace fromCitrusunshiuMarc. and Changshan Hu-You before and after fermentation
%
3 討論
本研究通過比較不同發酵工藝條件下贛南臍橙皮渣發酵產物中的SDF、TDF含量和SDF/TDF,提出能夠顯著提高臍橙皮渣中SDF、TDF含量和SDF/TDF的混菌發酵聯合分段控溫工藝。利用該工藝發酵臍橙皮渣后,SDF、TDF含量和SDF/TDF高于單獨以青霉菌發酵條件下的對應指標。該工藝同樣適用于以溫州蜜柑和常山胡柚皮渣為原料生產高品質膳食纖維。
植物乳桿菌是以纖維類原料制備膳食纖維的常用菌株之一,發酵過程中產生以乳酸為主的大量有機酸,使纖維素的糖苷鍵斷裂,打斷纖維素大分子的長鏈結構,破壞纖維素原料致密結構,從而提高可溶性膳食纖維的含量,但其作用部位一般在物料表面[16-17,21]。青霉菌分泌的纖維素酶(內切纖維素酶、β-葡萄糖苷酶和濾紙酶)具有較強的纖維素分解能力,可以結合到纖維素大分子上將其水解成可溶于水的分子量較小的糖類,同時降低纖維素的聚合度[17,22]。酶水解纖維素是目前兼具環保綠色、轉化效率高等優點的處理方式[23]。因此,利用青霉菌發酵提高柑橘皮渣中可溶性膳食纖維含量的效果優于植物乳桿菌,這與本研究結果一致。目前報道的可用于發酵法制備膳食纖維的菌種主要為綠色木霉,但前期研究表明,本研究所用青霉菌對柑橘皮渣的發酵性能亦優于綠色木霉[19]。
利用發酵法制備膳食纖維過程中,植物乳桿菌和青霉菌的作用原理不同[16,24]。已有研究表明,先通過物理作用使纖維素結構膨大,然后添加適量纖維素酶,可大幅提高纖維素的水解率[25]。常用纖維素酶的最適溫度范圍為45~75 ℃,但發酵過程中的溫度僅適合菌體大量生長和酶的合成,并不是纖維素酶水解底物的最適溫度[22,24]。因此,單獨接種青霉菌的發酵條件下,雖然菌體大量生長并分泌了足夠的纖維素酶,但纖維素酶的活力并沒有達到最大,導致臍橙皮渣中纖維素水解率較低,使得SDF和TDF含量的提高幅度較小。因此,有必要將不同發酵條件組合進行分步發酵,充分發揮不同條件的優勢作用,進一步提高SDF、TDF含量及SDF/TDF[1]。本試驗結果顯示,在混菌發酵聯合分段控溫條件下,發酵產物中SDF含量和SDF/TDF比單獨接種青霉菌發酵條件下顯著提高33.8%和30.1%。據此,我們推測:首先接種植物乳桿菌發酵后,所產乳酸會破壞臍橙皮渣中表面的纖維結構,使得臍橙表面纖維結構膨大、疏松,暴露出更多的纖維素酶作用位點[21],這使得第二步接種青霉菌發酵所產的纖維素酶與皮渣中纖維素的可及度和有效接觸面積增加,從而提高了臍橙皮渣中纖維素的水解率,最終使得發酵后的臍橙皮渣中SDF含量和SDF/TDF大幅提高。
浙江省是我國柑橘主產區之一,不僅種植面積大,而且品種繁多。混合菌種發酵聯合分段控溫工藝是以臍橙皮渣為原料提出的,因此,本研究特別選擇了另外2種具有代表性的柑橘品種——溫州蜜柑和常山胡柚驗證該工藝的適用性。結果顯示,該工藝對于不同品種的柑橘皮渣適用性良好,且該工藝對柑橘皮渣中SDF含量和SDF/TDF提高幅度高于已有的研究報道[18]。
今后,筆者團隊將從原料纖維結構變化、發酵產品粒徑分析及纖維素組成等方面深入研究該工藝提高SDF、TDF含量和SDF/TDF的作用機理,進一步指導、改進發酵工藝,充分運用柑橘皮渣資源生產高品質膳食纖維。

