基于網絡藥理學預測白藜蘆醇抗胰腺癌靶點與分子機制研究*
徐宵宵 黎榮 陳健,△
(1.桂林醫學院基礎醫學院病理生理學教研室,廣西 桂林 541004;2.廣西腫瘤免疫與微環境調控重點實驗室,桂林醫學院,廣西 桂林 541004)
胰腺癌是一種快速侵襲性和高度轉移性的癌癥,對大多數的臨床化療藥物已產生了耐藥性[1]。因此,開發高效價和低毒性的替代藥物是抗胰腺癌的研究新重點。白藜蘆醇是一種多酚植物抗毒素,存在于葡萄、漿果、花生和葡萄酒中,具有抗氧化、抗炎、抗凋亡和抗癌等藥理活性[2]。白藜蘆醇對治療癌癥有良好的療效,是預防和治療胰腺癌的潛在候選化合物[3]。實驗證明,白藜蘆醇血漿滯留時間較長,能更好地發揮藥物的治療效果,安全且耐受良好[4]。真核拓撲異構酶II是白藜蘆醇的分子靶點之一,它是染色體分離和DNA超螺旋內環境穩定所必需的酶[5]。
網絡藥理學是在系統生物學和多向藥理學快速發展的基礎上提出的藥物設計新方法和新策略,它基于“疾病-基因-靶點-藥物”相互作用網絡的基礎,通過分析基因網絡庫、蛋白網絡庫、疾病網絡庫、藥物網絡庫等現有數據庫的信息資料,結合從實驗中獲得的譜圖數據,利用專業網絡分析軟件及算法,系統的、整體的揭示疾病-疾病、疾病表型-靶點蛋白、靶點蛋白-藥物、藥物-藥物之間的聯系[6],因而為中藥成分-靶點-疾病-機制的研究提供了新的方法。
目前,對白藜蘆醇治療胰腺癌的作用靶點及其分子機制研究較少,為進一步挖掘和整合,本文利用網絡藥理學方法構建“成分-靶點-疾病-通路”相互作用關系網絡,預測白藜蘆醇治療胰腺癌的作用靶點及其可能作用機制,為后續實驗提供參考性依據。
1 材料與方法
1.1 實驗設計
首先,根據實驗設計制定本課題的研究思路流程圖,如圖1。
1.2 白藜蘆醇抗胰腺癌作用靶點的獲取
運用Superpred數據庫獲得白藜蘆醇已驗證靶點和預測靶點,通過Swiss Target Prediction數據庫找到白藜蘆醇的預測靶點;應用DisGeNET數據庫查找胰腺癌相關作用靶點。最后,將各個數據庫白藜蘆醇靶點與胰腺癌相關靶點相映射,獲得白藜蘆醇治療胰腺癌作用的靶點。利用Uniprot數據庫將靶點蛋白名稱轉換成相對應的基因名稱并去除非人源的靶點基因名稱,為后期蛋白互作網絡(PPI)的拓撲分析做準備。
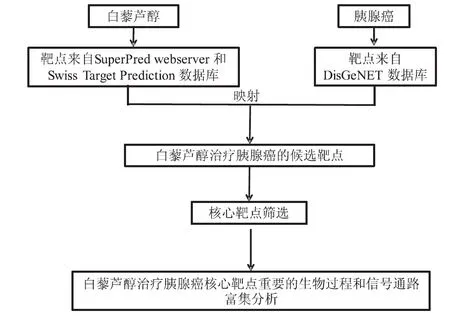
圖1 研究思路設計流程圖
1.3 白藜蘆醇-靶點-胰腺癌PPI網絡構建與拓撲分析
將映射后獲得的白藜蘆醇抗胰腺癌作用靶點在STRING數據庫中獲得靶點-靶點功能相關蛋白間的作用,設置置信度得分>0.9的蛋白相互作用,剔除重復項;并將結果導入Cytoscape_v3.2.1構建白藜蘆醇-靶點-胰腺癌PPI網絡;運用Cytoscape_v3.2.1中Network-Analyzer分析白藜蘆醇-靶點-胰腺癌PPI網絡中平均自由度和最大自由度等拓撲參數,并根據Degree值篩選核心靶點,篩選范圍上限為拓撲數據中的最大Degree值,下限為平均自由度的兩倍。
1.4 核心靶點生物功能和通路富集分析
應用DAVID數據庫獲得核心靶點生物功能和通路富集結果,整理導入Omicshare云平臺對白藜蘆醇抗胰腺癌核心靶點可能調節的生物過程及涉及的信號通路進行可視化,并根據Pvalue繪制生物過程和信號通路高級氣泡圖。
2 結果
2.1 靶點信息
本文通過DisGeNET數據庫共收集到1868個基因作為本次研究疾病靶點。通過SuperPred webserver數據庫檢索到白藜蘆醇的171個驗證靶點,20個預測靶點,并通過Swiss Target Predictio數據庫檢索到15個res作用靶點。去除掉重復的30個靶點,共有176個白藜蘆醇的相關靶點。映射后得到64個交集靶點。
2.2 白藜蘆醇抗胰腺癌靶點及功能相關蛋白相互作用網絡
應用STRING數據庫收集這64個靶點功能相關的蛋白-蛋白相互作用數據,選取置信度得分大于0.9的數據,導入Cytoscape-v3.2.1中,構建白藜蘆醇抗胰腺癌靶點及功能相關蛋白相互作用網絡,如圖2所示,網絡有64個節點,由552條邊相互作用與關聯。
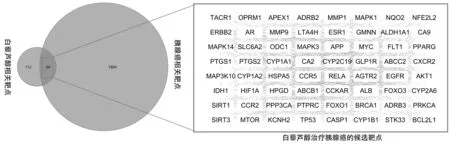
圖2 映射后的核心靶點集合
2.3 PPI網絡拓撲參數分析及核心靶點篩選
應用Network-Analyzer分析白藜蘆醇抗胰腺癌靶點及功能相關蛋白相互作用網絡的拓撲參數表,最短路徑長度越小,介數值越大說明蛋白越重要。通過計算得自由度的中位數為17.25,最大自由度為45,因此將核心靶點篩選條件范圍設為34.5~45,最終獲得7個核心靶點蛋白,分別為TP53、EGFR、PTGS2、AKT1、MAPK3、MYC以及ALB,見圖3。
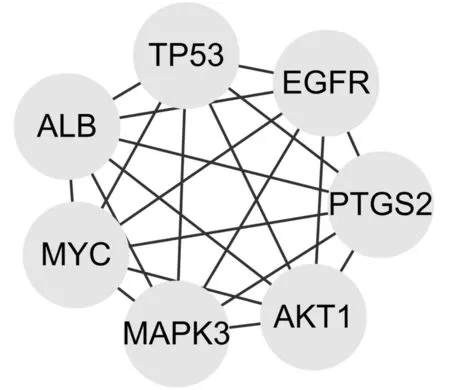
圖3 預測后的核心關聯靶點
2.4 核心靶點的生物功能和通路富集分析
通過DAVID數據庫及omicshare云平臺可視化分析,Top 20生物功能富集分析結果如圖4所示,結果表明,核心靶點的生物過程主要涉及平滑肌細胞增值正調控、細胞對機械刺激的反應、細胞凋亡過程的負調控、細胞對DNA損傷刺激的反應、血管收縮的正調控、細胞對表皮生長因子刺激的反應、一氧化氮生物合成的正調控、細胞對紫外線的反應、RNA聚合酶II啟動子轉錄的正調控、細胞增殖、細胞對藥物反應、磷脂酰肌醇3激酶信號通路的調節、細胞對缺氧的反應、對氧化應激的反應、蛋白磷酸化的正調控、對紫外線的反應、細胞周期蛋白依賴性蛋白絲氨酸的正調控、MAPK信號級聯、排卵、細胞凋亡過程的正調控等。這些生物過程多與炎癥、DNA損傷修復、氧化應激等的發生發展密不可分,表明白藜蘆醇可能是通過調節以上生物過程發揮其抗胰腺癌作用。
通過DAVID數據庫及omicshare云平臺可視化分析,Top 20信號通路富集分析結果如圖4所示。結果表明,核心靶點的KEGG通路主要涉及于宮內膜癌通路、中心碳代謝在癌癥中的通路、癌癥通路、膀胱癌通路、蛋白聚糖在癌癥的通路、非小細胞肺癌通路、結腸直腸癌通路、神經膠質通路、胰腺癌通路、MAPK信號通路、黑素瘤通路、小細胞肺癌通路、ErbB信號通路、前列腺癌通路、P13K-Akt信號通路、甲狀腺激素信號通路、丙型肝炎通路、乙型肝炎通路、甲狀腺癌通路。

圖4 與核心靶點相關的top 20生物學過程和信號通路
3 討論
胰腺癌是一種起病隱匿的高致死性疾病。大多數胰腺癌患者在病情發展到晚期才出現癥狀。大多數胰腺癌發生于胰腺導管內微小的非侵襲性上皮增生,即胰腺上皮內瘤變,并且胰腺癌細胞有廣泛的代謝重編程,使胰腺癌的治療難度大幅度增強[7]。研究表明,胰腺癌有四個主要的驅動基因:KRAS、CDKN2A、TP53和SMAD4[8]。白藜蘆醇的抗氧化和抗炎作用突出,能夠保護胰腺,在糖尿病小鼠試驗中作用顯著[9]。同時有研究表明,白藜蘆醇抑制胰腺癌細胞的增殖[10],誘導細胞凋亡和細胞周期阻滯。借助網絡藥理學的方法對白藜蘆醇抗胰腺癌的作用機制進行探討,發現其多靶點、多通路作用特點。
為了找到白藜蘆醇治療胰腺癌的關鍵靶點,本文利用網絡藥理學挖掘到了176個白藜蘆醇作用靶點以及1868個胰腺癌作用靶點,映射后獲得64個白藜蘆醇治療胰腺癌作用靶點,然后在STRING數據庫獲得白藜蘆醇治療胰腺癌作用靶點及功能相關蛋白相互作用,構建PPI網絡,經過篩選獲得7個核心靶點,分別為TP53、EGFR、PTGS2、AKT1、MAPK3、MYC和ALB。TP53是非常重要的抑癌基因,調節細胞生長和增殖的作用。免疫化學染色顯示,TP53突變的胰腺導管腺癌組織中WISP1蛋白水平的上調更為顯著[11]。白藜蘆醇抗腫瘤的分子機制與抑制表皮生長因子受體(Epidermal growth factor receptor,EGFR)信號有關。蛋白激酶B/AKT有三種亞型AKT1-3,由于其在各種癌癥中的本構激活,在調節細胞生長和增殖方面發揮著中心作用,其中AKT1過表達是高血糖觸發因素[12]。免疫組化和免疫熒光結果顯示,DKK4與MAPK3,VAV3在胰腺癌組織中共表達,推測其與MAPK信號通路激活有關[13]。MYC結合在小鼠腫瘤細胞的神經內分泌基因中富集,促進胰腺導管腺癌導管-神經內分泌譜系的可塑性,導致生存和化療耐受性差。CRP/Alb比值可能是胰腺癌炎癥預后的一個重要且有前途的評分指標[14]。根據文獻分析,我們可以推測白藜蘆醇通過調節胰腺癌細胞內的預測靶點表達,發揮有效的抗癌作用。同時,這些預測靶點可作為潛在的抗胰腺癌分子標記物。此外,通過靶點蛋白進行GO注釋分析和KEGG通路分析,結果顯示大多富集生物學信息與癌癥通路相關。因此,白藜蘆醇抗胰腺癌藥理活性可能是直接通過抑制這些癌癥相關通路有關。
綜上所述,白藜蘆醇抗胰腺癌的藥理機制可能與調控細胞調控及癌癥相關通路密切相關,表明基于網絡藥理學的技術手段預測藥物藥效及分子機制具有一定的準確性和實用性,為進一步探討白藜蘆醇抗胰腺癌的藥理靶點及分子機制奠定了良好基礎。

