MicroRNA-29a 在結直腸癌組織中的表達及意義
蔡銳文,梁偉成,黃冀華,梁華艷,黃開勁,鄧波
(廣東省高州市人民醫院 1.胃腸外科,2.檢驗科,廣東 高州 525200)
微RNA(MicroRNA,miR)作為廣泛存在于生物體內 的短鏈核糖核酸(ribonucleic acid,RNA),可通過影響 靶基因轉錄或翻譯而參與多種生理病理過程[1],同時,在多種惡性腫瘤發生、進展中發揮重要作用[2]。miR-29a 作為miR-29 家族重要成員,與乳腺癌[3]、膠質瘤等[4]惡性腫瘤發生、進展密切相關。本研究擬分析miR-29a 在結直腸癌組織中表達,采用反義寡核苷酸(antisense oligonucleotides,ASO)特異性抑制結直腸癌LoVo 細胞中miR-29a 表達,觀察其對細胞增殖、凋亡的影響。
1 資料與方法
1.1 一般研究
1.1.1 臨床資料 選取2013年3月—2016年4月在廣東省高州市人民醫院治療的結直腸癌患者195 例,術前均未行放化療治療,均經術后病理檢查證實。其中,男性109 例,女性86 例;年齡33 ~82 歲,平均(60.1±12.8)歲;腫瘤部位:結腸91 例,直腸104 例;TNM 分期:Ⅰ期35 例,Ⅱ期64 例,Ⅲ期81 例,Ⅳ期15 例;分化程度:低分化17 例,中分化166 例,高分化12 例。所有患者均于術中留取結直腸癌及距離腫瘤邊緣>4 cm 處的癌旁組織,生理鹽水清洗后置于液氮中,置入-80℃冰箱冷凍保存。研究經本院醫學倫理委員會批準,所有患者均行知情同意。
1.1.2 主要試劑和設備 人結直腸癌LoVo 細胞株購自中科院上海生命科學研究院細胞庫,Trizol 總RNA 提取試劑盒、LipofectamineTM2000 轉染試劑盒、Matrigel 膠購自美國Invitrogen 公司,DMEM 培養基、胎牛血清、胰酶購自美國Gibco 公司,逆轉錄和聚合酶鏈式反應(polymerase chain reaction,PCR)試劑盒購自日本TaKaRa 公司,MTT 試劑盒、DMSO 購自美國Sigma 公司,Transwell 小室購自德國Millipore 公司。
1.2 方法
1.2.1 利用實時熒光定量聚合酶鏈反應(qRT-PCR) 檢測結直腸癌和癌旁組織中miR-29a 表達 取結直腸癌和癌旁組織,研磨后,加入細胞裂解液,用Trizol總RNA 提取試劑盒提取細胞中總miR,利用紫外分光光度計檢測總miR 純度,以A260/A280 在1.80 ~2.10作為合格樣品。將總miR 逆轉錄為模板鏈cDNA,利用PCR 試劑盒進行PCR,引物序列為:正向5'-CG GCGGTAGCACCATCTGAAAT-3',反向5'-CCAGTGCA GGGTCCGAGGTA-3';U6 引物:正向5'-GGAGAGTGT TTCCTCGTCCC-3',反向5'-ATGAAGGGGTCGTTGATG GC-3'。PCR 反應條件:95℃預變性2 min,94℃變性30 s,54℃退火30 s,73℃延伸30 s,重復循環38 次,每個樣品設3 個平行復孔。用2-△△Ct法計算結直腸癌和癌旁組織中miR-29a 相對表達量[5-6]。
1.2.2 細胞培養及分組處理 將LoVo 細胞株置于含10%胎牛血清的DMEM 培養基中,于含5%二氧化碳CO2的37℃恒溫培養箱中常規培養。待細胞對數生長時,胰酶消化后,接種于6 孔板中,調整細胞密度為2×105個/孔,繼續恒溫培養,待細胞融合度在80%左右時,對細胞進行分組轉染:①ASO-miR-29a 組:利用LipofectamineTM2000 轉染試劑盒轉染miR-29a 的ASO 序列5'-ACTGATTTCTTTT GGTGTTCAG-3';②ASO-對照序列組:5'-TCATTGGC ATGTACCATGCAGCT-3';③空白對照組:不作任何處理。轉染后各組細胞繼續恒溫培養,完成后續實驗。
1.2.3 qRT-PCR檢 測 各 組 細 胞 中miR-29a 表 達 取各轉染組轉染后培養48 h 細胞,加入細胞裂解液,其余步驟同1.2.1。
1.2.4 MTT 法檢測各組細胞增殖能力 取各組細胞,胰酶消化后,離心取細胞沉淀,重懸后調整細胞密度為2×104個/ml,各取100 μl 加入96 孔板,各組均設6 個平行反應復孔,于含5% CO2的恒溫培養箱中培養,分別于轉染后12、24、48、72 和96 h 時,將20 μl 的MTT 液加入各孔,孵育4 h,將孔內培養液去除,各加入150 μl 的DMSO 液,振蕩15 ~20 min 待沉淀完全溶解后,利用酶標儀取570 nm 處對各孔吸光度(A)值進行檢測[7]。
1.2.5 Transwell 小室檢測各組細胞遷移能力 取各組轉染后培養48 h 細胞,胰酶消化后收集細胞,利用無血清培養液制備單細胞懸液,調整細胞密度為2×105個/ml。取200 μl 單細胞懸液置于Transwell 小室上室,將800μl 的含20%胎牛血清的培養液加入小室下室,于含5% CO2的培養箱中37℃恒溫培養24 h。將小室取出后,用PBS 沖洗3 次,用棉簽輕輕將小室上散落細胞擦除,多聚甲醛室溫下固定15 min,1%結晶紫染色15 min,PBS 沖洗3 次,用倒置顯微鏡觀察,拍照,計數穿膜細胞數[7]。
1.2.6 Transwell 小室檢測各組細胞侵襲能力 取Matrigel 膠預先平鋪于Transwell 小室上室,風干后以備用。其余步驟同1.2.5。
1.3 統計學方法
數據分析采用SPSS 21.0 統計軟件,計量資料以均數±標準差(±s)表示,比較采用t檢驗、方差分析或重復測量設計的方差分析,兩兩比較采用LSD-t檢驗,影響因素分析采用多元線性回歸分析,P<0.05為差異有統計學意義。
2 結果
2.1 結直腸癌和癌旁組織中miR-29a 表達比較
結直腸癌組織中miR-29a 相對表達量為(1.93± 0.19),癌旁組織中miR-29a 相對表達量為(1.26± 0.12),經t檢驗,差異有統計學意義(t=41.596,P= 0.000)。
2.2 結直腸癌組織中miR-29a 表達與臨床病理特征之間的關系
不同年齡、性別、腫瘤部位、腫瘤大小和分化程度結直腸癌組織中miR-29a 相對表達量差異無統計學意義(P>0.05),而TNM 分期Ⅲ、Ⅳ期和發生淋巴結轉移結直腸癌組織中miR-29a 相對表達量增加,差異有統計學意義(P<0.05),TNM 分期和淋巴結轉移是影響結直腸癌組織中miR-29a 表達的因素。見表1。
2.3 結直腸癌組織中miR-29a 表達影響因素分析
多元線性回歸分析結果顯示,TNM 分期和淋巴結轉移是影響結直腸癌組織中miR-29a 表達的因素(P<0.05)。見表2。
2.4 各組細胞中miR-29a 表達比較
3 組細胞中miR-29a 相對表達量分別為(1.14± 0.07)、(1.84±0.12)和(1.82±0.21),經方差分析,差異有統計學意義(F=45.940,P=0.000),兩兩比較,ASO-miR-29a 組細胞中miR-29a 相對表達量低于ASO-對照序列組和空白對照組(P<0.05)。
2.5 各組細胞增殖能力比較
3 組細胞24、48、72 和96h 時A 值比較,采用重復測量設計的方差分析,結果:①不同時間點的A 值有差異(F=46.351,P=0.000)。②3 組時間A 值有差異(F=102.861,P=0.000),ASO-miR-29a 組與ASO-對照序列組和空白對照組相比A 值比較低,細胞增殖被抑制。③3 組的A 值變化趨勢有差異(F=21.573,P=0.000)。見表3。
表1 不同因素對結直腸癌組織中miR-29a 表達水平的影響 (±s)
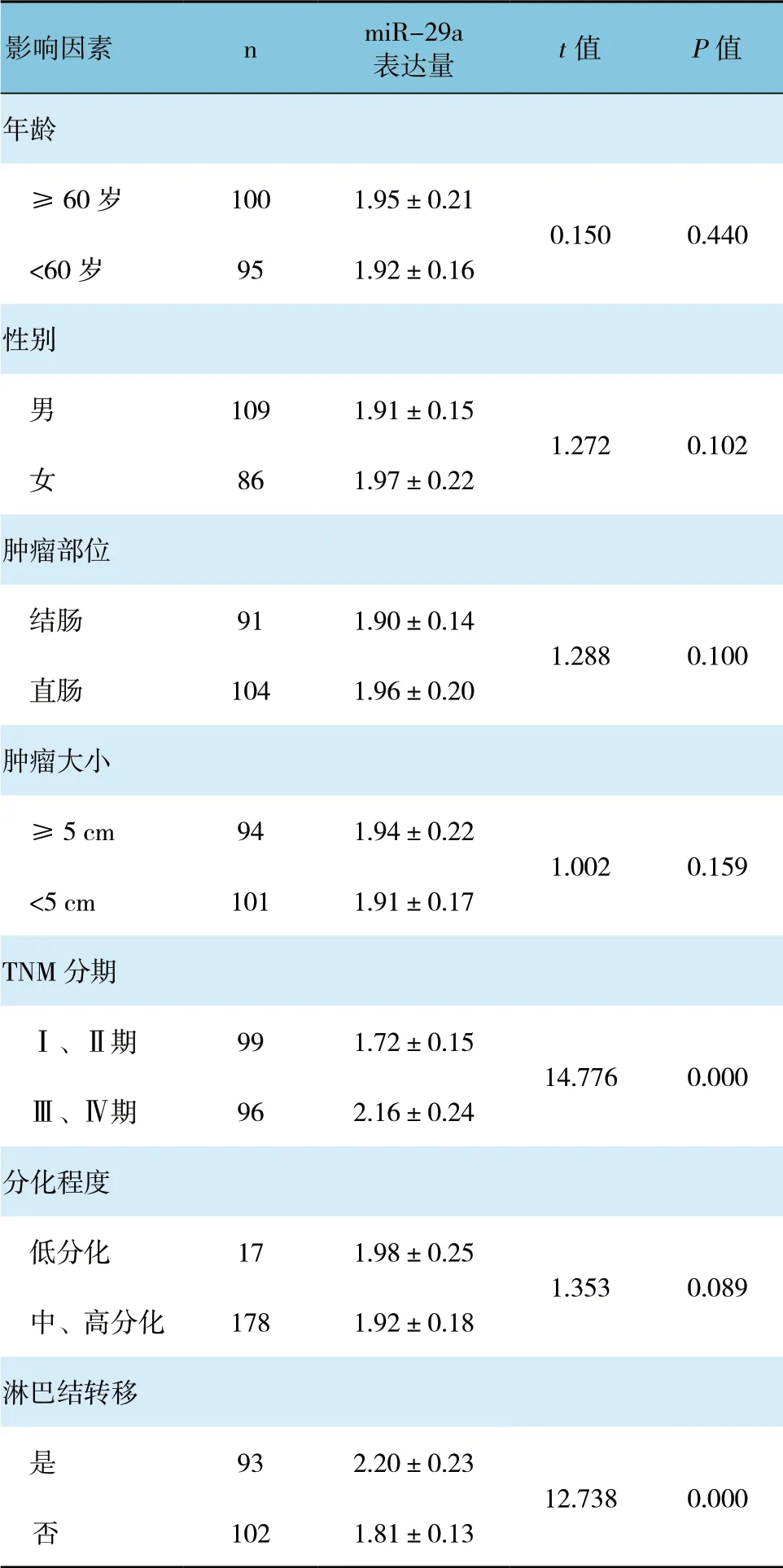
表1 不同因素對結直腸癌組織中miR-29a 表達水平的影響 (±s)
影響因素 n miR-29a 表達量 t 值 P 值年齡 ≥60 歲 100 1.95±0.21 0.150 0.440<60 歲 95 1.92±0.16性別 男 109 1.91±0.15 1.272 0.102 女 86 1.97±0.22腫瘤部位 結腸 91 1.90±0.14 1.288 0.100 直腸 104 1.96±0.20腫瘤大小 ≥5 cm 94 1.94±0.22 1.002 0.159<5 cm 101 1.91±0.17 TNM 分期 Ⅰ、Ⅱ期 99 1.72±0.15 14.776 0.000 Ⅲ、Ⅳ期 96 2.16±0.24分化程度 低分化 17 1.98±0.25 1.353 0.089 中、高分化 178 1.92±0.18淋巴結轉移 是 93 2.20±0.23 12.738 0.000 否 102 1.81±0.13
2.6 各組細胞遷移和侵襲能力比較
3 組遷移細胞數和侵襲細胞數差異有統計學意義(P<0.05),與ASO-對照序列組和空白對照組比較,ASO-miR-29a 組遷移細胞數和侵襲細胞數均減少,差異有統計學意義(P<0.05)。見圖1、2 和表4。

表2 結直腸癌組織中miR-29a 表達影響因素的多元線性回歸分析
表3 各組細胞增殖能力比較 (±s)

表3 各組細胞增殖能力比較 (±s)
組別 12 h 24 h 48 h 72 h 96 h ASO-miRNA-29a 組 0.15±0.04 0.26±0.05 0.31±0.05 0.41±0.14 0.57±0.10 ASO-對照序列組 0.17±0.06 0.40±0.07 0.48±0.05 0.64±0.12 0.80±0.12空白對照組 0.18±0.02 0.41±0.12 0.49±0.06 0.60±0.10 0.87±0.14
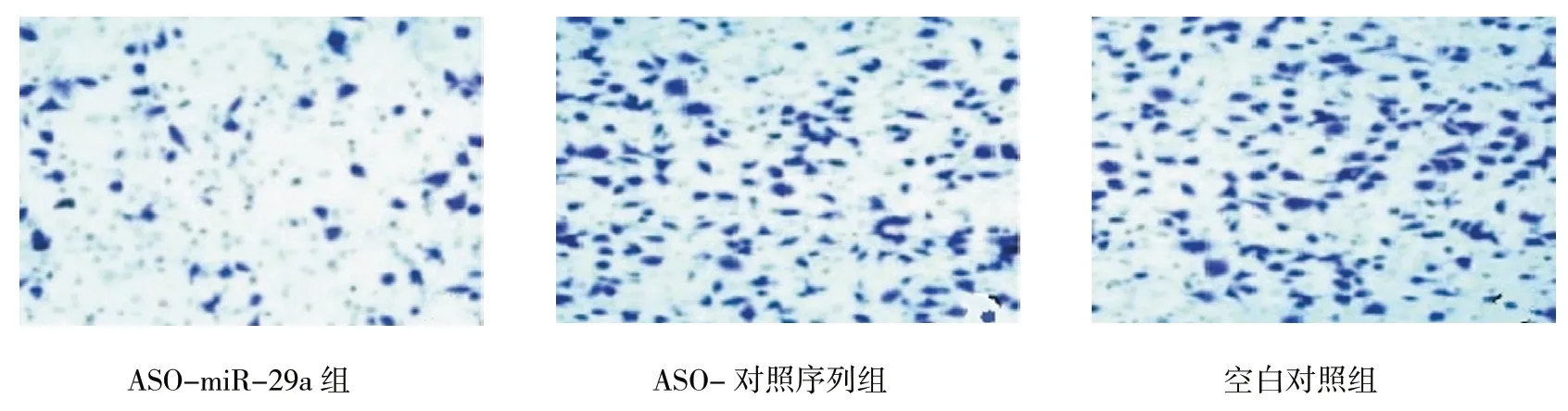
圖1 各組細胞遷移能力比較 (結晶紫×400)
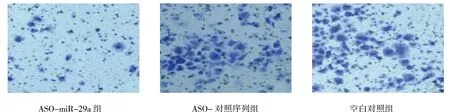
圖2 各組細胞侵襲能力比較 (結晶紫×400)
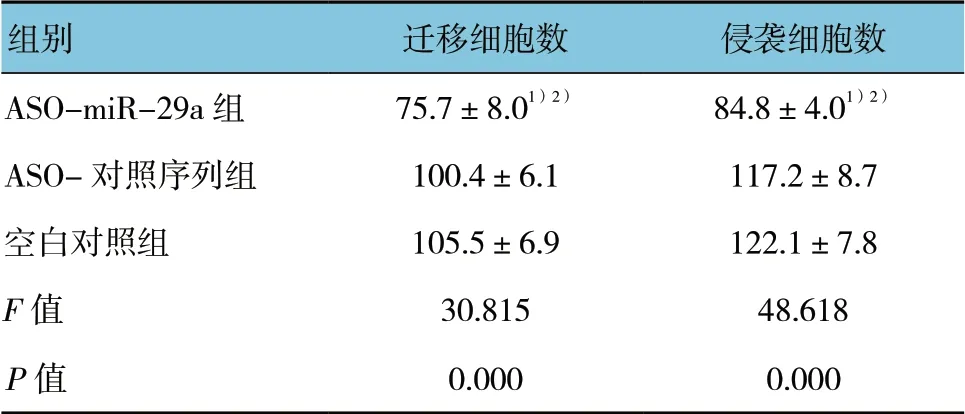
表4 各組細胞遷移和侵襲能力比較 (個,x±s)
3 討論
結直腸癌作為消化道發病率僅次于胃癌的惡性腫瘤,是我國三大癌癥之一,目前尚無特效的治療手段,多數患者預后較差,給我國人群及社會帶來沉重的疾病負擔[8]。近年來研究發現[9],miR 可通過發揮類似癌基因或抑癌基因的作用而參與腫瘤發生、進展過程。亦有研究指出[10],miR 參與調控腫瘤細胞增殖、凋亡、遷移、侵襲等過程。有研究指出[11],結直腸癌患者外周血中多種miR 出現表達異常,其靶基因可能在結直腸癌生長、轉移等過程中發揮關鍵性作用。miR-29a 位于人染色體7q32 上,可通過發揮促癌或抑癌基因功能而參與多種腫瘤發生[12-13]。本研究結果顯示,結直腸癌組織中miR-29a 相對表達量高于癌旁組織,說明miR-29a 在結直腸癌組織中呈高表達,可能參與了結直腸癌發生過程。
本研究結果顯示,TNM 分期和淋巴結轉移是結直腸癌組織中miR-29a 相對表達量的影響因素,TNM分期Ⅲ、Ⅳ期、發生淋巴結轉移的結直腸癌組織中表達量增加,進一步說明miR-29a 可能參與結直腸癌病程進展過程。為進一步探討miR-29a 在結直腸癌發生、進展中的作用,本研究利用ASO 技術特異性抑制結直腸癌LoVo 細胞中miR-29a 表達,結果顯示,ASO-miR-29a 組細胞中miR-29a 相對表達量低于ASO-對照序列組和空白對照組,說明LoVo 細胞中miR-29a 基因表達被抑制。MTT 實驗結果顯示,ASO-miR-29a 組與ASO-對照序列組和空白對照組相比A 值降低,說明特異性抑制miR-29a 基因表達可減少LoVo 細胞增殖,提示miR-29a 可能與結直腸癌細胞增殖有關。本研究結果顯示,與ASO-對照序列組和空白對照組比較,ASO-miR-29a 組遷移細胞數和侵襲細胞數均減少,說明特異性抑制miR-29a 基因表達可有效減少LoVo 細胞遷移和侵襲能力,提示miR-29a 可能參與結直腸癌細胞遷移和侵襲過程。
目前,miR-29a 已證實與多種惡性腫瘤發生、進展有關,且參與了腫瘤多藥耐藥[14],為腫瘤期診斷、分期及預后判定提供了可靠生物學標志物,有望為包括結直腸癌在內的多種惡性腫瘤的靶向治療提供新的靶點,但鑒于腫瘤發生涉及多基因、多步驟,miR-29a在腫瘤發生、進展中的具體作用機制尚待進一步開展后續研究以明確。
綜上所述,miR-29a 在結直腸癌組織中呈高表達,參與結直腸癌發生、進展過程,特異性抑制結直腸癌細胞中miR-29a 表達可減少細胞增殖,抑制細胞遷移和侵襲能力。

