阻塞性睡眠呼吸暫停低通氣綜合征患者不同程度氧減指數(shù)與腎功能早期損害
龐 礴 李濤平 孫耕耘
阻塞性睡眠呼吸暫停低通氣綜合征(obstructive sleep apnea hypopnea syndrome, OSAHS)是以睡眠時(shí)打鼾并伴有呼吸暫停和呼吸表淺,反復(fù)夜間低氧血癥、高碳酸血癥、覺醒和睡眠結(jié)構(gòu)紊亂為主要表現(xiàn)和特征的慢性疾病,在慢性腎臟病中有較高的患病率[1]。早期腎功能損害起病隱匿,臨床表現(xiàn)不典型,易被忽略,目前關(guān)于OSAHS與早期腎功能損害的報(bào)道較少。氧減指數(shù)(oxygen desaturation index, ODI)反映了OSAHS患者夜間期間的間歇性低氧發(fā)生次數(shù),并且與睡眠呼吸暫停指數(shù)(apnea hypopnea index, AHI)有較好的相關(guān)性[2]。本研究探討不同程度ODI的OSAHS患者是否存在早期腎功能損害。
資料與方法
一、研究對(duì)象
研究對(duì)象均來(lái)自南方醫(yī)科大學(xué)南方醫(yī)院睡眠醫(yī)學(xué)中心2014年1月至2015年12月診斷為OSAHS的患者共187例,根據(jù)多導(dǎo)睡眠(polysomnography, PSG)監(jiān)測(cè)結(jié)果中ODI指數(shù)分為三組(輕度5≤ODI<15、中度15≤ODI<30、重度30≤ODI),記錄患者病史、體征及一般情況(性別、年齡等)。監(jiān)測(cè)內(nèi)容包括:腦電、眼電、下頜肌電、口鼻氣流、胸腹運(yùn)動(dòng)、經(jīng)皮氧飽和度及心電、鼾聲、體位。根據(jù)美國(guó)睡眠醫(yī)學(xué)會(huì)(AASM)睡眠及相關(guān)事件判讀手冊(cè)分析睡眠報(bào)告。高血壓、糖尿病、冠心病的診斷分別采用2017年中國(guó)高血壓防治指南、2017中國(guó)2型糖尿病防治指南、2018中國(guó)冠心病診斷與治療指南診斷標(biāo)準(zhǔn)。所有對(duì)象經(jīng)過(guò)嚴(yán)格篩選,排除泌尿系統(tǒng)疾病、前列腺疾病、未控制的高血壓、糖尿病、惡性腫瘤、血液系統(tǒng)疾病及其他可能影響腎臟功能的自身免疫性疾病等,妊娠、哺乳期及服用避孕藥的女性排除在本研究之外。所有受試者均簽署知情同意書。
二、研究方法
實(shí)驗(yàn)者要求在晚上進(jìn)入睡眠監(jiān)測(cè)室,22:00前排出小便并進(jìn)行PSG監(jiān)測(cè),監(jiān)測(cè)大于7 h,次晨6:00臥位空腹抽取靜脈血、留取尿液送檢我院檢驗(yàn)科采用全自動(dòng)生化分析儀查血尿素氮(blood urea nitrogen, BUN)、肌酐(creatinine, Cr)、血清胱抑素C(serum cystine C, sCys-C)、血清β2微球蛋白(serum β2microglobulin, β2-MG)、超氧化物歧化酶(superoxide dismutase, SOD)、尿N-乙酰-β-D氨基葡萄糖苷(N-acetyl-β-d glucosamine, NAG)等指標(biāo)。所有受試者睡前禁止大量飲水、飲濃茶、咖啡及應(yīng)用利尿劑,排空夜間潴留尿液后,采集第一次晨尿檢測(cè)NAG,采用MPT-NAG法測(cè)定。試劑盒由合肥澤木生物科技有限公司提供,所有標(biāo)本均嚴(yán)格按照試劑盒說(shuō)明書操作。
三、統(tǒng)計(jì)學(xué)方法

結(jié) 果
一、患者一般資料比較
各組患者隨著ODI指數(shù)增高,男性比例有逐漸增高趨勢(shì),中重度組患者男性比例明顯偏高,與輕度組患者比較有統(tǒng)計(jì)學(xué)差異(P<0.05);AHI指數(shù)、體重指數(shù)(BMI)及高血壓發(fā)病率隨著ODI指數(shù)升高呈明顯升高趨勢(shì),中重度組與輕度組患者比較有統(tǒng)計(jì)學(xué)差異(P<0.05);各組患者年齡比例分析中,雖然中重度組患者年齡偏大,但各組比較無(wú)顯著統(tǒng)計(jì)學(xué)差異(P>0.05);基礎(chǔ)疾病統(tǒng)計(jì)發(fā)現(xiàn)各組患者糖尿病、冠心病發(fā)病率隨著ODI指數(shù)升高有升高趨勢(shì),但組間比較無(wú)顯著統(tǒng)計(jì)學(xué)差異(P>0.05);各組間相關(guān)性分析發(fā)現(xiàn),ODI指數(shù)與AHI、BMI、性別、高血壓發(fā)病率存在明顯正相關(guān)(r=0.832、0.257、0.578、0.381,P<0.05),見表1。
二、患者腎功能指標(biāo)比較
各組患者指標(biāo)分析中sCys-C、β2-MG、尿NAG隨著ODI指數(shù)升高有明顯升高趨勢(shì),組間比較有統(tǒng)計(jì)學(xué)差異(P<0.05);SOD隨著ODI指數(shù)升高有下降趨勢(shì),組間比較有統(tǒng)計(jì)學(xué)差異(P<0.05);BUN、Scr隨著ODI指數(shù)增高有升高趨勢(shì),但各組間比較無(wú)明顯統(tǒng)計(jì)學(xué)差異(P>0.05);各組間相關(guān)性分析發(fā)現(xiàn),ODI指數(shù)與sCys-C、β2-MG、尿NAG存在正相關(guān)(r=0.0.312、0.245、0.267,P<0.05);ODI指數(shù)與SOD呈負(fù)相關(guān)(r=-0.383,P<0.05),見表2。
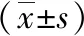
表1 各組臨床特征的統(tǒng)計(jì)描述及單因素分析比較結(jié)果
注:a與1組比較P<0.05;b與2組比較P<0.05
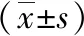
表2 各組患者ODI與生化檢驗(yàn)結(jié)果
注:a與輕度組比較P<0.05;b與中度組比較P<0.05
討 論
OSAHS是一種常見的睡眠結(jié)構(gòu)紊亂性疾病,可導(dǎo)致高血壓、腦血管疾病、2型糖尿病、脂代謝異常及肝腎功能損害等多種并發(fā)癥[3-4],流行病學(xué)調(diào)查顯示OSAHS的平均發(fā)病率在中年人群中達(dá)2%~4%[5]。目前OSAHS的診斷及嚴(yán)重程度的判定主要標(biāo)準(zhǔn)是AHI,但AHI需經(jīng)多導(dǎo)睡眠監(jiān)測(cè)獲取,而ODI為夜間平均每小時(shí)指尖血氧飽和度下降4%的次數(shù),臨床上較容易獲取,與AHI一致性高,能有效的反映夜間間歇性低氧的發(fā)生次數(shù)[2,6- 7]。
從1990年到2010年的二十年間,全世界慢性腎臟疾病(chronic kidney disease, CKD)的死亡率增加了82%,OSAHS作為CKD的獨(dú)立致病因素,已經(jīng)受到臨床醫(yī)師的注意[8-11]。早期腎功能損害起病隱匿容易被人忽略,許多患者由此進(jìn)展為腎病終末期,嚴(yán)重影響了生活質(zhì)量和壽命[3]。
對(duì)于OSAHS引起腎功能損害的機(jī)制,Sim等[12]研究報(bào)道OSAHS對(duì)腎臟功能的影響涉及濾過(guò)功能、重吸收功能和分泌功能等多方面。Mavanur等[13]報(bào)道,慢性間歇性缺氧通過(guò)刺激交感神經(jīng)系統(tǒng)、內(nèi)皮功能紊亂、氧化應(yīng)激及炎癥反應(yīng)引起腎損害。鐘旭等[14]研究報(bào)道,OSAHS夜間發(fā)生的間歇性缺氧刺激交感神經(jīng)使其興奮性升高,進(jìn)一步激活腎素-血管緊張素-醛固酮系統(tǒng)產(chǎn)生強(qiáng)大的縮血管作用,其收縮腎出球小動(dòng)脈的作用強(qiáng)于入球小動(dòng)脈,繼而引起缺血性腎損害和蛋白尿;反復(fù)低氧血癥,高碳酸血癥,可相繼引起肺動(dòng)脈高壓,右心房壓力升高,中心靜脈壓升高,腎靜脈壓力升高,腎小球毛細(xì)血管靜脈壓升高,從而使腎小球基底膜的晶體結(jié)構(gòu)發(fā)生可逆性改變,產(chǎn)生蛋白尿。
臨床上常用BUN、SCr評(píng)估腎小球?yàn)V過(guò)功能,但敏感性較差。一般認(rèn)為當(dāng)腎小球?yàn)V過(guò)率降至正常50%以下時(shí),血清BUN才開始升高,而當(dāng)腎小球?yàn)V過(guò)率降至正常的1/3以下時(shí),SCr才會(huì)迅速升高,因此不能作為腎臟早期損害的指標(biāo)[15]。sCys-C能自由通過(guò)腎小球?yàn)V過(guò)膜,并在近曲小管幾乎完全被重吸收和降解,可反映腎功能早期損害和腎小球?yàn)V過(guò)率迅速變化[16]。β2-MG也能自由通過(guò)腎小球?yàn)V過(guò)膜,當(dāng)腎小球?yàn)V過(guò)功能下降時(shí)血β2-MG 升高,故血β2-MG 也是評(píng)價(jià)腎小球?yàn)V過(guò)功能的理想指標(biāo)。NAG是細(xì)胞內(nèi)溶酶體水解酶,來(lái)自于腎近曲小管上皮細(xì)胞溶酶體中,是腎小管損傷的敏感指標(biāo)[17]。sCys-C、血β2-MG、NAG升高均可提示存在早期腎功能的損害。
有學(xué)者認(rèn)為OSAHS患者由于慢性間歇性低氧所致的大量的氧自由基和炎癥反應(yīng)會(huì)造成腎小球上皮足突融合,減小腎小球?yàn)V過(guò)膜的通透性,進(jìn)而導(dǎo)致sCys-C濃度升高[18]。而國(guó)內(nèi)外學(xué)者在研究中發(fā)現(xiàn)OSAHS患者sCys-C的平均水平明顯高于健康對(duì)照組,此外重度OSAHS組sCys-C濃度較輕、中度組明顯升高[19-21]。Zhang等[22]發(fā)現(xiàn)sCys-C濃度與AHI、低氧指數(shù)有正相關(guān)。而在對(duì)β2-MG的研究中,有學(xué)者發(fā)現(xiàn),輕、中度OSAHS 組血清β2-MG 含量與健康對(duì)照組相比無(wú)顯著性差異,重度OSAHS 組血β2-MG 含量明顯升高[23],提示當(dāng)腎小球?yàn)V過(guò)功能下降時(shí),血β2-MG的升高早于血肌酐和尿素氮的升高,早于GFR的下降。同樣,相關(guān)研究表明OSAHS患者夜間發(fā)生的慢性間歇性低氧可破壞腎小管上皮細(xì)胞膜結(jié)構(gòu),使尿NAG水平明顯升高[24]。NAG在腎功能早期損傷時(shí)的敏感度、特異性、準(zhǔn)確性分別為96.9%、90.2%、91.6%[25]。研究發(fā)現(xiàn),OSAHS組患者尿NAG水平顯著高于健康組,OSAHS患者重度組尿NAG明顯高于輕、中度組,并且尿NAG濃度與AHI呈正相關(guān),與MSaO2和LSaO2均呈負(fù)相關(guān),聯(lián)合檢測(cè)尿NAG和尿α1-MG較單一指標(biāo)陽(yáng)性更高,可動(dòng)態(tài)觀察腎小管間質(zhì)病變過(guò)程[26-27]。慢性間歇性低氧可促使機(jī)體活性氧的產(chǎn)生增加,啟動(dòng)炎癥級(jí)聯(lián)反應(yīng),分泌多種細(xì)胞因子、趨化因子及黏附分子,影響小血管緊張度的調(diào)節(jié)、血管的收縮及激素類產(chǎn)物的修飾,從而導(dǎo)致廣泛的血管內(nèi)皮損傷、內(nèi)皮功能不良[28],而SOD是反映機(jī)體抗氧化能力的客觀指標(biāo),其下降提示重度OSAHS患者處于氧化應(yīng)激狀態(tài)。
本研究中發(fā)現(xiàn)隨著ODI程度的增加,BUN、SCr未有明顯升高,但sCys-C、β2-MG、NAG呈升高趨勢(shì),且3組患者的差異有統(tǒng)計(jì)學(xué)意義,SOD隨著ODI指數(shù)升高有下降趨勢(shì),重度OSAHS患者的sCys-C、β2-MG、NAG較輕、中度患者明顯升高,而SOD較輕、中度患者明顯降低,提示在BUN、SCr未出現(xiàn)異常時(shí),重度OSAHS患者已發(fā)生了早期腎功能損害。其損害機(jī)制可能與慢性間歇性低氧誘發(fā)的氧化應(yīng)激和炎癥反應(yīng)有關(guān)。
- 中華肺部疾病雜志(電子版)的其它文章
- CP和PBL教學(xué)在呼吸內(nèi)科護(hù)理帶教中的聯(lián)合應(yīng)用
- 塵肺合并肺結(jié)核患者心理健康與社會(huì)支持相關(guān)性分析
- 一體化護(hù)理對(duì)老年慢性支氣管炎患者睡眠質(zhì)量及負(fù)性情緒的影響分析
- 多索茶堿聯(lián)合無(wú)創(chuàng)呼吸機(jī)治療對(duì)AECOPD合并呼吸衰竭患者血?dú)狻⑸笜?biāo)及不良反應(yīng)的影響
- FeNO與誘導(dǎo)痰細(xì)胞分類檢測(cè)的相關(guān)性
- 快速康復(fù)外科護(hù)理對(duì)單孔胸腔鏡肺葉切除術(shù)后患者肺功能的影響分析

