胰島素抵抗合并高尿酸血癥大鼠模型的建立及其比較
劉孟淵, 馮學軒, 黎莉斯, 張美藝
(1. 廣州市中醫醫院, 廣州 510130; 2. 廣東省醫學實驗動物中心, 佛山 528248)
高尿酸血癥(hyperuricemia, HUA)目前已經成為繼糖尿病之后最為常見的代謝性疾病。HUA 是痛風最重要的生化基礎[1]。臨床上,單純HUA 及痛風較為少見,尤其在中老年患者。大量流行病學及臨床研究顯示,HUA 和代謝綜合征(metabolic syndrome, MS)往往聚集性出現在同一個體,MS 患者70%同時合并HUA,HUA 也常與MS 各項指標伴發,如HUA 合并3 種以上代謝性危險因素的比例,男性和女性分別高達76.92%和67.64%[2,3]。MS 的發病率隨著血尿酸水平的增加而升高,而HUA 亦常伴隨著MS 、IR 及高胰島素血癥。因此有人認為MS 與HUA 可能互為因果關系,提出將HUA 納入MS 的一個組分[4]。
胰島素抵抗(insulin resistance, IR)是MS 的病理基礎和病理生理過程的核心環節[5]。從HUA 與MS的緊密聯系亦可以推測HUA 與IR 密切相關,大量的臨床研究也證實了這一點[6-8]。鑒于目前尚無理想而符合人類HUA發病過程的HUA動物模型。本實驗模擬人類高脂高糖飲食誘導IR 狀態,,分別制備了大鼠IR-HUA 模型、HUA 模型及IR 模型,并對這三種模型之間的相關性進行了比較分析。
1 材料與方法
1.1 實驗動物
SPF級雄性SD 大鼠40 只, 體質量146.5~172.8 g,由廣東省醫學實驗動物中心提供 [SCXK(粵)2013-0002]。飼養于SPF 級動物實驗室[SYXK(粵)2013-0002]。
1.2 藥物、試劑與儀器
自制高脂飼料(每千克高脂飼料含15 g 食鹽、100 g 白糖、200 g 豬油、22.5 g 蛋黃粉, 662.5 g普通飼料), 由廣東省醫學實驗動物中心生產。結晶果糖購自山東西王糖業有限公司(批號201606232),使用時配制成質量分數10%果糖水。酵母膏購自北京奧博星生物技術有限責任公司生產( 批號20161028),使用時用純凈水配制成0.8 g/mL 酵母膏。多聚甲醛購自廣東光華科技股份有限公司(批號20161107)。日立7020 全自動生化分析儀購自日本日立公司。
1.3 方法
1.3.1 動物分組 40只雄性SD大鼠適應性喂養后,測量身長和稱重,按體質量隨機分為正常對照組(A 組)、HUA 組(B 組)、胰島素抵抗-高尿酸血癥(IR-HUA)組(C 組)、IR 組(D 組),每組10 只大鼠。
1.3.2 動物造模 動物分組后, A 組、B 組喂飼普通飼料, 飲用動物飲用水; C 組、D 組喂飼自配高脂飼料, 飲用10%果糖水; 共造模8 周。第6 周始,HUA 組、IR-HUA 組按20 mL/kg 體質量每日灌胃0.8 g/mL 濃度的酵母膏(相當于16 g/kg), 連續21d。
1.3.3 指標檢測 造模第6 周末,各組大鼠稱重,測體長,采集各大鼠6 h 尿液,采集尿液期間禁食并換為正常飲用水, 其后大鼠按10 mL/kg 體質量腹腔注射(i.p.)質量分數3%戊巴比妥鈉溶液麻醉,眼眶靜脈竇采血,3 000 r/min 離心10 min 收集血清,檢測空腹血糖(fasting plasma glucose, FPG),空腹胰島素(fasting insulin, FINS),血尿酸(serum uric acid, SUA)及尿尿酸(urine uric acid, UUA)含量。
造模第8 周末,試驗結束前1 d,各大鼠稱重,量體長,并收集6 h 尿液,測量尿液體積,檢測UUA 及尿肌酐(urine creatinine, UCr)。試驗結束當日, 禁食6 h 并換為正常飲用水后, 每只大鼠按20 mL/kg 體質量i.p.3% 戊巴比妥鈉溶液麻醉, 腹主動脈采血致死, 3 000 r/min離心10 min收集血清, 檢測FPG、FINS、SUA 及血清肌酐(serum creatinine,SCr); 并摘取兩側腎臟、胰腺、小腸(空腸),以質量分數4% 多聚甲醛固定,作組織病理學檢測。
完成各組大鼠的理化檢測后,計算以下指標:①Lee’s指數體 長 ( c m ) , ,②尿酸排泄總量=尿尿酸濃度×排尿體積,③尿酸排泄分數(fraction excretion of uric acid, FEUA)=(尿尿酸×血肌酐/尿肌酐×血尿酸)×100%, ④穩態模型胰島素抵抗指數(insulin resistance index in homeostasis model, HOMA-IR)=FPG×FINS/22.5。
1.4 統計學處理
2 結果
2.1 各組大鼠體質量
與A 組比較, 各組大鼠體質量均下降。B 組自實驗開始至酵母膏灌胃前的大鼠體質量與A組的差別無統計學意義, 而給予酵母膏灌胃后的體質量下降較明顯(均為P<0.01)。喂飼高脂高糖的C 組、D組大鼠體質量自8 d 始下降,而且體質量下降較明顯(均為P<0.01)。
各模型組之間比較,造模56 d,B 組大鼠體質量高于C 組和D 組(均為P<0.01)。
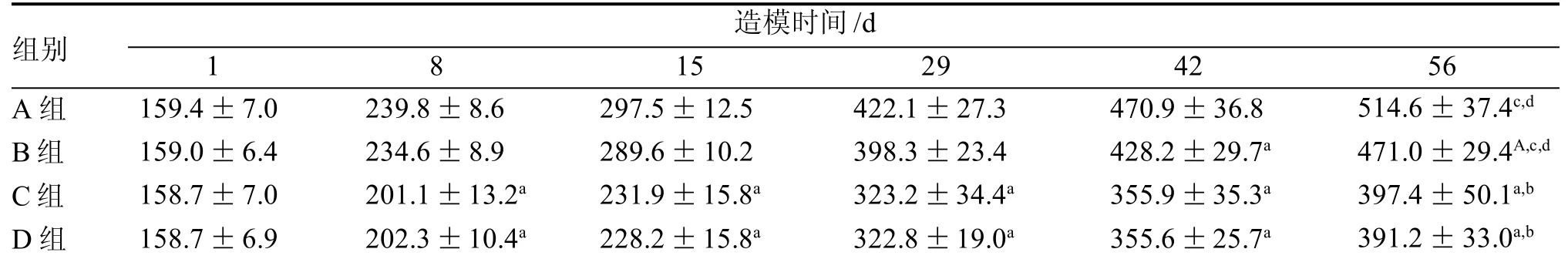
表1 HUA、IR-HUA、IR 模型的建立及比較實驗期間各組大鼠體質量 g
2.2 各組大鼠Lee’s 指數
與A 組相比, 第6 周末,B 組Lee’s 指數下降(P<0.01); 第8 周末,D 組Lee’s 指數下降(P<0.05)(表2)。
PCR擴增法檢測99株CNS的耐藥基因mecA,了解β-內酰胺類藥物耐藥機制。本研究中從A組結核合并感染患者中分離的CNS中,PCR法與MIC法檢出率均為92.6%,50株MRCOS檢出了mecA基因;從B組非結核患者中分離的CNS中,PCR法檢出率為84.4%,而通過MIC法檢出率為86.7%,39株MRCOS只有38株檢出了 mecA基因;PCR法檢測B組MRCOS中有1株沒有檢出mecA基因,考慮與mecA基因存在異質性改變有關[14],但兩組MRCNS的耐藥性及耐藥基因檢出率基本相符。因而可以推斷mecA基因在結核和非結核感染的MCNS中有很高攜帶率,嚴重耐藥性不容小覷。
各模型組之間比較, 第6 周末, B 組Lee’s 指數低于C 組及D 組(均為P<0.01); 第8 周末,C 組的Lee’s 指數高于D 組(P<0.05)。

表2 各組大鼠Lee’s 指數比較
2.3 各組大鼠相關生化指標
2.3.1 大鼠SUA、UUA、SCr、UCr含量 與A組相比,第8 周末B 組SUA 升高(P<0.05),其余各模型組于第6 周末、第8 周末的SUA均略有升高,但差異無統計學意義(P>0.05)(表3)。
與A 組相比,第6 周末,D 組UUA 濃度上升(P<0.01),C 組和B 組的UUA 濃度分別略有升、降(但P>0.05); 第8 周末,B 組、C 組及D 組UUA 的濃度上升(均為P<0.01)。
與A 組相比,第8 周末,D 組SCr 濃度及UCr濃度均升高(分別為P<0.01、P<0.05)。
各模型組之間比較,第6、8 周末,各模型組的SUA 水平之間差異無統計學意義。
第6 周末,B 組的UUA濃度低于C 組(P<0.05)和D 組(P<0.01); C 組的UUA 濃度高于B 組而低于D組(均為P<0.05); D組的UUA濃度高于B組(P<0.01)和C 組(P<0.05); 第8 周末,B 組的UUA 濃度低于D 組(P<0.05);
第8 周末, D 組的SCr 及UCr 均值最高。D 組的SCr 高于C 組(P<0.05), D組的UCr高于B組(P<0.01)。
各模型組之間比較, 第6 周末,B 組的排尿體積高于其余兩個模型組(均P<0.01); 第8 周末,B組的排尿體積高于C 組(P<0.05)和D 組(P<0.01)。
第6、8 周末, B 組的尿酸排泄總量均高于C 組和D 組(均P<0.01); 第8 周末,C 組的尿酸排泄總量低于B 組(P<0.01)而高于D 組(P<0.05); D 組的尿酸排泄總量低于B 組(P<0.01)和C 組(P<0.05)。
第8 周末,依B 組→C 組→D 組,FEUA 逐漸下降,但各模型組間差異無統計學意義。
2.3.3 大鼠FPG、FINS、HOMA-IR水平 與A組相比(表5),第6 周末,各組FPG 值差異無統計學意義(P>0.05); 第8 周末, D 組FPG 值升高(P<0.05)。與A 組相比, 第6、8 周末, C 組、D 組的FINS 含量均下降(分別為P<0.05、P<0.01); 第6、8 周末,B 組FINS 含量與A 組差異均無統計學意義。FINS含量下降可能與胰島損傷,胰島素分泌減少有關。

表3 各組大鼠SUA、UUA、SCr、UCr 水平的比較
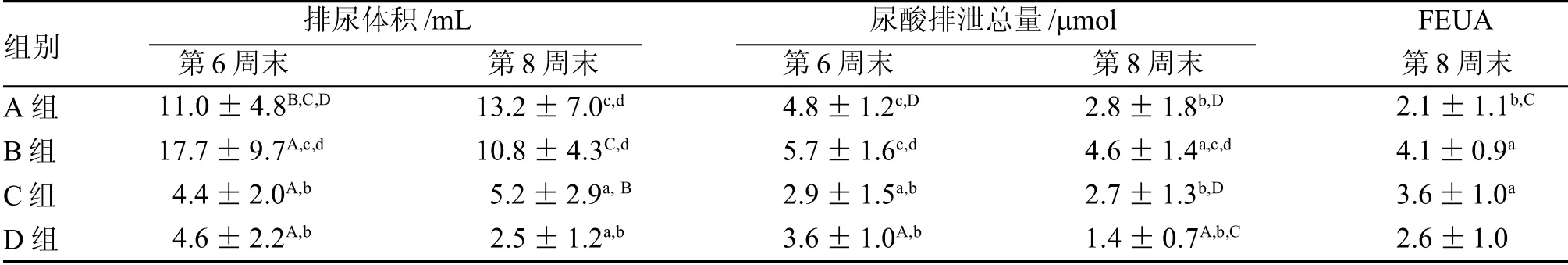
表4 各組大鼠排尿體積、尿酸排泄總量及尿酸排泄分數的比較
第8 周末, 各模型組HOMA-IR 指數值均下降,其中C 組與A 組的差異有統計學意義(P<0.05)。
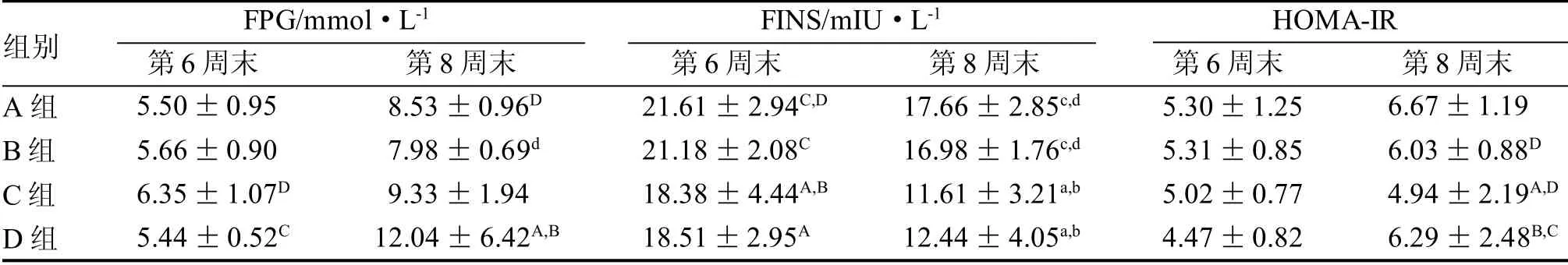
表5 各組大鼠FPG、FINS、HOMA-IR 的比較
各模型組之間比較, 第6 周末, C 組的FPG 水平高于D 組(P<0.05); 第8 周末, B 組的FPG 水平低于D組(P<0.05); D組的FPG水平高于B組(P<0.01)。
第6周末,B組的FINS水平高于C組(P<0.05);第8 周末,B 組的FINS 水平高于C 組、D 組(均為P<0.01)。
第8周末,D 組的HOMA-IR指數值高于B組、C 組(均為P<0.05)。
2.4 大鼠腎臟、胰腺及小腸組織的病理變化
各組大鼠腎臟組織病理檢測均可見腎小管擴張(≤20%), 腎小球形態規則, 未見異常病理改變; 胰腺組織病理檢測均可見腺泡萎縮, 分泌減少(>40%);小腸組織病理檢測均可見腸絨毛萎縮(>40%); 顯示A 組及各模型組的腎臟、胰腺、小腸組織的病理檢測結果無明顯差異(圖1)。
3 討論
本實驗基于臨床HUA常與MS的組分聚集出現即HUA常伴有IR的臨床特征[9],提出模擬人類HUA乃至MS 發病的常見飲食習慣,以高脂高果糖膳食喂飼聯合酵母膏灌胃誘導IR-HUA 大鼠模型,期望為制備IR-HUA 動物模型創建新的方法,并為研究IR在HUA發病機制中的作用,以及HUA治療藥物的研究開發提供新的HUA 動物模型。
為探索有效、穩定、優化的IR-HUA 模型的制備方法,本文開展了IR-HUA 模型、HUA 模型、IR 模型的制備及其比較研究, 上述三種動物模型的評價方法參考楊傳經等文獻[10,11]報道制訂: ①IR-HUA模型: SUA、HOMA-IR 水平大于A 組均數+2 倍標準差,則可判定IR-HUA模型造模成功, IR-HUA模型大鼠在SUA 升高的同時存在HOMA-IR 指數、Lee’s 指數均升高等IR 表現; ②HUA模型血清SUA水平大于A組均數+2倍標準差者為HUA合格動物模型; ③IR 模型血清FPG、HOMA-IR水平大于A組均數+2 倍標準差者, 則可判定合格IR 動物模型。
結果顯示,造模6周時各組大鼠模型特征不明顯。實驗第8 周末,各模型組動物的表現如下:①B 組的SUA、UUA 均升高, 尿酸排泄總量增加,FEUA 升高,顯示HUA 模型初步顯現,提示給予大鼠酵母膏每日16 g/kg灌胃21 d可制備HUA模型,但需增加酵母膏灌胃的劑量,以期增加SUA 升高的幅度。②C 組的UUA 和FEUA 升高,INS 下降、HOMA-IR 值下降、排尿體積減少; FPG、SUA升高,但差異無統計學意義; Lee’s 指數值、UUA 排泄總量均無明顯變化; 提示給予大鼠喂飼高脂高糖飼料、飲用10%果糖水5周后再予酵母膏每日16 g/kg灌胃21 d, 制備的IR-HUA 模型FPG、SUA 升高幅度不足, IR 表現不明顯, 模型欠理想。③D 組的FPG、UUA 水平升高,Lee’s 指數、FINS、排尿體積及UUA 排泄總量下降;而SUA、FEUA 略升高、HOMA-IR值略下降,但均無統計學意義; 提示給予大鼠喂飼自配高脂高糖飼料、飲用10%果糖水造模8 周制備的IR 模型, 雖FPG 升高、但HOMA-IR值亦略下降,該IR 模型尚欠理想,可能造模時間較短之故。實驗結果顯示,SUA 升高多伴隨著UUA、FEUA 的升高,提示SUA 的升高,導致腎臟尿酸排泄增加,UUA 濃度上升。

圖1 各組大鼠腎臟、小腸、胰腺組織病理學觀察 (HE ×200)
本實驗D 組的SCr、UCr 同步升高, 提示SCr濃度升高, 可致UCr 排泄增加,UCr 濃度升高。實驗結果表明, 高脂高糖飲食可致大鼠排尿體積減少,尿酸排泄下降; 并可致大鼠胰島素分泌減少,導致血糖升高。實驗結束后,各組大鼠腎臟、胰腺、小腸組織的病理檢測結果未見明顯差異,提示本實驗各造模條件未造成大鼠組織的病理性損害。
綜上所述,本實驗結果表明,雄性SD 大鼠酵母膏每日16 g/kg灌胃21 d可制備HUA模型。可能因造模時間過短,單純給予高脂高糖飲食8 周誘導大鼠IR 模型,大鼠未出現明顯的IR 特征。因此,以高脂高果糖膳食喂飼聯合酵母膏灌胃誘導大鼠IR-HUA 模型,亦有待進一步完善造模方法,是否高脂高果糖飼料口感不佳、以及灌胃酵母膏可影響大鼠食欲,導致攝食減少及體質量減輕明顯,可能亦是建模不理想的原因。

