光合作用中光反應的機制和由來(3)
朱欽士 (美國南加州大學醫學院)
(上接2019年第3 期第10 頁)
4 所有傳遞電子的蛋白質都含有輔基
蛋白質在催化化學反應上似乎是“無所不能”的,生命活動所需要的數千種化學反應,絕大多數都是由蛋白質催化的。然而,蛋白質自身在催化氧化還原反應、在分子間傳遞電子上卻是“無能為力”的,因為在氨基酸的側鏈中,沒有一個是可用于傳遞電子的。 但細胞中的氧化還原反應又需要蛋白質分子進行催化并傳遞電子,怎么辦?蛋白質分子采取的辦法是“搬救兵”,即將那些能傳遞電子的結構成為自己的一部分,稱為“輔基”(prosthetic group)。所有傳輸電子的蛋白質都帶有輔基。輔基主要有以下幾類。
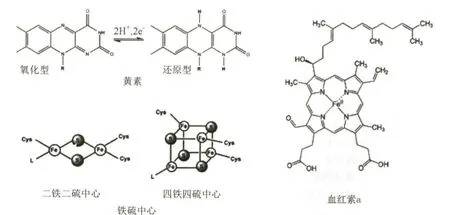
圖3 進行氧化還原反應的蛋白質的輔基
4.1 含有黃素的輔基 黃素(flavin)是3 個環并聯組成的雜環分子(“雜環”表示組成環的原子除碳原子外,還有其他元素的原子,例如氮原子或氧原子)(圖3),黃素分子上連一個核糖,就成為“核黃素”(riboflavin)。 核黃素分子上再連一個磷酸根,就成為“黃素單核苷酸”(flavin mononucleotide,簡稱FMN)。 如果黃素通過2 個磷酸根與腺苷相連,就形成“黃素腺嘌呤二核苷酸”(flavin-adenine dinucleotide,簡稱FAD)。 黃素上的2 個氮原子能反復接收和送出2 個氫原子, 因此像醌分子一樣可以傳遞氫原子:FAD 可接收2 個氫原子變為FADH2,FADH2也可失去2 個氫原子變回FAD;同樣,FMN 可接收2 個氫原子變為FMNH2,FMNH2也可失去2 個氫原子變回FMN。 FMN 和FAD 都可結合在蛋白質分子上,作為傳遞氫原子的輔基。
4.2 鐵硫中心 鐵原子和硫原子本來就容易在自然界中彼此結合,形成各種含鐵和硫的結構,并且可能在催化初期的生命活動中起過作用, 后來被蛋白質分子“收容”,成為傳遞電子的輔基,這樣的蛋白質稱為“鐵硫蛋白”(iron-sulfur protein),其中含有鐵和硫的結構稱為鐵硫中心(iron-sulfur clusters,或寫為Fe-S clusters)。鐵硫中心主要有2種:一種含有2 個鐵原子和2 個硫原子,稱為“二鐵二硫中心”(2Fe-2S cluster);另一種含有4 個鐵原子和4 個硫原子,稱為“四鐵四硫中心”(4Fe-4S cluster)(圖3)。 根據其所處環境的不同,鐵硫中心的氧化還原電位變化很大, 可存在于各種傳遞電子的蛋白質中,成為傳遞電子的中心。它們既可存在于脫氫酶中,也可存在于氧化酶中,還存在于光合作用的光系統中。 細胞色素bc1復合物中也含有一個二鐵二硫中心, 它總是與細胞色素b(見下文)一起工作,在醌分子轉化能量的過程中起重要作用。 該蛋白為美國科學家John Samuel Rieske 所發現,稱為“Rieske 鐵硫蛋白”。
4.3 血紅素 血紅素(heme)是紅色的,含有血紅素的蛋白分子也是紅色的,因此被稱為“細胞色素”(cytochrome),其實細胞色素是蛋白質。 血紅素是一個非常復雜的環形分子,由4 個吡咯環(由4 個碳原子和1 個氮原子組成的5 原子環) 通過次甲基(=CH-)相連圍成的一個方形結構,稱為卟啉環(porphrin),卟啉環上還連有其他化學基團(圖3)。4 個吡咯環中的氮原子伸向中心方向, 與一個鐵離子相互作用。 該鐵離子可以在3 價(Fe3+)和2價(Fe2+)之間轉換,故可用于傳遞電子(圖3)。 根據卟啉環上所帶的其他化學基團的不同, 血紅素可分為a 型、b 型、c 型、d 型、o 型等(細胞色素的類型用小寫的斜體字母表示)。每一型的細胞色素在不同的蛋白質中性質也有所差異, 可進一步分類。 例如可將細胞色素c 進一步分為c1和c2,細胞色素b 可根據其吸收峰的位置分為b562和b566,也可根據其位置分為bd(distal,即遠端的)和bP(proximal,即近端的)等。
除作為細胞色素的輔基,血紅素還有其他生理功能, 例如b 型血紅素就是血紅蛋白(hemoglobin)的輔基,但其作用不是傳遞電子,而是運輸氧氣,“血紅素”(heme)的名稱也由此而來,其實血紅素傳遞電子的功能遠早于運輸氧氣。
4.4 金屬離子 除了鐵硫中心中和結合在血紅素上的鐵離子,金屬離子本身也可以結合在蛋白質分子上,作為傳遞電子的輔基。 這些金屬離子主要是鐵離子和銅離子, 其中鐵離子因為不是在血紅素中,所以稱為“非血紅素鐵離子”(non-heme iron),以與血色素中的鐵離子相區別。 雖然不是在血紅素中,但這些鐵離子也是在3 價(Fe3+)和2 價(Fe2+)之間來回變化, 以傳遞電子。 銅離子則是在2 價(Cu2+)和1 價(Cu+)之間變化,同樣可以傳遞電子。 除了鐵離子和銅離子, 有些氫酶還含有鎳離子,與鐵離子一起組成“鎳鐵中心”(Ni-Fe)。 一些硝酸鹽還原酶還含有鉬離子, 但在這里鉬離子不是直接結合在蛋白質上, 而是結合在一種叫 “蝶呤”(pterin)的分子上,共同作為硝酸鹽還原酶的輔基。 鐵、銅、鎳、鉬都是“過渡金屬元素”(transition metal),即d-軌道的電子層沒有“填滿”的元素。這些元素的離子常以變價(即多于一種化學價)的形式存在,因而可用于傳遞電子。
有了對氫離子不通透的細胞膜, 有了各種能傳遞電子的蛋白質,其中包括像黃素、血紅素、鐵硫中心、金屬離子這樣的輔基,以及在電子傳遞鏈中能轉化和儲存能量的醌分子, 原核生物利用氧化還原反應以獲取和儲存能量的機制已經非常完善。 真核生物也繼承了原核生物以醌為核心樞紐的電子傳遞鏈,將α-變形菌(α-proteobacteria)變成了自身細胞中的“線粒體”(mitochondria),成為真核細胞中氧化還原性分子合成ATP 的“動力工廠”。 人體每個細胞(紅血球除外)中,都有許許多多這樣的“動力工廠”,為生命活動提供源源不絕的能量。
但這樣的電子傳遞鏈仍有缺點, 只能利用現成的還原性分子(例如氫氣和硫化氫)和氧化性分子 (例如硝酸鹽) 之間的氧化還原反應以獲得能量,而這些物質的供給是沒有保證的。
5 化能生物的發展有限, 太陽光才是無處不在的長期能源
以醌為核心樞紐的電子傳遞鏈雖完美, 但畢竟只是消耗性的, 如果沒有還原性物質和氧化性物質大量持續的供給,生命是不可能繁榮的。而氫氣、 硫化氫這樣的還原性物質和硝酸鹽這樣的氧化性物質,卻不能大量永久供應,因此,依靠這些物質的生物(化能生物)也沒有大規模發展的機會。
1)氫氣。氫雖是宇宙中含量最豐富的元素,按原子數計算,宇宙中的氫占普通物質(不包括“暗物質”)的90%以上,在太陽系中,81.75%的分子也是氫,地球早期的大氣中,也含有大量的氫。 但星際空間的物質密度是非常低的, 每立方厘米大約只有一個微觀粒子,相當于地球上的高真空。由于大氣中的氫氣很少有補充的來源, 又由于它是最輕的氣體,容易逃逸至外太空中,且不斷被微生物(包括細菌和古菌)所消耗,氫氣的含量就越來越低。目前地球的大氣中,氫氣只占體積的千萬分之五,微生物已無法靠這種低濃度的氫生活。利用氫的細菌常“躲”在地表下幾百米甚至幾千米的巖層中,在那里水和巖石的反應還能產生一些氫氣。一些微生物也能將多余的還原物以氫氣的形式釋放,但數量有限。
2)硫化氫。 雖然早期地球的大氣中含有許多硫化氫,但經不斷消耗,現在大氣中硫化氫的濃度已非常低,只有不到0.3×10-9,即不到100 億分之三。 現在硫化氫的來源主要包括火山爆發噴出的氣體、海底熱泉冒出的氣體,天然氣及微生物的活動, 包括用氫氣還原硫酸鹽、 含硫有機物的代謝等。 但這些硫化氫數量不大,也不是到處都有。
3)硝酸鹽。 作為化能生物使用主要氧化劑的硝酸鹽,主要存在于硝酸鹽礦(例如鈉硝石nitratine)中,也不是到處都有。
由于氧化還原反應的“原料”供應有限,靠這種反應生存的原核生物的生存和發展只能保持在很低的水平。地球上的生物要大發展,就需要一種無處不在,且在長時期內都不會枯竭的能源,這就是太陽光。 地球軌道上的平均太陽輻射強度為1 369 W/m2。 以地球赤道周長約為4 萬km 計算,地球獲得的能量可以達到173 000 TW(太瓦),即17 億億瓦。 地球在1 h 中獲得的太陽能,比人類1年使用的能量還要多。
太陽輻射能的99% 集中于波長為150 ~7 000 nm 的電磁波中,其中可見光區(390~700 nm)約占總輻射能的50%;紅外光區(波長大于700 nm)約占43%;紫外光區(波長小于390 nm)約占7%。光輻射能量的大小與其頻率成正比,即E=hν, E是光子的能量,ν 是它的頻率,h 為普朗克常數,為6.63×10-34J·s。 所以光子的能量與它的頻率成正比,而與波長(光速除以頻率)成反比。 波長越長,能量越低,因此紫外光的能量高于可見光,可見光的能量又高于紅外光。
在這些光線中,紫外光的能量太高,易造成化學鍵的斷裂,紅外線的能量太低,只能增加分子的熱運動,都不適合作為生物的能源,能作為生物有效能源的, 主要是可見光和波長接近可見光波長的紅外光。
生物要利用可見光中的能量, 就需要能吸收可見光、將其能量轉移出去并保存下來的分子。這主要是由色素分子完成的。 在介紹這些色素分子在光合作用中的功能之前, 先介紹為什么它們能吸收可見光。
(待續)

