第四類脲酶抑制劑對土壤脲酶活性和微生物量的影響
王趁義, 陳仙仙, 黃兆瑋, 付佳佳, 汪少奇
(1.浙江萬里學院, 生物與環境學院, 浙江 寧波 315100; 2.寧波晟乾環境技術開發有限公司, 浙江 寧波 315100)
土壤微生物是土壤生態系統的重要組分之一,幾乎所有的土壤物理、化學和生物學性質都直接或間接地與土壤微生物有關,土壤微生物參數變化將有可能成為土壤生態系統變化的預警及敏感指標[1]。其中的細菌、真菌和放線菌不僅是土壤有機物質轉化的執行者,又是植物營養元素的活性庫[2]。因此土壤微生物在有機質轉化、養分循環、肥力形成、污染物降解以及能量流動方面具有重要的作用[3-5]。另外由于微生物生長繁殖的最適溫度、濕度及養分條件與植物相似,故可以綜合反映土壤肥力和環境質量狀況[6]。尿素作為主要的化學氮肥品種,約占氮肥消耗總量60%以上,然而在生產實踐中我國水稻、玉米、小麥三大糧食作物氮肥的當季平均利用率僅為33%,遠低于美國、歐洲糧食作物的氮肥利用率(分別為50%,65%左右)[7]。主要原因是土壤中的脲酶能將尿素迅速催化水解成NH3,其速率是未經催化水解的1014倍[7],極大地降低了動植物對氮素的利用,而我國每年因氮肥利用率低下導致的直接經濟損失達450億元[8]。尿素的快速分解,不僅造成農業資源的嚴重浪費,同時也會引起一系列的生態環境問題[8-9],如導致植物“燒苗”[10];引起嚴重的環境氮污染和農村面源污染[11];加速土壤酸化、耕地板結的進程[12];造成大氣污染,比如溫室效應[13],臭氧層破壞[14]等。因此,如何在保障土壤供肥能力的同時,提高氮肥利用率,減少氮肥引起的環境污染和生態效應,已成為一個世界性研究課題[8,15-16]。脲酶活性的抑制劑調控技術已成為提高尿素利用率最有效的生物化學方法。但現有的3類脲酶抑制劑中,金屬鹽類毒性較大;有機類的則因高殘留、有耐藥性、有效抑制時間短等原因,難以被大范圍推廣應用;而植物源類抑制劑有效成分小、藥效慢、植物的采集具有季節性等缺點不易為農民接受[7]。基于前3類脲酶抑制劑的弊端,目前新型高效綠色的配合物型脲酶抑制劑(以下簡稱第四類抑制劑)已引起國內外學者的廣泛關注[8],尤其是Schiff堿配合物型,因其結構中N原子上含有孤對電子,毒性小,與金屬離子的配位能力較強,可以與多種過渡金屬離子形成配合物,表現出優良的抗菌、抗癌、抑制脲酶活性,有望成為一類性能優良的新型脲酶抑制劑[8,17]。但其施加后對土壤環境的影響還鮮有報道,只有在探明其對土壤影響的基礎上方可推廣應用于大田作物生產或肥料企業。郭晨[18]認為土壤微生物的數量與土壤肥力存在正比例關系,通過測量土壤微生物的多少就能夠知道土壤肥力以及肥料、農藥或者進入土壤中的外來化學物質對土壤狀況的影響,這種方式相較于正常的化學測定方式而言更為便捷與高效。目前,針對第四類脲酶抑制劑對土壤脲酶活性和土壤微生物生長影響的研究報到極少,僅有的一些研究也只報道了一些傳統的脲酶抑制劑如N-丁基硫代磷酰三胺(nBPT)[19]、氫醌(HQ)[20]、腐植酸[21-22]等對土壤微生物類群分布、土壤酶活性及土壤微生物種類和數量的影響。本文的研究結果能為第四類脲酶抑制劑的安全性評價及相關脲酶抑制劑產品的開發與應用提供科學依據。
1 材料和方法
1.1 供試材料
第四類脲酶抑制劑來自項目組前期合成的Schiff堿銅配合物型抑制劑,化學式C14H15N3O6Cu[23];尿素(N≥46%)購于國藥集團有限公司;供試土壤采自寧波市鄞州區首南街道月浦稻田的水稻土,按5點法采取5—20 cm層土樣,風干、混勻、研磨,過2 mm篩備用。土壤基本理化性質為:水分含量32.2%,pH值6.7,有機質14.5%,全氮2.26 g/kg,硝態氮0.77 mg/kg,銨態氮3.58 mg/kg,有效磷62.96 mg/kg。
1.2 試驗設計
取500 g風干土樣于若干個10 cm×14 cm培養容器中,調節土樣的含水量至田間持水量的60%,然后置于28 ℃人工氣候箱中培養1周以恢復生物活性,并定期攪拌土壤,保持土壤通氣性。預培養結束后,將上述土壤分成5組,第1組為空白(K),第2組僅加入5 g尿素(U),第3—5組分別加入尿素和尿素量的0.1%,0.5%和1%的第四脲酶抑制劑,所組成的混合物分別記作UI 0.1%,UI 0.5%和UI 1%。各組所加肥料均溶于水之后再施用,每個處理3次重復。然后將上述試驗組置于20 ℃的人工氣候箱中于4月18號開始培養,4月24號開始取樣并且每隔6 d取樣測定一次微生物數量和土壤脲酶活性,總共取樣7次于5月31號結束,試驗期間每天通過稱重法加1次水以保持土壤含水量不變。
1.3 測定項目與方法
土壤脲酶活性測定采用靛酚藍比色法[24];土壤微生物的計數采用采用稀釋涂平板計數法[25]。稱取土樣1 g,放入盛有99 ml無菌水的三角瓶中振蕩20 min,使土樣與水充分混合,制成10-2土壤懸液。用無菌吸管從中吸取1 ml土壤懸液加入盛有9 ml無菌水的試管中充分混勻,以此類推制成10-2,10-3,10-4,10-5等不同稀釋度的土壤懸液。然后用無菌吸管各吸取不同稀釋度的土壤懸液0.2 ml對號放入已制好的平板培養基中。細菌采用牛肉膏蛋白胨培養基于37 ℃培養箱中培養1 d,稀釋梯度選用10-5,10-6,10-7;放線菌采用高氏Ⅰ號培養基于28 ℃培養箱中培養4 d,稀釋梯度選用10-3,10-4,10-5;真菌采用虎紅瓊脂培養基于27 ℃培養箱中培養3 d,稀釋梯度選用10-2,10-3,10-4[26]。
1.4 數據統計分析
土壤微生物數量計算公式為:每克土壤樣品菌數=某稀釋倍數的菌落平均數×稀釋倍數。
采用Excel軟件進行數據處理,Origin 8.0軟件對數據進行繪圖,SPSS軟件對數據進行統計學分析。
2 結果與分析
2.1 第四類脲酶抑制劑對土壤脲酶活性的影響
抑制劑不同施用濃度對脲酶活性的影響如圖1所示。由圖1可見,尿素表施到土壤后,U,UI 0.1%,UI 0.5%,UI 1%處理土壤脲酶活性逐漸增強,在第12 d土壤脲酶活性達到最大,而空白處理的土壤脲酶活性基本不變,這表明尿素在早期能夠被土壤中的脲酶快速分解成碳酸銨。在脲酶抑制劑的作用下,UI 0.1%,UI 0.5%,UI 1%處理組在第12 d,24 d和第36 d土壤脲酶活性受到了顯著抑制,其中UI 1%處理的土壤脲酶活性在第12 d,24 d和36 d分別比僅加尿素處理組降低了22.1%,32.2%和40.8%,第36 d UI 1%處理和僅加尿素處理達到顯著差異(p<0.05),說明此類脲酶抑制劑的抑制作用施用后期大于施用前期,這可能與抑制劑本身穩定性有關,由于Schiff堿金屬配合物是由Schiff堿配體和金屬銅離子配位反應合成的,它的熱穩定性會比一般有機物要好一點,因此普通脲酶抑制劑在前期幾天就分解完了而第四類脲酶抑制劑在后期還能繼續作用,但是具體作用機制有待進一步深入研究。而UI 0.5%和UI 0.1%處理對土壤脲酶活性的抑制率低于UI 1%處理,這表明了當抑制劑的濃度配比達到了1%時,對土壤脲酶活性抑制效果最好。U,UI 0.1%,UI 0.5%,UI 1%的土壤脲酶活性在第12 d之后開始下降并在第42 d之后基本一致,表明了第四類脲酶抑制劑對土壤脲酶活性的抑制時效性達42 d。
2.2 第四類脲酶抑制劑對土壤細菌數量的影響
第四類脲酶抑制劑對土壤細菌數量的影響如圖2所示。5個處理組的土壤細菌數在培養第6 d時差別不大(2.00×107),第6 d之后都有不同程度的增加,其中UI 1%和UI 0.5%處理組較僅加尿素處理增加的幅度較大,而UI 0.1%處理與僅加尿素處理的細菌數差別不大。12 d之后UI 0.1%和UI 0.5%處理組的土壤細菌增長數量基本一致。各處理的土壤細菌數在第24 d達到最大,之后逐漸減少并在第42 d達到與空白組細菌一樣的數量。在整個培養期間,空白組細菌一直處于較低水平。僅加尿素處理的土壤細菌數比空白處理土壤的細菌數多,表明了尿素對土壤細菌生長有促進作用,最大增長率為63.6%。與空白處理組細菌數量相比得出的第四類脲酶抑制劑處理組細菌增長率明顯超過了僅加尿素處理組,其最大增長率為86.2%,這主要與以下兩個原因有關,一個原因是脲酶抑制劑可以減少尿素水解產生的高濃度氨和銨對細菌生長的脅迫作用,另外能夠保證后期有足夠的碳源和氮源供細菌生長[27-28]。另一個原因是脲酶抑制劑的加入使細菌生長環境發生了變化(pH值升高、滲透壓增加、脲酶活性降低等),給細菌提供了一個良好的生長環境。UI 0.1%和UI 0.5%處理的土壤細菌數量趨向一致,明顯低于UI 1%處理的土壤細菌數量,對比圖1與相應濃度處理的土壤脲酶活性差距相一致,因此可以得出這可能與抑制抑制土壤脲酶活性強弱有關。在培養第42 d時,各處理的土壤細菌數達到一致,說明尿素已全部水解,不再為細菌生長提供碳源和氮源。
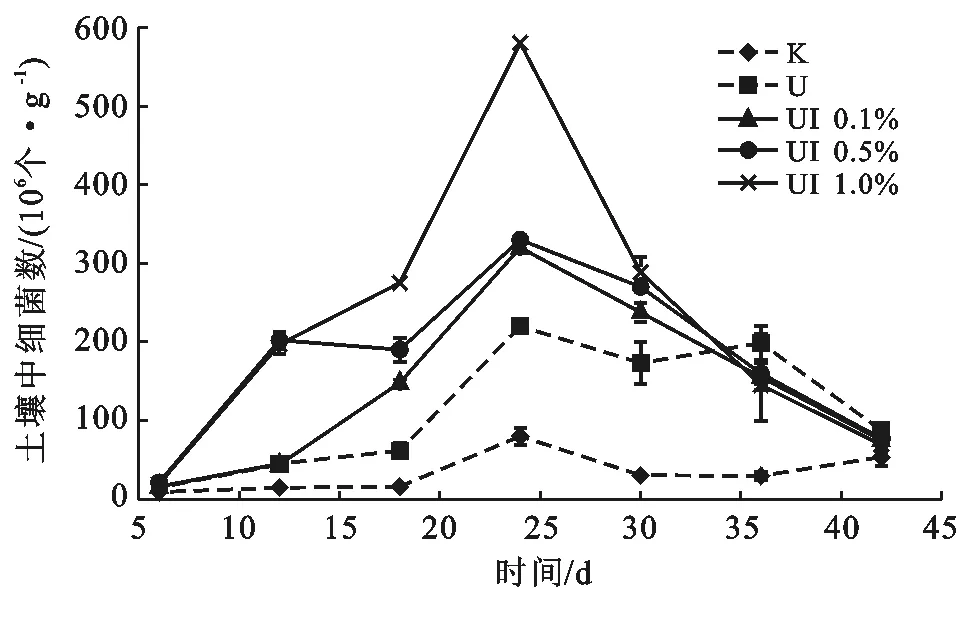
圖2 第四類脲酶抑制劑對土壤細菌數量的影響
2.3 第四類脲酶抑制劑對土壤放線菌數量的影響
第四類脲酶抑制劑對土壤放線菌數量的影響如圖3所示,各處理的土壤放線菌數量變化規律大致相同,先上升后下降最后趨于平穩。土壤放線菌數量在第18 d達到最高值,在第30 d趨于平穩。在第42 d,施用脲酶抑制劑處理組的放線菌數量與僅加尿素處理組放線菌數量趨向一致,而空白組的放線菌數量遠高于其它4個處理組的放線菌數量。空白組的放線菌數量在整個培養期間要遠高于僅加尿素處理組的放線菌數量,這說明尿素對放線菌的生長有抑制作用,最大抑制率達46.4%。3種加了第四類脲酶抑制劑的處理組放線菌數量要高于僅加尿素組放線菌的數量,其中在第12 d和第18 d,UI 0.5%,UI 1%處理組和僅加尿素組達到顯著差異(p<0.05),說明第四類脲酶抑制劑對放線菌的生長有顯著促進作用。
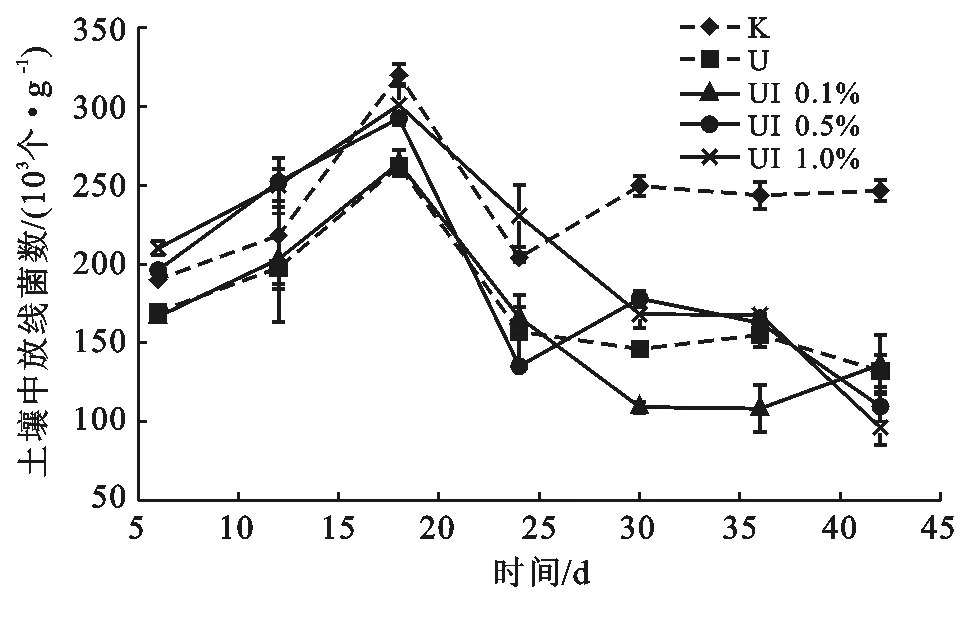
圖3 第四類脲酶抑制劑對土壤放線菌數量的影響
2.4 第四類脲酶抑制劑對土壤真菌數量的影響
第四類脲酶抑制劑對土壤真菌數量的影響如圖4所示,在整個培養期間,UI 1%處理組真菌的數量要高于其它4個處理組真菌的數量。UI 1%處理組真菌的數量在第6 d后有一個較大幅度的升高,而其它4個處理組的真菌數量在第18 d后才有一個較大幅度的增長。各個處理組的真菌數量在第24 d達到生長高峰期,之后開始下降,其中U,UI 0.1%,UI 0.5%處理組真菌數量在第42 d與空白組真菌數量趨向一致。僅加尿素處理組的真菌數量比其它幾組真菌數量要低,表明尿素抑制了土壤真菌的生長,最大抑制率達89.7%。UI 0.1%和僅加尿素處理組的真菌數量基本相同,說明低濃度的抑制劑對土壤真菌生長沒有太大的影響,當抑制劑濃度繼續增大,土壤真菌數量相較于僅加尿素處理組有一個較大的增長,UI 0.5%處理組最大增長率為46.9%,UI 1%處理組最大增長率為83.6%,由此說明第四類脲酶抑制劑的加入能夠促進土壤真菌的生長。在第42 d,U,UI 0.1%,UI 0.5%處理組和空白處理組的土壤真菌增長率趨向一致說明尿素已基本水解完全,UI 1%處理組真菌的數量在第42 d有一個小幅度的增長,說明高濃度的第四類脲酶抑制劑抑制土壤脲酶活性時效性比較長,能延長對土壤真菌的影響。
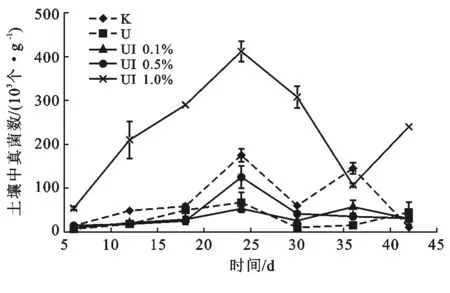
圖4 第四類脲酶抑制劑對土壤真菌數量的影響
3 討 論
土壤脲酶活性受到諸多因素的影響,與基質濃度、溫度、pH值、有機質含量等因素相關,在一定時間內可被脲酶抑制劑所抑制[29-30]。研究表明,施加第四類脲酶抑制劑處理的抑制效果都是隨施用時間的延長而增強,抑制活性在第36 d達到最強,施入的后期作用大于前期,這與其它類別的脲酶抑制劑的研究結果不一致。趙略[31]研究結果表明第二類脲酶抑制劑nBPT的抑制效果隨施用時間的延長而減弱,施入的前期作用大于后期,抑制劑對脲酶的抑制活性在抑制劑施入后的第10 d達到最強,這說明與第二類脲酶抑制劑相比,第四類脲酶抑制劑對土壤脲酶活性抑制的時效性明顯延長,這可能是由于第四類抑制劑的兩種組合單元(Schiff堿配體、植物生長必需的金屬元素)被限制在配合物骨架中,同時擁有了雙活性位點的原因,兼具了無機和有機功能基團各自的性質和功能,從而使它作用時間延長,毒性大為降低[32]。然而,這些認知只是停留在理論意義上,尚需進一步地進行試驗驗證。
土壤脲酶主要來源于土壤當中的一些菌體[33],第四類脲酶抑制劑對土壤脲酶的抑制活性隨著抑制劑濃度的增大而增強,抑制劑濃度為1%的抑制作用要遠高于抑制劑濃度為0.5%和0.1%。土壤脲酶主要來源于土壤中的一些微生物菌體[32],第四類脲酶抑制劑對土壤脲酶的抑制活性隨著抑制劑濃度的增大而增強,抑制劑濃度為1%的抑制作用要遠高于抑制劑濃度為0.5%和0.1%。主要原因是由于土壤脲酶為誘導酶,底物濃度對酶活性影響較大。在脲酶蛋白合成過程中,第四類脲酶抑制劑降低了底物對脲酶合成的誘導和促進作用,從而阻礙了酶的活性中心形成[29]。
土壤微生物是土壤生物中最活躍的部分,他們參與土壤的有機質分解、腐殖質合成、養分轉化和土壤的發育及形成,既是土壤中營養元素的“源”,又是營養元素的“庫”。施肥后,由于肥料在土壤中要分解(有機肥)或溶解(化肥)成更小的分子或離子,就形成了局部高濃度現象,這些短時間內產生的局部高濃度會對土壤微生物產生明顯的影響。但土壤3大微生物對尿素的敏感程度不一樣,其中土壤放線菌和土壤真菌對尿素比較敏感,尿素會抑制其生長,這可能與尿素水解產生的銨過度累積有關。Arnebrandt等[34]的研究表明,施用氮肥對土壤微生物群落特別是菌根真菌有直接的抑制作用,其機制是抑制酶活力和積累毒性化合物。而細菌相反,尿素可促進其生長,這可能與尿素水解產生的氮源類物質會給細菌生長提供氮源和碳源有關。

在土壤的3大微生物群體中,第四類脲酶抑制劑對土壤放線菌的生長影響作用較小,對土壤真菌的生長影響較大,對土壤細菌的影響最大。有研究表明土壤中細菌數量的增加有利于土壤養分的轉化,能為植物的生長提供良好的環境,土壤中放線菌數量的增加不僅能轉化土壤有機質,對植物的土傳病原菌也起到一定的拮抗作,促進土壤微生物區系向健康方向發展[35]。探討第四類脲酶抑制劑對土壤微生物的影響,對于實現化肥零增長,發展綠色和生態農業的戰略需求具有重要的理論意義和應用價值。
4 結 論
(1) 第四類脲酶抑制劑濃度為1%對土壤脲酶活性的抑制作用遠高于抑制劑濃度為0.5%和0.1%,最大抑制率達40.8%,可以實現適度調控的目的。
(2) 尿素對土壤細菌生長有促進作用,最大促進率達83.6%;對真菌和放線菌有抑制作用,最大抑制率分別為89.7%,46.4%。
(3) 第四類脲酶抑制劑能夠促進土壤細菌、放線菌和真菌的生長,抑制劑濃度為1%時促進作用最明顯。綜合不同濃度抑制劑對土壤脲酶抑制活性的強弱,可以得出第四類脲酶抑制劑施用濃度為1%是最佳用量。

