例談初中化學試題中物質性質的重要載體
梁俏維
摘要:碳酸鈉是初中化學物質的典型代表物質之一,通過碳酸鈉可以非常靈活的考察初中學生對酸、堿和鹽三類化合物的化學性質的熟練掌握程度,常常會成為初中化學命題的熱點物質。
關鍵詞:碳酸鈉 物質性質 化學試題 知識網絡
碳酸鈉在日常生活和化工生產中都有著廣泛的應用,是初中化學學習中鹽類物質的典型代表物質之一,由于其組成中的CO32-離子的性質能跟酸反應放出CO2氣體,還能跟多種金屬離子反應生成沉淀,可以非常靈活的考察初中學生對酸、堿和鹽三類化合物的化學性質的熟練掌握程度。所以,碳酸鈉常常會成為初中化學命題的熱點物質,因而在初中化學教學和復習過程中引導學生以碳酸鈉作為特例,將酸、堿和鹽的化學性質科學的串聯,形成系統的知識網絡是十分重要的。而在初中化學命題中以碳酸鈉作為中心素材物質,從不同的角度對化學概念、原理、實驗、計算等一系列知識進行全面考查是非常常見的,現回顧整理分析如下。
一、有關常見物質分類題型
例1(2016年廣東)下列有關物質的分類正確的是( )
A.純堿、燒堿都屬于堿 B.塑料、羊毛屬于合成材料
C.淀粉、蛋白質屬于有機物 D.生石灰、熟石灰屬于氧化物
【考點】常見的氧化物、酸、堿和鹽的判別;有機物與無機物的區別;合成材料的使用及其對人和環境的影響.
【分析】根據已有的物質的類別進行分析解答即可.
【解答】解:A.純堿是碳酸鈉,屬于鹽,錯誤;
B.羊毛屬于天然材料,錯誤;
C.淀粉和蛋白質屬于有機物,正確;
D.熟石灰是氫氧化鈣,不是氧化物,錯誤;
故選C.
二、有關常見物質俗名的題型
例2(2014年廣東 )下列物質的名稱和俗名對應正確的是
A.碳酸鈣一純堿 B.氯化鈉一食鹽
C.碳酸鈉一小蘇打 D.氧化鈣一熟石灰
【考點】:物質的元素組成
【分析】:根據常見物質的俗名、名稱和化學式進行分析解題。
【解答】:A.碳酸鈉俗稱純堿,碳酸鈣俗稱石灰石,錯誤;
B.氯化鈉俗稱食鹽,正確;
C.碳酸氫鈉的俗稱是小蘇打,錯誤;
D.氫氧化鈣的俗稱是熟石灰或消石灰,氧化鈣是生石灰,錯誤;
故選B
三、有關溶液酸堿度的題型
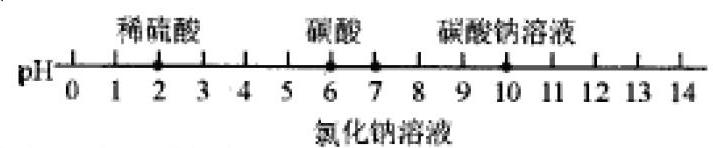
例3(2009年安徽)實驗測得下列四種溶液的pH值如下圖所示
其中溶液呈堿性的是( )
A.稀硫酸 B.碳酸
C.碳酸鈉溶液 D.氯化鈉溶液
【考點】:本題考查常見溶液pH的酸堿性判斷
【分析】:解答本題要充分理解溶液的酸堿性與溶液pH大小才能做出正確的判斷
【解答】:A.稀硫酸的pH小于7,顯酸性,錯誤;
B.碳酸的pH小于7,顯酸性,錯誤;
C.碳酸鈉溶液的pH大于7,顯堿性,正確;
D.氯化鈉溶液的pH等于7,顯中性,錯誤;
故選C
四、有關物質鑒別的題型
例4(2016泰安)下列各組物質的溶液不用其他試劑無法鑒別的是( )
A.H2SO4 NaCl Na2CO3 CaCl2 B.HCl NaOH CuSO4 MgSO4
C.Na2CO3 K2SO4 BaCl2 HCl D.NaNO3 HCl CaCl2 KOH
【考點】:本題是不另加試劑型的物質鑒別題目
【分析】:本類型題目解題的方法是首先觀察有無特殊顏色的物質,若有,將有顏色的溶液首先鑒別出來,然后再借用這種溶液來鑒別其它待確定的物質;若都沒有特殊顏色,就將溶液兩兩混合,根據混合后的現象進行分析得出結論,而這種題型中如果有Na2CO3溶液,那么Na2CO3往往會成為解題的鑰匙。
【解答】:A.組內無特殊顏色,兩兩混合時,其中一種溶液與其它三種溶液混合時出現一次白色沉淀和一次放出氣體,該溶液為Na2CO3溶液;與Na2CO3溶液混合產生氣體的溶液為H2SO4,產生白色沉淀的為CaCl2溶液;與Na2CO3溶液混合無明顯現象的為NaCl溶液;故不加其它試劑可以鑒別。
B.組內CuSO4溶液是藍色的,能與CuSO4溶液混合產生藍色沉淀的是NaOH溶液,能與NaOH溶液混合產生白色沉淀的是MgSO4溶液,無明顯變化的是HCl,故本組不加其它試劑也可以鑒別。
C.組內四種溶液兩兩混合時,其中有一種溶液與其它三種溶液混合時出現一次白色沉淀和一次放出氣體,該溶液為Na2CO3溶液;與Na2CO3溶液混合產生氣體的為HCl,產生白色沉淀的為BaCl2溶液,與Na2CO3溶液混合無明顯現象的為K2SO4溶液;故本組不加其它試劑也可以鑒別。
D.組內四種溶液兩兩混合時,HCl能與KOH反應生成KCl和H2O,但無明顯現象,其余不加其它試劑無法鑒別。
故本題選:D
五、有關物質除雜質的題型
例5(2014年廣東)下列除去雜質(括號內)的方法正確的是
A.CO(CO2):通過灼熱的氧化銅 B.NaOH溶液(Na2CO3):加適量稀鹽酸
C.NaCl溶液(鹽酸):加熱蒸發 D.鐵粉(氧化銅粉末):加入足量稀硫酸
【考點】:本題考查物質的除雜(提純)和混合物的分離。
【分析】:根據原物質和雜質的性質選擇適當的除雜劑和分離方法,所謂除雜(提純),是指除去雜質,同時被提純物質不得改變(不能消失、減少但可以增多),除雜質題至少要滿足兩個條件:①加入的試劑只能與雜質反應去除,不能與原物質反應;②反應后不能引入新的雜質。
【解答】:A.CO能與灼熱的氧化銅反應生成銅和CO2,反而會把原物質除去,不符合除雜原則,錯誤。
B.NaOH和Na2CO3均能與稀鹽酸反應,不僅把雜質除去,也會把原物質除去,不符合除雜原則,錯誤。
C.鹽酸易揮發,加熱蒸發時能揮發除去,且沒有帶入新雜質,符合除雜原則,正確。
D.鐵粉和氧化銅粉末都能與足量稀硫酸反應,不但能把雜質除去,也會把原物質除去,不符合除雜原則,錯誤。
故本題選:C
六、有關物質共存的題型
例6 (2014年揭陽) 下列各組物質在溶液中能大量共存的一組是( )
A.Na2CO3 NaHCO3 HCl B.NaCl AgNO3 HNO3
C.KNO3 KCl NaOH D.NaOH BaCl2 H2SO4
【考點】:本題考查離子或物質的共存問題。
【分析】:根據復分解反應發生的條件可知,若物質之間相互交換成分不能生成水、氣體、沉淀,則能在溶液中大量共存,據此進行分析即可。
【解答】:A.碳酸根離子和碳酸氫根離子都會與氫離子反應生成CO2和H2O而不能共存,錯誤;
B.NaCl中的氯離子會跟AgNO3中的銀離子反應生成氯化銀沉淀而不能共存,錯誤;
C.三種物質之間兩兩互換都不會生成水、氣體、沉淀,正確;
D.H2SO4中的硫酸根離子會跟BaCl2中的鋇離子反應生成硫酸鋇沉淀,H2SO4中的氫離子會跟NaOH中的氫氧根離子發生中和反應生成水,錯誤;
故選C
七、有關實驗探究的題型
例7 (2014年山西)同學們在初中化學實驗室中發現一瓶如下圖所示久置的瓶口有白色固體、瓶塞丟失的無色溶液。已知原溶液可能是NaCl、NaOH或Na2CO3三種溶液中的一種,為確定溶液的成分,同學們進行了如下探究: 小張同學取待測液測得PH=10,他得出的關于溶液成分的結論是:_______ ,他取少量待測液于試管中,加入過量的稀HCl,看到 _______ ,由此小張同學認為,溶液為Na2CO3溶液。
小李同學對小張同學的結論提出疑問,又進行了以下實驗:取少量待測液于試管中,加入過量的CaCl2溶液,生成白色沉淀,該反應方程式為 _______,靜置。(寫出還需要進行的操作及現象)_______ ,通過實驗,小李認為小張結論正確。二位同學給試劑瓶貼上新標簽:Na2CO3。
實驗結束后,同學們通過討論認為試劑瓶原標簽可能不是Na2CO3,你認為他們的理由是_______ 。
【考點】:本題考查物質的性質和溶液的酸堿性。
【分析】: NaCl溶液呈中性,pH=7;Na2CO3和HCl反應產生CO2;Na2CO3和CaCl2反應生成CaCO3沉淀和NaCl;NaOH溶液顯堿性等物質性質。
【解答】:小張同學取待測液測得PH=10,而NaCl溶液呈中性,pH=7,故該溶液一定不是NaCl溶液(可能是NaOH、Na2CO3或NaOH和Na2CO3的混合溶液);
滴加稀鹽酸,結論是Na2CO3,Na2CO3和鹽酸反應會產生CO2氣體,故會觀察到有氣泡產生;
取少量待測液于試管中,加入過量的CaCl2溶液,生成白色沉淀,是Na2CO3和CaCl2反應生成CaCO3沉淀和NaCl,反應方程式為:
Na2CO3+ CaCl2=CaCO3↓+2NaCl;
為驗證溶液不是NaOH變質產生Na2CO3,滴加過量的CaCl2溶液后向上層清液中加入無色酚酞溶液,溶液不變色,說明沒有NaOH,故小張的結論正確;
若NaOH完全變質也使溶液的成分是Na2CO3,因此試劑瓶原標簽可能不是Na2CO3,原標簽可能是NaOH;
故答案為:一定不是NaCl溶液(可能是NaOH、Na2CO3或NaOH和Na2CO3的混合溶液); 有氣泡冒出;
Na2CO3+ CaCl2=CaCO3↓+2NaCl;
向上層清液中加入無色酚酞溶液,溶液不變色;原標簽可能是NaOH。
八、有關物質性質推斷題型
例8(2016年廣東) 初中化學常見物質A﹣I分別是下列物質中的一種:鋅、氫氧化鈉、硫酸銅溶液、稀鹽酸、碳酸鈉溶液、石灰水、生石灰、石灰石和水.他們之間相互的反應(每種物質只能用一次)恰好包含了化合反應(A+B)、分解反應(C)、置換反應(D+E)、中和反應(F+G)、復分解反應(H+I)等反應類型.試回答下列問題:
(1)A+B的反應化學方程式是 _______ 。
(2)C的化學式為 _______ ;硫酸銅溶液參加 _______ 反應(填反應類型)。
(3)H+I的反應方程式是 _______ 。
【考點】本題考查物質的鑒別、推斷;反應類型的判定;書寫化學方程式、文字表達式。
【分析】根據初中化學常見物質A﹣I分別是下列物質中的一種:鋅、氫氧化鈉、硫酸銅溶液、稀鹽酸、碳酸鈉溶液、石灰水、生石灰、石灰石和水,化合反應(A+B),所以A、B是氧化鈣和水,分解反應(C),所以C是碳酸鈣,中和反應(F+G),所以F、G是鹽酸和氫氧化鈉,置換反應(D+E),所以D、E是硫酸銅和鋅,復分解反應(H+I),所以H、I是碳酸鈉、氫氧化鈣,然后將推出的物質進行驗證即可。
【解答】解:初中化學常見物質A﹣I分別是下列物質中的一種:鋅、氫氧化鈉、硫酸銅溶液、稀鹽酸、碳酸鈉溶液、石灰水、生石灰、石灰石和水,化合反應(A+B),所以A、B是氧化鈣和水,分解反應(C),所以C是碳酸鈣,中和反應(F+G),所以F、G是鹽酸和氫氧化鈉,置換反應(D+E),所以D、E是硫酸銅和鋅,復分解反應(H+I),所以H、I是碳酸鈉、氫氧化鈣,經過驗證,推導正確,所以
(1)A+B的反應是氧化鈣和水反應生成氫氧化鈣,化學方程式是:CaO+H2O=Ca(OH)2;
(2)C的化學式為CaCO3,硫酸銅溶液參加置換反應;
(3)H+I的反應是氫氧化鈣和碳酸鈉反應生成碳酸鈣沉淀和氫氧化鈉,化學方程式是:Na2CO3+ Ca(OH)2=CaCO3↓+2NaOH.
故答案為:(1)CaO+H2O= Ca(OH)2;(2)CaCO3,置換;
(3)Na2CO3+ Ca(OH)2=CaCO3↓+2NaOH.
通過以上例題可以看到:Na2CO3這種物質已經滲透到初中化學各個知識點的試題中去,占據了足夠大的分數比例,它提醒我們:在日常化學教與學時要善于總結,特別在復習備考過程中,對于特殊的典型物質,我們要多跟學生一起,從物質的組成、結構、性質、變化規律、分類以及用途等方面全面橫向對比總結,聯系每一個知識點,形成系統的知識網絡,便于教與學,使教與學達到事半功倍效果。
參考文獻
[1]錢永飛.初中化學“碳酸鈉、碳酸氫鈉和碳酸鈣”考點探究[J].中學化學,2016,(5):27-28
[2]王安.中考化學熱點—碳酸鈉與碳酸氫鈉[J].數理化解題研究,2016,2(5):78-79
[3]朱建兵① 袁春仙②.將學科觀念的培養貫穿于教學設計中—以蘇教版化學1《碳酸鈉的性質與應用》為例[J].化學教與學,2013,(13):15-16

