“電解質”迷思概念的探查與轉變方式研究
鐘思敏
(吉林師范大學 136000)
迷思概念是指存在于學生頭腦之中,與科學概念不符的認識.它的存在具有隱蔽、頑固性等特點,影響著學生對科學概念的理解,使學生在學習過程中不知所錯,亦不知為何錯.在學科教育中,越來越多的學者關注并對其進行研究,其中物理、化學、生物等理科性學科研究尤為深入,也得出了一些相應的概念轉變策略,如PDODE策略、認知沖突策略等.
電解質內容是高中化學必修一第二章第二節的內容,是學習離子反應的基礎,且在化學選修四《化學反應與能量》中第三章電離水解平衡的要求對強弱電解質有更進一步的理解.對電解質的理解與掌握程度會直接影響學生對后續離子反應及相應水解平衡的學習.然而,初中所學酸堿鹽溶液能導電對高中階段電解質知識的學習僅僅是一個簡單的鋪墊過渡,基礎一般的同學對于溶液導電的認識幾乎處于空白狀態,并且電解質內容較細,學習時也不能靠死記硬背.
電解質的學習內容主要包括三大類:定義(即判斷),強弱電解質,電離方程式的書寫.電解質定義即在水溶液或熔融狀態下能導電的化合物.首先從上一章節分類的觀點出發,將電解質牢牢歸屬于化合物的范圍之內,包括酸,堿,鹽,部分金屬氧化物(熔融狀態).其次,導電是由于電離產生的自由移動的離子.再次,水溶液或熔融狀態二者選一即可.一句話四個關鍵詞一個重點字,圍繞電解質由宏觀世界轉向微觀世界,其中的微觀現象肉眼無法可見,只能通過表面現象去演化推算.強調重點在于:電離是本質,導電是現象.
一、迷思概念的探查
1.主次不分
在與學生的交流中,筆者發現存在的迷思概念有:主次不分,認為一個物質如果不是電解質那就應該是非電解質.而存在的迷思概念的原因可能在于,上課期間老師對非電解質含義一筆帶過,或者非電解質僅僅強調在水溶液和熔融狀態下的“和”字,對于物質如氧氣不導電那就會迷惑,下意識看到有非電解質的空就選填上了.在電解質判斷上,對于給定的物質,首先應下意識觀察其是否為化合物,其次再去判斷是否導電的問題.因此,這一類問題的關鍵在于分清主次,在延續上一章節分類的觀念時乘熱打鐵強調為進一步學習的需要,對化合物進行分類.在判斷物質屬于化合物的基礎上,再對電解質和非電解質進行分析.
2.因果倒置
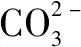
3.知識的錯誤遷移
學生在強弱電解質的判斷還存在的迷思概念有:知識的錯誤遷移.關于強弱電解質的判斷,對于酸的判斷明顯優于堿,提到弱堿腦海中只有NH3·H2O,部分學生對氫氧化銅和氫氧化鎂的弱堿性認識還不足.有學生對知識進行錯誤的遷移,認為BaSO4和CaCO3作為難溶性物質,溶于水的那一部分是完全電離,屬于強電解質,直接的認定沉淀都屬于強電解質,Mg(OH)2以及Cu(OH)2是強電解質.當然也存在部分教輔資料不全面,學生太過于依賴教輔沒有注重總結積累的結果.電解質的強弱是由物質內部的結構決定的,與外界因素無關.如鹽的溶解度大小不是強弱電解質判斷的依據.然而學生并不了解物質的內部結構,為什么硫酸就是完全電離,醋酸就是部分電離,教師要想解釋清楚時間安排不允許,學生的理解能力也不足.因此,對于強弱電解質的判斷唯一的方法就是通過做題積累,例如化學方程式書寫進行書寫與練習對比.
在平時的練習題講解中,對電解質本質的理解尤其是酸堿鹽的知識反復多次的進行訓練,對于主次及因果關系的講解圍繞主要點,從原因本質出發,由里向外的延展,完全電離在前強電解質定義在后,電解質的強弱是由物質的內部結構決定的,與外界因素無關,鹽的溶解度大小與強弱電解質的判斷無關,并且強電解質溶液的導電能力不一定比弱電解質溶液的導電能力強,溶液的導電能力與電解質的強弱沒有必然的聯系,只取決于溶液中自由移動離子的濃度和所帶電荷數.電離才是核心的本質,導電只是外部表現出來的現象.
在學生的實際練習題中會遇到需要單獨記憶的特殊情況,如CO2、SO3,其水溶液能夠導電,但不是化合物自身電離,而是它們與水反應的產物發生的電離,
在離子方程式中,存在物質拆與不拆的問題,弱電解質在水溶液中屬于部分電離,反應物中能拆離子在不斷的生成更難電離的物質,弱電解質在生成物中是相對于反應物更難電離的存在,因此不可以拆.由此當遇到這樣一個題目時:
判斷下列哪個物質屬于電解質( ).
A.NaOH固體溶于水后能導電,所以NaOH溶液是電解質
B.CO2的水溶液能夠導電,所以C02是電解質
C.NH3不是電解質,氨水可以導電是電解質
D.CaCO3難溶于水,其溶液幾乎不導電所以不是電解質
E.NaCl晶體不導電,NaCl是電解質
F.Cu是可以導電的,因此Cu是電解質
這個題目考察的是對電解質定義的理解, A、C、F選項是對關鍵詞中化合物的考察NaOH溶液、氨水屬于混合物,Cu屬于單質.B、D則是屬于需要理解實質性的電離含義,電離是本質物質在水作用下自身產生自由移動的帶電離子,CO2是溶于水,與水反應的產物碳酸導電,不屬于自身的原因造成的導電,CaCO3難溶不代表完全不溶,少部分溶于水的CaCO3是完全電離的存在.E是對物質的所處狀態的探析,NaCl的水溶液能導電,熔融狀態的晶體也能導電,滿足要求的是物質所處的狀態.因此,只有在對電解質定義理解深刻后才能保證正確率的.
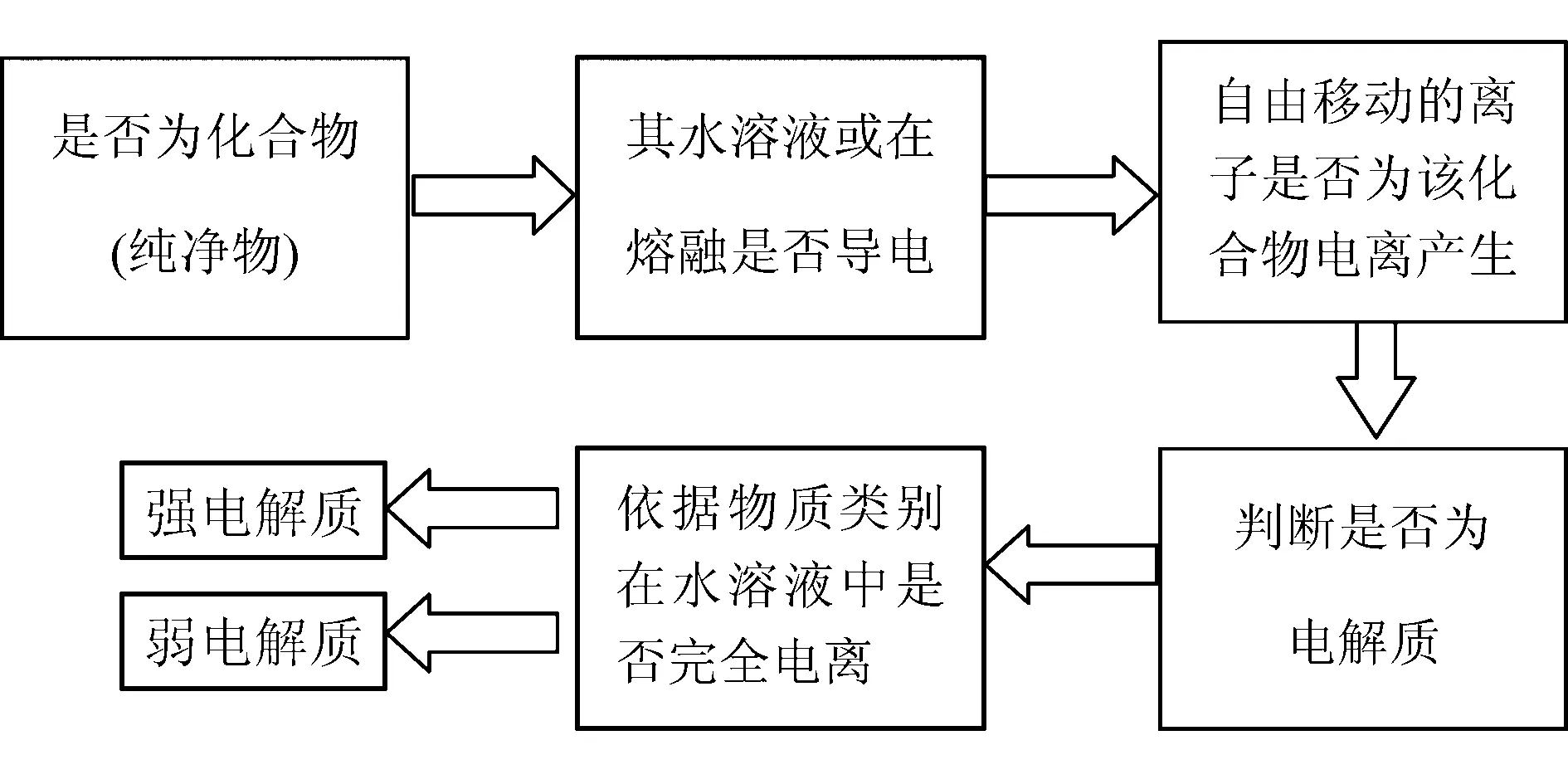
對于電解質的判斷:可以通過以下流程圖進行理解:
二、概念的轉變方式
由此,關于電解質存在的迷思概念主要有主次不分,因果倒置、知識的錯誤遷移等.針對上述存在的迷思概念,筆者認為可以通過兩種方式進行概念的轉變.
1.化學史引入
對于電解質的研究,開始于法拉第時代,法拉第在研究電解反應時,把電解以前未被分解的物質叫做電解質(electrolyte),認為它是一種能夠被電流分解的物質.他還認為,溶液中的電流是由帶電荷的被分解的物質輸送的,這種物質叫做離子,它的含義是被電流分解出來的物質.但這樣的認識是不足片面的.隨著科學家的進一步研究,特別是阿累尼烏斯通過研究發現在通電以前,電解質就已經在水溶液中離解了.電離并不需要電流,但由于歷史原因電解質這個名詞被保留了下來,并一直沿用至今.就像鉛筆的主要成分是石墨,因為最初鉛筆是由鉛制作的,其名稱未改變一直延續下來.因此,讓學生理解電解質的緣由,能更好的幫助他們理解電解質這個名詞.
2.學生實驗探究
電離并不需要電流的參與,電離產生的條件又是什么呢?
這時,可以讓學生對電解質的電離內容進行活動探究,尋找原因,例如:
①Ba(OH)2少量固體,放入盛有水的燒杯中,觀察前后水的pH變化將新制的HCl 氣體通入水中后,觀察前后水的pH變化.
②取2支相同的試管,加入等量BaCl2固體,加入相同量的水.其中一只試管滴加加入硝酸酸化的硝酸銀溶液,觀察反應現象:另一只試管滴加稀硫酸溶液,觀察反應現象.
③取2支相同的試管,加入等量BaCl2溶液(由①中Ba(OH)2溶液和②中鹽酸反應制得)其中一支試管滴加加入硝酸酸化的硝酸銀溶液,觀察反應現象:另一支試管滴加稀硫酸溶液,觀察反應現象.
通過上述實驗的探究,酸、堿、鹽在水的作用下發生電離,產生自由移動的離子.通過實踐發現電離的真相,理解電解質的真實定義.
3.互聯網“+”微課
互聯網+時代,相信大部分老師都掌握對于PPT的使用,因此在利用office軟件中PPT自帶的動畫效果基礎上,年輕教師可以嘗試接觸微課的設計,利用Focusky,EVC 手繪或相應動畫剪輯軟件等,將微觀粒子的不可視離子反應,用“可視化”動畫效果的間接展示,比起板書上一筆一劃的文字會更讓學生感興趣,例如在NaCl溶于水的過程環節,適當加入一些動畫及聲音的特效.就同一信息的接受程度而言,文字的接受程度小于圖片及視頻接受程度.同時視頻使學生更易理解電離的實質,方便后續離子反應教學的進行.其次每個教師對于動畫的表現形式都可以是不一樣的,在與學生互動交流中可以根據學生的腦海中關于電離的理解想象進行制作動畫或者短視頻編輯.
高中階段關于強弱電解質的分類條數對于該階段的學生而言,是存在一定困難的,綜合來看,電解質知識點細又多教輔書知識點收錄不全,多數為易錯點提醒分析,學生注意平時添磚加瓦的積累,務實打基礎,考試時才不會出現分數忽高忽低的情況.最后決定電解質學習的好壞,就是本質的理解加日常的積累.迷思概念的存在也是在理解不到位的基礎上滋生出來的,如果教師不及時發現,它就會越發的牢固扎根學生頭腦之中,影響學生對正確科學概念的理解,因此,希望大家能對電解質迷思概念引起重視,將問題消滅在萌芽狀態.

