乙酰左旋肉堿對順鉑誘導的學習記憶損傷的神經保護作用
王晨瑩,董曉輝,王 貝,王冬梅
化療相關的認知障礙(chemotherapy-related cognitive impairment,CRCI),也稱化療腦(chemo brain),是在進行化療藥物治療后出現的認知障礙,包括廣泛的神經問題,如注意力、執行功能、記憶力和處理速度方面的障礙[1-2]。這些認知障礙通常會持續很長時間,并對生活質量產生負面影響[3-5]。研究顯示,鉑類化療藥物順鉑在臨床的應用與CRCI的高發率密切相關。目前,大多數關于化療腦的研究都集中在乳腺癌患者身上[6-7]。對于嚙齒類動物的臨床研究表明,通常用于乳腺癌的藥物(如甲氨喋呤、5-氟尿嘧啶和環磷酰胺等)會引起認知障礙,這與神經炎癥和神經發生障礙有關[8-10]。但化療相關認知障礙的潛在機制尚不清楚,目前尚無有效的治療方法。最近研究發現,化療引起的大腦線粒體損傷在CRCI中發揮著關鍵性作用[11-12]。乙酰左旋肉堿具有線粒體和神經保護的作用[13-14],本研究探討乙酰左旋肉堿對順鉑誘導的學習記憶損傷的神經保護作用,現報道如下。
1 材料與方法
1.1 材料實驗動物:C57BL/6小鼠38只,體質量25~30 g。藥品與試劑:順鉑(購自sigma公司);乙酰左旋肉堿(上海TCI化成工業發展有限公司);高爾基染色試劑盒購自美國Hitobiotec公司;尼氏染色試劑盒、線粒體—胞質蛋白制備試劑盒和線粒體膜電位檢測試劑盒(碧云天生物技術公司);線粒體ATP合成生物發光檢測試劑盒、線粒體細胞色素c氧化酶活性測定試劑盒(美國GENMED SCINTIFICS INC生物公司)。儀器:MT-200 Morris水迷宮視頻跟蹤分析系統(荷蘭Noldus公司Ethovision XT軟件)。
1.2 分組與給藥C57BL/6小鼠(25~30 g)38只隨機分為4組(n=8~10):對照組(Control組),乙酰左旋肉堿單獨組(Acetyl-L組),化療腦組(Cisplatin組),乙酰左旋肉堿治療化療腦組(Cis/Acetyl-L)。連續5 d腹腔注射2.3 mg·kg-1順鉑,5 d不注射,為1個周期,連續進行3個周期構建化療腦模型(Cisplatin組),在順鉑注射1 h前腹腔注射乙酰左旋肉堿(150 mg·kg-1)進行治療(Cis/Acetyl-L)。Control組腹腔注射等劑量的Cisplatin溶劑(無菌生理鹽水)和腹腔注射乙酰左旋肉堿溶劑,Acetyl-L組腹腔注射等劑量的Cisplatin溶劑和腹腔注射乙酰左旋肉堿(150 mg·kg-1)。
1.3 檢測指標
1.3.1 用Morris水迷宮實驗檢測學習和記憶功能平臺隱藏實驗中:每天在同一時間段訓練小鼠4次,分別從4個不同象限將小鼠面壁置入池內,不同的小鼠在相同的位置下水。每次游泳時間60 s,找到平臺,并在上面停留3 s以上者,視為找到平臺;60 s內沒有找到平臺的要將其引導到平臺上,停留15 s;小鼠沒有找到平臺按60 s計算潛伏期。每次訓練間隔1 h左右。空間探索實驗:第五天,把放置在第三象限的平臺拿走,任選一個入水點將小鼠放入水中,小鼠在水中游泳60 s,主要記錄小鼠在平臺區出現的頻次,小鼠在目標象限(原平臺所在象限)和其他各象限的游泳時間,數據搜集和處理由Morris水迷宮系統軟件完成。
1.3.2 用尼氏染色觀察海馬CA1區神經元形態行為學實驗后,每組隨機抽出3~4只小鼠進行形態學分析。用4%多聚甲醛心臟灌注取腦、固定、石蠟包埋,常規脫蠟至水。切片入尼氏染色液1(cresyl violet stain),56 ℃浸染1 h,冷蒸餾水沖洗后,入尼氏染色液2(Nissl differentiation)分化1~3 min,至顯微鏡下觀察至背景接近于無色為止。隨后無水乙醇迅速脫水。二甲苯透明,中性樹膠封固。顯微鏡下觀察海馬CA1區神經元形態,并拍照。
1.3.3 用高爾基染色觀察樹突棘密度行為學實驗后,每組隨機抽出2~3只小鼠,迅速取出腦組織,嚴格按照高爾基染色試劑盒說明書進行浸泡、包埋、切片(厚度80 μm)、染色、脫水、透明、封片、觀察結果。
1.3.4 線粒體分離和功能檢測頸椎脫臼法犧牲小鼠后,剝離的海馬置于預冷的生理鹽水沖洗,線粒體分離具體方法參照文獻[8]。細胞色素C氧化酶活性以還原型細胞色素C(Cyt C)在550 nm,下被氧化的速度,以變化的吸光度值表示細胞色素C氧化酶活性。提取的線粒體與外源底物谷氨酸鉀及ADP孵育,采用熒光法檢測ATP產生速率。線粒體膜電位(mΔΨ):線粒體懸液中加入含2 μM JC-1的檢測體系中,微型轉子攪拌下室溫孵育30 min,離心去除未結合線粒體的JC-1,488 nm激發光下讀取熒光強度。

2 結果
2.1 Morris水迷宮
預實驗中選擇了低中高3個不同的劑量(50、100、150 mg·kg-1·d-1)作用化療腦(Cisplatin組)小鼠,通過行為學確定乙酰左旋肉堿的最佳劑量。結果顯示,只有高劑量(150 mg·kg-1·d-1)乙酰左旋肉堿,治療后均能顯著改善化療腦組小鼠的認知能力(表現為與化療腦組小鼠相比,空間探索實驗中靶象限滯留時間顯著增加)。據此,高劑量的乙酰左旋肉堿(150 mg·kg-1·d-1)被選作進一步研究的最佳用量。
為了研究乙酰左旋肉堿對順鉑誘導的認知障礙模型小鼠空間學習記憶能力的作用,4組實驗鼠進行Morris水迷宮實驗。定位航行實驗,重復測量數據的方差分析結果顯示,不同組間的小鼠潛伏期差異有統計學意義[F(3,34)=6.75,P<0.05]。如圖1所示,隨著訓練天數的增加,各組小鼠找到平臺的潛伏期較之前一天均逐漸縮短[F(4,136)=126.01,P<0.05]。然而,與對照組小鼠相比,Cisplatin組小鼠尋找平臺的潛伏期顯著延長(P<0.05);而乙酰左旋肉堿(200 mg·kg-1·d-1)治療可以明顯縮短化療腦小鼠的潛伏期(P<0.05)。結果表明乙酰左旋肉堿能夠促進化療腦小鼠的空間學習能力。
空間探索實驗結果顯示,4個實驗組小鼠在靶象限滯留時間[F(3,56)=31.16,P<0.05]差異無統計學意義。Cisplatin組小鼠在靶象限滯留時間[(16.60±1.61) s VS (27.80±1.01) s,P<0.05]明顯少于對照組小鼠;而乙酰左旋肉堿(200 mg·kg-1·d-1)治療可以顯著增加Cisplatin組小鼠在靶象限限滯留時間[(25.07±1.23) s VS (16.60±1.61) s,P<0.05](圖2-3)。4個實驗組小鼠在速度(圖4)上差異無統計學意義,表明乙酰左旋肉堿并不是通過速度或者其他動力因素改善了記憶功能。見圖1。
2.2 尼氏染色與對照組小鼠相比,Cisplatin組小鼠海馬CA1區膠質細胞增生、排列紊亂、尼氏小體數目明顯減少,細胞體積明顯縮小、形態不規則、核仁少見,細胞間距增大、輪廓模糊、界限不清。乙酰左旋肉堿治療后能夠顯著增加尼氏小體數目。對照組與乙酰左旋肉堿單用組相比,CA1區細胞排列整齊、胞核核仁明顯,尼氏小體數目較多、輪廓清晰。結果表明:乙酰左旋肉堿對順鉑誘導的海馬神經元損傷具有保護作用。見圖5。
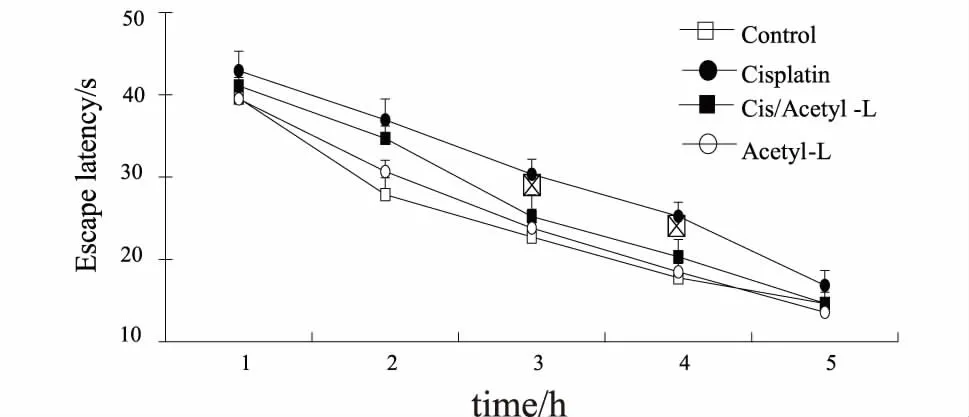
①與對照組相比,P<0.05;②與Cisplatin組相比,P<0.05。圖1 定位航行實驗潛伏期分析
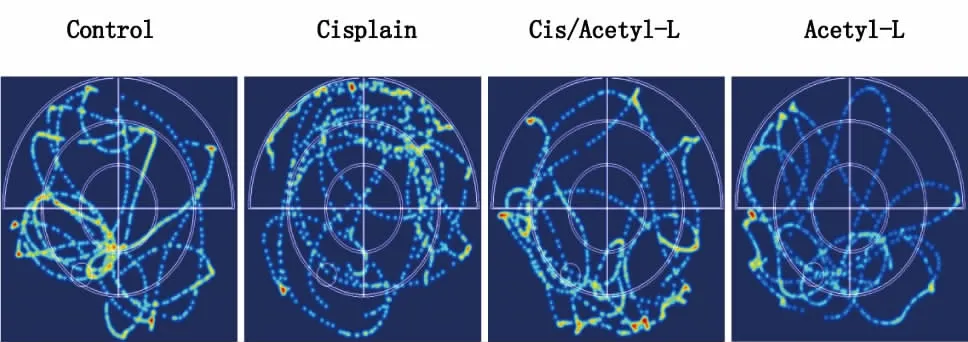
圖2 空間探索實驗軌跡圖
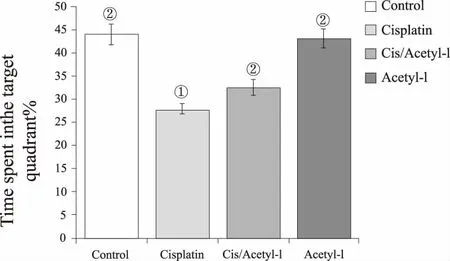
①與對照組相比,P<0.05;②與Cisplatin組相比,P<0.05。圖3 空間探索實驗平臺象限滯留時間分析
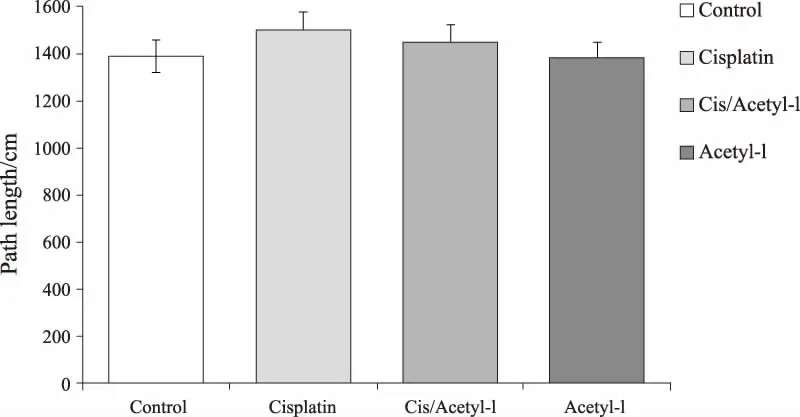
圖4 空間探索實驗總路徑
2.3 高爾基染色與對照組小鼠相比,Cisplatin組小鼠CA1區錐體神經元樹突棘密度顯著減少(P<0.05);而乙酰左旋肉堿治療后能夠顯著增加Cisplatin組小鼠的樹突棘密度(P<0.05)。對照組與乙酰左旋肉堿單用組相比,CA1區錐體神經元樹突棘密度沒有差異。結果表明:乙酰左旋肉堿緩解Cisplatin誘導的小鼠CA1區錐體神經元樹突棘的丟失,緩解突觸損傷(見圖6-7)。
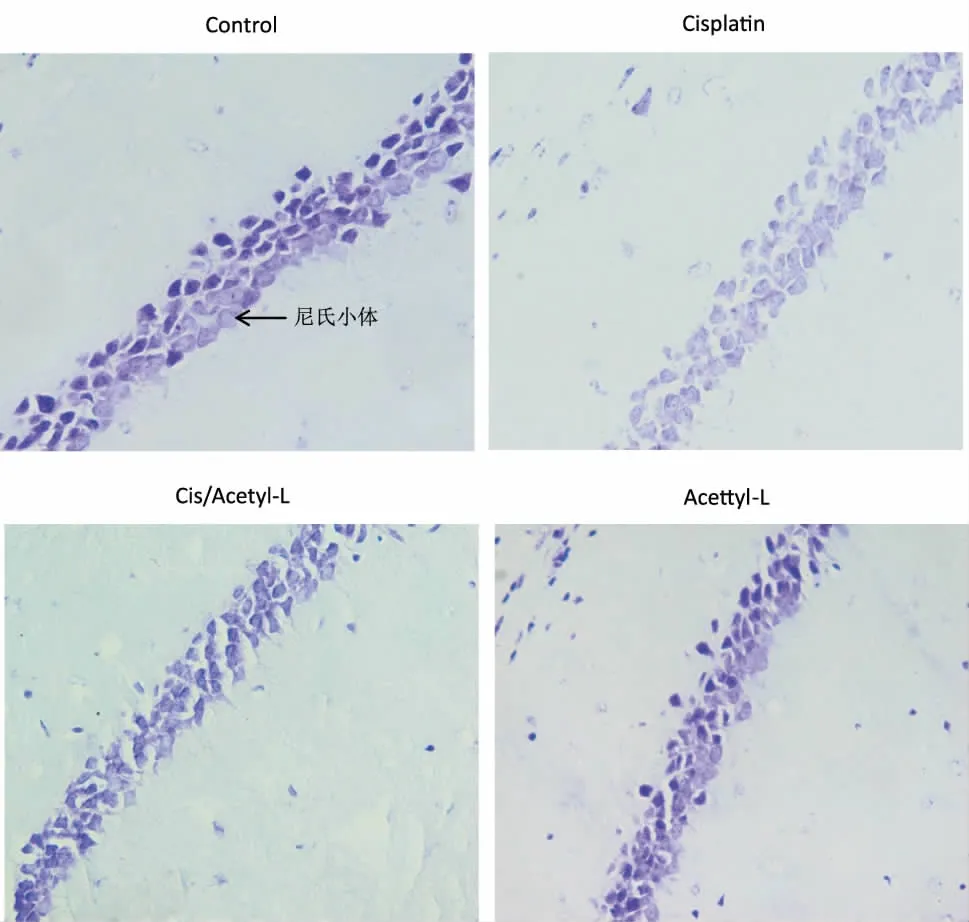
圖5 實驗組小鼠CA1區錐體神經元尼氏染色情況(尼氏染色,×400)
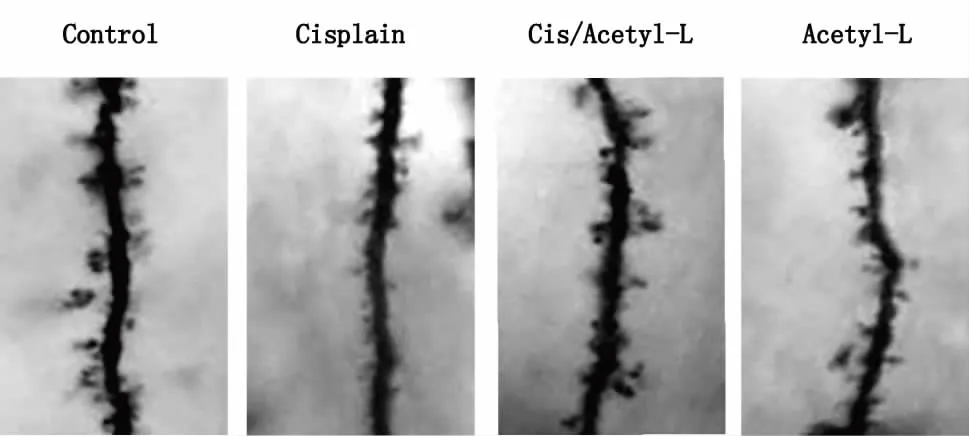
圖6 CA1區錐體神經元樹突棘密度(高爾基染色,×100)
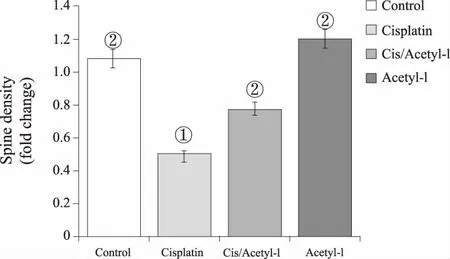
①與對照組相比,P<0.05;②與Cisplatin組相比,P<0.05。圖7 樹突棘密度分析
2.4 線粒體功能順鉑能夠損傷線粒體功能,引起ATP合成減少,能量缺乏(表現為與對照組小鼠相比,Cisplatin組小鼠細胞色素c氧化酶活性降低(P<0.01),ATP合成能力(P<0.05)以及線粒體膜電勢均下降(P<0.05)。與Cisplatin組小鼠相比,Cis/Acetyl-L組小鼠腦組織細胞色素c氧化酶活性增加了50.13%(P<0.05),ATP合成能力增加了33.28%(P<0.05),線粒體膜電勢增加了31.32%(P<0.05)。對照組與乙酰左旋肉堿單用組相比,細胞色素c氧化酶活性,ATP合成能力以及線粒體膜電勢均沒有差異。結果表明:乙酰左旋肉堿緩解Cisplatin誘導的小鼠腦組織線粒體失功能。見圖8-10。
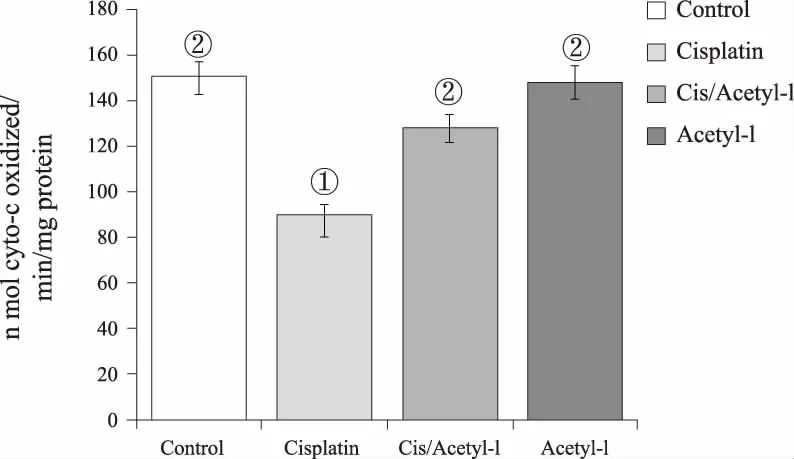
①與對照組相比,P<0.05;②與Cisplatin組相比,P<0.05。圖8 細胞色素c氧化酶活性
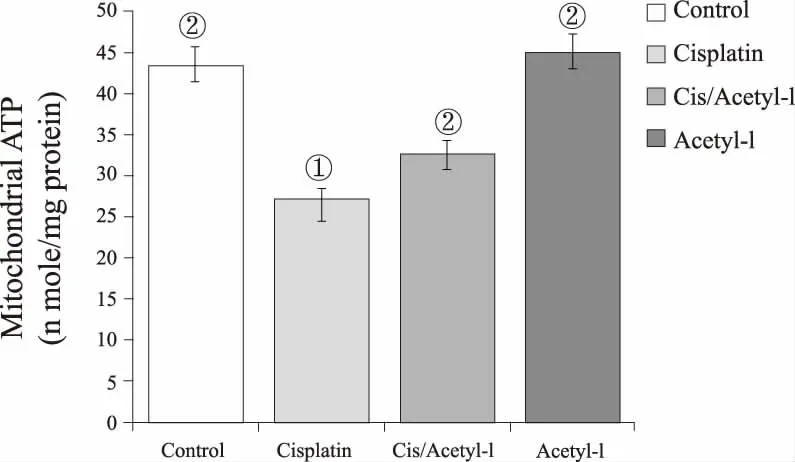
①與對照組相比,P<0.05;②與Cisplatin組相比,P<0.05。圖9 ATP合成能力
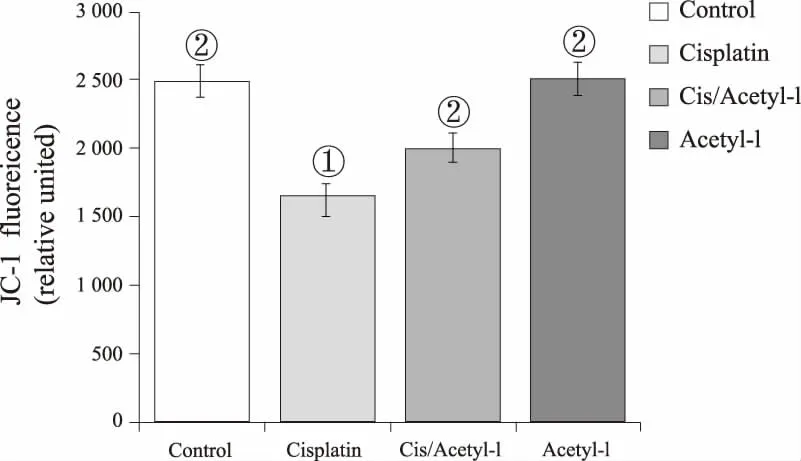
①與對照組相比,P<0.05;②與Cisplatin組相比,P<0.05。圖10 線粒體膜電勢
3 討論
對CRCI的深入研究表明,化療誘導的腦線粒體病變在CRCI的發生發展中發揮著重要的作用。順鉑化療對中樞神經系統產生神經毒性,與CRCI的高發率密切相關。順鉑能夠通過血腦屏障,在腦實質和海馬區域聚集。順鉑引起的氧化磷酸化效率損傷、ATP供應障礙、氧化應激和鈣穩態紊亂作為神經元線粒體功能損傷的重要病理基礎,參與CRCI的發生發展。順鉑可以誘導線粒體DNA(mtDNA)損傷,并在培養的大鼠海馬神經元和NSCs中損害呼吸活性。順鉑通過促進活性氧的產生,誘導線粒體氧化損傷和凋亡,抑制抗氧化酶和釋放自由基。線粒體功能障礙會增加氧化應激,從而刺激自由基的產生,導致樹突棘的損失。在動物模型中順鉑引起的認知損傷與神經元樹突棘和突觸密度的急劇減少呈正相關[15]。順鉑引起的ATP供應障礙、氧化應激和鈣穩態紊亂作為神經元線粒體功能損傷的重要病理基礎,參與CRCI的發生發展。在培養的海馬神經元中,順鉑誘導mtDNA損傷,引起線粒體腫脹或空泡變性,神經元死亡。因此,改善線粒體功能的方法和策略能夠緩解化療誘導腦損傷和認知功能。本研究通過對小鼠海馬CA1區神經元樹突棘密度的測定,表明乙酰左旋肉堿可以通過緩解線粒體功能損傷而減少樹突棘損失,改善突觸功能,同時還可促進海馬組織內尼氏體的修復,改善順鉑誘導的認知障礙模型小鼠學習記憶功能。
乙酰左旋肉堿(ALCAR)具有線粒體保護功能,能有效防止氧化應激引起的線粒體損傷和隨之產生的線粒體依賴性凋亡[13-14]。乙酰左旋肉堿已經被證明可以保護細胞免受線粒體和自由基相關的核DNA損傷,通過減少氧化劑產生和提高抗氧化能力來改善線粒體的功能。乙酰左旋肉堿是一種內源性的代謝中間體,在大腦中存在,參與了乙酰基在代謝和合成代謝過程中的傳輸,并緩沖了乙酰輔酶A。ALCAR是在許多組織中,包括大腦、肝臟、心臟、腎臟、肌肉等,通過將乙酰基轉移到肉堿中合成的,它已經被證明可以保護細胞免受線粒體和自由基相關的核DNA損傷,通過減少氧化劑的產生和提高抗氧化的能力來改善線粒體的功能。
本研究結果顯示,乙酰左旋肉堿能夠明顯改善順鉑誘導的線粒體功能損傷,表現為細胞色素c氧化酶活性降低,ATP合成能力以及線粒體膜電勢均下降。線粒體功能障礙會增加氧化應激,從而刺激自由基的產生,導致樹突棘的損失。因此,線粒體失功能被認為是引起突觸損傷的重要因素,改善者線粒體功能的方法和策略可以有效地保護突觸可塑性,延緩認知的神經退行性病變。本研究對小鼠海馬CA1區神經元樹突棘密度的測定,表明乙酰左旋肉堿可以通過緩解線粒體功能損傷而減少樹突棘損失,改善突觸功能,同時還可促進海馬組織內尼氏體的修復,最終達到改善順鉑誘導的認知障礙模型小鼠學習記憶功能。但乙酰左旋肉堿對順鉑誘導的認知障礙的詳細分子機制,還有待進一步探討。

