銀電解液中游離硝酸、銅和銀的連續測定分析
蒙英寧
廣西南丹南方金屬有限公司 廣西南丹 547204
銀電解液中游離硝酸、銀和銅一直都是單獨進行取樣和測定,操作比較繁瑣,試劑消耗比較大,丟棄具有大量銀的試液,導致出現浪費。本文使用一份試樣進行連續測定,不僅能夠使工作效率得到提高,還能夠節約試劑。
1 主要試劑和操作方法
使用8+1硝酸,配制之后煮沸冷藏到室溫。溴甲酚綠1g/L,氫氧化鈉0.02mmol/L,乙醇1g/L,硫酸高鐵銨100g/L。
使用32g的無水乙酸鈉和適量的水相互融合,添加冰乙酸200ml,使用水稀釋到1L,攪拌均勻。
使用1ml銀電解液放置到100mL蒸餾水的燒杯中,添加兩滴溴甲酚綠指示劑,利用氫氧化鈉標準溶液滴到藍色定(為終點),通過消耗的氫氧化鈉標準溶液對硝酸游離(游離硝酸)含量進行計算[1-2]。
對杯壁進行沖洗,使燒杯放置到電爐中加熱到50-60℃,添加兩滴PAP指示劑與3ML醋酸鈉緩沖液,使用EDTA標準溶液進行滴定,溶液從紫紅色轉變成為黃綠色表示終點。通過消耗EDTA標準溶液對銅含量進行計算。如果試液中的Br3+和Fe3+含量比較多,能夠使用硝酸調整pH1.5-1.7,添加1mL坦試劑,滴定溶液為亮黃色,以以上步驟絡合滴定。
沖洗杯壁,添加20mL硝酸與10mL鐵銨礬指示劑,利用硫磬酸鉀(硫氰酸鉀)標準溶液滴定,溶液為淺紅色為終點,對銀含量計算。
2 結果和討論
2.1 選擇指示劑
利用氫氧化鈉進行測試過程中,能夠使用溴甲酚綠、甲基紅等酸堿指示劑,但是因為下步滴定Cu2+的時候,PAR-Cu2+(II)屬于紅色絡合物,藍色能夠對紅色進行襯托,從而明確滴定的終點,所以使用溴甲酚綠[3-4]。
2.2 消除Fe3+和Br3+干擾
銀電解液中的Fe3+和Br3+微量,在電解液電解期限不斷增加的過程中增加。相關原始資料表示,鉍含量在0.01-0.40g/L范圍中波動,鐵在0.01-0.15g/L范圍中波動。以此可以看出來,在Fe3+和Br3+含量比較高的時候,對于Cu2+滴定結果就會出現一定的誤差。因為Fe3+和Br3+與EDTA絡合穩定常數比較大,所以能夠使用酸效應方法將干擾消除。本文基于pH值1.5-1.7,將鉭試劑作為指示劑,首先使用EDTA對Fe3+和Br3+滴定,之后調整pH值3.5,使用EDTA對Cu2+進行滴定。通過消除情況表示,假如pH值比較低,那么1mg以下Fe3+和Br3+對于Cu2+測定影響比較小。表1為不同pH值中EDTA滴定Cu2+結果。
2.3 滴定Cu2+的pH值
通過EDTA酸效應曲線可以看出來,在pH>3的時候,Cu2+能夠使用EDTA定量進行滴定,但是在實際測定過程中并沒有充分考慮其他的因素。比如試液中具有其他微量,在滴定Cu2+時pH>3.5的時候,微量也會被滴定。另外,Cu2+在高pH值的時候會出現水解沉淀的情況,從而拖長了終點。在不同pH值條件中滴定Cu結果(表2),通過結果表示,在pH>4.0的時候,Pb2+、Zn2+的干擾比較大。所以,EDTA滴定Cu2+最佳的pH值為pH3.5-4.0之間。
2.4 選擇滴定Bi3+、Fe3+的指示劑
滴定Bi3+、Fe3+中具有多種指示劑能夠進行選擇,比如黃基水楊酸(磺基水楊酸)、二甲酚橙、鉭試劑等。通過實驗表示,二甲酚橙能夠封閉Bi3+、Fe3+,磺基水楊酸在測定高含量Cu2+過程中顯色并不明顯,鉭試劑適合。在Fe3+完全絡合滴定之后,在10%的硝酸溶液中,鉭試劑和Fe3+絡合物破壞,基本無色,不會對鐵銨礬指示劑測定銀造成影響[5]。
2.5 試樣分析和加標回收的結果
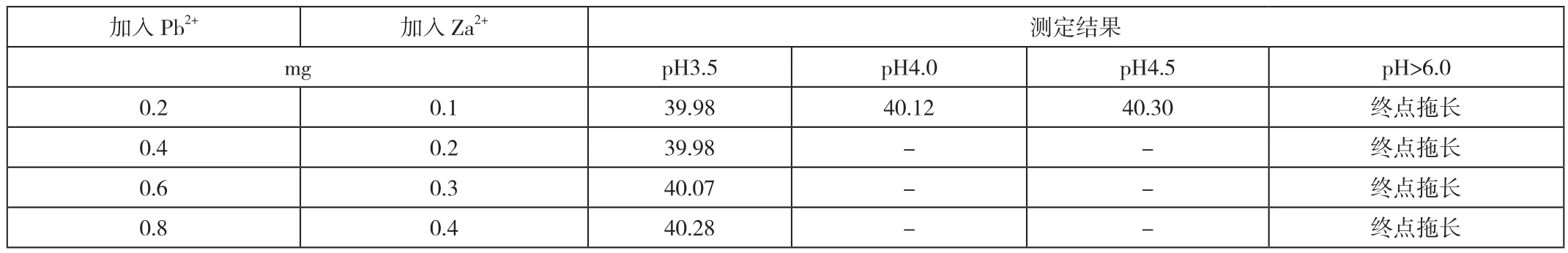
表1 不同pH值中EDTA滴定Cu2+結果
以實驗步驟,表3為實驗分析與加標測定的結果。
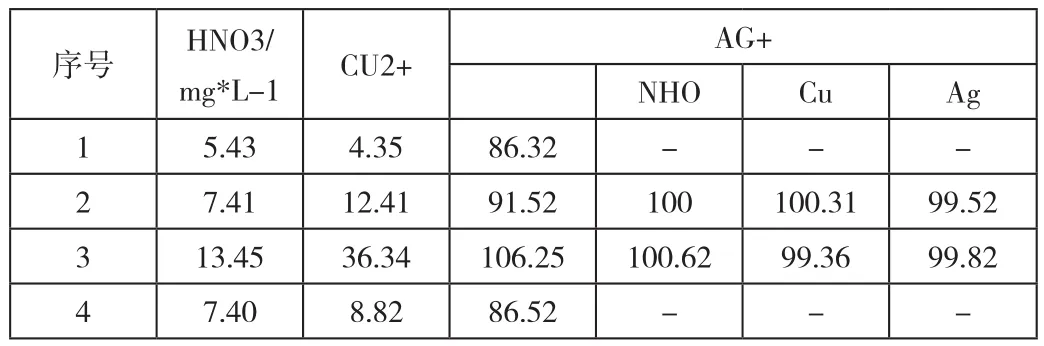
表3 實驗分析與加標測定的結果
通過試樣平行測定十次,銅、硝酸、銀測定標注偏差為0.72%、0.47%、0.1%。
3 結語
通過本文實驗表示,并且實現同個試樣測定十次,銀電解液中有利銅、硝酸與銀的連續測定方法精準,操作方便。

