滋腎降糖丸聯合西藥治療氣陰兩虛證糖尿病腎病(G3aA2期)的臨床觀察及對Galectin-3的影響
楚淑芳, 趙恒俠, 劉德亮, 劉雪梅, 渠昕, 李惠林
(深圳市中醫院內分泌病科,廣東深圳 518033)
糖尿病常伴有危及生命的并發癥,如糖尿病腎病(diabetic kidney disease,DKD)、視網膜病變和神經病變等[1]。DKD是糖尿病患者最常見的微血管并發癥之一,與其他腎臟疾病相比,它是導致腎功能衰竭的主要原因[2],其發生發展機制尚不清楚,目前臨床上西醫治療措施主要有控制血糖、降壓、調脂及降低尿蛋白等對癥處理以延緩腎臟的進一步損害,但不能阻止DKD病程的進展。近年來,中醫對DKD的研究頗多,隨著對其病因病機、臨床癥狀等研究的深入,認為其病位主要在脾腎,并形成了“消渴腎病”這一中醫病名[3]。在治療方面也初步顯示出中醫藥療法能有效改善臨床癥狀、減緩病情進展和不良反應小等獨特優勢。滋腎降糖丸為本院自主研發的中藥復方制劑,是用于治療糖尿病的有效臨床協定方,具有益氣養陰、健脾滋腎的作用,切合DKD的早期病機特點。
半乳糖凝集素-3(Galectin-3)是半乳糖凝集素家族的重要成員之一,也是晚期糖基化終末產物(advanced glycation end products,AGEs)的受體之一,在DKD發生、發展過程中發揮重要作用。Kikuchi等[4]研究表明,DKD患者的腎小球Galectin-3陽性細胞明顯增多,且與尿蛋白呈正相關,與腎功能呈負相關。最近的一項臨床研究[5]進一步證實,血清Galectin-3與DKD獨立相關,推測其可能是DKD的一個生物標志物。基于此,本研究旨在觀察滋腎降糖丸對氣陰兩虛證DKD(G3aA2期)患者的臨床療效及其對血清Galectin-3的影響,為進一步研究中藥治療氣陰兩虛證DKD的作用靶點及機制提供新的研究切入點。
1 對象與方法
1.1 研究對象及分組 收集2016年3月至2017年2月在深圳市中醫院內分泌科住院治療的2型糖尿病病例中符合DKD氣陰兩虛證診斷標準的患者,共60例。采用隨機數字表法將患者隨機分為對照組和觀察組,每組各30例。本研究符合醫學倫理要求并獲醫院倫理委員會審核批準。
1.2 病例選擇標準
1.2.1 診斷標準 (1)糖尿病西醫診斷和分型標準參照1999年世界衛生組織(WHO)提出的糖尿病診斷標準[6];(2)DKD的診斷參照2001年中華醫學會編著的《臨床診療指南腎臟病學分冊》中對DKD的臨床診斷標準[7];(3)G3aA2分期:參照腎臟病改善全球預后(KDIGO)指南建議,聯合慢性腎臟病(chronic kidney disease,CKD)分期(G1~G5)和白蛋白尿分期(A1期:UACR<30 mg/g;A2期:UACR30~300mg/g;A3期:UACR>300mg/g)描述和判定DKD的嚴重程度[8]。(4)中醫辨證標準:依據2007年中華中醫藥學會腎病分會《糖尿病腎病診斷、辨證分型及療效評定標準(試行方案)》[9]中對氣陰兩虛證的定義。主癥:倦怠乏力,心悸氣短,頭暈耳鳴,自汗、盜汗;次癥:面色白,心煩失眠,遺精早泄,口渴喜飲;舌脈:舌淡紅、少苔或花剝,脈濡細或細數無力。
1.2.2 納入標準 ①年齡30~70歲;②符合上述中西醫診斷標準;③中醫證型經2位副主任及以上高級職稱醫師嚴格辨證后,確定診斷為氣陰兩虛證;④自愿參加本試驗并簽署知情同意書的患者。
1.2.3 排除標準 ①1型糖尿病或近期出現糖尿病急性并發癥的患者;②合并其他原發性或繼發性腎臟疾病的患者;③合并有嚴重心腦血管、呼吸、血液系統疾病、腫瘤及肝功能嚴重損害的患者;④妊娠期或哺乳期婦女;⑤依從性差,意識障礙和拒簽知情同意書的患者。
1.2.4 脫落及終止標準 ①已進入研究但未完成規定療程的患者;②試驗過程中出現過敏、安全性指標異常或不良反應,根據評估應終止試驗的患者;③試驗過程中受試者病情持續加重或出現其他嚴重疾病等情況的患者;④試驗方案發生了重要偏差,導致藥物療效無法評價的患者;⑤主動退出試驗及失訪者。
1.3 藥物、試劑及儀器
1.3.1 藥物 滋腎降糖丸為本院自行研發的中藥復方制劑,藥味組成:生地黃、黃芪、黨參、五味子、黃精、懷牛膝、三七等;批準文號:粵Z20070085;規格:50 g/瓶。
1.3.2 試劑 空腹血糖(FPG)、餐后2 h血糖(2hPG)、甘油三酯(TG)、總膽固醇(TC)、低密度脂蛋白膽固醇(LDL-C)、血肌酐(Scr)檢測試劑盒購自德國Roche公司;C肽測定試劑盒購自美國雅培公司;空腹胰島素(FINS)化學發光法檢測試劑盒購自美國Beckman Coulter公司;糖化血紅蛋白(HbA1c)測定所用試劑為美國Primus公司U1tra2原裝試劑。尿微量白蛋白/肌酐比值(UACR)檢測試劑盒購自挪威Axis-Shield PoC AS。人Galectin-3酶聯免疫吸附法(ELISA)定量檢測試劑盒購自美國R&D公司。
1.3.3 儀器 Cobas 8000全自動生化分析儀(Roche,德國);U1tra2親和層析高壓液相糖化血紅蛋白檢測儀(Primus,美國);全自動免疫分析系統ARCHITECT i2000SR(Abbrot,美國);全自動酶標儀(Bio-Rad,美國)。
1.4 治療方法 對照組:給予西醫常規治療,包括:糖尿病健康教育,DKD飲食,規律的合適運動,藥物治療[根據患者病情選擇合適的降糖方案,合并脂代謝紊亂者給予調脂藥物治療,合并高血壓者則首選血管緊張素轉換酶抑制劑(ACEI)和血管緊張素Ⅱ受體拮抗劑(ARB)類降壓藥]。觀察組:在對照組基礎上加服滋腎降糖丸,每日3次,每次6 g。2組療程均為1個月。
1.5 觀察指標
1.5.1 一般項目及中醫證候積分 (1)一般項目:主要包括姓名、性別、年齡、體質量、身高、糖尿病病程、收縮壓(SBP)及舒張壓(DBP)等。(2)中醫證候積分:根據2002年《中藥新藥臨床研究指導原則》[10]中的證候積分量表,主證按無、輕、中、重分別計0、2、4、6分,次證按無、輕、中、重分別計0、1、2、3分,觀察2組患者治療前后中醫證候積分的變化情況。
1.5.2 血生化指標檢測 患者均空腹8 h以上,于次日7∶00-8∶00采空腹肘靜脈血,離心,分離血清,FPG、2hPG、TC、TG、LDL-C及Scr等指標由本院檢驗科Roche全自動生化儀檢測;FINS檢測使用化學發光法;HbA1c應用親和層析法測定;C肽檢測方法為化學發光微粒子免疫檢測法。胰島素抵抗指數(HOMA-IR)=FINS(μU/mL)×FBG(mmol/L)/22.5;腎小球濾過率估計值(eGFR)利用簡化的腎臟病膳食改良試驗(MDRD)公式計算:eGFR(mL/min1.73 m2) =186 × Scr(mg/dL)-1.154×年齡(y)-0.203×(0.742女性)。觀察2組患者治療前后各項血生化指標的變化情況。
1.5.3 尿蛋白指標檢測 收集患者晨尿約15 mL,離心取上清液,應用快速免疫比濁法檢測UACR。觀察2組患者治療前后UACR的變化情況。
1.5.4 血清Galectin-3檢測 患者均禁食8 h以上,于次日7∶00-8∶00空腹采肘靜脈血,采集于普通干燥管中,離心,取上清,并將標本放于-80℃冰箱保存備用。采用ELISA法檢測血清Galectin-3水平,嚴格按照說明書程序操作。
1.6 統計方法 應用State12.0統計軟件進行數據的統計分析和處理。計量資料用均數±標準差(±s)表示,組內比較采用配對t檢驗,組間比較采用兩獨立樣本t檢驗;各組間差異采用單因素方差分析,組間多重比較用Bonferroni檢驗;不符合正態分布或方差不齊者采用Wilcoxon秩和檢驗。以P<0.05為差異有統計學意義。
2 結果
2.1 2組患者的基線特征比較 對照組30例患者中,男19例,女11例;年齡35~65歲,平均年齡(54.80±7.85)歲;病程6~18年,平均病程(12.53± 4.09)年;體質量指數(BMI)為(25.11± 3.35)kg/m2。觀察組30例患者中,男21例,女9例,年齡35~68歲,平均年齡(51.07±8.35)歲;病程6~19年,平均病程(11.90±4.09)年;BMI為(26.33±3.68)kg/m2。2組患者的性別、年齡、病程、BMI等基本特征比較,差異均無統計學意義(P>0.05),具有可比性。
2.2 2組患者治療前后中醫證候總積分比較 表1結果顯示:治療前,2組患者的中醫證候總積分比較,差異無統計學意義(P>0.05)。治療后,2組患者的中醫證候總積分均較治療前明顯下降(P<0.01),且觀察組對中醫證候總積分的下降作用明顯優于對照組,差異有統計學意義(P<0.01)。
表1 2組患者治療前后中醫證候總積分比較Table 1 Comparison of overall TCM symptom scores in the two groups before and after treatment(±s,s/分)

表1 2組患者治療前后中醫證候總積分比較Table 1 Comparison of overall TCM symptom scores in the two groups before and after treatment(±s,s/分)
①P<0.01,與治療前比較;②P<0.01,與對照組治療后比較
治療后20.27±2.86①13.40± 2.98①②組別對照組觀察組N 30 30治療前23.13±3.45 21.33±4.97
2.3 2組患者治療前后收縮壓和舒張壓比較 表2結果顯示:治療前,2組患者的SBP和DBP比較,差異均無統計學意義(P>0.05)。治療后,2組患者的SBP和DBP均較治療前明顯下降(P<0.01),且觀察組對SBP和DBP的下降作用明顯優于對照組,差異有統計學意義(P<0.05)。
2.4 2組患者治療前后腎功能及UACR比較 表3結果顯示:治療前,2組患者的Scr、eGFR和UACR水平比較,差異均無統計學意義(P>0.05)。治療后,2組患者的Scr、UACR水平均較治療前明顯下降(P<0.01),eGFR水平均較治療前明顯升高(P<0.01),且觀察組對Scr、UACR水平的下降作用及對eGFR水平的升高作用均明顯優于對照組,差異均有統計學意義(P<0.01或P<0.05)。
表2 2組患者治療前后收縮壓和舒張壓比較Table 2 Comparison of SBP and DBP in the two groups before and after treatment (±s,p/mmHg)
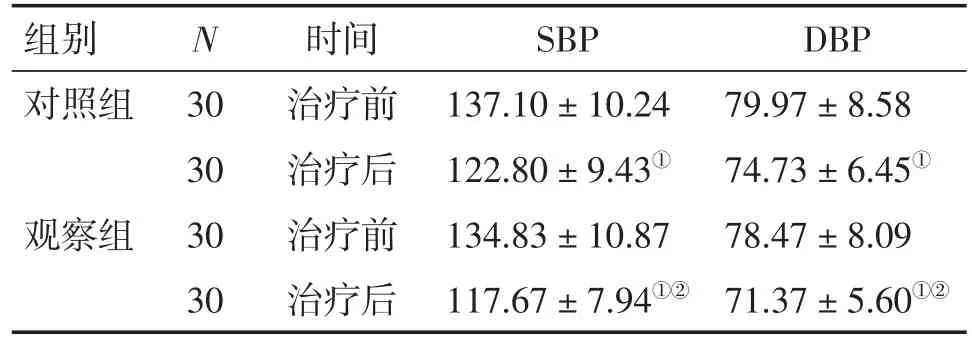
表2 2組患者治療前后收縮壓和舒張壓比較Table 2 Comparison of SBP and DBP in the two groups before and after treatment (±s,p/mmHg)
①P<0.01,與治療前比較;②P<0.05,與對照組治療后比較
DBP 79.97±8.58 74.73±6.45①78.47±8.09 71.37± 5.60①②組別對照組N觀察組30 30 30 30時間治療前治療后治療前治療后SBP 137.10±10.24 122.80±9.43①134.83±10.87 117.67± 7.94①②
表3 2組患者治療前后腎功能及UACR比較Table 3 Comparison of renal function and UACR in the two groups before and after treatment (±s)
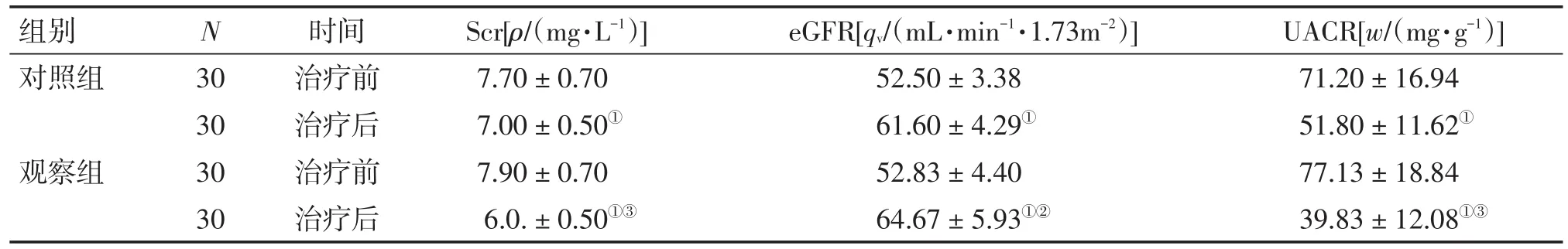
表3 2組患者治療前后腎功能及UACR比較Table 3 Comparison of renal function and UACR in the two groups before and after treatment (±s)
①P<0.01,與治療前比較;②P<0.05,③P<0.01,與對照組治療后比較
組別對照組N觀察組UACR[w/(mg·g-1)]71.20±16.94 51.80±11.62①77.13±18.84 39.83± 12.08①③30 30 30 30時間治療前治療后治療前治療后Scr[ρ/(mg·L-1)]7.70±0.70 7.00±0.50①7.90±0.70 6.0.± 0.50①③eGFR[qv/(mL·min-1·1.73m-2)]52.50±3.38 61.60±4.29①52.83±4.40 64.67± 5.93①②
2.5 2組患者治療前后糖代謝指標比較 表4結果顯示:治療前,2組患者的FPG、2hPG、FINS、HbAlc、HOMA-IR等各項糖代謝指標比較,差異均無統計學意義(P>0.05)。治療后,2組患者的FPG、2hPG、FINS、HbAlc、HOMA-IR等各項糖代謝指標均較治療前明顯下降(P<0.01),且觀察組對上述各項糖代謝指標的下降作用均明顯優于對照組,差異均有統計學意義(P<0.01或P<0.05)。
2.6 2組患者治療前后脂代謝指標比較 表5結果顯示:治療前,2組患者的TG、TC和LDL-C等各項脂代謝指標比較,差異均無統計學意義(P>0.05)。治療后,2組患者的TG、TC和LDL-C等各項脂代謝指標均較治療前明顯下降(P<0.01),且觀察組對上述各項脂代謝指標的下降作用均明顯優于對照組,差異均有統計學意義(P<0.05)。
表4 2組患者治療前后糖代謝指標比較Table 4 Comparison of glucose metabolism indicators in the two groups before and after treatment (±s)

表4 2組患者治療前后糖代謝指標比較Table 4 Comparison of glucose metabolism indicators in the two groups before and after treatment (±s)
①P<0.01,與治療前比較;②P<0.05,③P<0.01,與對照組治療后比較
組別對照組N觀察組HOMA-IR 4.68±1.13 2.02±0.49①4.29±0.88 1.77± 0.38①②30 30 30 30時間治療前治療后治療前治療后FPG[c/(mmol·L-1)]9.70±1.07 7.23±0.73①9.25±0.64 6.71± 0.64①③2hPG[c/(mmol·L-1)]15.17±1.92 11.31±1.20①14.31±1.89 9.93± 1.10①③HbAlc(p/%)8.75±0.60 7.57±0.37①8.88±0.69 7.38± 0.35①②FINS[J/(mU·L-1)]10.84±2.15 6.78±1.55①10.45±2.13 5.94± 1.08①②
表5 2組患者治療前后脂代謝指標比較Table 5 Comparison of lipid metabolism indicators in the two groups before and after treatment[±s,c/(mmol·L-1)]
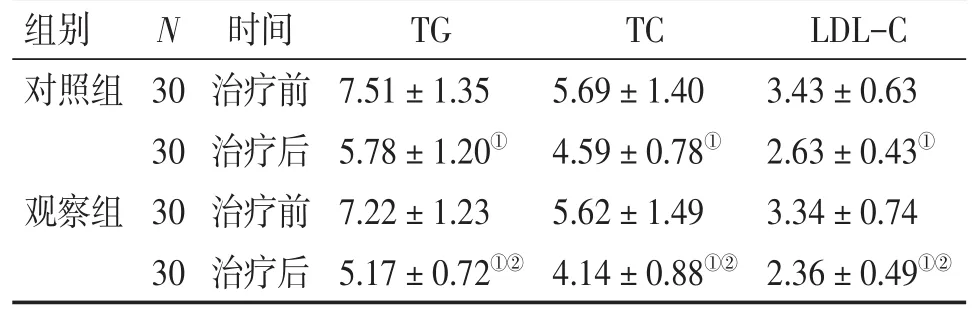
表5 2組患者治療前后脂代謝指標比較Table 5 Comparison of lipid metabolism indicators in the two groups before and after treatment[±s,c/(mmol·L-1)]
①P<0.01,與治療前比較;②P<0.05,與對照組治療后比較
LDL-C 3.43±0.63 2.63±0.43①3.34±0.74 2.36± 0.49①②組別對照組N觀察組30 30 30 30時間治療前治療后治療前治療后TG 7.51±1.35 5.78±1.20①7.22±1.23 5.17± 0.72①②TC 5.69±1.40 4.59±0.78①5.62±1.49 4.14± 0.88①②
2.7 2組患者治療前后血清Galectin-3水平比較 表6結果顯示:治療前,2組患者血清Galectin-3水平比較,差異無統計學意義(P>0.05)。治療后,2組患者血清Galectin-3水平均較治療前明顯下降(P<0.01),且觀察組患者血清Galectin-3水平的下降作用明顯優于對照組,差異有統計學意義(P < 0.05)。
表6 2組患者治療前后血清Galectin-3水平比較Table 6 Comparison of serum galectin-3 in the twogroups before and after treatment (±s)

表6 2組患者治療前后血清Galectin-3水平比較Table 6 Comparison of serum galectin-3 in the twogroups before and after treatment (±s)
①P<0.01,與治療前比較;②P<0.05,與對照組治療后比較
治療后2.45±0.29①2.26± 0.35①②組別對照組觀察組N 30 30治療前2.76±0.40 2.80±0.52
3 討論
本研究發現,滋腎降糖丸聯合西藥治療氣陰兩虛證糖尿病腎病(DKD)G3aA2期患者,具有較好療效,可有效改善患者的中醫證候,降低患者的血壓;其次,可有效降低Scr水平,提高eGFR水平,從而改善患者的腎功能,還可有效降低患者的UACR水平以減少尿蛋白;同時,可顯著降低患者的 FPG、2hPG、FINS、HbA1c、HOMA-IR 水平,改善患者的糖代謝,減輕患者的胰島素抵抗;此外,可有效降低TG、TC及LDL-c水平,改善患者的脂代謝,且其對上述指標的改善作用均明顯優于單純西藥治療的對照組。本研究同時還發現,滋腎降糖丸可明顯降低氣陰兩虛證DKD(G3aA2期)患者的血清Galectin-3水平。
DKD是糖尿病患者最常見的微血管并發癥之一,與其他腎臟疾病相比,它是導致腎功能衰竭的主要原因,約占終末期腎病患者的30%~47%,但其發生發展機制尚不清楚,可涉及血流動力學異常、多元醇通路的激活、晚期糖基化終末產物(AGEs)產生、脂代謝紊亂以及氧化應激等多種因素[2]。Galectin-3是廣泛表達的多功能半乳糖凝集素家族的一員,它可發揮多種功能,參與細胞—細胞和細胞外基質黏附、細胞生長分化、凋亡和血管生成[11],因此,Galectin-3作為廣譜生物反應調節劑,參與組織纖維化、腫瘤發生、免疫和炎癥反應[12]。Galectin-3在糖尿病及其并發癥中的研究也越來越多,研究表明腎功能正常的2型糖尿病患者血清Galectin-3水平較非糖尿病患者升高,并與脂聯素水平、胰島素敏感指數、葡萄糖清除率呈正相關,與FINS及HOMA-IR呈負相關[13,14]。Kikuchi等[4]的研究表明Galectin-3陽性細胞的浸潤可能在DKD的進展中發揮重要作用,因此,Galectin-3表達的程度可能是預后不良的一個預測因子。Song等[15]的研究表明,與健康對照組相比,T2DM和DKD患者血清Galectin-3水平升高,與Scr、β2微球蛋白、FPG、年齡、HbA1c、SBP以及eGFR有關,進一步的回歸分析顯示,血清Galectin-3水平升高與2型糖尿病腎病患者eGFR降低、UACR升高有獨立關系。Li等[16]的研究表明,Galectin-3是一種造血細胞分泌因子,可直接降低胰島素信號傳導和胰島素抵抗,同時促進脂肪組織炎癥,這表明抑制Galectin-3表達可能是一種改善胰島素敏感性和糖耐量的抗糖尿病治療途徑。最近的一項臨床研究[5]亦進一步證實,血清Galectin-3與DKD獨立相關,推測其可能是DKD的一個生物標志物。
中醫古籍中并無“糖尿病腎病”這一病名記載,隨著現代醫家對其研究的深入,目前其病名已統一為“消渴腎病”。對于其治療,多采用分期論治[17],2011年中華中醫藥學會編寫的糖尿病腎病中醫防治指南中對其病機、演變規律以及辨證論治均有描述,認為DKD早期以氣陰兩虛證為主,治以益氣養陰為主;中期以脾腎陽虛證為主,治以溫腎健脾;晚期以陰陽兩虛證為主,治以陰陽雙補[18]。滋腎降糖丸為本院自主研發的中藥復方制劑(批準文號:粵Z20070085),是用于治療糖尿病的有效臨床協定方。方中以黃芪、熟地黃益氣養陰、健脾滋腎共為君藥,臣以生地黃、黨參等益氣養陰,佐以淫羊藿、骨碎補、三七等滋腎活血,共奏益氣養陰、健脾滋腎之功效。而本試驗納入研究的病例均為氣陰兩虛證DKD(G3aA2期)患者,符合DKD早期的辨證及治法。本研究結果亦證實,滋腎降糖丸可降低氣陰兩虛證DKD(G3aA2期)患者的中醫證候積分,同時有降壓、改善腎功能、降低尿蛋白、改善糖代謝、減輕胰島素抵抗以及改善脂代謝等作用,此外,還可明顯降低血清Galectin-3水平。
綜上,本研究結果表明,滋腎降糖丸聯合西醫常規治療氣陰兩虛證DKD(G3aA2期)患者,具有較好療效,可有效改善中醫證候,降低血壓,改善腎功能,降低尿蛋白,改善糖脂代謝和胰島素抵抗,降低血清Galectin-3水平,其療效優于單純西藥治療的對照組。對于其機制,我們推測其可能是通過改善胰島素抵抗來降低血清Galectin-3水平。但由于本次研究樣本量較小、機制研究不深入,故仍需要大規模的隨機對照試驗的臨床研究加以證實,并進一步開展動物實驗研究以探討其作用機制。

