優先離斷直腸在低位直腸癌中的應用研究
張慧嫦 李君久 熊秋華 黎東偉
廣東省東莞東華醫院普外科,廣東東莞 523110
在臨床中結腸癌是常見且多發的一種疾病,屬于惡性腫瘤的范圍[1],大部分直腸癌患者屬于中低位直腸癌[2]。輔助化療等治療手段雖然提高了保肛的幾率,但是治療直腸癌仍以手術為主[3]。低位直腸癌主要是指位于肛管直腸環至腹膜反折平面,距離肛緣7 ~8cm 下,屬于惡性腫瘤的范圍,伴隨著人們生活水平的提升,人們對術后生活質量也有了更高的要求,因此低位直腸癌保肛手術逐漸在臨床興起,且被認可[4]。手術一般先進行腹部手術再進行會陰部手術。病變直腸優先處理具有極大的優勢。現回顧性分析2015 年1月~2016 年11 月接受腹腔鏡腹會陰聯合直腸癌根治術32 例患者的臨床資料,根據病變直腸的先后處理分為改良手術組和對照手術組,現報道如下。
1 資料與方法
1.1 一般資料
選擇2013 年1 月~2016 年11 月同一手術主刀醫生的腹腔鏡腹會陰聯合切除術的低位直腸癌患者32 例。根據對病變直腸處理的先后順序分給對照組和改良組。其中對照組16 例,改良組16例。對照組男10 例、女6 例;年齡39 ~65 歲,平均(52.7±7.1)歲。改良組男11 例、女5 例。年齡37 ~67 歲,平均(52.6±8.7)歲。兩組患者一般資料比較,差異均無統計學意義(P >0.05)。具有可比性。
1.2 手術方式
術前準備同常規腹腔鏡直腸癌手術,麻醉采用氣管插管全麻。
1.2.1 改良組 在麻醉藥物起效后采取俯臥折刀位,常規消毒鋪巾,暴露出會陰,肛門閉鎖時采用7號絲線。將肛門作為中線,切口在尾骨尖直至會陰中點部且兩側至坐骨結節內側緣側,切口形狀為梭形。將肛周附近的脂肪組織去除掉,在沒有受到腫瘤侵犯時不需要將尾骨去除,將兩側肛提肌切斷,自盆筋膜臟層至Denonvilliers 筋膜層銳性剝離全直腸系膜,在直視的狀態下將兩側韌帶切除,剝離至直腸腹膜返折下方(男性以精囊腺上方、女性以陰道后穹窿上方為界),見圖1。經會陰將直腸拖出,直線切割閉合器于腹膜返折下方切斷、閉合腸管,病變直腸離體,見圖2。在沒有出血時采用碘伏與蒸餾水對創面進行清洗,清創完成后放置骶前引流管自會陰部引出并固定。縫合切口,見圖3。患者采取仰臥位并將雙腿分開,對鋪巾進行消毒,在臍上部位將穿刺鞘置入其中,然后建立氣腹,將氣腹壓力維持在12mm Hg 氣腹。利用腹腔鏡進行探查。在腹腔鏡下將三個穿刺鞘置入,同時將抓鉗和各種操作器械置入。左側腹壁穿刺孔位置作為術前選取的造瘺口位置。對乙狀結腸系膜進行游離,離斷腸系膜下動脈根部后對其外側離斷腸系膜下靜脈,同時在下方對輸尿管與生殖血管進行游離,從而進入Toldt 間隙。將乙狀結腸、直腸,與會陰組會師進行游離,見圖4,將腸管殘端提出骨盆后利用蒸餾水對盆腔進行徹底的沖洗,見圖5,在盆底沒有活動性出血的癥狀之后,對盆底腹膜進行縫合,縫合時采用3-0 可吸收線。在左下腹穿刺孔部位做切口,切口的大小約3cm,在逐層進入腹膜之前,先在腹壁部位作一條隧道進入腹腔中,將直腸斷端提出,在確定造口外露腸管長度后利用3-0 可吸收線間斷縫合腹膜及乙狀結腸漿肌層,逐層將乙狀結腸間斷縫合固定于腹直肌前鞘、皮下組織、皮膚,一期開放造口。
1.2.2 對照組 麻醉成功后患者取仰臥截石位,對鋪巾進行消毒后在臍上部位將穿刺鞘(10mm)置入其中,同時建立氣腹,將氣腹壓力維持在12mmHg。將腹腔鏡進行探查。利用腹腔鏡將三個穿刺鞘置入,然后將抓鉗與各操作器械置入。在下腹穿刺鞘的部位作為術前選好的造瘺口。將乙狀結腸系膜提起,然后利用超聲刀離斷腸系膜下動脈根部,然后在其外側對腸系膜下靜脈進行離斷,同時對輸尿管及生殖血管進行游離,然后進入Toldt 間隙。對乙狀結腸、直腸至肛提肌平面進行游離。常規消毒陰部,縫合肛門閉鎖,使用的是7 號絲線,將肛門作為中心,切口位于尾骨尖直至會陰中點部且兩側至坐骨結節內側緣部位,切口的形狀為梭形。清除肛周脂肪組織,在沒有腫瘤侵犯不必去除尾骨,切斷兩側肛提肌,自盆筋膜臟層至Denonvilliers 筋膜層銳性剝離全直腸系膜,與腹腔組會師。用保護套套扎遠端腸管及腫瘤后回納腹腔內。蒸餾水沖洗盆腔及會陰部,確定無活動性出血后,放置骶前引流管從會陰部引出、固定,用3-0 可吸收線連續縫合盆底腹膜。逐層關閉會陰部切口。與改良組手術同法開放一期造口。
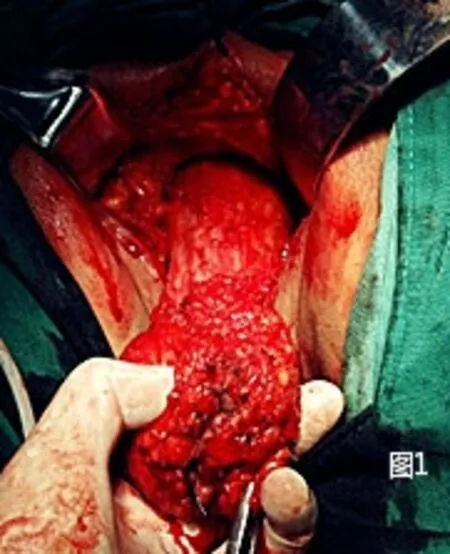
圖1 折刀位下游離直腸下段和肛管
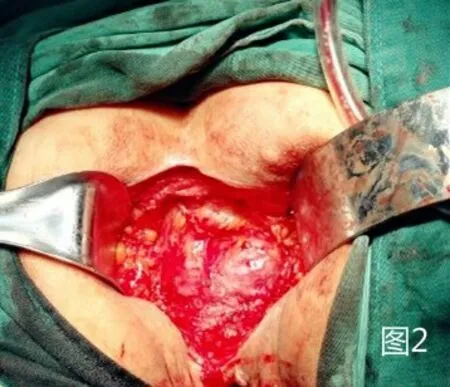
圖2 于腹膜返折下方離斷直腸
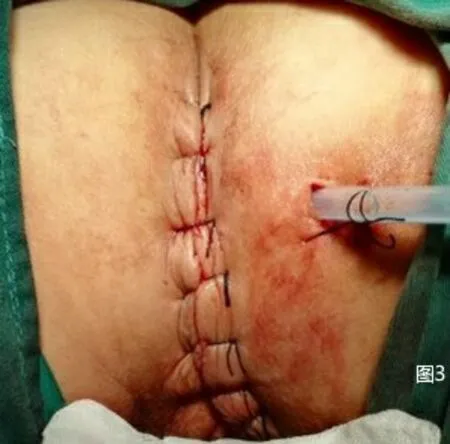
圖3 放置骶前引流管和縫合會陰部
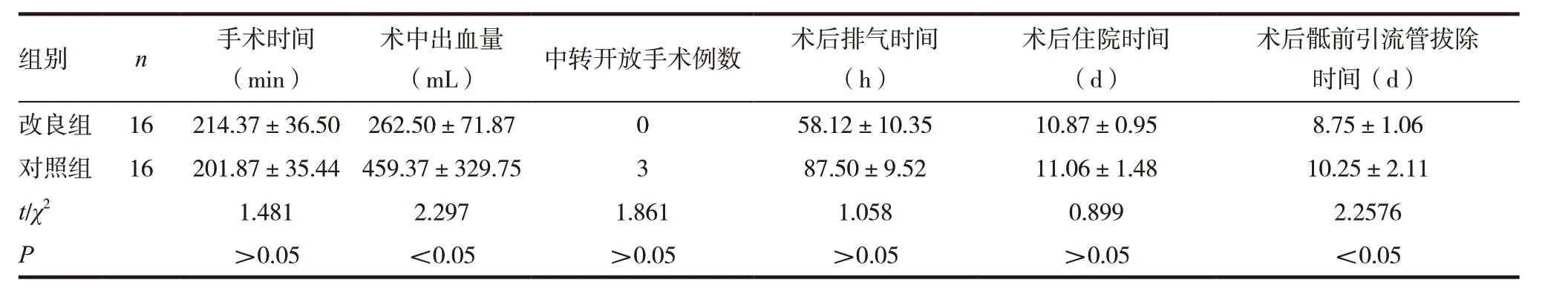
表1 兩組患者術中、術后情況分析比較

表2 改良組與對照組術后并發癥分析比較
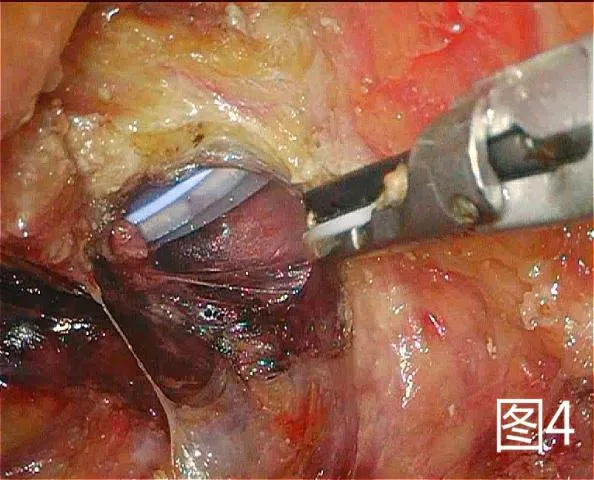
圖4 游離直腸與會陰組會師

圖5 檢查盆底情況
1.3 觀察指標
比較分析兩組患者手術時間、出血量、中轉開腹手術率、排氣時間、術后住院時間、會陰部切口感染、局部復發率的差異。
1.4 統計學處理
所有數據經SPSS19.0 統計軟件進行研究,計量資料以()表示,采用t 檢驗,計數資料以百分數表示,采用χ2檢驗,P <0.05 為差異有統計學意義。
2 結果
2.1 兩組患者術中、術后情況比較
兩組患者手術時間內、中轉開放手術例數、術后排氣時間、術后住院時間比較,差異無統計學意義(P >0.05);改良組患者術中出血量與術后骶前引流管拔除時間具比對照組患者少,差異有統計學意義(P <0.05)。見表1。
2.2 兩組患者術后并發癥比較
兩組患者勃起功能障礙、局部復發發生例數比較,差異無統計學意義(P >0.05);改良組患者尿潴留、會陰部切口感染發生例數低于對照組患者,差異有統計學意義(P <0.05)。見表2。
2.3 兩組患者隨訪結果比較
術后隨訪6 個月~5 年,未出現失訪的現象,且無死亡病例。
3 討論
腹會陰聯合直腸癌根治術具有創傷大的特點,因此術后極易發生性功能障礙與排尿功能障礙,另外永久性的傷口更是威脅著患者的生活質量,可造成精神心理負擔[5]。目前腹部手術組方式已逐漸規范[6],然而在會陰手術組中仍有一些問題,如暴露困難等,在進行手術的過程中極易出現直腸穿孔、出血、切口感染等并發癥,不利于術后的康復[7]。因此,如何促進術后恢復、減少術中出血和術后并發癥具有重要意義。既往腹腔鏡直腸癌根治術多采取先游離乙狀結腸和直腸。此方法對于中高位直腸癌等情況是安全可行的,但對于進展期低位直腸癌,常由于腫瘤可能侵犯臨近臟器而導致游離困難或骶前難以控制的出血而需中轉開腹。此報道改良了手術步驟及方式,主要特點為:(1)手術順序不同:手術先行離斷直腸和移除腫瘤[8];(2)體位不同:折刀位行會陰部手術暴露良好;(3)切除范圍不同:改良組要求切除提肛肌[9-10]。
鮑楊等[11]提出折刀位下處理會陰組手術,可改善暴露不良的問題,減少術中出血和神經、鄰近器官損傷等并發癥。此報道先從會陰組直視下處理,減少手術的難度和縮短手術時間。本文研究組手術出血量明顯少于對照組,分析其原因主要是由于在折刀位下直視下游離直腸至精囊腺/陰道后穹隆上方,可減少損傷和出血。其次,術中先切斷、移除腫瘤及病變腸管,對腫瘤不會產生任何不良影響,因不需要進行反復的牽拉,更是防止了腫瘤出現轉移的現象。會陰組手術方式具有一定的污染性,需要對直腸至腹膜反折下方進行游離,所以不能與腹腔相通,在移除直腸后會陰部空間相對較大,止血更確切[12];縫合會陰部前大量碘伏水及蒸餾水沖洗,能減少腹腔感染機會;在腹膜返折下方切除下段直腸,亦可減少術中把直腸拖拽進入腹腔后導致腹腔感染的因素[13];在對會陰進行關閉之前將直腸切斷,使操作變得更簡單,縫合的也比較徹底,降低了發生不良反應,故會陰部感染率低[14]。研究中兩組患者勃起功能障礙、局部復發發生例數比較無明顯差異,但是改良組患者尿潴留、會陰部切口感染發生例數低于對照組患者,便進一步證實了改良后手術方式是明顯優于會陰組手術方式,減少了污染性,降低尿潴留、會陰部切口感染發生率。再者,使用病變直腸優先處理的方法可以減少中轉開放手術,因折刀位下游離直腸后壁可減少骶前靜脈叢的損傷所致不可控制的出血。雖然報道中改良組和對照組的手術時間無明顯差異,主要考慮為反復改變體位所致,但整體操作時間是明顯縮短的。由研究證實,改良后的手術方式具有操作簡單、安全性高等優勢[15],更利于患者術后的康復,此外通過長達5 年的隨訪證實,未出現死亡的案例,說明治療效果的質量有很大的保障。
綜上所述,優先離斷直腸在腹腔鏡腹會陰聯合直腸癌根治術中有明顯的優勢,可降低手術難度、減少出血、減少術后骶前引流管留置時間和切口感染率。值得注意的是此次研究選取的例數有限,因此受到一定的限制,需要長期隨訪。

