不同溶氧濃度下非離子氨和亞硝酸鹽對中華絨螯蟹的急性毒性
王煜恒 ,李慶 ,陳軍 ,王會聰 ,張坤 ,桑曉軍
(1.江蘇農林職業技術學院畜牧獸醫學院,江蘇 鎮江 212400;2.宿遷東湖生態農業有限公司,江蘇 宿遷 223800)
目前,氨氮和亞硝酸鹽對水產動物的急性毒性研究已有研究。陳佳毅等[3]研究表明:氨氮和亞硝酸氮對不同發育階段羅氏沼蝦Macrobrachium rosenbergii幼體均有毒性,育苗生產過程應控制育苗水體非離子氨和亞硝酸氮濃度分別不高于0.10mg/L和1.00mg/L。樊海平等[4]發現,大刺鰍Mastacembelue armatus幼魚總氨氮、非離子氨和亞硝酸鹽的安全濃度分別為7.61mg/L、0.46mg/L和0.0798mg/L。李波等[5]研究認為,氨氮和亞硝酸鹽對黃顙魚Pelteobagrus fulvidraco的半致死濃度和安全濃度隨水中溶解氧含量的升高而增大,水體增氧能提高黃顙魚對氨氮和亞硝酸鹽的耐受能力。江敏等[6]和洪美玲[7]分別研究了氨氮和亞硝酸鹽對河蟹溞狀幼體和河蟹幼體半致死濃度和安全濃度,但是不同的溶氧濃度下上兩種物質對河蟹毒性影響的研究還未見報道。
本文通過研究不同溶氧濃度下非離子氨和亞硝酸鹽對河蟹的急性毒性,以了解河蟹在兩種溶氧情況下對非離子氨和亞硝酸鹽的耐受能力,并為河蟹養殖水質管理及病害防治提供參考。
1 材料與方法
1.1 材料
試驗蟹來自宿遷東湖生態農業有限公司河蟹養殖場,選取健康活潑、規格一致的優質個體,甲寬(5.52±0.35)cm,甲長(3.55±0.12)cm,體質量(10.06±1.23)g,暫養7 d。試驗用水為曝氣2d的自來水,水溫為(21±1)℃,pH 為(7.8±0.2),溶解氧含量(DO)為6.0~7.0 mg/L,氨氮濃度低于0.02 mg/L,亞硝酸鹽濃度低于0.01 mg/L。
試驗毒物為NaNO2和NH4Cl(分析純),烘干至恒重后,分別精確配制成10g/L的母液,試驗時按比例稀釋至試驗所需濃度。水體中氨氮含量采用納氏試劑分光光度法測定,亞硝酸鹽氮含量采用(N-1-萘基)乙二胺光度法,利用UV2100紫外分光光度計(上海/尤尼柯)測定。
1.2 方法
預試驗確定了氨氮(非離子氨)和亞硝酸鹽在正常溶氧量和過飽和溶氧下24h 100%死亡(24 h LC100)及 96h 0%死亡的質量濃度(96hLC0),在 24 h LC100及96hLC0之間按等對數間距設置6個濃度梯度,每個濃度設置3個平行,并設對照,具體濃度見表1。
過飽和溶氧條件下的毒性試驗采用96h半靜水法[8]。在50cm×30cm×23cm的塑料箱(試驗水體為30L)中放入河蟹10只(養殖密度為3.33g/L),加入配置的母液至試驗濃度,然后向水中充氧至水中溶解氧濃度為10~12 mg/L。用溶氧檢測儀(美國YSI DO200)監測水中溶解氧的濃度,當氧氣的濃度低于10mg/L時就向水體中充氧,以維持溶解氧的濃度。每24h全部換水一次,用水為含有與各個試驗梯度相同濃度(溶氧、亞硝酸鹽、氨氮)的水。試驗中不投餌。
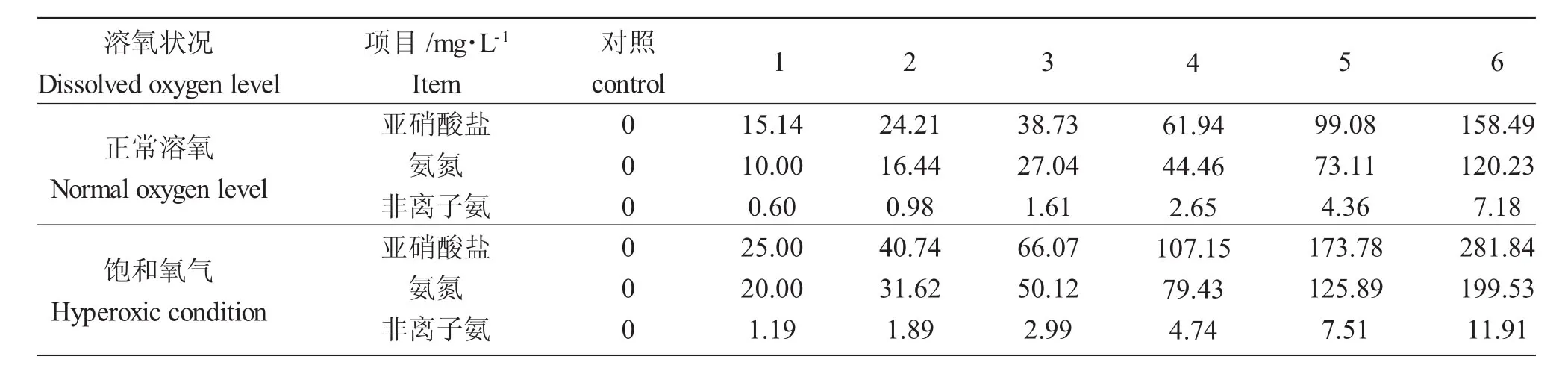
表1 試驗中各組的氨氮和亞硝酸鹽濃度Tab.1 The various concentrations of ammonia nitrogen and nitrite in the experiment
同時進行正常氧條件下的毒性試驗,水體中溶解氧濃度維持在6.0~7.0mg/L,除了不向水體充氧外(當氧氣的濃度低于5mg/L時向水體中充空氣),其他試驗步驟與過飽和溶氧條件下的毒性試驗相同。
試驗中檢查、記錄各個試驗組河蟹的死亡情況,觸動5s,河蟹無任何生理反應即視為死亡。
移民工程相關數據采集需要將經過評估后的移民基礎開發數據導入程序和數據錄入編輯工具,進行有效數據集中。首先將基礎評估數據通過Excel文件直接存入數據庫,根據收集到的實物指標和調查階段數據,進行數據集中收錄。為了減少數據錄入工作量,提高工作效率,整個數據導入以Excel文件格式形式保證文件數據和數據庫列表數據完全一致。通過Excel軟件內部的COM組件,根據相應操作規則,對數據格式源文件進行文件域名檢測,完全合格后,即可進行數據導入,其整體流程如圖3。
1.3 數據處理與統計
采用SPSS18.0 Litchfied-Wilcoxon法(非參數檢驗法)計算不同溶氧濃度下氨氮(非離子氨)、亞硝酸鹽對河蟹 24h、48h、72h、96h 的半致死濃度(LC50)和安全濃度(SC),按下式計算安全濃度:SC=0.1×96hLC50[8]
氨氮濃度為水體中的總氨氮濃度,采用《淡水水質標準》(GB3097-1997)規定的換算公式求得,由離子氨和非離子氨兩部分組成,非離子氨的含量計算公式如下[9]。

其中,pKa=0.09018+2729.92/T(T為開氏溫度,T=273+t℃)
2 結果與分析
2.1 中毒癥狀
試驗結果表明:氨氮和亞硝酸鹽對河蟹均有毒性,中毒癥狀類似。在最高濃度的氨氮和亞硝酸鹽組中,從0.6h至lh開始呈現中毒征兆:河蟹最后一對步足拖著在水底來回爬動,其他步足頻繁觸碰盆壁,大約4h后,河蟹活動能力減弱,只有螯和步足輕微顫動,隨著時間的延長,逐漸靜止不動直至死去。較低濃度組的河蟹出現上述中毒癥狀的時間明顯推遲,濃度越低出現中毒癥狀的時間越晚。
2.2 非離子氨對河蟹的毒性
2.2.1 正常溶氧條件下NH3對河蟹的毒性
進入正常溶氧條件下低濃度非離子氨組(低于1.61mg/L)的河蟹吐水頻繁,活動明顯,1.5h后活動能力減弱,只有步足輕微抖動,頻繁碰觸盆壁,3h后身體蜷縮,待在水底不動。3.5h后開始死亡,隨時間的推移,24h后的死亡率為25%;高濃度NH3組(高于2.65mg/L)中毒癥狀同上,1h后開始死亡,24h的死亡率接近40%,96h后的死亡率在80%以上(表2)。正常氧條件下 NH3對河蟹的 24h、48h、72h 和96h LC50(95%可信限)分別為4.85mg/L(7.81~10.92 mg/L)、3.51mg/L(6.37~9.06mg/L)、2.74mg/L(5.37~7.95mg/L)和 2.00mg/L(3.96~7.30mg/L),安全濃度為 0.20mg/L(表 4)。

表2 正常溶氧條件下NH3對河蟹的毒性Tab.2 The acute toxicity of nonionic ammonia to Chinese mitten handed crab Eriocheir sinenisis at normal dissolved oxygen level
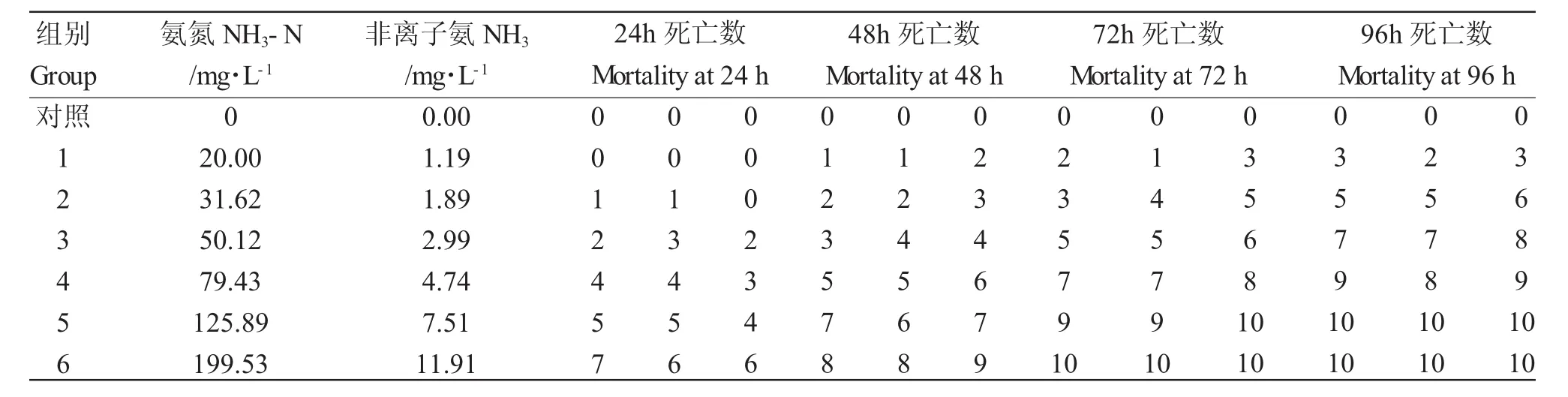
表3 過飽和溶氧濃度下NH3對河蟹的毒性Tab.3 The acute toxicity of nonionic ammonia to Chinese mitten handed crab Eriocheir sinenisis under hyperoxic conditions
2.2.2 過飽和溶氧條件下NH3對河蟹的毒性
在過飽和溶氧條件下低濃度NH3組(低于2.99mg/L)的河蟹0.5h后吐水頻繁,活動明顯,3h后活動力減弱,步足輕微顫動,頻繁觸碰盆壁,12h后身體蜷縮,待在水底不動。14h后開始出現死亡,隨著時間的推移,24h后的死亡率約為20%;高濃度NH3組(高于4.74mg/L)中毒癥狀同上,2h后開始死亡,30h死亡率達50%,96h后死亡率為95%左右(表3)。由表4可知,過飽和氧條件下NH3對河蟹的24h、48h、72h和96h LC50(95%可信限)分別為8.07mg/L(13.31~17.56mg/L)、5.69mg/L(11.10~15.11 mg/L)、3.80mg/L(7.60~12.17mg/L)和 3.15mg/L(6.22~11.91mg/L),可見,過飽和氧使NH3對河蟹的半致死濃度大幅度提高,NH3的安全濃度為0.32 mg/L,為正常氧含量條件下的1.6倍。
2.3 亞硝酸鹽對河蟹的毒性
2.3.1 正常溶氧條件下NO2-N對河蟹的毒性
在正常溶氧條件下,低濃度NO2-N組(低于38.73mg/L)的河蟹活動頻繁,2h后活動能力減弱,只有螯和步足輕微抖動,待在水底不動,6h后開始出現死亡,12h的死亡率為20%;高濃度亞NO2-N組(高于61.94mg/L)中毒癥狀同上,2h后開始出現死亡,40h后死亡率達到 50%,72h后死亡率為100%(表5)。正常溶氧條件下,NO2-N對河蟹的24h、48h、72h和96 hLC50(95%可信限)分別為109.39 mg/L(169.30~218.33mg/L)、75.77mg/L(125.30~181.64 mg/L)、59.90mg/L(105.41~157.19mg/L)和 52.69 mg/L(92.00~153.28mg/L),SC 為 5.27mg/L(表 7)。
2.3.2 過飽和溶氧條件下NO2-N對河蟹的毒性
過飽和溶氧條件下低濃度NO2-N組(低于66.07mg/L)的河蟹1.5h時活動頻繁,4h后活動能力減弱,僅螯和步足輕微的抖動,約8h后待在水底不動,12h后開始出現死亡,48h的死亡率為30%;高濃度NO2-N組(高于107.15mg/L)的河蟹0.5h開始出現上述中毒癥狀,3h后開始出現死亡,48h的死亡率為50%,96h后死亡率為90%(表6)。過飽和溶氧條件下,NO2-N對河蟹的24h、48h、72h和96h LC50(95%可信限)分別為182.41mg/L(295.21~403.57 mg/L)、131.92mg/L(234.16~293.98mg/L)、102.60mg/L(192.72~280.39mg/L) 和 80.61mg/L(143.92~267.51mg/L),較正常溶氧條件有大幅度提高。過飽和溶氧條件下,SC為8.06mg/L,為正常氧條件下的1.53倍(表7)。

表4 NH3對河蟹的半致死濃度(LC50)和安全濃度(SC)Tab.4 The LC50and SC values of non-ionic ammonia for Chinese mitten handed crab Eriocheir sinenisis

表5 正常溶氧條件下NO2-N對河蟹的毒性Tab.5 The acute toxicity of nitrite to Chinese mitten handed crab Eriocheir sinenisis at normal dissolved oxygen level
3 討論
3.1 NH3的毒性危害

多種甲殼動物的氨氮和NH3的LC50和SC已有報道,如紅螯螯蝦Cherax quadricarinatus[11]、克氏原螯蝦Procambarus clarki[14]以及河蟹幼體[15]。本試驗結果表明:在正常溶氧含量下NH3對河蟹24h、48h、72h和 96h的 LC50分別為 4.85mg/L、3.51mg/L、2.74 mg/L和2.00mg/L,SC為0.20mg/L。石俊艷等[15]研究結果顯示:NH3對河蟹大眼幼體在4個時間段的LC50分別為 8.2mg/L、5.67mg/L、2.87mg/L和1.85mg/L,SC為0.185mg/L。本結果與之接近但又略有差異,這可能與試驗動物的規格等有關。鐘君偉等[16]認為,水產動物規格越大,其氨氮耐受力越強。在過飽和氧條件下,NH3對河蟹 24h、48h、72h和 96h的 LC50分別為 8.07mg/L、5.69mg/L、3.80mg/L 和 3.15mg/L,SC為0.32mg/L,是正常溶氧條件下的1.6倍。Thurston等[17]研究結果表明,隨著溶解氧含量的降低,虹鱒Oncorhynchus mykiss呼吸頻率增加,進入魚體內氨量增大,毒性增強,證實了NH3的毒性與溶解氧濃度呈負相關。當水體中的溶解氧升高后,可以直接影響進入血液中非離子氨的量,增強血液的載氧能力和機體對NH3的代謝能力,降低了NH3的毒性作用[18]。水中溶氧增加后,可促進N的循環,加速將氨氮氧化成無毒的硝酸鹽。NH3所占的比例不僅與溶氧有關,也與水體溫度、pH及鹽度有關。因此,在其他條件相同的情況下,提高水體中的溶解氧濃度可大幅度提升河蟹對氨氮和NH3的耐受能力。

表6 過飽和溶氧條件下NO2-N對河蟹的毒性Tab.6 The acute toxicity of nitrite to Chinese mitten handed crab Eriocheir sinenisis under hyperoxic conditions

表7 NO2-N對河蟹的半致死濃度LC50和安全濃度SCTab.7 The LC50and SC values of nitrite for Chinese mitten handed crab Eriocheir sinenisis
3.2 亞硝酸鹽的毒性危害
亞硝酸鹽是養殖水體中另一種常見的含氮毒性污染物,是氨氮在細菌硝化作用過程或硝酸鹽在反硝化作用過程中產生[19]。NO2-N進入水生動物血液后,作為強氧化劑將血液中血紅蛋白分子的Fe2+氧化成Fe3+,使血紅蛋白失去載氧能力,造成有機體組織缺氧、代謝紊亂、神經麻痹甚至窒息死亡[20]。石俊艷等[15]研究顯示:亞硝酸鹽對河蟹3期和5期溞狀幼體(Z3、Z5)、大眼幼體的SC分別為0.993、1.754和2.086 mg/L。江敏等[6]研究表明:亞硝酸鹽對河蟹 3 期、4 期和 5 期溞狀幼體(Z3、Z4、Z5)的 SC分別為 0.713 mg/L、1.348 mg/L、2.173 mg/L。本試驗正常溶氧條件下,亞硝酸鹽對幼蟹的SC是5.27mg/L,這與以上結果相差較大。這可能與河蟹的規格有關,河蟹規格越大,耐受亞硝酸鹽的能力越強。本試驗在氧氣過飽和條件下亞硝酸鹽的SC是8.06 mg/L,較正常溶氧條件下高53%。亞硝酸鹽是氨轉化為硝酸鹽的中間產物,當水中溶解氧充足時,NO2-N在硝化細菌的作用下轉化成毒性較小的硝酸鹽,但在缺氧時反硝化菌可能會將其轉化成毒性更強的NH3-N[6]。水體中溶解氧濃度的升高可以降低進入血液的NO2-N含量,提高血液的載氧能力和魚體對NO2-N的代謝能力,降低了亞硝酸鹽對魚體的毒性[21]。
3.3 影響非離子氨和亞硝酸鹽毒性的因素
影響NH3和NO2-N對水生動物毒性的因素可分為生物因素(水生動物的種類、發育階段與規格及生理活動等)和非生物因素(棲息環境如水溫、鹽度、溶解氧含量和水質等)[7]。
NH3和NO2-N對不同種類水生動物的毒性相差巨大。本試驗結果表明:正常溶氧條件下,河蟹對NH3較NO2-N更為敏感,毒性更易受過飽和氧的影響,這可能與兩者對河蟹的致毒原理有關。養殖水體中高溶氧能有效抑制NH3和亞硝酸鹽的產生,使有毒的NH3-N和NO2-N轉化為無毒的硝酸鹽,高濃度的溶解氧可以提高河蟹對NH3-N和NO2-N的耐受力。因此,在河蟹養殖中,可通過換水、種植水草、安裝微孔增氧管和使用微生態制劑調水等方法增加養殖水體的溶解氧,來降低NH3和NO2-N對河蟹的毒性。
3.4 結論
正常溶氧條件下,非離子氨和亞硝酸鹽對河蟹幼蟹的SC分別為0.20 mg/L和5.27 mg/L,而氧氣過飽和條件下則分別為0.32mg/L和8.06mg/L。水體溶解氧濃度的升高可增強河蟹對非離子氨和亞硝酸鹽的耐受能力。因此,在河蟹養殖中提高水體的溶解氧,可降低非離子氨和亞硝酸鹽對河蟹的毒性效應,有利于河蟹的生長與健康。

