土三七致肝竇阻塞綜合征9例報道
李國梅,王巍,何池義
(皖南醫學院弋磯山醫院消化內科,安徽 蕪湖 241001)
肝竇阻塞綜合征(hepatic sinusoidal obstruction syndrome,HSOS),又稱為肝小靜脈閉塞綜合征,是由多種原因導致的肝血竇、肝小靜脈和小葉間靜脈內皮細胞損傷而形成微血栓,引起肝內淤血、肝細胞損傷和門靜脈高壓的一種疾病[1]。
HSOS病因復雜,國內常見于服用含吡咯烷生物堿(pyrrolidine alkaloids,PA)植物。本文回顧性分析了我院收治的9例土三七致HSOS的臨床資料,總結分析HSOS的臨床特點,從而提高其臨床診治的水平。
1 資料與方法
1.1 研究對象 收集2015年7月至2018年6月于皖南醫學院弋磯山醫院住院治療的土三七致HSOS的9例臨床資料(1例住院2次)。其中女6例,男3例,年齡43~73歲,平均年齡(62.56±0.24)歲。1例患者既往戊肝肝炎病史,8例患者既往無肝炎及肝硬化病史,其中1例有飲酒史,但無酒精性肝硬化的表現。
1.2 診斷標準 根據2017年南京標準[1],有明確服用含PA植物史,且符合以下3項或病理確診:(1)腹脹和(或肝區疼痛)、肝大及腹水;(2)血清總膽紅素升高或其他肝功能異常;(3)典型的腹部增強CT或MRI表現;病理典型表現為光鏡下可見肝腺泡Ⅲ區肝竇內皮腫脹、損傷、脫落,肝竇顯著擴張、充血。排除Budd-Chiari綜合征、心源性肝淤血、肝靜脈狹窄、病毒性肝硬化等原因導致肝損傷和門靜脈高血壓,與此同時排除結核、腫瘤、自身免疫性疾病等導致的腹水。
1.3 方法 收集本院患者發病前服用藥物情況,分析臨床表現、實驗室和影像學結果、診治經過及預后,實驗室檢查均取自入院后首次檢查結果。并查閱相關文獻,將土三七導致的HSOS病例資料進行總結分析。
1.4 診治療效評估 (1)治愈:肝功能恢復,腹水完全消退;(2)有效:癥狀減輕,肝功能好轉;(3)無效:肝功能指標無好轉或惡化,腹水無減少;甚至死亡。
2 結果
2.1 基本情況 9例患者均有服用土三七病史,服用時間為10~240 d,服藥劑量約10~20 g/d;服用方式有5例口服粉劑,1例飲酒史者為泡酒,3例口服含土三七成藥病史。用藥與起病時間間隔2~3個月。因活血化瘀者功效服用有5例,因保健養生服用有3例,因治療高血壓病服用有1例。9例患者中有4例患者有高血壓病史,其中3例合并腦梗死病史;1例糖尿病史,1例冠心病史。9例患者服用土三七后均出現不同程度的乏力、納差、腹脹等癥狀,腹水9例,腹脹9例,下肢水腫2例,腹痛2例,1例出現黃疸,1例出現肝性腦病。見表1。
2.2 實驗室檢查結果 丙氨酸氨基轉移酶(ALT)升高有6例,天冬氨酸氨基轉移酶(AST)升高有7例,ALT與AST同步升高有2例;4例總膽紅素(TBIL)明顯升高;所有患者均出現白蛋白降低;6例凝血酶原時間(PT延長,延長超過4 s者1例,延長超過2 s者1例);血小板數目減少者5例。所有患者丙型肝炎病毒指標、自身免疫性肝炎指標、甲胎蛋白均是陰性。所有患者均行腹腔穿刺引流,腹水檢查為漏出液。見表1。
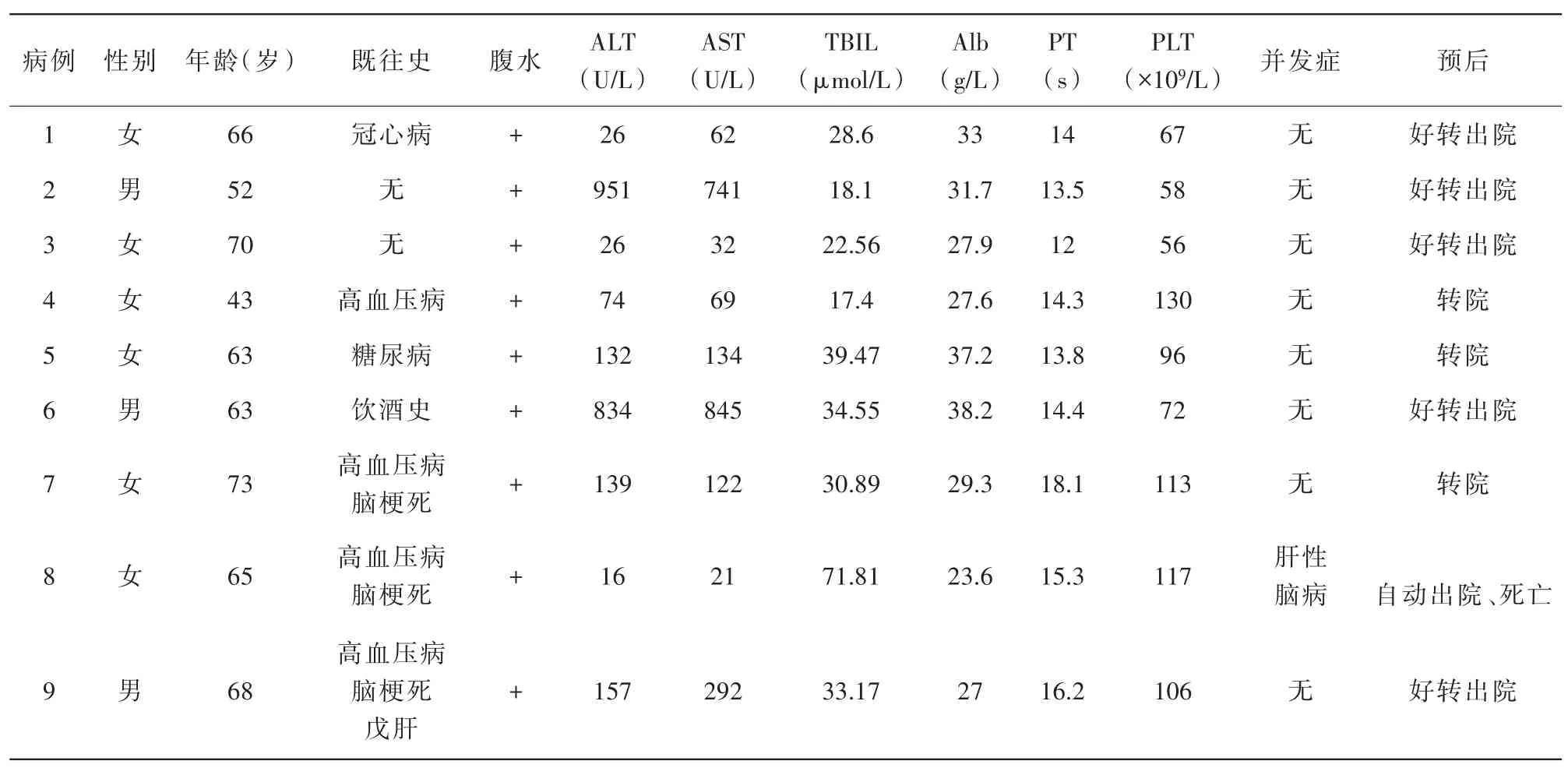
表1 9例HSOS患者的一般資料
2.3 影像學檢查及病理學檢查結果 8例患者行腹部CT檢查,腹部CT平掃檢查均出現肝臟體積增大,肝臟實質密度不均勻減低(圖1),增強后肝實質強化程度減低,延遲期呈“地圖樣”、“斑片狀”不均勻強化(圖2)。門靜脈期肝靜脈顯示不清者6例,2例肝靜脈明顯狹窄,下腔靜脈肝內段明顯狹窄者4例。中到大量腹水者8例,雙側胸水者3例。膽囊壁增厚,增強后可見環形強化者8例。5例行腹部B超檢查,其中1例提示下腔靜脈肝段狹窄,肝臟回聲改變。2例行門靜脈CTA檢查,其中1例提示下腔靜脈肝段較細,肝靜脈閉塞。
1例患者外院行肝臟病理穿刺,病理檢查:肝竇擴張充血、出血及小血湖形成,大片狀肝細胞退變壞死。肝細胞萎縮,肝板較薄,散在肝細胞內淤膽。

圖1 腹部CT平掃
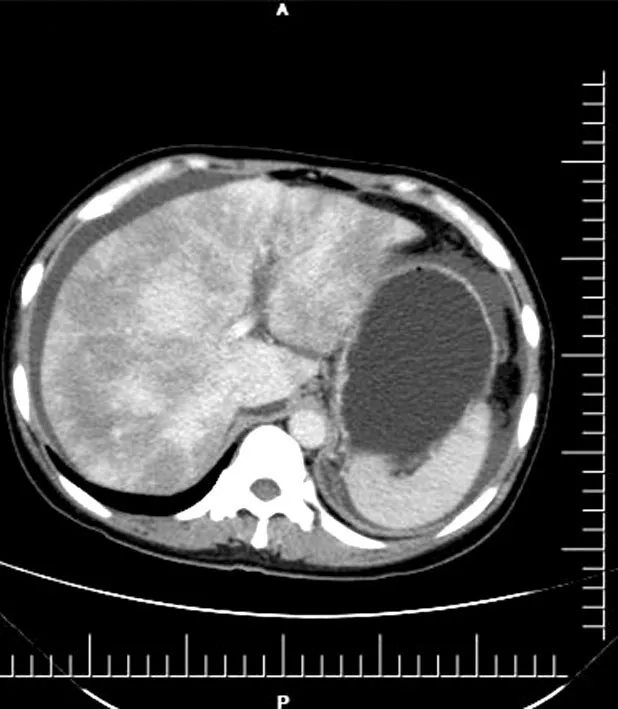
圖2 腹部增強CT
2.4 治療及預后 治療方案主要是停止服用土三七,護肝、限制液體攝入、利尿、補充白蛋白、腹水引流、退黃、改善微循環等處理。2例用低分子肝素抗凝,效果不佳。1例使用糖皮質激素治療,效果尚可,好轉出院。1例外院行經頸靜脈肝內門腔靜脈分流術(TIPS)治療出現肝性腦病予以降氨處理。5例好轉出院,3例轉入上級醫院,1例自動出院后死亡。
3 討論
土三七又稱為菊葉三七、景天三七,是一年多生的草本植物,因同樣具有止血、消腫等功效,常與五加科三七相混淆,而用于外傷、骨折的治療及被當做保健品養生,誤服后肝竇內皮損傷導致HSOS。此外HSOS在國外常見于以骨髓造血干細胞移植前預處理使用細胞毒性藥物和免疫抑制劑[2-3]。HSOS的臨床表現無特異性,主要表現為腹脹、肝區疼痛、乏力、納差、腹水、黃疸等表現[4]。土三七致HSOS的發病機制不明確,研究表明與所含吡咯烷生物堿有關。絕大多數吡咯烷生物堿本身及其水解物對于人體沒有毒性,但到達肝臟后在細胞色素P450酶的作用下生成脫氫吡咯烷生物堿,其具有肝臟毒性,從而導致肝竇內皮細胞損傷[5]。研究表明,HSOS的發病與肝竇內皮細胞谷胱甘肽耗竭有關[6]。肝腺泡Ⅲ區富含細胞色素P450酶,谷胱甘肽含量較低,因此吡咯烷生物堿易導致肝腺泡Ⅲ區損傷[2]。
HSOS診斷的金標準是肝臟病理組織學檢查,其典型表現為肝竇明顯淤血擴張、紅細胞滲出。多見于小葉中心區域(肝腺泡Ⅲ區),可連接成充血帶。肝小靜脈內皮腫脹,管壁硬化,不完全閉塞,肝細胞腫脹出現無菌性壞死,壞死區可有網狀纖維支架殘留[7]。大多數患者出現腹水、凝血功能障礙、血小板減少,依從性差,故臨床上行肝臟穿刺病理活檢者數量較少。國內研究表明,在土三七所致HSOS患者血清中可檢測到吡咯-蛋白共價結合物,有望成為診斷該病的血液檢查標志物[6]。
由于缺乏特異性血清學診斷指標及病理組織檢查,因此根據患者臨床特點、詳細用藥史、影像學資料進行診斷顯得至關重要。各種影像學方法可提高HSOS的診斷準確性,對于鑒別診斷(Budd-Chiari綜合征、肝硬化失代償期、急性重癥肝炎等)有重要臨床價值,可以監測疾病發展與轉歸。腹部超聲檢查無創、便捷、可重復檢查,可以清楚顯示臟器形態及血流動力學變化。典型表現可見:肝臟彌漫性腫大,肝區回聲密集分布不均,呈“斑片狀”改變;不同程度門靜脈高壓,肝靜脈變細、肝動脈阻力指數增高、側支循環形成;膽囊壁增厚;脾大;不同程度腹腔積液[8]。腹部增強CT及MRI可見典型的“地圖樣”、斑片狀不均勻強化。CT平掃可見彌漫性肝腫大,密度不均勻減低;增強期可見肝臟不均勻強化,呈斑片狀改變;門靜脈期可見“地圖狀”改變,肝靜脈周圍實質強化程度較高,呈“三葉草征”,肝靜脈顯示不清,下腔靜脈肝段受壓變細;延遲期肝內仍有斑片影存在,此外常合并腹水、胸水、膽囊壁水腫等征象[8-9]。特異性影像學表現有重要臨床診斷意義,但需要影像科醫生加強對HSOS的認識,避免誤診為不均勻脂肪肝、肝臟惡性腫瘤等。
HSOS目前無特效治療,主要是停止服用土三七,避免使用肝毒性藥物。對癥支持治療主要為護肝、退黃、改善肝臟微循環、限鈉利尿等處理。早期使用抗凝、活血具有一定的療效,臨床上常使用低分子肝素[10]。采用糖皮質激素治療尚有爭議,國內有研究表明激素可改善預后[11],國外報道應用大劑量激素進行沖擊治療有一定療效[12]。去纖苷是具有抗血栓、促進纖溶作用的單鏈寡核苷酸混合物,對HSOS有明確療效[13]。但由于國內尚未上市,對于土三七所致HSOS的治療缺乏經驗。內科治療效果不佳者,可考慮TIPS緩解難治性腹水和降低門靜脈高壓[14],但TIPS并不能改善預后[15]。最新研究表明,直接肝內門腔分流術聯合下腔靜脈支架置入術可有效緩解難治性腹水和復發性出血有顯著療效[16]。對于重癥患者合并肝功能衰竭,可選擇行肝移植[17]。
我國具有悠久的中草藥服用史,因此加強宣傳土三七的肝臟毒性,避免與三七等藥物混淆而誤服。我院收治9例患者均來自于農村中老年人群,積極開展科普宣教,以預防HSOS的發生。土三七致HSOS的臨床表現無特異性,應詳細詢問既往史及口服藥物情況。此外,增強CT及血管造影是目前的主要診斷方法,應需要影像科醫生了解病史。治療上仍以對癥支持治療為主,預后較差,臨床醫生應加強對土三七所致HSOS的認識。

