水溶液中四種脫氧核苷酸與水合鈾酰離子相互作用的理論計算
牟永曉 曹建平 陳媛媛 衛 濤 王朝杰
(溫州醫科大學藥學院,溫州 325035)
0 引 言
隨著核能事業的高速發展,人類對能源的需求量與日俱增,其中以鈾(U)為基礎的核能發電占比越來越大,隨之產生的核廢料也在不斷增加。核廢料具有成分復雜、化學毒性和放射性強以及半衰期長達數十萬年的特性,因此如何安全轉化和處置核廢料,同時如何防范核泄漏等問題一直備受關注。但是,目前對鈾生物毒性的化學機制認識遠不如放射性機制,而DNA是生命體系中儲存和傳遞遺傳信息最重要的分子,鈾酰離子(UO22+)是鈾在水體環境中最穩定的存在形式,且在六價錒酰陽離子中尤為突出,故對鈾酰離子與DNA片段相互作用的研究對理解鈾酰離子在生物環境中的遷移以及合成對鈾酰有較高絡合能力的功能核酸分子具有重要的意義。
至今針對鈾酰離子對DNA分子結構及正常生理功能影響的研究已廣為報道。研究顯示,鈾在生物體內的化學毒性遠大于其放射性毒性,低濃度下鈾酰離子可引起生物毒性并造成DNA和多肽結構的氧化損傷[1]。朱壽彭[2]等發現濃縮鈾(尤其是可溶性的UO2F2)可誘發精原細胞染色體斷片,并隨著攝入量的增加,染色體斷片發生率隨之增高,濃縮鈾還可誘發初級精母細胞染色體畸變和精子DNA鏈斷裂。Nielsen課題組[3]在420 nm可見光條件下,發現UO22+能催化單鏈DNA產生缺口,其機制是UO22+與脫氧核苷酸的磷酸基團結合進而破壞了DNA結構的完整性。除了鈾酰離子對DNA分子正常生理功能影響的研究,近年來功能核酸也廣泛應用于環境水體中鈾元素的檢測。李弘楊等[4]報道了基于鈾酰離子特異性脫氧核酶的熒光分光光度法檢測鈾酰離子。Tang[5]等利用二茂鐵修飾的脫氧核酶通過電化學檢測技術實現了對鈾酰離子的檢測。相比于實驗研究,國內外對鈾酰離子與DNA基本結構單元作用體系的理論計算研究仍然較少[6-7],兩者具體如何發生作用還待細究。
有關核酸分子結構單元的理論計算研究主要集中在其與主族和過渡金屬離子的相互作用[8-9]。Mohamadi[7]等首先對化學合成的[UO2(L)(DMSO)2](L為芳酰席夫堿)進行了表征,并結合分子對接方法對該化合物與鮭魚精子DNA的相互作用進行了研究,發現該化合物與DNA親和力強,有部分嵌入到了DNA雙鏈小溝中。Terron[10]等報道了金屬銀與5′-單磷酸胞苷配合物的X射線固態表征,同時采用M06-2X方法計算了銀與胞嘧啶的相互作用性質。李振彰[11]等應用B3LYP方法研究了鉻(Cr)金屬團簇與堿基相互作用體系,發現鉻團簇與堿基環上氮原子及氧原子結合形成的鉻-堿基復合物較為穩定。張淑琴[12]在B3LYP/6-311++G**(LANL2DZ)水平詳細探討了Cu2+與胞嘧啶(鳥嘌呤)核苷分子相互作用體系的空間構型及其穩定性,研究表明Cu2+易于與胞苷分子以共價作用形成配位鍵,當形成四配位鍵且結構處于同一平面時較為穩定。
本文應用密度泛函理論方法M06-2X[13]結合不同的有效核勢(effective core potential,ECP),計算了系列由4種單磷酸脫氧核苷酸(deoxynucleotide monophosphate,dNMP)與鈾酰離子在水溶液中形成的配離子結構,探索其紅外振動光譜和電子結構性質,并考察4種dNMP與鈾酰離子的相互作用特征。
1 計算方法
采用明尼蘇達系列泛函中的M06-2X計算水合鈾酰離子與脫氧核苷酸分子的相互作用體系,該泛函對計算非共價結合配合物的相互作用能、熱化學能和異構化能等性質性能較佳[14-17],已有較多研究使用該泛函計算鈾酰離子配合物[18-21]。計算中對鈾原子分別采用Stuttgart RLC ECP的“大核勢”贗勢基組[22]和ECP60MWB-SEG價層基組[23],對其它原子(H、C、N、O 和 P)采用 6-31++G(d,p)基組。其中 RLC ECP 對鈾內層電子 1s~5s、2p~5p、3d~5d 和 4f共 78 個電子做凍芯處理,外層14個電子(5f36s26p66d17s2)做價電子處理,ECP60MWB-SEG則對鈾內層60個電子做凍芯處理,外層的32個電子(5s25p65d105f36s26p66d17s2)為價層電子。應用Gaussian16[24]程序對水合鈾酰脫氧核苷酸配離子體系[UO2(dNMP)(H2O)3]2+進行結構優化和振動頻率計算,解析頻率結果顯示無任何虛頻,表明計算所得構型穩定。應用Multiwfn3.6程序[25]對配離子U-dNMP和U-OH2鍵臨界點進行QTAIM[26](quantum theory of atoms in molecules)拓撲分析,并通過原子電荷和分子軌道成分分析探討了在配位前后各片段的電荷轉移以及配離子的軌道組成和能級分布情況,根據Lu等[27]研究結果,使用6-31G(d,p)結合小核勢基組進行波函數計算分析。采用極化連續介質模型(polarized continuum model,PCM)[28]模擬水溶液對結構的溶劑效應。
2 結果與討論
2.1 水合鈾酰脫氧核苷酸配離子的結構性質
根據堿基的不同,有脫氧腺苷酸(dAMP)、脫氧胸苷酸(dTMP)、脫氧鳥苷酸(dGMP)和脫氧胞苷酸(dCMP)共4種脫氧核苷酸。自然界游離脫氧核苷酸中,磷酸最常見是位于戊糖的C-5′上,故本文主要以 5′-脫氧核苷酸(5′-dNMP)配位進行分析,其化學結構式如圖1所示。鑒于脫氧核苷酸分子柔性較大,空間效應明顯,首先用GaussView 6.0[29]程序中GMMX分子構象搜索模塊分別篩選出 4種5′-dNMP的最低能量構象,并在M06-2X/6-31++G(d,p)水平對水溶液中4種脫氧核苷酸的優勢構象進行優化和振動頻率計算,其結構繪于支持信息圖S1。從圖S1中發現磷酸基團P=O鍵均與堿基環上和戊糖相連的氮原子鄰位的C-H鍵中氫原子形成了P=O…H氫鍵,其鍵長范圍在0.218 6~0.227 6 nm,同時磷酸基團羥基與戊糖環氧原子(Os)形成了長約0.194 5~0.198 1 nm 的 O-H…Os鍵 (除了 5′-dGMP結構)。與其它3種脫氧核苷酸不同的是,5′-dGMP分子磷酸基團上P=O鍵和羥基分別與鳥嘌呤氨基氫(N11-H鍵)和N3原子作用形成了距離為0.190 1和0.166 6 nm的氫鍵。由于5′-dNMP中磷酸基團(H2PO4-)的p Ka值為7.20,在水溶液中幾乎不發生電離,主要以分子形態存在,故本文以中性的5′-dNMP進行計算。
在錒酰陽離子赤道平面配位的配體數量一般取決于配位鍵性質和配體的空間體積,以配體與鈾原子作用形成四齒至六齒配位的結構最為常見[30-34]。5′-dNMP結構中磷酸基團、戊糖環羥基和堿基3個部分均可與鈾酰離子配位形成多種不對稱性配離子,同時5′-dNMP分子的柔性和空間效應較強,因此本文對一分子脫氧核苷酸與三水合鈾酰離子配位的結構進行計算討論。采用M06-2X/6-31++G**(RLC ECP)和 M06-2X/6-31++G**(ECP60MWB-SEG)兩 種水平計算配離子結構[UO2(dNMP)(H2O)3]2+,以M06-2X/6-31++G**(ECP60MWB-SEG)水平計算得到的吉布斯自由能由低到高的順序,依次編號為UdN-j(dN代表 4 種 5′-dNMP,分別記為 dA、dT、dG 和 dC,j=1~5)。共計算得到4種UdA穩定結構,5種UdT結構,4種UdG結構,4種UdC結構,2種水平計算得到的結構和能量數據如圖S2和表S1所示。下文的分析討論中括號內數值為M06-2X/6-31++G**(ECP60MWB-SEG)水平的計算結果。

圖1 四種單磷酸脫氧核苷酸(5′-dNMP)的結構示意圖Fig.1 Schematic structures of the four kinds of deoxynucleotide monophosphate(5′-dNMP)
脫氧核苷酸與三水合鈾酰離子的配位形式主要有4種情況:第一種是磷酸基團P=O鍵與鈾原子形成的單齒配位, 如結構 UdA-1、UdG-1、UdC-1和UdT-3,我們發現在所有配離子中以該配位類型作用形成的結構最為穩定(除了UdT體系)。第二種是堿基環上原子參與的配位,結構UdA-2是氮原子與鈾原子作用形成的單齒配位,其中2個水分子分別與磷酸基團的羥基和堿基環上的氨基發生了弱相互作用。UdT-1、UdT-2、UdG-2和UdC-2結構是羰基氧與鈾原子作用形成的單齒配位,發現羰基氧與鈾原子的作用距離比U-OH2配位鍵稍短。第三種是戊糖環C-3′位羥基氧(O3′)與鈾酰離子作用形成的單齒配位,如結構 UdA-3、UdT-4、UdG-3 和 UdC-3,羥基氧與鈾原子的作用距離比水分子與鈾原子的作用距離稍長。第四種是磷酸基團上2個羥基氧均與鈾酰離子作用形成的雙齒配位,如結構UdA-4、UdT-5、UdG-4和UdC-4,其配位鍵距離同樣比U-OH2配位鍵長。與其它3種體系不同的是,UdT體系最穩定構型是以堿基環上的O4原子與鈾酰離子配位(UdT-1),而磷酸基團P=O鍵作用結構(UdT-3)的吉布斯自由能比UdT-1結構高15.4(9.9)kJ·mol-1。2種計算水平得到的構型相對吉布斯自由能順序大致相同。為比較4種脫氧核苷酸與鈾酰離子配位行為的差異,下文對5′-dNMP中磷酸基團P=O鍵與中心鈾原子配位的配離子結構進行詳細討論。
優化得到的四水合鈾酰離子及UdN體系在水溶液中的結構如圖2所示(以M06-2X/6-31++G**(ECP60MWB-SEG)水平下優化構型為例),幾個關鍵的鍵長和鍵角參數列于表1中。計算得到四水合鈾酰離子U=O鍵和U-OH2配位鍵的平均鍵長分別為0.169 8(0.172 6)nm和0.251 6(0.243 2)nm,結構中水分子排列類似于“梯形”,與孫曉玲[35]采用M06-2X/6-311++G**(RLC ECP)水平計算得到的水溶液中UO2(H2O)42+構型一致,其U=O鍵和U-OH2配位鍵長分別為0.169 4和0.255 7 nm,與本文計算值相接近。 Cao[36]等采用 B3LYP/RLC ECP和 MP2/RLC ECP計算水平得到水溶液中四水合鈾酰離子U=O鍵長分別為0.174 0和0.177 4 nm,U-OH2鍵鍵長分別為0.239 7和0.238 2 nm,與本文在大核勢下的計算結果相差較大,可能是由于密度泛函方法選取不同。在ECP60MWB-SEG基組水平下的計算結果與通過X光吸收精細結構譜(EXAFS)實驗方法[37]測得的U=O鍵0.176 0 nm、U-OH2鍵0.241 0 nm符合較好,表明應用小核勢基組計算鈾酰離子脫氧核苷酸體系是較為合適的。

圖2 在M06-2X/6-31++G**(ECP60MWB-SEG)水平水合鈾酰脫氧核苷酸配離子在水溶液中的結構Fig.2 Structures of hydrated deoxynucleotides coordination uranyl ions in aqueous phase obtained from the M06-2X/6-31++G**(ECP60MWB-SEG)level
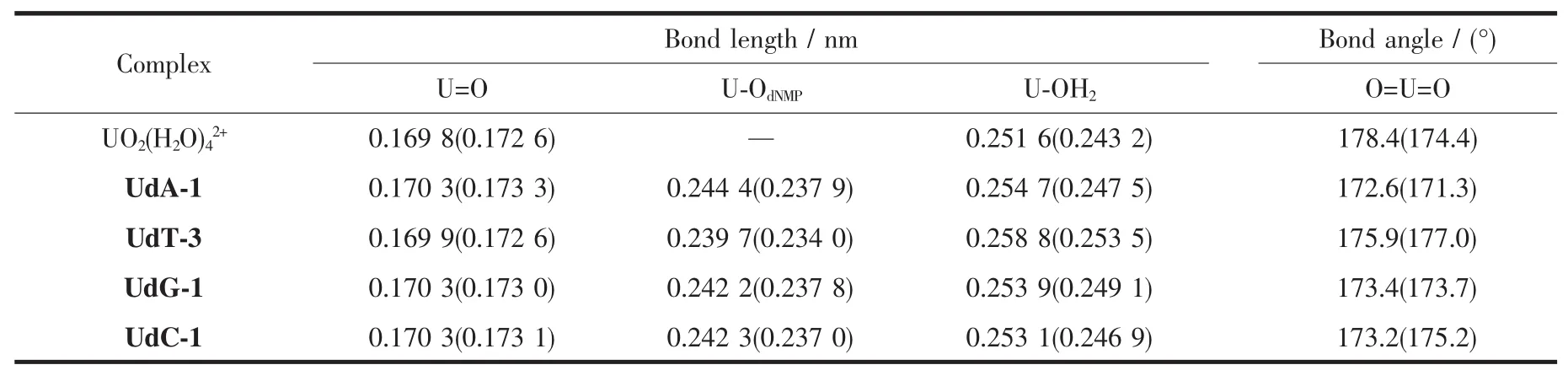
表1 水合鈾酰脫氧核苷酸配離子在兩種水平上的結構參數,括號中為M06-2X/6-31++G**(ECP60MWB-SEG)方法的計算結果Table 1 Equilibrium structure parameters of hydrated deoxynucleotides coordination uranyl ions at the M06-2X/6-31++G**(RLC ECP)and M06-2X/6-31++G**(ECP60MWB-SEG)levels,the results of the M06-2X/6-31++G**(ECP60MWB-SEG)are in parentheses
對采用ECP60MWB-SEG贗勢基組的計算結果進行比較,我們發現UdN體系中一水分子均傾向于與脫氧核苷酸配體發生協同作用。4種配離子的U=O鍵長值較接近,最大相差不超過0.000 7 nm,平均鍵長為0.173 0 nm,與UO2(H2O)42+的U=O鍵長相比有伸長趨勢。而U-OdNMP鍵鍵長有所不同,最大差值為0.003 9 nm,配離子U-OdNMP鍵長按照UdA-1(0.237 9 nm)>UdG-1(0.237 8 nm)>UdC-1(0.237 0 nm)>UdT-3(0.234 0 nm)的順序遞減。 文獻[38]采用B3LYP/6-31++G*(RSC ECP)方法計算水溶液中三水合鈾酰氨甲酰磷酰胺酸配合物體系[UO2(CPO)(H2O)3]2+,配合物結構中U-OP鍵長0.238 0 nm,與本文在小核勢基組水平得到的配離子結構U-OdNMP鍵鍵長相接近。優化得到U-OH2鍵長在0.246 9~0.253 5 nm范圍內,這一距離在已報道的水合鈾酰配合物UOH2距離范圍內[39-42],計算結果顯示UdT-3配離子的U-OH2鍵最長,UdC-1配離子的U-OH2鍵最短。4種配離子的O=U=O角度在171.3°~177.0°之間,近似為線形結構,以UdA-1配離子的O=U=O鍵角最小。對兩種基組水平的計算結果進行比較,ECP60MWB-SEG基組計算U=O鍵長比RLC ECP基組計算值長約0.002 8 nm,但配位鍵鍵長比RLC ECP基組計算值短,表明在ECP60MWB-SEG基組下配位鍵合更強,與辜家芳等[43]分別通過大核和小核有效贗勢基組計算環辛四烯與金屬鈾有機配合物的結果相一致。
2.2 水合鈾酰脫氧核苷酸配離子的能量分析
為了分析比較4種配離子穩定性及脫氧核苷酸與水合鈾酰離子的結合強度,并考察形成配離子前后脫氧核苷酸由于形變所產生的能量變化。我們分別計算了UdN體系的總結合能(ETotal),脫氧核苷酸的變形能(ED),計算公式如下:
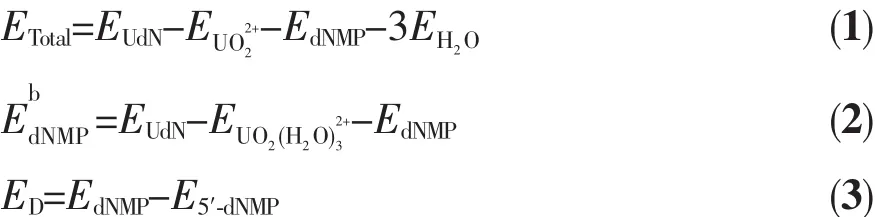

表2 水合鈾酰脫氧核苷酸配離子在兩種水平上的結合能和變形能Table 2 Binding energies and deforming energies of hydrated deoxynucleotides coordination uranyl ions at the M06-2X/6-31++G**(RLC ECP)and M06-2X/6-31++G**(ECP60MWB-SEG)levels
除了總結合能,UdT-3結構的單結合能也較其它3種配離子的低,這是由于UdT-3結構中的一分子水與磷酸的羥基氧作用形成氫鍵,而另3種配離子中一分子水是與堿基環上氮原子和(或)戊糖環氧原子作用形成了氫鍵,前者形成的氫鍵強度相對較弱。對比2種贗勢基組的計算結果,ECP60MWBSEG基組計算的配離子單結合能數值均比RLC ECP基組的計算值大,與前文U-dNMP配位鍵鍵長計算結果相對應,同時2種計算水平得到的單結合能強弱順序是一致的,按照UdC-1>UdG-1>UdA-1>UdT-3的順序依次減弱。變形能數值最小是5′-dAMP,說明5′-dAMP在形成配離子后構型變化最小。比較不同配位類型的總結合能(表S1),結果表明,磷酸基團P=O參與配位時,配離子總結合能最大,而當磷酸基團上雙羥基氧進行配位時,總結合能最小。
2.3 水合鈾酰脫氧核苷酸配離子的振動光譜
UdN體系的紅外光譜模擬圖如圖3所示,圖中標注了 U=O 鍵對稱(νss)和反對稱(νas)伸縮振動頻率及P=O鍵的伸縮振動頻率。例如在ECP60MWBSEG贗勢基組下,UdA-1結構970和1 021 cm-1處吸收峰分別歸屬于U=O鍵的對稱和反對稱伸縮振動,1 223 cm-1處吸收峰歸屬于P=O鍵的伸縮振動。U=O鍵反對稱伸縮振動峰強度明顯高于對稱伸縮振動峰強度,與文獻[36]報道的結果一致。計算得到在ECP60MWB-SEG基組下四水合鈾酰離子U=O鍵對稱和反對稱振動頻率分別為1 004和1 050 cm-1,文獻[48-49]應用EXAFS方法測定五水合鈾酰離子U=O鍵對稱和反對稱振動頻率分別為869和965 cm-1,比本文計算值分別低了135和85 cm-1,其原因是理論方法的不同會對頻率計算造成系統性偏差,同時隨著鈾酰赤道面配體數的增加,U=O鍵伸縮振動頻率逐漸減弱[6]。

圖3 水合鈾酰脫氧核苷酸配離子在兩種水平上的紅外光譜圖Fig.3 Infrared spectra of hydrated deoxynucleotides coordination uranyl ions at the M06-2X/6-31++G**(RLC ECP)and M06-2X/6-31++G**(ECP60MWB-SEG)levels
與四水合鈾酰離子U=O鍵的伸縮振動頻率相比,UdN體系中U=O鍵伸縮振動頻率均發生紅移,以UdA-1配離子變化程度最大,對稱和反對稱伸縮振動頻率分別紅移了34和29 cm-1。4種配離子U=O鍵的對稱伸縮振動頻率按照UdA-1(970 cm-1)<UdC-1(980 cm-1)<UdG-1(982 cm-1)<UdT-3(991 cm-1)的順序遞增,表明對應U=O鍵變強,鍵長逐漸減小,與上文給出的鍵長結果相對應。文獻[50]表明U=O鍵的振動頻率紅移程度越大,則配合物穩定性越強,結合前文結合能分析,我們得到的結果與文獻結論一致。與自由狀態下5′-dNMP的振動頻率值(表S2)相比,形成配離子后P=O鍵的振動頻率均發生紅移,紅移范圍在20~61 cm-1間,表明P=O鍵強度減弱,其中UdA-1配離子的P=O鍵紅移程度最大,紅移最小的是UdC-1配離子。2種計算水平的結果表明,RLC ECP基組下計算得到的紅外振動頻率值稍大于ECP60MWB-SEG贗勢基組下的計算結果。
2.4 電子密度拓撲分析
為進一步分析配離子中U-OdNMP和U-OH2配位鍵性質和強度,我們對其進行QTAIM分析。根據QTAIM理論[26],2個相互作用原子之間會有一鍵臨界點(BCP),它是電子密度曲線上的鞍點,對應于電子對電子密度的最小值。當BCP處的電子密度ρ(r)大于0.2且拉普拉斯電子密度▽2ρ(r)小于0時,說明該配位鍵具有共價鍵性質(開殼層作用),反之當ρ(r)小于0.2且▽2ρ(r)大于0時,該配位鍵具有離子鍵性質(閉殼層作用)。表3為采用2種計算水平得到的U-OdNMP和U-OH2配位鍵在鍵臨界點處的電子密度和電子密度拉普拉斯值。以ECP60MWB-SEG贗勢基組計算結果為例,UdN體系中U-OdNMP鍵在BCP處的 ρ(r)和▽2ρ(r)分別在 0.061~0.066 和 0.258~0.288范圍內,U-OH2鍵在 BCP 處的 ρ(r)和▽2ρ(r)分別在0.045~0.053 和 0.177~0.208 范圍內,說明 U-OdNMP和U-OH2配位鍵具有離子鍵性質。U-OdNMP鍵臨界點參數值均比U-OH2鍵的參數值大,表明5′-dNMP與鈾原子的作用鍵強度大于水分子與鈾原子的作用鍵強度。與四水合鈾酰離子U-OH2鍵的臨界點參數值相比,形成配離子后U-OH2鍵各參數值均減小,表明U-OH2配位鍵有減弱趨勢。2種水平的計算結果的定量差異也較為明顯,在RLC ECP基組下計算的臨界點參數值偏小。
2.5 電荷轉移分析
為考察形成配離子后各片段的電荷轉移變化情況,我們將UdN體系分為3個片段(鈾酰離子、脫氧核苷酸和水分子)進行Mulliken電荷分析。在2種計算水平下鈾酰離子和配體所帶的Mulliken電荷于表4中列出。
自由狀態下鈾酰離子所帶電荷為2.000,具較強的吸電子能力,可吸引配體向其轉移電子。從表4中可以看出,在配位前后,鈾酰離子電荷減少的同時配體片段電荷有所增加。文獻[36]采用B3LYP/RLC ECP和MP2/RLC ECP水平計算得到水溶液中四水合鈾酰離子 UO22+的Mulliken電荷分別為 1.150和1.440,本文對應的計算值在上述2種水平范圍內。比較ECP60MWB-SEG贗勢基組計算結果,顯示UdA-1中鈾酰離子片段帶有最少的正電荷,UdC-1配離子次之,表明5′-dAMP和水分子向中心鈾酰離子轉移電子數最多,共為0.822,而鈾酰離子所帶電荷數最多的是UdT-3配離子,表明5′-dTMP和水分子向鈾酰離子片段轉移電子數最少,共為0.767,與前文配離子的總結合能結果相一致,說明配體與鈾酰離子之間轉移電子數越多,配離子結合強度越大。5′-dNMP失去的電子數比水分子片段失去的電子數多(0.138~0.235),表明 5′-dNMP 更容易轉移電子,形成的U-OdNMP配位鍵亦較強。比較2種水平的計算結果,RLC ECP基組下計算得到的配體間電子轉移數較多。

表4 水合鈾酰脫氧核苷酸配離子中各配體在兩種水平上的Mulliken電荷Table 4 Mulliken charges of each ligand in hydrated deoxynucleotides coordination uranyl ions at the M06-2X/6-31G**(RLC ECP)and M06-2X/6-31G**(ECP60MWB-SEG)levels
2.6 前線分子軌道分析
圖4為UdN體系的前線分子軌道能級圖,圖中Δε表示最高占據軌道和最低空軌道的能級差,表5為使用Mulliken方法計算得到體系原子對前線分子軌道的貢獻結果。下文中將最高占據軌道HOMO簡寫為H,最低空軌道LUMO簡寫為L。結合圖4和表5可知,4種配離子的高占據軌道H~H-1主要為堿基或戊糖環貢獻。對于H-1軌道,UdA-1中是堿基環上N1、N3和C5原子各自的2p軌道形成的離域π鍵,其中N1、N3和C5原子2p殼層的貢獻分別為28.6%、14.6%和12.3%。UdC-1配離子H-1軌道與UdA-1類似,同為堿基環上原子的貢獻。UdT-3和UdG-1配離子中戊糖環氧原子(Os)和C-3′位羥基氧(O3′)原子2p殼層對H-1軌道有主要貢獻,后者鳥嘌呤環上N9原子的2p殼層對此分子軌道也有少量貢獻。再如4種配離子的H軌道,主要對應堿基環上雙鍵碳原子2p殼層形成的π鍵,同時N或O原子的2p殼層也有不同程度的貢獻。4種配離子的L~L+5分子軌道基本屬于U(5f)軌道(圖S3),且配離子的軌道圖形類似 (除了UdT-3結構),L~L+1和 L+2~L+3 分別對應為 U(5f啄)和 U(5fφ)軌道,L+4~L+5軌道描述的是U(5fπ)與軸向氧原子的2p軌道作用成鍵, 而UdT-3結構中 L+1~L+3為 U(5fφ)軌道。有研究顯示[51-52],錒系酰基離子(AnO22+)鍵合作用中5f軌道成分愈多,錒酰離子軸則愈趨近于線形,而本文計算的UdA-1配離子O=U=O鍵角變化最大,可能與該結構中U(5f)軌道總貢獻量最少有關。UdG-1配離子HOMO-LUMO軌道能級差最小,為5.51 eV,UdC-1軌道能級差最大。
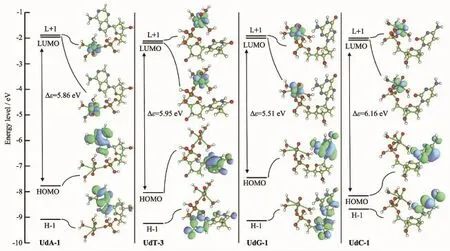
圖4 在M06-2X/6-31G**(ECP60MWB-SEG)水平上水合鈾酰脫氧核苷酸配離子的部分前線分子軌道能級圖,軌道等值面為0.04Fig.4 Partial frontier molecular orbitals energy level diagrams of hydrated deoxynucleotides coordination uranyl ions at the M06-2X/6-31G**(ECP60MWB-SEG)level,and the orbital isovalue is set to 0.04

表5 在M06-2X/6-31G**(ECP60MWB-SEG)計算水平水合鈾酰脫氧核苷酸配離子中前線分子軌道的組成Table 5 Contribution of hydrated deoxynucleotides coordination uranyl ions to frontier molecular orbitals at the M06-2X/6-31G**(ECP60MWB-SEG)level
3 結 論
運用密度泛函理論方法M06-2X在2種 相對論有效勢和 6-31++G(d,p)基組水平研究了[UO2dNMP(H2O)3]2+配合物。對幾何結構、振動光譜、結合能、電子密度拓撲參數、原子電荷轉移及軌道成分等方面進行了闡述,得到以下幾點結論:(1)應用小核勢基組可以更好地描述鈾酰離子脫氧核苷酸體系的結構特征。(2)脫氧核苷酸與三水合鈾酰離子存在4種穩定配位方式,以磷酸基團P=O鍵與中心鈾原子形成的單齒配位結構最穩定 (除了UdT體系)。(3)4種配離子U=O鍵長值相接近,但配位鍵距離有所不同。(4)能量分析表明,配離子的總結合能呈UdA-1>UdC-1>UdG-1>UdT-3 的趨勢,5′-dAMP 的變形能最小,ECP60MWB-SEG基組計算的結合能均比RLC ECP基組計算值大。(5)紅外振動光譜分析發現,配離子中U=O鍵和P=O鍵伸縮振動頻率均發生紅移,且以UdA-1配離子變化程度最大。(6)QTAIM分析表明U-dNMP配位鍵具有離子鍵性質,脫氧核苷酸與鈾原子的作用鍵強度大于水分子與鈾原子的作用鍵強度。(7)Mulliken電荷分析發現配體片段向鈾酰離子轉移了電子,且配體與鈾酰離子之間轉移電子數越多,形成的配離子結合強度越大。(8)分子軌道分析表明,高占據軌道貢獻主要來自脫氧核苷酸配體的π軌道,而低階空軌道基本為U的5f電子軌道,UdG-1配離子的HOMO-LUMO能級差最小。
鈾酰離子與脫氧核苷酸配合物的DFT計算研究結果將為我們進一步拓展其它酰離子與更復雜的生物大分子如核酸片段或多肽結構的作用體系奠定基礎。
Supporting information is available at http://www.wjhxxb.cn

