體外siRNA- Nav1.5干擾口腔鱗癌HSC- 3細胞生物學行為研究
戴永錚,錢成煒,徐小立,蔣 勇
口腔鱗狀細胞癌復發(fā)率高、生存周期短,手術治療的局限性造成治療效果差,因而新的治療方法對提高患者生存率具有重要意義。電壓門控鈉離子通道(voltage- gated sodium channel,VGSC)是一種跨膜糖蛋白,由一個α亞基和多個β亞基組成。根據(jù)α亞基的不同可將其分為9種,即Nav1.1- Nav1.9[1]。近年來一些研究發(fā)現(xiàn), Nav1.5在包括前列腺癌[2]、乳腺癌[3]、卵巢癌[4]、宮頸癌[5]和非小細胞肺癌[6]等多種腫瘤中高表達,對腫瘤的增殖、侵襲等生物學過程具有明顯的調節(jié)作用。在口腔鱗癌中,研究[7]顯示Nav1.5在癌組織中的表達相比正常組織明顯升高,但其在口腔鱗癌中的表達調控機制研究甚少。該研究通過檢測Nav1.5的表達水平變化以及在增殖和侵襲中具有重要作用的相關蛋白檢測,來分析其對口腔鱗癌細胞增殖和侵襲的作用,為口腔鱗癌的靶向治療尋求新的思路。
1 材料與方法
1.1 主要材料和儀器DMEM培養(yǎng)基購自美國Hyclone公司;胎牛血清購自以色列Biolnd公司;胰酶消化液、細胞增殖核抗原(proliferating cell nuclear antigen,PCNA)、 RIPA 裂解液、蛋白酶抑制劑、磷酸酶抑制劑、苯甲基磺酰氟(phenylmethanesulfonyl fluoride,PMSF)、蛋白濃度測定試劑盒購自上海碧云天生物技術有限公司;Nav1.5多克隆抗體購自美國Abcam公司;基質金屬蛋白酶2(matrix metalloproteinase 2,MMP- 2)、 MMP- 9多克隆抗體購自美國santa cruz公司;山羊抗鼠、抗兔IG抗體購自北京中杉金橋公司;CCK8試劑盒購自日本同仁公司;PCR引物購自上海生物工程股份有限公司;逆轉錄試劑盒、 實時熒光定量PCR(Real Time- PCR,RT- PCR)試劑盒購自日本Takara公司; PVDF 膜購自美國Invitrogen公司;Matrigel膠、Transwell小室購自美國Corning公司;siRNA- Nav1.5購自上海吉瑪公司;lipo2000、CO2恒溫孵箱購自美國Thermo Fisher公司;RT- PCR儀購自美國Stratagene公司;酶標儀購自美國Bio- tek公司。收集安徽醫(yī)科大學第一附屬醫(yī)院口腔頜面外科口腔鱗癌組織(2例)和正常口腔黏膜組織(牙齦2例),標本取下直接保存于-80 ℃?zhèn)溆谩?/p>
1.2 實驗方法
1.2.1組織免疫組化 4%甲醛固定組織6 h,石蠟包埋,4 μm厚切片,60 ℃烤片4 h,脫蠟至水,抗原修復,3% H2O2室溫孵育10 min,1 ∶200稀釋Nav1.5一抗4 ℃孵育過夜(16 h左右),HRP二抗37 ℃、 30 min,DAB顯色,蘇木精復染,封片,鏡下觀察。
1.2.2細胞培養(yǎng) HSC- 3細胞在含10% FBS、100 U/ml青霉素和100 U/ml鏈霉素DMEM培養(yǎng)基中,放入37 ℃、5% CO2培養(yǎng)箱培養(yǎng)。每3 d傳代一次。
1.2.3免疫熒光實驗 將細胞以5×105個/ml的密度接種于共聚焦小皿,孵箱過夜。4%多聚甲醛室溫下固定30 min,0.5% Trixton X- 100室溫下穿通20 min,1% BSA封閉細胞30 min, 加入Nav1.5的一抗(6 μg/ ml)冰箱孵育24 h,次日室溫孵育1 h。 加入羅丹明標記的二抗(1 ∶50)避光孵育2 h,DAPI(1 ∶2 000)避光孵育8 min。在Zeiss LSM510共聚焦成像系統(tǒng)下觀察細胞。
1.2.4siRNA轉染實驗 美國國立生物技術信息中心(national center for biotechnology information,NCBI)上查找Nav1.5的序列,根據(jù)目的基因序列設計合成3條Nav1.5的小干擾RNA(small interfering RNA,siRNA)組,以及一條陰性對照(negative control,NC)組,同時設置空白對照(control,CON)組,序列見表1。轉染前1 d,將2×105個/ml細胞接種于培養(yǎng)板中,每孔中加入約500 μl無抗生素的培養(yǎng)基。取1 μl/孔lipo2000,用50 μl opti- MEM無血清培養(yǎng)基稀釋,并室溫孵育5 min。取2 μl siRNA,以50 μl opti- MEM無血清培養(yǎng)基稀釋,混勻。2種液體輕輕混勻,室溫靜置20 min。加入含有細胞及培養(yǎng)液的孔中,混勻。轉染6 h后,換為含血清的完全培養(yǎng)基。見表1。
1.2.5RT- PCR檢測 按TRIzol試劑盒說明書提取各組細胞總RNA,使用PrimeScriptTM- PCR kit逆轉錄試劑盒逆轉錄成cDNA,然后以此為模板,用目標基因的引物進行擴增和檢測。反應條件:95 ℃、1 min,60 ℃、30 s,72 ℃、30 s。每個樣品設置3個復孔,PCR的所有引物均由上海生物工程公司進行設計合成,序列見表2。

表2 引物序列
1.2.6Western blot 檢測 用RIPA細胞裂解液提取各組細胞總蛋白。BCA試劑盒測定各組蛋白濃度,調整各組濃度一致后,99 ℃、10 min使蛋白變性,SDS- PAGE凝膠電泳,然后轉移至0.45 μm的PVDF膜上,5% BSA封閉,一抗、二抗孵育,經ECL曝光成像。
1.2.7Transwell實驗 Matrigel膠與DMEM培養(yǎng)基按1 ∶9混勻制成稀釋液。小室濾膜均勻涂抹50 μl稀釋液,37 ℃、5% CO2恒溫箱滯留2 h。取3組培養(yǎng)24 h細胞,0.25%胰酶消化,1 000 r/min離心5 min,棄上清液得下層細胞,DMEM重懸計數(shù),細胞密度調為1×106個/ml。上室加細胞懸液各100 μl,下室加600 μl 20% FBS的DMEM培養(yǎng)液,37 ℃、5% CO2恒溫箱孵育24 h,每組細胞設3個復孔。取出小室,吸出上室培養(yǎng)液,擦凈上室表面Matrigel膠,4%多聚甲醛固定20 min,結晶紫染色20 min,晾干,拍照,200倍顯微鏡下計算穿膜細胞數(shù)。
1.2.8CCK8檢測細胞增殖活性 待檢測細胞計數(shù),并鋪于96孔板。確定細胞貼壁后,繼續(xù)培養(yǎng)2~4 h使其貼壁緊密。96孔板每個孔加10 μl CCK8溶液,在培養(yǎng)箱孵育1 h,顯色反應后,酶標儀測定450 nm處吸光度值(optical density,OD),每組設5個復孔。根據(jù)OD450值繪制12 、24 、48 、72 h柱狀圖。

2 結果
2.1 組織和細胞中Nav1.5的表達臨床收集的正常口腔黏膜組織和口腔鱗癌組織做免疫組化,光鏡下觀察組織中Nav1.5蛋白表達情況,癌組織中于細胞的胞膜和胞質中出現(xiàn)不同程度的棕黃深染,即Nav1.5蛋白呈陽性表達,在正常口腔黏膜組織中幾乎看不到棕黃色,見圖1。HSC- 3細胞中免疫熒光染色激光共聚焦鏡下觀察,在胞質和胞膜上可見熒光標記的Nav1.5呈紅色,胞核呈藍色,Nav1.5在HSC- 3細胞中陽性表達,見圖2。

圖1 免疫組化法檢測Nav1.5蛋白的表達 ×100A:正常組織染色陰性;B:癌組織染色陽性

圖2 免疫熒光法檢測HSC- 3細胞中Nav1.5的表達 ×200
A:細胞核的染色呈藍色;B:Nav1.5蛋白的染色呈紅色; C:A和B的合成圖
2.2 HSC- 3細胞Nav1.5的沉默效率FAM標記的siRNA轉染HSC- 3細胞,鏡下觀察細胞,與明場視野下對比,轉染效率較高。RT- PCR和Western blot 結果顯示與CON組比較,S1、S2和S3組Nav1.5的mRNA表達均有所下調,S2和S3組下調較多,差異有統(tǒng)計學意義(P<0.01)。CON組和NC組之間差異無統(tǒng)計學意義,見圖3。因此以下實驗均采用S3轉染。
2.3 Nav1.5對HSC- 3細胞增殖和侵襲的影響CCK8檢測干擾后的細胞在450 nm處OD值,測量結果顯示,在轉染48 h后siRNA組(1.31±0.21)與CON組(1.06±0.22)和NC組(0.67±0.09)比較差異有統(tǒng)計學意義(F=9.006,P<0.01),CON組和NC組之間差異無統(tǒng)計學意義,見圖4。Transwell侵襲實驗結果表明,siRNA組(7.33±1.55)與CON組(55.0±3.00)和NC組(47.0±4.00)比較,穿過小室細胞數(shù)明顯減少,差異有統(tǒng)計學意義(F=222.7,P<0.001),CON組和NC之間差異無統(tǒng)計學意義,見圖5。

圖3 經siRNA轉染后Nav1.5沉默效率
A:轉染FAM標記siRNA明場視野下;B:同一視野下熒光觀察×200;C:轉染后各組Nav1.5 mRNA相對表達水平;與CON組比較:**P<0.01;D:轉然后各組Nav1.5蛋白表達水平;S1、S2和S3分別代表轉染不同序列siRNA- Nav1.5

圖4 經siRNA干擾后HSC- 3細胞OD450值比較
2.4 RT- PCR和Western blot檢測轉染siRNA- Nav1.5對相關蛋白表達的影響經siRNA- Nav1.5轉染后的HSC- 3細胞內PCNA、MMP- 2和MMP- 9基因水平表達和蛋白水平表達均有所下降,差異有統(tǒng)計學意義(F=15.12、22.89、11.72,P<0.05),見表3和圖6、7。
3 討論
口腔鱗狀細胞癌作為頜面部最常見的惡性腫瘤,常常發(fā)生區(qū)域淋巴結轉移,晚期可發(fā)生遠處轉移,嚴重威脅著人類的健康。為了克服傳統(tǒng)手術加放化療治療方法的弊端,分子靶向治療越來越重要。為了尋找更為有效的治療靶點,在本課題組的早期研究中,劉偉佳 等[7]發(fā)現(xiàn)在口腔鱗狀細胞癌中,Nav1.5的表達與正常組織相比顯著提高,本研究免疫組化結果也得到證實。此外,Nav1.5的表達與組織分化程度和淋巴結轉移有關,這提示著Nav1.5有望成為口腔鱗癌治療的新靶點。

圖5 經siRNA轉染后HSC- 3細胞侵襲性比較 ×200
A:CON組;B:NC組;C:siRNA組; 與CON組比較:***P<0.001;與NC組比較:###P<0.001
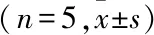
表3 轉染siRNA及空白組相關蛋白mRNA表達量
與CON組比較:*P<0.05,**P<0.01,***P<0.001; 與NC組比較:#P<0.05,##P<0.01
近年來,越來越多的研究[8-11]發(fā)現(xiàn)Nav1.5與癌癥密切相關,并表明Nav1.5在癌癥增殖轉移中發(fā)揮著重要作用。Mohammed et al[8]研究顯示Nav1.5在高侵襲性乳腺癌細胞的胞質和核周區(qū)域以及板狀偽足中表達。本研究免疫熒光共焦顯微鏡的結果顯示HSC- 3細胞中也有著相同分布。為探討Nav1.5對HSC- 3細胞增殖和侵襲能力的影響,本研究對HSC- 3細胞進行siRNA- Nav1.5干擾實驗,RT- PCR和Western blot檢測干擾后HSC- 3細胞中Nav1.5出現(xiàn)明顯下調后再分別進行Transwell侵襲實驗和CCK8檢測干擾后細胞增殖OD值,實驗結果顯示經siRNA- Nav1.5干擾后的HSC- 3細胞的增殖和侵襲能力顯著下降。說明Nav1.5在口腔鱗癌細胞生物學特性方面具有重要的調節(jié)作用。在乳腺癌的研究[9]中也有著相似的結果,沉默Nav1.5基因后,MDA- MB- 231細胞的侵襲能力顯著降低。在結腸癌中,研究[10]表明Nav1.5基因涉及廣泛的信號調節(jié)并參與腫瘤細胞侵襲的調節(jié),是癌細胞侵襲的關鍵驅動因子。在動物體內研究[11]中,發(fā)現(xiàn)敲低Nav1.5顯著抑制了腫瘤的生長和體內局部侵襲。盡管證明了Nav1.5在口腔鱗狀細胞癌的生長和轉移中起重要作用,但其具體機制尚不清楚。
PCNA與細胞的DNA合成密切相關,在細胞的增殖中起關鍵作用,也是細胞異常增殖的關鍵蛋白,有研究[12]表明,相比正常口腔組織在口腔鱗狀細胞癌中PCNA過表達,提示其與口腔鱗癌的發(fā)生發(fā)展過程有關。在本實驗中,RT- PCR和Western blot結果顯示經siRNA- Nav1.5轉染的HSC- 3細胞內PCNA表達下降。對腫瘤侵襲和轉移機制的研究發(fā)現(xiàn):細胞外基質(extracellular matrix,ECM)的降解是腫瘤侵蝕正常組織并引發(fā)轉移的重要途徑。基質金屬蛋白酶(matrix metalloproteinase ,MMPs)是最重要的,可以降解ECM的所有成分,近年來已成為腫瘤侵襲和轉移研究的熱點,其中又以MMP- 2和MMP- 9最為重要。Chandolia et al[13]研究發(fā)現(xiàn):相比正常口腔黏膜上皮,口腔鱗癌中MMP- 9表達水平顯著提高。在本實驗中,轉染siRNA- Nav1.5 48 h后HSC- 3細胞內MMP- 2和MMP- 9表達均下調。以上結果說明口腔鱗癌中Nav1.5可能通過直接或間接地調控PCNA、MMP- 2和MMP- 9的表達進而影響著細胞生物學行為的改變。

圖6 RT- PCR檢測MMP- 2、MMP- 9和PCNA mRNA表達
A:MMP- 2 mRNA相對表達量; B:MMP- 9 mRNA相對表達量; C:PCNA mRNA相對表達量;與CON組比較:*P<0.05,**P<0.01,***P<0.001; 與NC組比較:#P<0.05,##P<0.01

圖7 Western blot檢測干擾后HSC- 3細胞PCNA、MMP- 2和MMP- 9蛋白的表達變化
與CON組比較:*P<0.05; 與NC組比較:#P<0.05
為了進一步研究證明動物體內Nav1.5的生物學作用,下一步將進行裸鼠皮下造瘤后的進一步動物實驗,從而推進Nav1.5作為臨床口腔鱗癌治療靶點的應用。

