真武湯治療慢性心力衰竭的網絡藥理學機制研究
伍燕宏, 鄭景輝, 朱梓銘, 羅蔚
(1.廣西中醫藥大學研究生院,廣西南寧 530001;2.廣西中醫藥大學附屬瑞康醫院,廣西南寧 530011)
慢性心力衰竭(chronic heart failure,CHF)是由于心臟結構或功能異常致使心室充盈受阻或射血分數降低的復雜臨床綜合征[1],也是心血管疾病發展進程的最終階段。近年來,心力衰竭患者在全球高達兩千萬人,且仍在繼續以二百萬的速度在遞增。據《中國心血管病報告2017(摘要)》最新發布統計,我國心力衰竭患者已有450萬[2]。大量數據資料顯示,CHF已嚴重危及人類健康。西醫學認為CHF治療以改善心室重塑為主,但總體效果不佳[3],而中醫藥治療CHF具有明顯的優勢及鮮明的特色。
中醫學認為CHF病機主要包括心氣不足和水濕痰瘀兩方面,治療應溫陽益氣、化痰逐瘀[4,5]。真武湯源于《傷寒論》,是陽虛水泛證CHF治療的常用方劑。但是真武湯治療CHF的機制尚未明確,本研究運用網絡藥理學對真武湯治療CHF的機制進行了探討,現將研究結果報道如下。
1 資料與方法
1.1資料來源登錄在線中醫藥生物信息學分析工具(BATMAN-TCM)(http://bionet.ncpsb.org/batmantcm/),輸入關鍵詞“真武湯”,進行系統查詢。再從上述查詢的真武湯內容中尋找治療CHF的數據,顯示有11種預測靶蛋白,具體見圖1。
1.2方法分別利用Metascape對上述11種預測靶蛋白富集總分析,通過David 6.7在線進行基因本體論(GO)功能富集分析和京都基因和基因組百科全書(KEGG)信號通路分析,同時基于BATMAN-TCM自身的網絡繪制工具得出疾病——靶點——成分相關數據[6]。
2 結果
2.1預測靶蛋白選取查詢到真武湯治療CHF的預測蛋白共有11種,分別是血管緊張素轉換酶(ACE)、α2A腎上腺素能受體(ADRA2A)、α2B腎上腺素能受體(ADRA2B)、腎上腺素能β受體激酶1(ADRBK1)、血管緊張素II 1型受體(AGTR1)、鈉鉀ATP酶α1亞基(ATP1A1)、鈉鉀ATP酶α2亞基(ATP1A2)、α1G T型鈣離子通道蛋白(CACNA1G)、α1LT型鈣離子通道蛋白(CACNA1L)、可溶性鳥苷酸環化酶(GUCY1B3)、腫瘤壞死因子(TNF)。調整后的P值為2.70E-03。
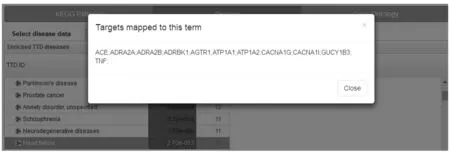
圖1 BATMAN-TCM系統查詢結果Figure 1 The search results from BATMAN-TCM
2.2 Metascape分析對11種預測靶蛋白進行Metascape熱圖富集總分析及預測靶蛋白途徑和通路富集分析。對于每個給定的基因列表,本研究都使用以下的本體來源進行路徑和過程富集分析:KEGG通路、GO生物學進程、靶基因表達集合、典型通路和蛋白復合體數據庫(CORUM)。基因組中的所有基因都被用作富集背景。此次收集P<0.01的項,最小計數為3,富集因子>1.5(富集因子是觀察到的計數與隨機期望的計數之比),并根據它們的隸屬度相似性將其分組到集群中。因此,本研究結果發現,這些預測靶蛋白與血液循環、環磷酸鳥苷酸(cGMP)——蛋白激酶G(PKG)信號通路、肌肉收縮、心臟收縮、細胞分泌的調節、腎素分泌、脂質代謝負調控、氮化合物細胞應答有關。其中血液循環、cGMP-PKG信號通路、平滑肌收縮3項占比高。詳見圖2和表1。
2.3 GO富集分析及KEGG通路分析通過David 6.7在線對GO富集分析的結果顯示:這些蛋白主要的生物學過程(biological process,BP)分析共47條,P≤0.01有28條,涉及血管收縮的調節、平滑肌收縮的調節、血壓調控、糖苷化反應、G蛋白偶聯受體信號通路激活表皮生長因子受體、腎上腺素分泌的負調節、通過腎上腺素能受體信號通路激活絲裂原活化蛋白激酶(MAPK)活性、腎素——血管緊張素調節全身動脈血壓、心臟收縮的負調節、鉀離子通過質膜內流、膜復極化等方面,見圖3。細胞組件(cellular component,CC)分析顯示 14條,P≤0.05有11條,其預測蛋白主要在質膜、核內體、鈉鉀交換ATP酶復合體、電壓門控鈣通道復合體、橫小管、膜的完整成分、閏盤、細胞外囊泡、質膜的完整成分、細胞內膜結合細胞器、小窩等,見圖4。分子功能(molecular function,MF)分析12條,P≤0.05有11條,預測蛋白涉及緩激肽受體結合、低電壓門控鈣通道活性、α2腎上腺素能受體活性、甾類激素綁定、腎上腺素結合、鈉鉀交換ATP酶活性、鈉離子綁定、鉀離子結合、核苷酸綁定、藥物綁定、分子伴侶等功能,見圖5。從數據中我們發現,GO分析生物學過程排位靠前的主要是血管調節、平滑肌調節、血壓調節。生細胞組件分析結果提示,質膜、膜及其組成部分比例較大。分子功能分析結果提示,核苷酸綁定占比明顯。KEGG通路分析共顯示14條,P≤0.05有12條,其中9條信號通路與本研究疾病相關。炎癥相關通路(1條):MAPK信號通路;與神經——體液代謝有關(6條):心肌細胞腎上腺素能信號傳導、腎素分泌、醛固酮的合成與分泌、腎素——血管緊張素系統、近端小管重碳酸鹽吸收、醛固酮調節鈉重吸收;與心臟功能和血管舒張有關(2條):cGMP-PKG信號通路、鈣信號通路。見圖6。
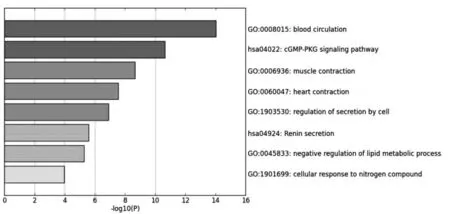
圖2 Metascape熱圖富集總分析Figure 2 Metascape enrichment total analysis

表1 預測靶蛋白途徑和通路富集分析Table 1 The predicted target protein pathways and pathway enrichment analysis
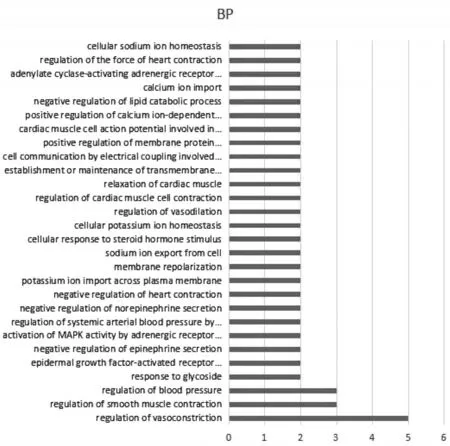
圖3 BP分析Figure 3 BP analysis
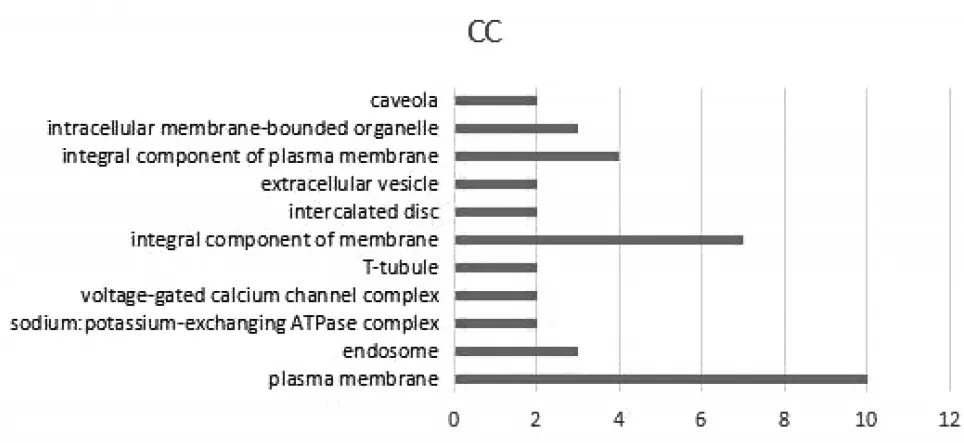
圖4 CC分析Figure 4 CC analysis

圖5 MF分析Figure 5 MF analysis
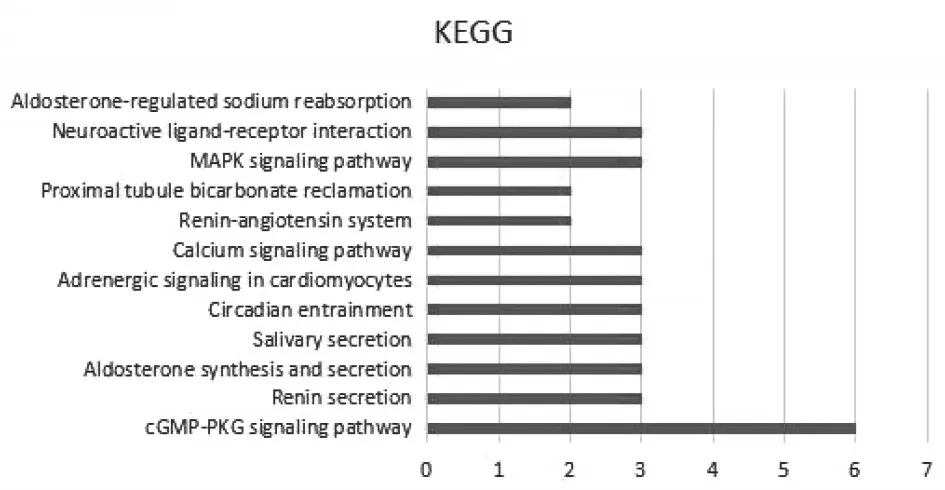
圖6 KEGG通路分析Figure 6 KEGG pathway analysis
2.4 “靶點——通路——疾病”網絡對BATMANTCM自身預測到的候選目標(包括已知目標)Score cutoff≥124的每種成分,進一步進行生物信息學分析。顯著富集KEGG通路/GO分析/TTD疾病/OMIM疾病,調整后P<0.05,獲得“靶點——通路——疾病”網絡。為清晰呈現,本文僅提供部分“靶點——通路——疾病”網絡圖,見圖7,圖中顯示:與心力衰竭疾病相關的預測靶蛋白ADRA2B與神經——體液代謝、cGMP-PKG信號通路有關。
3 討論
網絡藥理學是依托組學和大數據高速發展基礎,結合系統生物學、網絡生物學、藥理學等多門學科的交叉互接,運用網絡組學分析對基因、靶點、藥物、疾病間復雜關系進行新藥開發及新興方法設計[7,8]。可以說,網絡藥理學打破常規“一藥、一靶,一病”的局限研究模式,對復方藥物“多成分、多路徑、多靶點”的開展提供廣闊前景,尤其是中藥配伍規律的探索。中藥復方運用網絡藥理學研究可更明確中藥治療疾病的機制,為臨床選擇中藥治療疾病鋪設了一個較好的基礎。
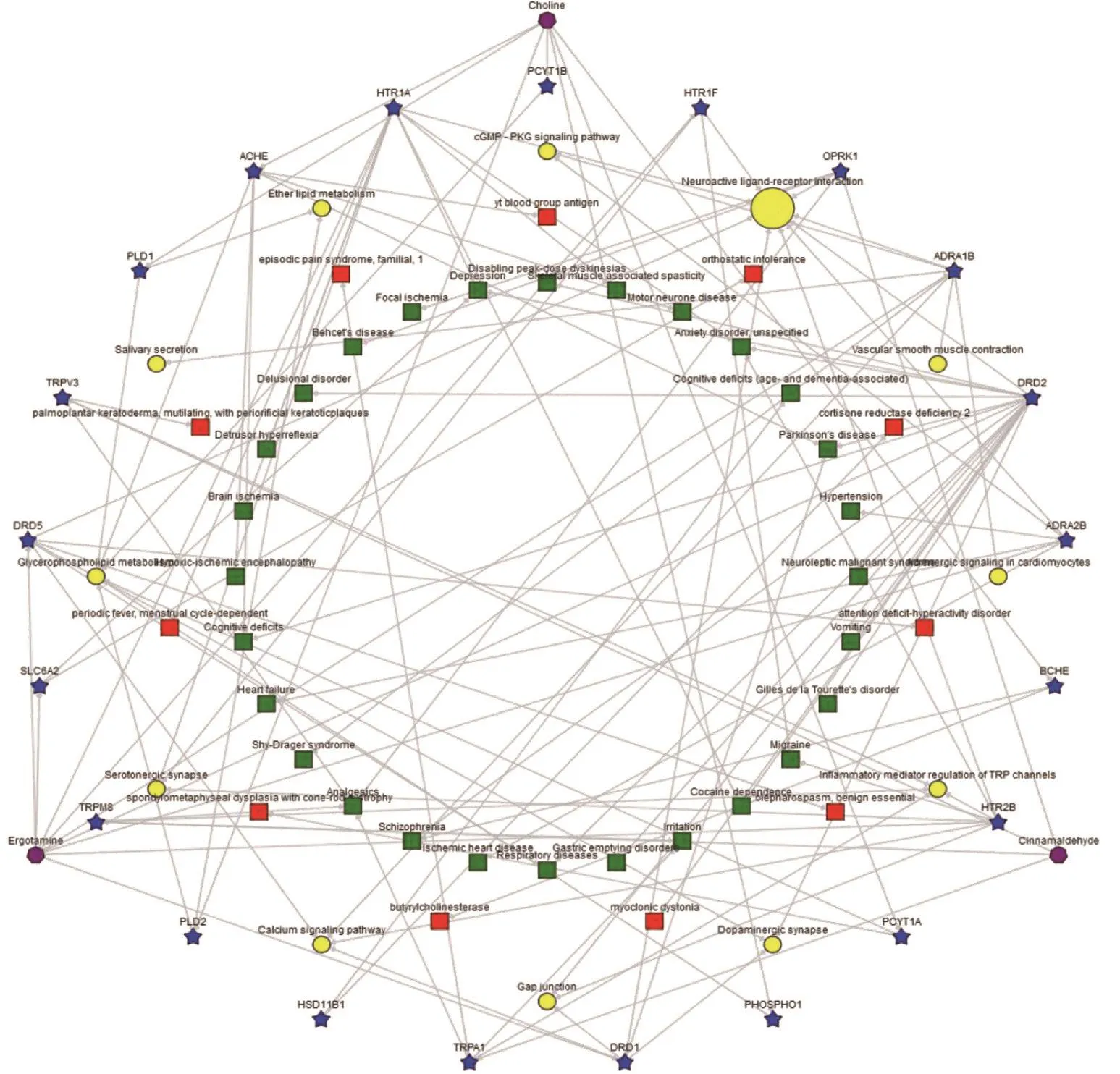
圖7 部分“靶點——通路——疾病”網絡圖Figure 7 Part“Target-pathway-disease”network
CHF屬于心血管器質性疾病中最嚴重的并發癥。雖然目前治療遵循“強心”、“利尿”、“擴冠”為基礎原則,旨在阻止心肌重構過程的發展,但仍不能扭轉終末期心力衰竭快速進展演變的過程。同時,西藥對患者個體存在差異,出現許多不良反應,致使西醫治療CHF最終束手無策。真武湯具有強心利水、擴血管、改善血液循環及護腎之功,其在現代藥理學研究中已被證實[9]。方中:附子溫腎利水,兼暖脾;茯苓、白術健脾化濕、利水;白芍一者利小便、行水氣,二者柔肝同時可止腹痛,三者斂陰舒筋;配之生姜溫散兼助附子散寒氣。諸藥配伍共奏溫陽利水治療心力衰竭有效[10]。但其治療CHF的機制尚未明確,因此,本研究運用網絡藥理學理論探討真武湯治療CHF的機制。
本次研究運用網絡藥理學發現,通過BATMAN-TCM系統檢索真武湯后,共有11種預測靶蛋白,將11種預測靶蛋白進行David 6.7在線GO功能富集分析和KEGG信號通路分析得出,預測靶蛋白與血管、平滑肌調節,細胞器、核苷酸結合關系較密切。KEGG通路分析結果發現,這些預測蛋白基本與神經——體液調節、信號通路有關聯,且腎素——血管緊張素——醛固酮系統(RAAS)是主要的調節機制,MAPK信號通路產生炎癥反應影響疾病病理過程,cGMP-PKG信號通路、鈣信號通路共同調節血管收縮及舒張。
RAAS系統主要由神經——內分泌系統調節,也是影響CHF預后的重要因素[11]。預測靶蛋白ACE在RAAS中起重要作用,它是ACEI的作用靶點,可將AngI催化水解成AngⅡ,調節電解質、血壓和體液穩態。機體AngⅡ被ACE激活后,兒茶酚胺和ALD不斷釋放、分泌,加速膠原沉積及心肌細胞增殖,致使左心室肥厚、心室重構改變,誘導心肌細胞快速凋亡,最終促進CHF形成。陳亮等[12]研究ACE基因多態性與老年CHF心室重構發現,ACE DD型水平較Ⅱ型水平高,且DD型組的左室射血分數明顯低于ID型及II型基因組,證明ACE DD型患者血清及心肌內ACE活性相對較高。現學者一致認為造成此現象與ACE DD基因型有關。孫勇[13]研究ACE多態性與CHF患者運動實驗的結果表明,DD/ID型基因患者運動耐力低的同時還有較高的對抗運動訓練。張博等[14]研究也發現DD型患者CHF左心室較ID、Ⅱ基因型患者明顯增大,且心功能亦較差,經ACEI治療后DD型基因組患者出現良性心室重構的逆轉,而ID及Ⅱ型基因組患者左心室改善幅度較小,提示ACE DD型基因與CHF發病率有關。ADRA2A、ADRA2B兩個同源亞型屬于α2腎上腺受體(α2-AR),作用機制是α2-AR選擇性與兒茶酚胺類物質識別結合后,啟動細胞內信號轉導通路,誘發CHF病理、生理的多種反應[15,16]。預測蛋白AGTR1也是RAAS中一個關鍵影響因素。在CHF過程中,因腎血流量灌注減少,AngⅡ與AGTR1受體結合后,激活磷脂酶C,二磷脂酞肌醇隨之發生水解,促進細胞內Ca2+快速釋放,從而導致血管收縮,進一步使細胞凋亡,最終誘發心室重構的演變。目前研究學者認為AGTR1影響CHF可能與A1166C等位基因有關。因此,AGTR1靶蛋白在CHF中的作用仍需進一步探究,以期為今后的研究者提供新的突破口。
炎癥反應是心血管事件發生的一個重要機制,其活化程度與CHF過程有關。MAPK信號通路是細胞外信號調節激酶(ERK)、JNK、p38等3條主要通路的集合點,其形成的轉錄因子活化蛋白1(AP-1)可間接調控TNF-α、IL-6等多種炎性因子表達。李曉等[17]研究發現,通過ERK/MAPK通路促進心肌細胞凋亡,通過JNK/MAPK通路主要抑制AngⅡ、內皮素、兒茶酚胺激活,通過p38/MAPK通路促進白細胞聚集、活化等共同作用可控制炎性因子的表達,阻滯CHF發生。同期,趙欣等[18]在研究TLR4受體/MAPK信號通路在心源性惡病質發生機制中的作用時發現,JNK/MAPK通路中JNK被SP600125特異性抑制劑阻斷后,抑制組的TNF-α mRNA表達量降低,說明TNF-α與JNK/MAPK通路介導有關。TNF-α是評價炎癥最常用的細胞因子,在機體創傷機制中最早被激活,可產生炎性介質,促進IL-6因子釋放,擴大炎性損傷范圍,加速細胞壞死[19]。TNF-α被證實是CHF惡病質的主要炎癥因子之一[20]。吳勇進等[21]進行67名CHF和30名健康人的對比研究發現,不同心功能等級的CHF患者左心室射血分數不同程度下降,左心室舒張末期及收縮末期內徑亦不同程度升高,其機制與血清中腦鈉肽(BNP)、TNF-α、MMP-9、IL-6的表達量有關。心功能越差炎癥因子水平越高,這為臨床診斷CHF的嚴重程度提供了很高的參考價值。紀煥春等[22]對60例CHF男性患者的臨床研究證實TNF-α水平與CHF程度呈正相關。胡黎文等[23]觀察真武湯聯合桂枝茯苓丸對CHF患者炎癥因子表達情況的影響,發現真武湯聯合桂枝茯苓丸可降低CHF患者血清超敏C反應蛋白(hs-CRP)、IL-6及TNF-α水平,且均較西醫常規組明顯下降,這可能因其可拮抗神經——內分泌系統過度激活,從而逆轉心室重構,改善了CHF程度。可以認為TNF-α在CHF發生、發展過程中發揮著重要介導作用[24,25]。
cGMP是細胞內第二信使物質,可調控心血管功能、基因表達及形態學,其中以調控離子通道為主。而當它刺激其下游靶點PKG后可對抗心肌細胞凋亡。PKG主要調控血管平滑肌松弛過程中多種類型細胞表達,其中血小板和內皮細胞最為重要。前期證明,PKG磷酸化血管擴張刺激磷蛋白(p-VASP)后,可使血管平滑肌舒張[26]。對于其機制,現有學者認為,PKG是通過抑制心肌重塑的病理性Ca2+信號及其下游鈣調磷酸酶——活化T細胞核因子(NFAT)、鈣調素依賴蛋白激酶Ⅱ(CaMKⅡ)通路的激活作用,從而參與心臟的重構。這與萬淼等[27]對蛋白激酶G對左室重構的影響展開的討論結果相似。可見,cGMP-PKG信號通路主要是通過調控Ca2+濃度來調節心臟的收縮舒張功能,從而影響心室重構,最終發展成CHF。另外,鈣信號通路異常可影響心肌細胞在舒張期出現Ca2+從肌漿網內大量漏出現象,一旦Ca2+失穩出現,心肌收縮減弱,CHF將會加重[28]。儲存在CHF患者心肌細胞中的肌質網鈣泵(SERCA2α)磷酸化被下調后可造成Ca2+回收受阻減少[29],進而導致細胞遷移、心室重構發生。因此,SERCA2a是目前CHF治療中被視為最有潛力的蛋白。若蘭尼堿受體2(RyR2)Ca2+釋放通道失調,易促心肌細胞去極化,誘發CHF和心律失常[30]。故需保護RyR2泵的完整,避免Ca2+滲漏,以阻礙CHF發生。本研究中,本課題組還發現了 ADRBK1、ATP1A1、ATP1A2、CACNA1G、CACNA1L、GUCY1B3蛋白,它們在CHF發生及發展過程中應參與的調控作用尚未被清楚詮釋。
本次研究未能對基于數據庫挖掘發現的真武湯治療CHF的主要靶蛋白進行實驗認證,此為本研究存在的不足。本研究通過運用網絡藥理學挖掘真武湯治療CHF的蛋白,探討真武湯治療CHF的內在機制,增強了對其微觀整體的認識,揭示了疾病更深的內在調控機制,為CHF的發生、發展研究奠定了基礎,從未被詮釋的蛋白詮釋其作用機制無疑對后期的實驗研究打開了新空間,開辟了新的方向。

