轉染試劑Vigofect對HeLa細胞轉染的方案優化
李思琦 李春雅 翁夢露 楊 悅 張健翔 劉 進 商 瑜 張曉嫣
(北京師范大學生命科學學院 北京 100875)
0 前言
“轉染試劑Vigofect 對 HeLa 細胞轉染的方案優化”是為生物學一年級研究生開設的細胞及組織培養課程中,學生做的開放實驗課題。在學習了轉染技術基本原理與操作、熒光顯微鏡成像技術、蛋白印跡技術后,學生綜合運用以上技術,使用轉染試劑,對HeLa 細胞的轉染條件進行研究,分析影響轉染效率的因素,探究轉染條件的優化方案,以便為自己今后的實驗工作提供借鑒。同時,這種問題導向性實驗的設置,是為培養學生的創新性思維,改進研究生教學工作進行的探索。
轉染是采用除病毒感染外的其他方法將外源核酸(DNA 或者 RNA)人工導入真核細胞的過程。通過轉染能改變細胞內蛋白表達,改變細胞特性,是研究基因或其產物功能和調控機制的一種非常重要的技術手段[1]。將外源基因導入真核細胞的方法有很多種,例如:DEAE-葡聚糖轉染法、磷酸鈣轉染法、脂質體法、顯微注射法及電穿孔法等[2]。
目前常用的轉染試劑是陽離子脂質體和陽離子聚合物,它們容易透過細胞膜,其中陽離子脂質體在體外基因轉染中有很高的效率。但由于陽離子脂質體易被血清清除,有高水平毒性,因此陽離子聚合物轉染試劑被日益廣泛地研發與使用。陽離子非脂質體轉染試劑以陽離子聚合物為主要成分,其高度的分支結構確保了正離子電荷的高密度,使與帶有負電荷的外源基因結合更有效,容易被細胞吸收,適合多種類型的細胞系,可廣泛用于瞬時轉染和穩定轉染[3]。Vigofect 采用陽離子非脂性物質為主的配方,是一種高效真核轉染試劑,可與 DNA 形成穩定的復合物,透過細胞膜進入細胞內,并保護 DNA 免受核酸酶的降解。
HeLa 細胞是現代生命科學研究中經常使用的一種細胞,是種源自一位美國婦女海莉耶塔·拉克斯(Henrietta Lacks)的子宮頸癌細胞的細胞系。HeLa 細胞是生物學研究中非常重要的實驗材料,該細胞形態規則,生長速度較快,易于培養,且較易攝入外源質粒 DNA,是檢測轉染試劑效果的合宜材料。
轉染過程中影響轉染效率的因素包括:細胞狀態、細胞密度、DNA 與轉染試劑比例、轉染前細胞培養時間、轉染試劑孵育時間、培養液體積等。實驗室將長期使用Vigofect 對Hela 細胞進行細胞轉染,但轉染流程沿用原有方法,未做過轉染條件的優化,希望通過此次實驗,能在質粒使用跟細胞轉染時間上進行優化,既得到最大轉染效率,又能節省試劑,更合理地安排實驗時間。
1 實驗材料與方法
1.1 實驗材料與試劑 人子宮頸癌細胞(HeLa,由北京師范大學生命科學學院商瑜實驗室提供)、GFP 質粒、CHIP 過表達質粒(HA-CHIP)。
150 mmol/L NaCl(超純水配制,高壓或過濾滅菌)、Vigofect 轉染試劑(威格拉斯)、牛奶(伊利脫脂奶粉配制)、Anti-CHIP(本實驗室保存)、Anti-βactin(Sigma)、山羊抗小鼠 lgG/辣根酶標記(中杉金橋)、山羊抗兔 lgG/辣根酶標記(中杉金橋)、曝光試劑盒(顯色底物,Thermo Scientific)、DMEM basic(gibco)、PBS(gibco)、胎牛血清 FBS(康源生物)。
1.2 實驗儀器(表1)

表1 實驗儀器及來源
1.3 實驗步驟
1.3.1 細胞培養 將HeLa 細胞培養在含 10%胎牛血清的 DMEM 中(按 1∶1000 加入雙抗),37℃,5% CO2培養箱中培養。
1.3.2 細胞轉染及轉染效率分析 轉染前一天鋪細胞于12 孔板,使細胞在轉染當天達到指定匯合度(本實驗中涉及匯合度為40%~100%)。
轉染試劑為威格拉斯公司的Vigofect,根據該公司提供的產品說明步驟進行轉染。
配制 Vigofect 工作液,1 μL Vigofect 加入 49 μL 150 mmol/L NaCl 溶液中。輕輕混勻,靜置 5 min。工作體積每孔50 μL。
配制 DNA 工作液,工作體積為每孔50 μL。
將Vigofect 工作液分別逐滴加入DNA 工作液中,混勻后靜置15 min。將混勻后的液體加入細胞培養體系中,輕輕混勻,置于 37℃,CO2培養箱中培養。
1.3.2.1 DNA 與轉染試劑比例對轉染效率的影響 轉染前一天鋪細胞于12 孔板,使細胞在轉染當天達到匯合度70%。12 孔板中,固定Vigofect用量(1 μL),DNA 轉染用量分別為 0.4 μg、1 μg、2.5 μg 和 6.25 μg。
1.3.2.2 細胞密度對轉染效率的影響 12 孔板中,轉染前一天調整鋪入皿中的細胞數量,使細胞在轉染當天分別達到40%、70%、100%的匯合度。固定 Vigofect 用量(1 μL),DNA 用量為 2.5 μg。
1.3.2.3 接種后培養時間對轉染效率的影響分別在轉染前16 h 及11 h 在12 孔板中鋪入一定數量 HeLa 細胞,使兩者細胞在轉染當天分別達到 70%匯合度。固定 Vigofect 用量(1 μL),DNA用量為 2.5 μg。
以上轉染操作均在轉染試劑孵育5 h 后更換新鮮培養基。轉染36 h 后觀察細胞,用倒置熒光顯微鏡拍照,每孔細胞選取3 個視野,進行拍照,通過GFP 熒光表達量,判斷細胞轉染效率。利用Image J 軟件統計轉染效率。
1.3.3 Western Blot 檢測
1.3.3.1 收集細胞樣品 棄掉培養基,每個孔中加入 500 μL PBS,清洗細胞,每孔洗 2 遍。每孔中加入 200 μL 2×loading buffer,將細胞刮下,置于1.5 mL EP 管中,100℃煮 10 min,放入-20℃備用。
1.3.3.2 SDS-PAGE 凝膠電泳
1)清洗膠槽,組裝。
2)按照表2 配制分離膠和濃縮膠。

表2 分離膠和濃縮膠的配制
取出制備好的樣品上樣量為10 μL,電泳儀設定為 140 V 恒壓,30 min,160 V,1 h 30 min,至溴酚藍跑出膠底邊即可停止電泳。
1.3.3.3 轉膜及麗春紅染色 配制轉膜緩沖液1 L:100 mL 10×transfer buffer(250 mmol/L Tris-HCl,192 mmol/L甘氨酸 ,ddH2O 中 加 入 30.2 g Tris-HCl,144 g 甘氨酸)+700 mL ddH2O+200 mL無水甲醇。
將PVD 膜置于甲醇中激活5 min。
制作“三明治”轉膜結構:濾紙→膠→PVD 膜→濾紙按順序疊放,在其表層輕輕加transfer buffer。將轉膜裝置放入冰水混合物中,轉膜2 h。
轉膜完畢后,將膜取出,浸泡在配制好的麗春紅染色液(2%麗春紅,30%三氯乙酸,30%磺基水楊酸)中,直至條帶顏色完全顯現出來,后轉入清水中洗去浮色。
1.3.3.4 裁膜及封閉 裁下β-actin [相對分子質量(Mr)≈4.3×104]作為內參,將要檢測的蛋白放在膜的中心位置,將膜剪裁至合適大小并標記好所需抗體名稱。放入清水中。
配 制 1 L TBST buffer:900 mL ddH2O 加 入100 mL 10×TBS (5 mol/L NaCl 275 mL,pH=7.6 的Tris-HCl 100 mL 補齊至1 L)再加入1 mL 吐溫。
配制封閉使用的牛奶(10%):稱 10 g 奶粉,加 TBST 至 100 mL,攪拌 5~10 min 至溶解。
將洗好的膜按照與封口垂直的方向放入自封袋中,加入配好的牛奶,沒過膜,塑封機封住開口,37℃ 1 h 或 4℃過夜。
1.3.3.5 孵育一抗、二抗 用牛奶按照1∶1 000的比例配制一抗。封閉結束后,倒掉牛奶,加入一抗,封膜。4℃過夜或 37℃ 1~2 h。TBST 洗膜 4 遍,每遍5 min。
用 TBST 按照 1∶10 000 的比例配制二抗。將洗膜盒里的TBST 倒干凈,直接在洗膜盒里加入適量二抗,37℃ 1 h 或者室溫 2 h。TBST 洗膜 5遍,每遍 5 min。
1.3.3.6 曝光(化學發光儀) 將膜移入化學發光儀中。避光配制化學顯影液。將顯影液滴加到膜上,設置自動曝光參數(不顯示 marker,曝光 15次),曝光結束后選擇最合適曝光強度的照片,根據上樣順序按規范制作成實驗結果圖留存。
2 結果與討論
2.1 DNA 與轉染試劑比例對轉染效率的影響DNA 轉染用量為 0.4 μg、1 μg、2.5 μg 和 6.25 μg。實驗結果顯示,從表達GFP 細胞數目(圖1、表1)和蛋白表達水平上看(圖2),隨著DNA 對轉染試劑比例的增加,轉染效率會逐漸提高,但超過一定限度,隨著DNA 量的增加,轉染效率不再提高。這也說明Vigofect 在轉染時存在 DNA 轉染量的限制,并不是轉染的DNA 量越多轉染效率越高。對于該實驗體系,DNA 與 Vigofect 的最佳比例為1 μL Vigofect 轉染 2.5 μg DNA。
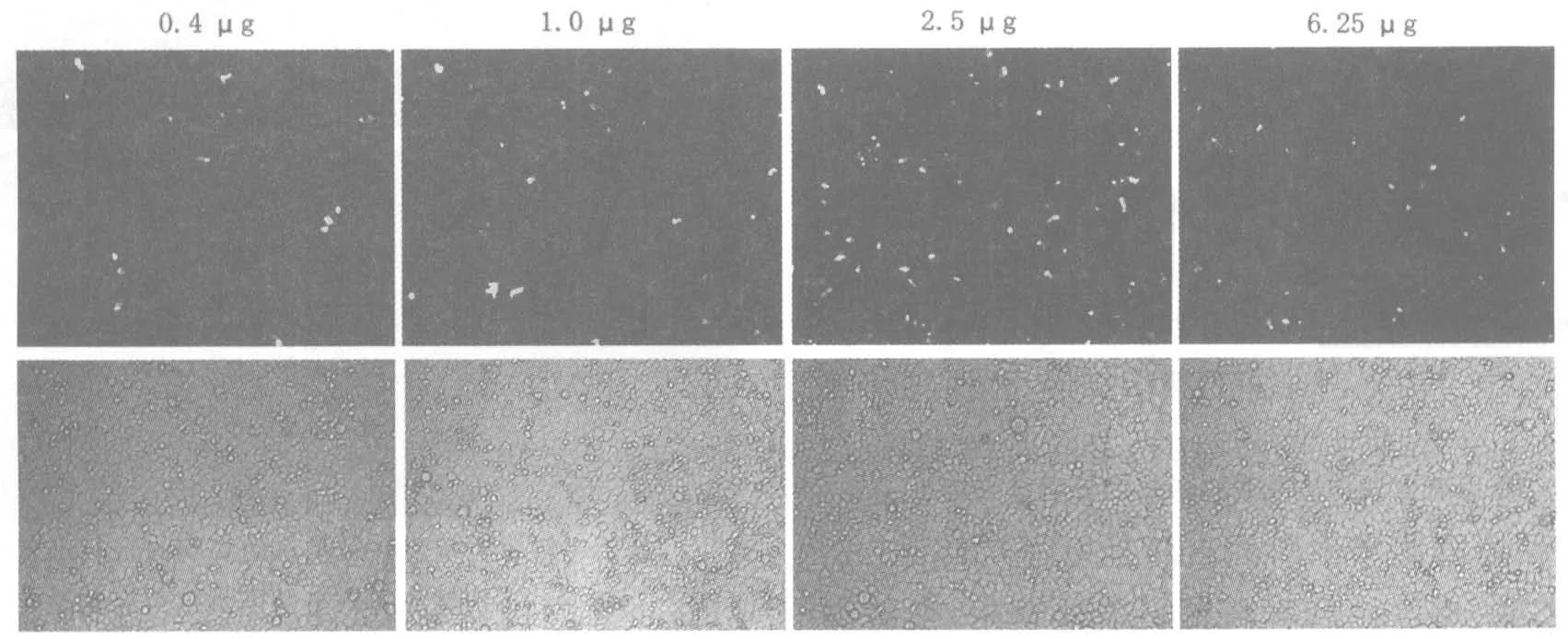
圖1 不同質粒轉染量對轉染效率的細胞水平觀察
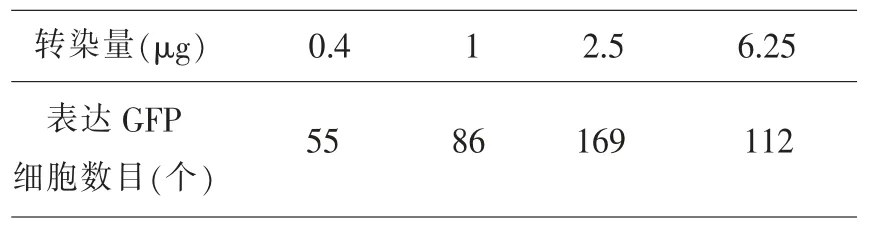
表1 不同質粒轉染量條件下細胞熒光數量統計
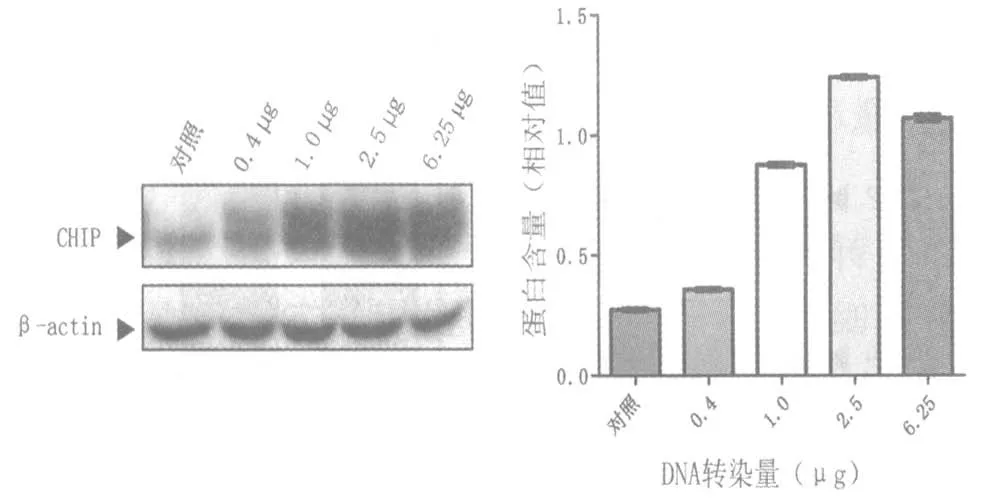
圖2 不同質粒轉染量對轉染效率的蛋白水平檢測
2.2 細胞密度對轉染效率的影響 實驗室原有固定的轉染流程都是在細胞匯合度達到70%時進行轉染,因此預測此時轉染效率應該最高。但出乎意料的是,實驗結果提示細胞密度達到 40%時進行轉染效率最高(圖3、表2、圖4)。經分析發現,實驗室原有流程選擇在70%細胞匯合度轉染是為了削減轉染試劑的細胞毒性作用,在保證細胞處于指數增長的前提下盡可能獲得更多存活細胞。此次實驗發現,對HeLa 細胞利用Vigofect 進行轉染時,選用40%的細胞匯合度其轉染效率更高:固定合適的轉染試劑與質粒DNA 比例后,其細胞毒性比較小;40%的細胞匯合度,細胞狀態更好,生長旺盛,攝取外源DNA 的能力也比較強。

圖3 細胞密度對轉染效率的影響的細胞水平觀察

表2 不同細胞轉染密度條件下細胞熒光數量統計
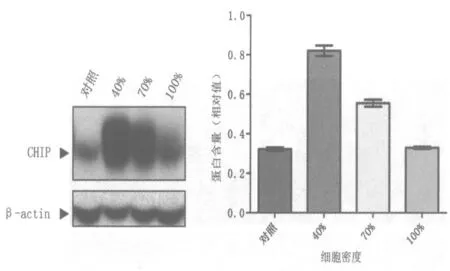
圖4 細胞密度對轉染效率的影響的蛋白水平檢測
2.3 轉染前細胞培養時間對轉染效率的影響在孵育之前,通常選擇較高密度接種細胞,在鋪細胞后的16 h 進行轉染,因為這樣細胞能以比較好的狀態貼壁生長且進入指數增長期,并通常都能達到常用的轉染匯合度。但16 h 是否是最佳條件并未驗證。
在本實驗中為了探討細胞接種后培養多長時間進行轉染比較好,并能盡量縮短轉染實驗的時間,分別選擇了16 h 后轉染和11 h 后轉染進行對比實驗。分別于轉染前 16 h 及11 h 在12 孔板中鋪入相應數量HeLa 細胞,使細胞在進行轉染時匯合度均達到 70%左右。固定 Vigofect 用量(1 μL),DNA 轉染用量 2.5 μg。從實驗結果來看,鋪入細胞11 h 后進行轉染的效率略高于16 h 轉染的效率(圖5、表3、圖6)。

圖5 轉染時間對轉染效率的影響的細胞水平觀察

表3 不同轉染時間條件下細胞熒光數量統計
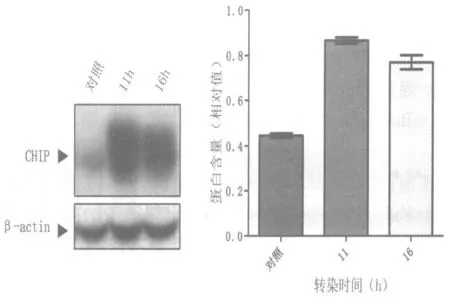
圖6 轉染時間對轉染效率的影響的蛋白水平檢測
3 總結與評述
學生所在實驗室經常會用轉染技術研究基因和蛋白的功能及調控機制。實驗室固有流程為細胞接種后16 h,細胞匯合度達到70%時,進行轉染實驗,轉染質粒DNA 時傾向于增加用量,但為什么這樣做,學生并不清楚。
本次探究實驗針對固有流程,以HeLa 細胞為實驗材料,通過調整轉染過程中DNA 與轉染試劑比例、轉染前細胞培養時間、細胞密度等因素,比較不同條件下轉染效率的變化,實現對細胞瞬時轉染的條件優化的目的。通過之前測試確定,轉染試劑孵育時間,以孵育4~6 h 換液轉染效率最佳,因此不再考察。
通過這種探究性實驗,學生發現細胞轉染時不一定要按照實驗室的原有經驗,轉染時細胞密度一定要達到70%,轉染一定要等接種后16 h。可適當降低細胞密度,適當提前轉染時間,選擇合適的轉染試劑與質粒DNA 的比例。本實驗中用Vigofect 轉染HeLa 細胞時最優條件為以合適密度接種細胞后培養11 h 進行轉染,轉染時細胞匯合度在 40%~50%,每孔的質粒用量為 2.5 μg。既節省了時間、試劑,還提高了轉染效率。
通過本次的探究性實驗,學生體會到方法不是一成不變的,需要不斷探索和優化。在繁忙的科研活動中,偶爾做一次簡單的方法優化小實驗,不僅可幫助提高科研效率,而且也為科研生活增添了樂趣。

