銻酸鋰與六氟銻酸鋰制備新技術集成
劉偉鋒,唐攢浪,陳霖,張杜超,楊天足
(中南大學冶金與環境學院,湖南長沙,410083)
銻酸鋰(LiSb(OH)6)的相對分子質量為230.74,密度為3.112 g/cm3,是一種六邊形層狀結構的白色粉末狀晶體,由[Li2Sb(OH)6]+和[Sb(OH)6]-沿c軸排列而成,其晶格常數a=5.381 2×10-10m,c=9.819 5×10-10m, Sb—O 鍵長為1.978×10-10m,Li—O 鍵長為2.137×10-10m。 LiSb(OH)6是一種制備偏銻酸鋰(LiSbO3)的前軀體,LiSb(OH)6晶體會在210 ℃左右發生熱分解并失去結晶水,形成LiSbO3晶體[1]。LiSbO3晶體可以作為鋰離子電池的負極材料,并且能提高電池的倍率性能、循環性能及庫侖效率,具有196 mA· h/g的初始比容量[2-3]。此外,LiSbO3也用作無鉛壓電陶瓷材料中的添加劑,改善壓電材料的電學性能[4-5]。HSbO3可用在含有6Li/7Li的溶液中選擇性地吸附鋰的同位素并生成6LiSbO3,以實現6Li 與7Li 的分離[6-7]。六氟銻酸鋰(LiSbF6)是一種斜六面體結構的白色狀晶體,該晶體中Sb—F 鍵長為1.88×10-10m,Li—F 鍵長為2.03×10-10m,Li—Sb—F 間的夾角為147.5°,整個晶體結構呈扭曲的立方NaSbF6排列[8],其中SbF-6在波數為294,350,558,668 和669 cm-1處存在特征頻率[9]。LiSbF6可用作鋰離子電池的電解質鋰鹽。利用溶劑模板法制備的聚合物電解質薄膜(TMC)nLiSbF6的熱穩定性良好,鋰鹽含量增加后電解質的離子導電率上升,在測試電壓低于5V(vs Li/Li+)時電解質的電化學性能穩定而不發生氧化分解[10]。LiSbF6能溶解于四氫呋喃和四丁基氟硼酸銨中形成電解液并進行伏安循環檢測。1 次循環后在1.10 V 和0.90 V(vs Li+/Li)附近有一對氧化還原峰,主要為Sb(V)還原為Sb(0)的反應[11],2 次循環后在2.20 V 和3.70 V 附近又出現Sb(Ⅲ)與Sb(0)之間可逆氧化還原反應峰[12]。在含Li+的有機電解質中,MF6-(M=P,As,Sb)的化學穩定性受對應五氟化合物(MF5)的路易斯酸強度影響,路易斯酸強度由弱到強的排序為PF5,AsF5和SbF5,且SbF5比PF5更易與F-配位結合。因此,LiSbF6比LiPF6有更穩定的化學性質,這有利于電解質長期穩定存在[11-13]。通過溶膠-凝膠法制備的聚合物電解質(d-U(2000)nLiSbF6)的熱分解溫度至少可達200 ℃。在30 ℃下d-U(2000)30LiSbF6離子導電率達1.32×10-5S/cm,在95 ℃下d-U(2000)15LiSbF6的離子電導率為5.62×10-4S/cm,測試電壓低于5 V(vs Li/Li+)時該電解質能穩定存在而不氧化分解[14-15]。聚氧化乙烯(PEO)能與LiSbF6形成結晶性良好的P(EO)6LiSbF6聚合物電解質。LiSbF6與相對分子質量為2 000 的PEO 形成P(EO)6LiSbF6晶體,該晶體在溫度為-100~90 ℃時穩定,在110 ℃發生由P(EO)6LiSbF6-2α到P(EO)6LiSbF6-2β 的熱轉變,在130 ℃時,P(EO)6LiSbF6-2β 發生熔化。LiSbF6與相對分子質量為100 000 的PEO 形成P(EO)6LiSbF6,該聚合物在溫度為-100~130 ℃時無結構轉變,這有利于該類聚合物鋰離子電池在更寬的溫度范圍內使用[16-18]。將LiSbF6與二甘醇二甲醚(diglyme)形成溶液后緩慢揮發掉溶劑會形成晶格常數a=11.38×10-10m,b=12.96×10-10m,c=14.837×10-10m的(diglyme)2LiSbF6晶體,其單胞由4個SbF-6和4個[Li(C6H14O3)2]+組成。通過差示掃描量熱法(DSC)研究發現,(diglyme)2LiSbF6晶體在21 ℃重結晶,在25.6 ℃開始吸熱熔化,再次熱掃描其熔化或重結晶峰未明顯改變,這表明其熱轉變的可逆性良好[19-22]。在LiSbF6與線性聚合物二甲亞胺(LPEI)形成的聚合物電解質體系中,提高溫度以及增大LPEI 與LiSbF6之間的物質的量比后,Li+與聚合物間的反應使得體系的無序性增加,其中SbF-6與聚合物骨架中的官能團NH發生反應而不與Li+結合。LiSbF6在聚合物中表現出的這些特性在電解質的離子遷移機理中起著重要的作用[23]。這些研究結果說明,銻酸鋰和六氟銻酸鋰都已經應用于鋰離子電池中,分別作為性能良好的負極材料前軀體和電解質鋰鹽。因此,對這2種銻化物合成工藝進行研究具有重要意義。
1 銻酸鋰制備方法的研究進展
LiSbO3?3H2O 的制備方法主要有干法工藝和濕法工藝。在無水高溫環境下一般采用干法工藝,最終產物是偏銻酸鋰(LiSbO3);在水溶液體系中一般采用濕法工藝,最終產物是含結晶水的銻酸鋰(LiSb(OH)6)。干法工藝主要有高溫固相法、離子交換法、逐步升溫氧化法、簡單固相合成法以及燒結法;濕法工藝有化學浴沉積法、多孔模板法、水熱法。各種制備銻酸鋰的方法比較如表1所示。
1.1 銻酸鋰制備的干法工藝
高溫固相法是將Sb2O3和LiCl按一定配比混合均勻后放入瓷方舟中后置于管式爐中,保持溫度為750~800 ℃,并通入空氣氧化反應約24 h形成熔融物后冷卻,其中LiCl 在高溫下具有揮發性,期間需要補加LiCl,冷卻后的產物用水浸洗后干燥處理得到針狀LiSbO3晶體[24]。在這種晶體中,氧原子緊靠著銻原子形成扭曲的六邊形結構,而鋰原子位于該結構的八面體孔隙之中,在沿c軸排列的鏈狀結構中,銻和氧排列于晶體的長軸方向,使得LiSbO3的結構與SbO-3和其他I價金屬離子形成的MSbO3結構不同。
離子交換法是將分析純的Sb2O3,NaNO3和Na2CO3按化學反應計量比混合均勻后置于550 ℃的反應爐中保溫1 h,取出產物充分研磨并在850 ℃下煅燒2 h后得到NaSbO3前軀體。一次煅燒后產物為單相物質,二次煅燒主要是除去多余的雜質和提高產物結晶性[25]。將銻酸鈉前軀體充分研磨成粉末,再加入物質的量為理論用量20 倍的LiNO3在310 ℃下反應2 h 后,產物用蒸餾水洗滌干燥后得到銻酸鋰晶體。由于NaSbO3和LiSbO3之間發生的固相反應不充分,在產物中能夠檢測到NaSbO3的存在。在850 ℃下煅燒后,交換反應完全,形成物相組成單一的LiSbO3晶體。逐步升溫氧化法是以Sb2O3和過量5%(質量分數)的Li2O 為原料混合均勻后放入銀質管中,然后置于石英管中并通入空氣,升溫到800 ℃并保溫72 h進行反應。在溫度低于400 ℃時生成LiSbO2穩定相,當溫度為400~580 ℃時生成Sb(Ш)與Sb(V)的共存相LiSbO2.5,最后在更高溫度(580~800 ℃)和O2共同作用下生成最終產物LiSbO3。當溫度為300 ℃時,低溫下生成的LiSbO2的Li+電導率可達10-6S/cm[26]。
簡單固相合成法是將LiNO3與Sb2O3均勻混合3 h后,在800 ℃下煅燒24 h制得正銻酸鋰(Li3SbO4)。將Li3SbO4粉末,PVDF黏結劑與乙炔黑導電劑按質量比65:25:10 加入到甲基吡硌烷酮(NMP)溶劑中,攪拌均勻后形成涂層漿料,再將該漿料涂在銅箔上形成鋰離子電池的負極,金屬鋰作為對應電極,LiPF6溶解于乙烯碳酸酯(EC)和碳酸二甲酯(DMC)體積比為1:2 的混合溶劑中作為電解質組裝成電池進行電化學性能檢測[3]。Li3SbO4的理論容量為259.5 mA·h/g,初始充電和放電容量分別為126 和53 mA·h/g,首次充電有58%的容量用于形成固體電解質界面(SEI)膜,其嵌鋰和脫鋰電位分別為0.72 V 和1.05 V,且Li3SbO4中Sb(V)還原為Sb(Ш)涉及2 個電子的轉化過程。經倍率性能檢測發現,在高倍率(40C)下循環至200 次的過程中,Li3SbO4的放電容量先降低至65 mA·h/g,然后增加至73 mA·h/g,庫侖效率接近100%,這一結果說明Li3SbO4在高能量密度的負極材料方面極具應用前景。
低溫燒結法以Li2CO3和Sb2O5為原料,按物質的量比1:1配料,采用乙醇作為分散劑,氧化鋯球作為球磨介質,球磨12 h 后產出的混合料在80 ℃下干燥10 h,然后研磨30 min,之后用孔徑為0.180 mm的網篩進行篩分,將篩下的物料置于氧化鋁坩堝中,在溫度為570~730 ℃的電阻爐中預焙燒2 h,然后將合成的LiSbO3冷卻至室溫,最后再研磨成粉末。將質量分數為0.06%的銻酸鋰粉末添加到鉛基五元壓電陶瓷材料中,使得壓電常數與燒結性能提高,介電耗損降低,有利于材料壓電性能的改善[4-5]。
1.2 銻酸鋰制備的傳統濕法工藝
化學浴沉積法是以SbCl5和LiOH·H2O 為原料,以0.5 mol/L的酒石酸作為穩定劑,調整SbCl5濃度到0.1 mol/L 后,在室溫下攪拌24 h。然后,將2 mol/L的LiOH 溶液緩慢加入SbCl5溶液中,使溶液體系的pH 為9.0~11.5,然后在30~70 ℃保溫3 h,將沉淀物在60 ℃下干燥4 h后得到銻酸鋰結晶粉末[27]。酒石酸的加入可以防止Sb5+水解并配位生成Sb(C4H4O6)35+。隨著沉淀時溶液pH 和沉淀物保存溫度的升高,沉淀物顆粒會由小顆粒狀向片狀顆粒轉化,這種小顆粒在800 ℃熱處理后成為斜方晶系的LiSbO3,而片狀顆粒經熱處理后成為斜方晶系的LiSbO3和四方晶系的Li3SbO4的共存物,這可能是由于片狀顆粒在高溫下更易失去結晶水。因此,在制備LiSbO3的過程中,應適當地控制形成沉淀物時的pH 和沉淀物的保存溫度。
多孔模板法是將由LiNO3和丙氨酸組成的溶液與含鹽酸的Sb2S5溶液充分混勻后,在150 ℃下磁力攪拌并用有孔的蜂窩狀樣板吸收該溶液以形成凝膠。將該凝膠在850 ℃下熱處理10 h,制備出粒徑為40~80 nm,分布均勻并呈立方結構的LiSbO3粉末[2]。將LiSbO3粉末、乙炔黑導電劑和PVDF黏結劑按質量比65:25:10 加入到甲基吡硌烷酮(NMP)溶劑,混勻后涂在銅箔上形成電池的一極,以金屬鋰作為對應電極,將LiPF6溶解于EC+DMC(體積比為1:2)的混合溶劑中,制成電解質,三者一起組裝成2032型紐扣電池,經檢測,嵌鋰電位為0.78 V(vs Li/Li+),脫鋰電位為1.1 和1.4 V(vs Li/Li+)。該粉末作為鋰離子電池的負極材料后具有196 mA·h/g的初始比容量,在100次充放電循環后能保持48%的初始比容量,而未采用多孔模板制備LiSbO3僅能保持28%的初始比容量,這種方法有效地改善了銻酸鋰的電化學性能。
水熱法是以KSb(OH)6和LiOH·H2O 為 原 料 在110 ℃的四氟內襯的水熱釜中保溫24 h,使晶體充分發育完整,取出分離的沉淀物先后用蒸餾水和丙酮洗滌除去鉀離子后,在50 ℃的空氣中干燥得到六邊形的層狀LiSb(OH)6晶體。檢測出該晶體在約210 ℃熱處理后,完全脫水得到LiSbO3晶體,LiSb(OH)6晶體由[Li2Sb(OH)6]+和[Sb(OH)6]-沿c軸排布而成,在空間群上為P31m結構[1]。采用水熱法還可以Sb2O3和高濃度LiOH為原料,按物質的量比為0.01~5.00,填充率為50~90%加入雙氧水或者蒸餾水,調節原料比,使LiOH 濃度在1~20 mol/L,然后加入到水熱釜中以1~5 ℃/min速率升溫并保持溫度在120~240 ℃,反應4~72 h后取出產物,多次浸洗除去氫氧化鋰,然后在40~100 ℃下干燥6 h得到銻酸鋰產品。在水熱轉化過程中,使Sb2O3發生溶解并且生成純度高且晶型發育良好的銻酸鋰[28-30]。
偏銻酸鋰與銻酸鋰制備方法對比如表1所示。由表1可知:干法制備工藝對反應溫度要求高,而且在高溫下會出現成分不均勻、鋰化物揮發后導致鋰與銻的配比發生偏差等問題,且可能會產生團聚現象。在濕法制備工藝中,雖然加入穩定劑可以避免銻水解,但沉淀產物中包裹有雜質離子,最終影響產品純度,且氫氧化鋰利用率較低。考慮到上述制備銻酸鋰方法的不足,本文作者提出濕法制備銻酸鋰的新技術。
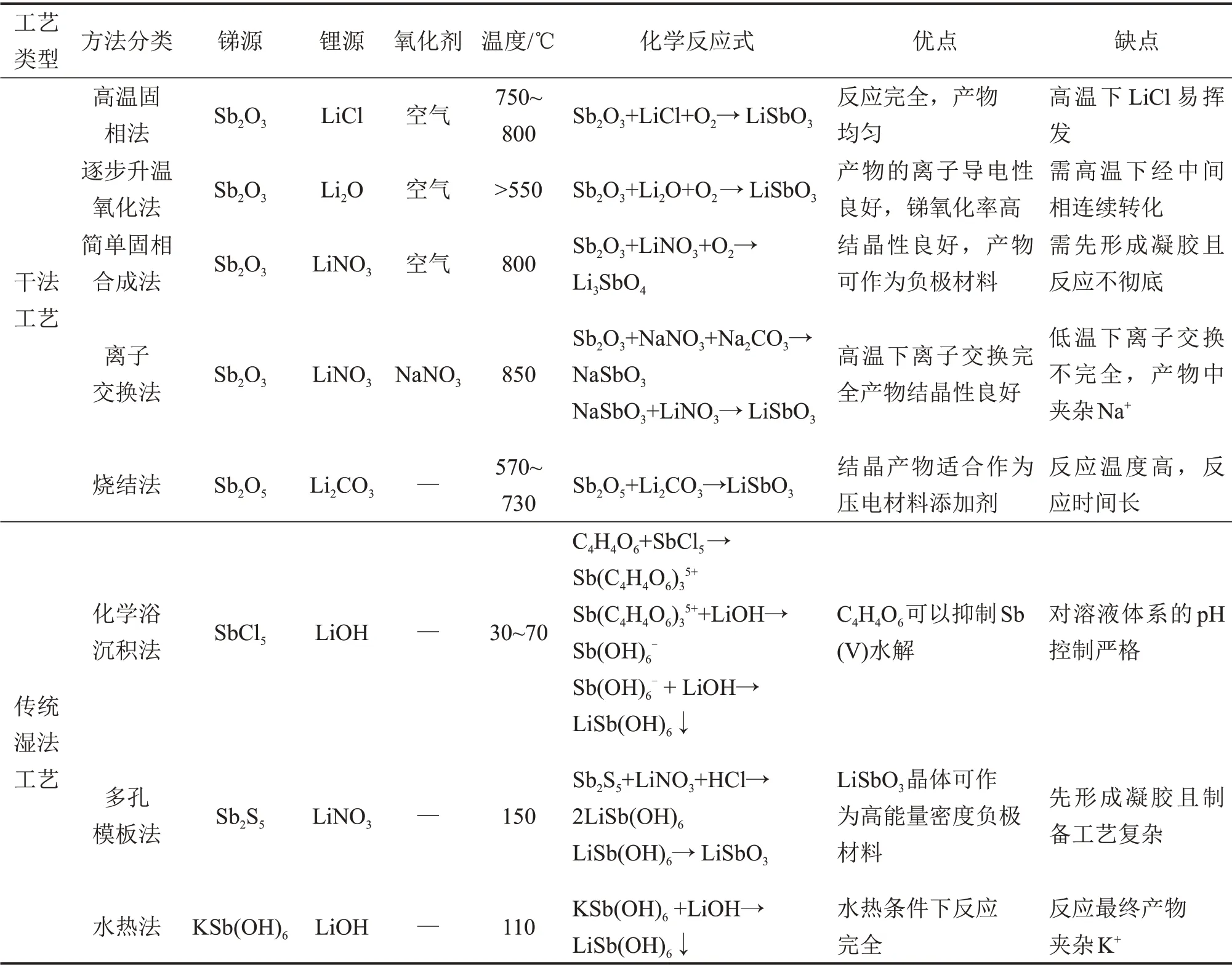
表1 偏銻酸鋰與銻酸鋰制備方法對比Table1 Comparison of preparation methods of LiSbO3 and LiSb(OH)6
2 濕法制備銻酸鋰的新技術
由于濕法制備銻酸鋰的新技術是在溶液體系下進行的,在一定程度上可以避免干法工藝中出現的產物成分不均及結晶水和鋰化物的揮發。本文提出的新技術是以銻白為原料,在常壓水溶液中以雙氧水為氧化劑制備銻酸鋰的工藝,反應條件容易控制,產物純度高,雜質離子的質量分數低,可作為制備六氟銻酸鋰的前驅體。LiSb(OH)6與LiSbF6制備流程如圖1所示。
2.1 間接鋰鹽法制備銻酸鋰的新技術
間接鋰鹽法是基于銻白為兩性氧化物,在高濃度的氫氧化鋰水溶液中溶解后生成可溶性LiSb(OH)4溶液,采用清潔氧化劑雙氧水將Sb(Ш)氧化生成銻酸鋰的沉淀。間接鋰鹽法主要發生的化學反應如下。
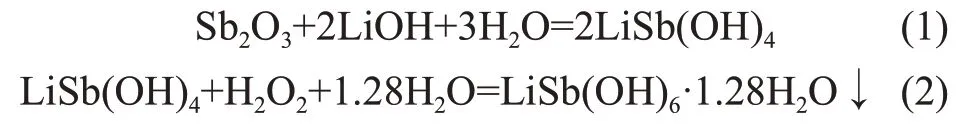
該工藝中產生的銻酸鋰沉淀物通過液固分離,沉淀物經干燥后即得到銻酸鋰產品,而濾液中仍含有大量的氫氧化鋰,可返回溶解工序繼續用于溶解銻白。該工藝在氧化沉淀過程中,發生的是液-固反應,避免了產品中包裹Sb2O3現象的發生,產品質量得以保證。
間接鋰鹽法中銻酸鋰制備過程如下:在濃度為6.40 mol/L 的氫氧化鋰水溶液中加入5 g 銻白,在90 ℃下溶解反應2 h 后趁熱過濾后得到105 mL 的LiSb(OH)4溶液,將該溶液升溫到85 ℃后,以1 mL/min的流速加入8 mL的雙氧水,氧化沉淀2 h再過濾。沉淀物在80 ℃下干燥10 h 后得到銻酸鋰產品(制備的工藝流程見圖1中的合成路線①)。本工藝中,配合溶解后液中LiSb(OH)4的質量濃度可達16.50 g/L,氧化沉淀工序中Sb(Ⅲ)的氧化率大于98%,銻沉淀率大于97%。
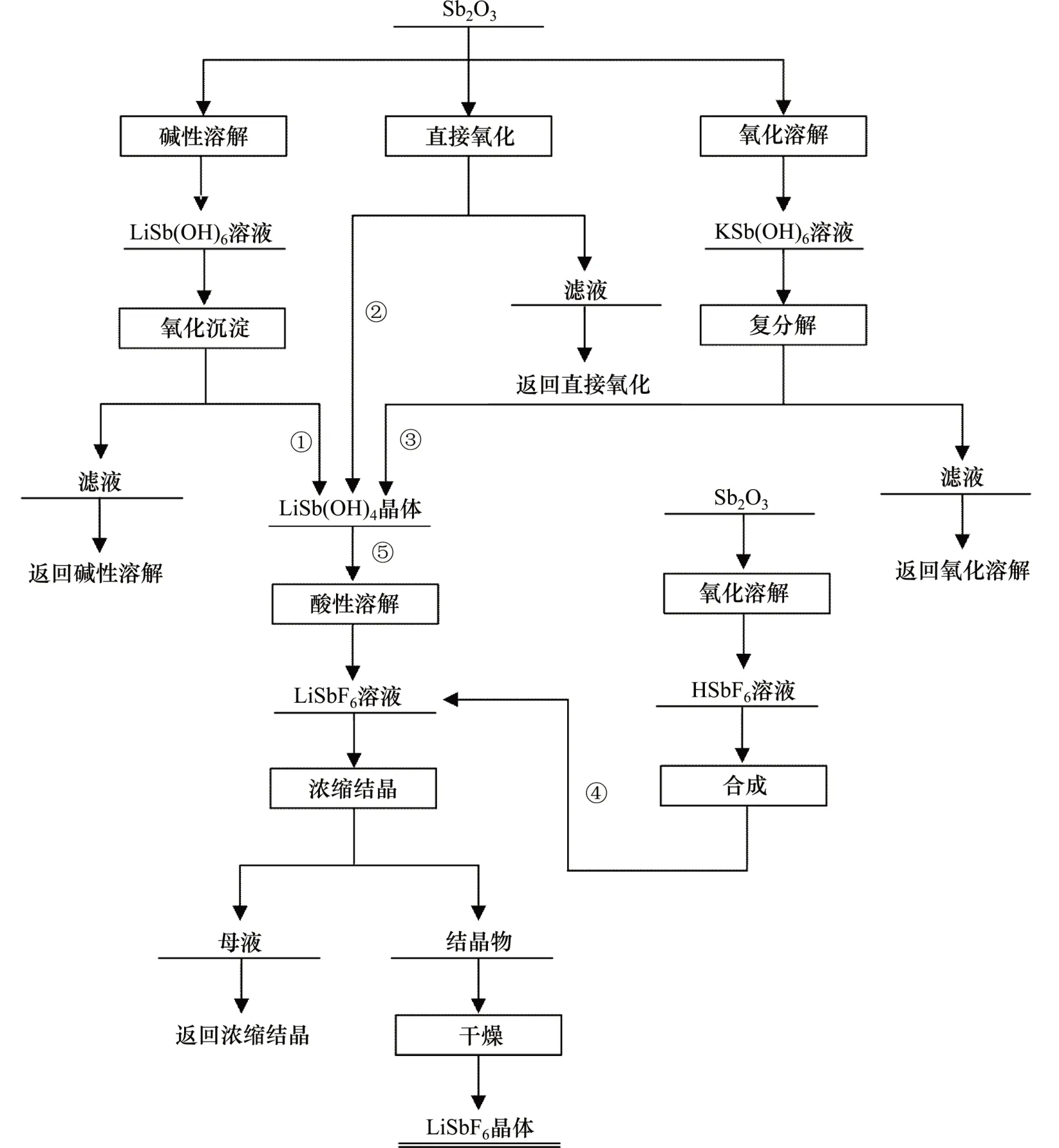
圖1 LiSb(OH)6與LiSbF6制備工藝流程圖Fig.1 Flow chart of LiSb(OH)6 and LiSbF6 preparation
不同方法制備的銻酸鋰晶體的化學成分如表2所示。由表2可以看出:間接鋰鹽法制備的銻酸鋰晶體中Li 和Sb 的質量分數接近理論值,Sb(Ⅲ)質量分數小于0.01%,說明該產品中鋰與銻的化學配比精準,Sb(Ⅲ)氧化完全。
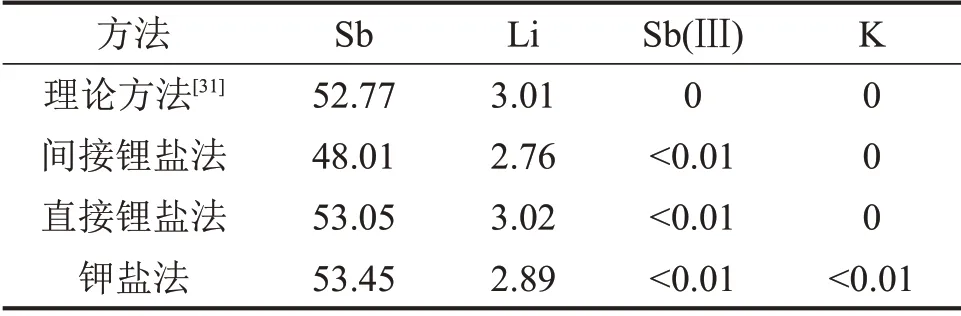
表2 不同方法制備的銻酸鋰晶體的化學成分(質量分數)Table2 Chemical composition of crystalline LiSb(OH)6 prepared by different methods %
不同方法制備的銻酸鋰晶體的X線衍射(XRD)圖譜如圖2所示。由圖2(a)可知:間接鋰鹽法制備的銻酸鋰物相以LiSb(OH)6·1.28H2O 的形態均勻分布,可能是因為在高濃度LiOH溶液體系下有部分水分子參與氧化沉淀而以結晶水的形態固化在產物中。
不同方法制備的銻酸鋰晶體的掃描電子顯微鏡(SEM)圖譜如圖3所示。由圖3(a)和(b)可知:間接鋰鹽法制備的沉淀產物形貌為分布均勻的六方柱結構。
2.2 直接鋰鹽法制備銻酸鋰的新技術
Sb2O3在氫氧化鋰溶液中,以雙氧水作為氧化劑直接將Sb(Ш)氧化成Sb(V)并以難溶性的LiSb(OH)6沉淀析出,其化學反應如下:
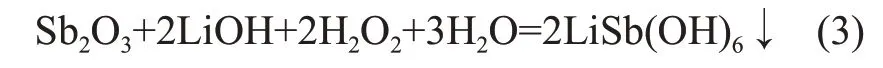
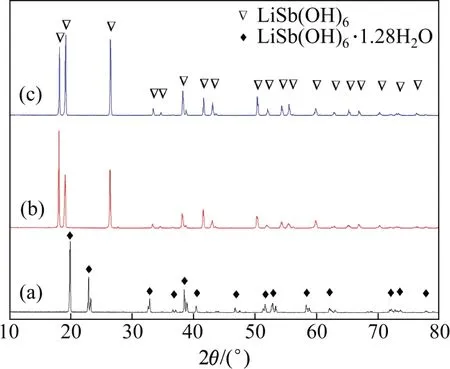
圖2 不同方法制備的銻酸鋰晶體的XRD圖譜Fig.2 XRD patterns of LiSb(OH)6 crystals with different methods
直接鋰鹽法具有工藝流程短,銻酸鋰的產率及氫氧化鋰利用率高的特點,但該方法是一種液相體系下的固-固轉化反應,如果條件控制不當就會出現銻酸鋰產品中包裹銻白的現象,因此,需要按照制備條件進行強化反應以消除這種包裹現象。
直接鋰鹽法制備銻酸鋰的工藝如下:向300 mL濃度為0.27 mol/L 的LiOH 水溶液,按液固比為30:1加入銻白10 g,在85 ℃下以1 mL/min 的流速加入11 mL 的雙氧水后反應4 h,再轉移至25 ℃的冷水浴中攪拌冷卻0.5 h后過濾。沉淀物在80 ℃的烘箱中干燥10 h 后得到銻酸鋰產品(制備工藝流程見圖1中的路線②)。本工藝中,Sb(Ⅲ)的氧化率大于98.5%,銻沉淀率大于98%。由表2還可以看出:直接鋰鹽法制備的沉淀產物中Li和Sb的質量分數同樣接近理論值,Sb(Ⅲ)質量分數小于0.01%,說明銻氧化完全,產品中LiSb(OH)6的純度高(≥98%)。從圖2(b)可知:直接鋰鹽法制備的沉淀物物相組成為單相的LiSb(OH)6,結晶發育良好。從圖3(c)和(d)可知:沉淀物微觀形貌為分布均勻的六邊形層狀結構,晶粒完整。

圖3 不同方法制備的銻酸鋰晶體的SEM照片Fig.3 SEM images of LiSb(OH)6 crystals prepared by different methods
2.3 鉀鹽法制備銻酸鋰的新技術
銻白在氫氧化鉀雙氧水體系下被氧化生成溶解度大的銻酸鉀溶液,向該溶液中加入氫氧化鋰后沉淀出粗銻酸鋰。粗銻酸鋰中一般含有4%~5%(質量分數)的鉀,用低濃度的氫氧化鋰水溶液充分洗滌凈化后二次沉淀出的高純銻酸鋰產品,發生的化學反應如下。
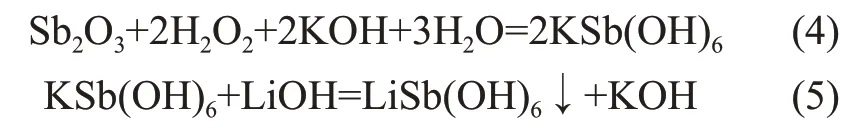
在氧化溶解過程中銻白溶解率達99.9%,在復分解沉淀工序中,銻的沉淀率可達95%以上。鉀鹽法制備銻酸鋰的過程為液相體系中的液-固轉化反應,避免了Sb2O3夾雜于沉淀物中,且經過低濃度的氫氧化鋰溶液洗滌后不僅可除去K+,而且由于Li+的同離子效應能降低銻酸鋰的溶解度使其產率提高。
鉀鹽法制備銻酸鋰的工藝過程如下:取10 g的銻白加入到100 mL 濃度為1.5 mol/L 的KOH 水溶液中,在85 ℃下以1 mL/min的流速加入21.20 mL的雙氧水進行氧化溶解,0.5 h 后過濾。將濾液升溫到85 ℃后,以1 mL/min的流速加入濃度為3.45 mol/L的氫氧化鋰水溶液20 mL 進行復分解沉淀反應,2 h 后轉移至室溫下冷卻,40 h后過濾;將粗銻酸鋰轉移至體積為700 mL,溫度為90 ℃的熱水中,攪拌溶解完全后再加入LiOH?H2O,使其在水溶液中維持0.2 mol/L的濃度,二次沉淀0.5 h后過濾,沉淀物在80 ℃下干燥10 h后得到銻酸鋰產品(制備的工藝流程見圖1中路線③)。從表2可知:鉀鹽法制備的沉淀產物中Li 和Sb的化學配比精準,K+和Sb(Ⅲ)質量分數均低于0.01%,說明凈化除鉀徹底且產物純度高(≥98%)。從圖2(c)可知:本法制備的沉淀物的物相組成為單一的LiSb(OH)6且結晶程度良好。從圖3(e)和(f)可知:本法制備的銻酸鋰為分布均勻的六邊形層狀結構。這進一步表明鉀鹽法和直接鋰鹽法制備的銻酸鋰在物相和微觀形貌上基本一致。
3 六氟銻酸鋰制備的新技術
3.1 六氟銻酸鋰制備的研究進展
六氟銻酸鋰制備的傳統方法為氫氟酸溶劑法[8-9],其主要制備過程如下:在無水氫氟酸體系中加入SbF5和LiF,反應生成LiSbF6溶液,產物經過濃縮結晶析出LiSbF6晶體,其化學反應方程如下。
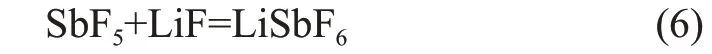
該方法采用腐蝕性極強的無水氫氟酸為反應介質,條件苛刻,而且SbF5的制備比較復雜,整體上這種生產工藝所需的成本較高。因此,為從工藝上解決LiSbF6的制備難題,本文提出2種在水溶液體系下制備六氟銻酸鋰的方法。第1 種方法為六氟銻酸法,即在水溶液體系中Sb2O3與氫氟酸和雙氧水進行氧化溶解反應后制備出HSbF6溶液,然后加入鋰源(Li2CO3)與HSbF6反應生成LiSbF6溶液,該溶液經過濃縮、結晶和干燥后得到LiSbF6晶體。第2種為銻酸鋰法,即以銻酸鋰為前驅體制備LiSbF6的方法。首先將LiSb(OH)6加入到HF 水溶液反應后產生LiSbF6溶液,然后經過濃縮結晶、干燥后得到LiSbF6晶體。與傳統制備方法比較,這2 種方法具有反應條件溫和、綜合成本低和產品質量較好的優勢,有望成為高效生產六氟銻酸鋰晶體的新技術。
3.2 六氟銻酸法制備六氟銻酸鋰的新技術
利用Sb2O3為原料直接通過六氟銻酸法制備六氟銻酸鋰可以減少中間前驅體銻酸鋰的制備。該法的基本原理是銻白在氫氟酸雙氧水體系下氧化溶解,使Sb(Ш)被氧化為Sb(V)并與F-配位生成HSbF6的強酸溶液,加入Li2CO3作為鋰源反應生成LiSbF6鹽溶液,該溶液經過濃縮、結晶和干燥后得到LiSbF6晶體。
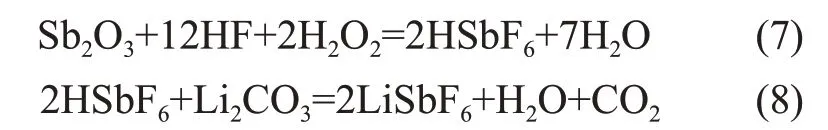
六氟銻酸法制備六氟銻酸鋰的工藝過程如下:稱取20 g 銻白,蒸餾水與銻白液固比為7:1(mL/g)加入300 mL 聚四氟乙烯燒杯中,在85 ℃下緩慢加入36.50 mL 的氫氟酸水溶液,同時按1 mL/min 的流速加入25 mL 的雙氧水,氧化反應2 h 后生成HSbF6溶液再過濾。將氧化后液裝入聚四氟乙烯燒杯中,在85 ℃下加入5.20 g 碳酸鋰反應1 h 后生成LiSbF6鹽溶液再次過濾。將反應后液裝入聚四氟乙烯燒杯,在95 ℃下濃縮至料液密度為2.5 g/cm3后,在25 ℃下水浴冷卻結晶4 h 后過濾,將結晶物在110 ℃下干燥15 h,得到LiSbF6晶體(制備工藝流程見圖1中路線④)。本工藝中,Sb(Ⅲ)的氧化率大于99%,中和轉化率接近100%。
不同方法制備的六氟銻酸鋰晶體的化學成分如表3所示。從表3可知:六氟銻酸法制備的六氟銻酸鋰晶體中Li,Sb和F的質量分數與理論值接近,說明其純度極高(≥98%)。不同方法制備的六氟銻酸鋰晶體的XRD圖譜如圖4所示。由圖4(b)可知:本法制備的結晶物的物相組成為單一的LiSbF6,衍射峰的位置和相對強度與粉末衍射文件(PDF 卡片)中標準的LiSbF6的衍射峰位置基本一致。不同方法制備的六氟銻酸鋰晶體的紅外光譜圖(FT-IR)如圖5所示。由圖5(a)可知:在波數為550~850 cm-1的范圍內存在SbF-6的特征峰,在1 636 cm-1附近存在Li-Sb 化學鍵的特征峰,在 3 480 cm-1附近主要為O-H 的特征峰,這與文獻[9]中的結果基本符合。
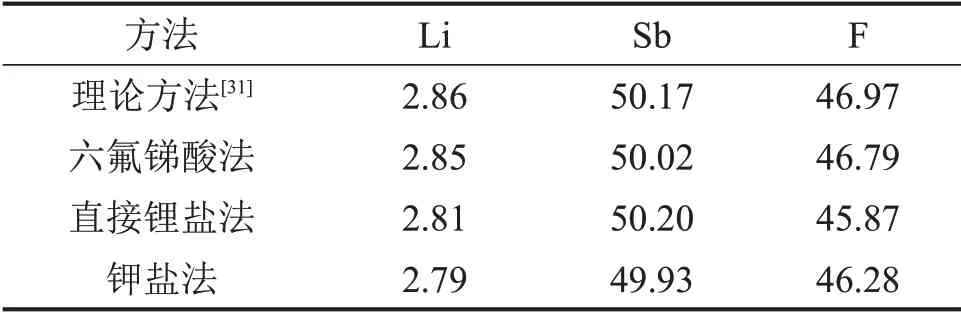
表3 不同方法制備的六氟銻酸鋰晶體的化學成分(質量分數)Table3 Chemical composition of crystalline LiSbF6 prepared by different methods %
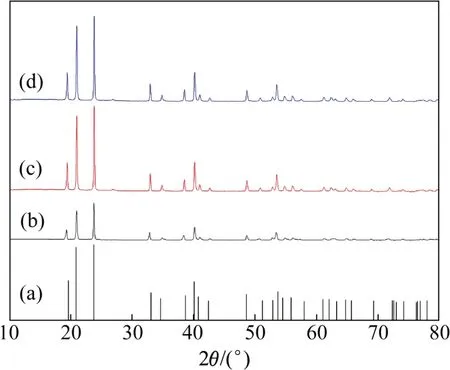
圖4 不同方法制備的六氟銻酸鋰晶體的XRD圖譜Fig.4 XRD pattern of crystalline LiSbF6 prepared by different methods
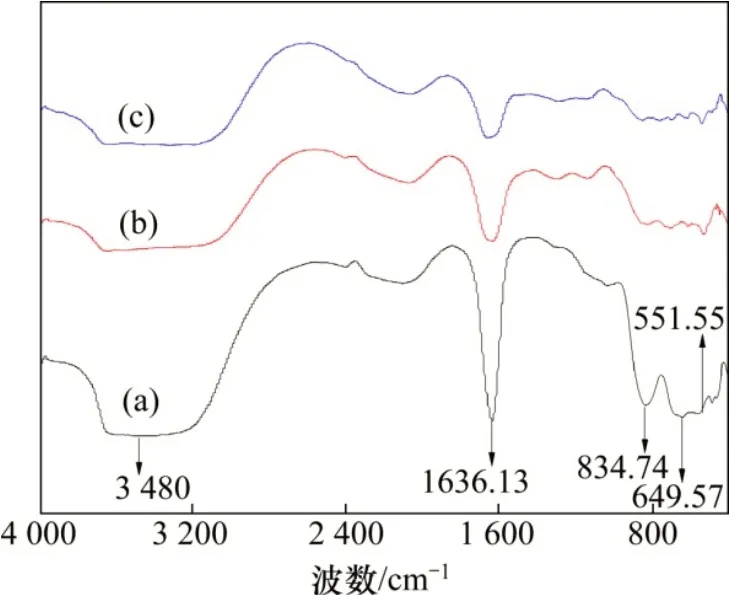
圖5 不同方法制備的六氟銻酸鋰晶體的紅外光譜圖Fig.5 Infrared spectrum of crystalline LiSbF6 with different methods
3.3 銻酸鋰法制備六氟銻酸鋰的新技術
銻酸鋰的一個重要用途是作為制備六氟銻酸鋰的前驅體。因此,本文進一步提出制備六氟銻酸鋰的新工藝。首先,利用LiSbF6中Sb-F 與LiSb(OH)6中Sb-OH 在鍵長、結合力上存在的差異,作為制備LiSbF6晶體的出發點。在氫氟酸體系下LiSb(OH)6進行酸性溶解反應生成溶解度大的LiSbF6鹽溶液。此外,銻酸鋰前驅體中含有的少量的Sb2O3可以通過向溶液中加入雙氧水氧化生成HSbF6后再與LiF 反應生成LiSbF6溶液。制備的LiSbF6鹽溶液經濃縮結晶、干燥后得到LiSbF6晶體,主要的化學反應如下:
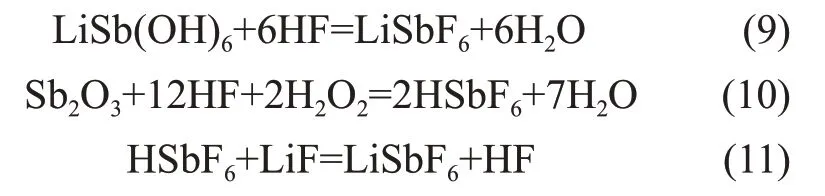
銻酸鋰法制備六氟銻酸鋰的工藝過程如下:取15 g銻酸鋰加入到裝有50 mL的蒸餾水的聚四氟乙烯燒杯中,在85 ℃下緩慢加入體積為17.40 mL 氫氟酸水溶液,并按雙氧水與銻酸鋰體積液固比1:4(mL/g)的比例加入雙氧水(3.75 mL的H2O2),中和反應2 h后過濾。將中和后濾液裝入聚四氟乙烯燒杯中,然后再添加0.20 g 的LiF,在80 ℃下反應2 h 后過濾,濾液在95 ℃下濃縮至料液密度為2.5 g/cm3,然后在25 ℃下冷卻結晶4 h 后過濾,將結晶物在110 ℃下干燥16 h后得到LiSbF6晶體(工藝流程見圖1中路線⑤)。本工藝中,反應物中Sb(Ⅲ)氧化率大于97%,酸性溶解反應完全。
從表3可知:在以直接鋰鹽法和鉀鹽法制備的銻酸鋰為前驅體,經過銻酸鋰法合成的LiSbF6晶體中,Li,Sb和F的質量分數與理論值極為接近,說明產物純度極高(≥98%)。從圖4(c)和(d)可知:本文制備的結晶產物的物相組成均為單一的LiSbF6相,且這些衍射的峰位置和相對峰強均與PDF 卡中標準LiSbF6完全一致,進一步說明制備的六氟銻酸鋰純度高、結晶程度良好。圖5(b)和(c)所示的紅外光譜結果與圖5(a)的基本相同,說明六氟銻酸鋰產品與六氟銻酸法制備的LiSbF6產品基本一樣。
與傳統的六氟銻酸鋰制備方法相比,上述2種方法具有如下特點:1)所需的氫氟酸質量分數為40%,與傳統無水氫氟酸相比對設備的要求降低;2)以Sb2O3和LiSb(OH)6作為原料,省去LiF和SbF5的復雜制備過程;3)反應條件容易控制,氧化劑為清潔的雙氧水,不會引入其他雜質。銻酸鋰與六氟銻酸鋰制備的新技術對比見表4。總體來看,這些關鍵新技術實現了對傳統的制備六氟銻酸鋰工藝的改進,為2種銻深加工產品的合成提供了新思路。
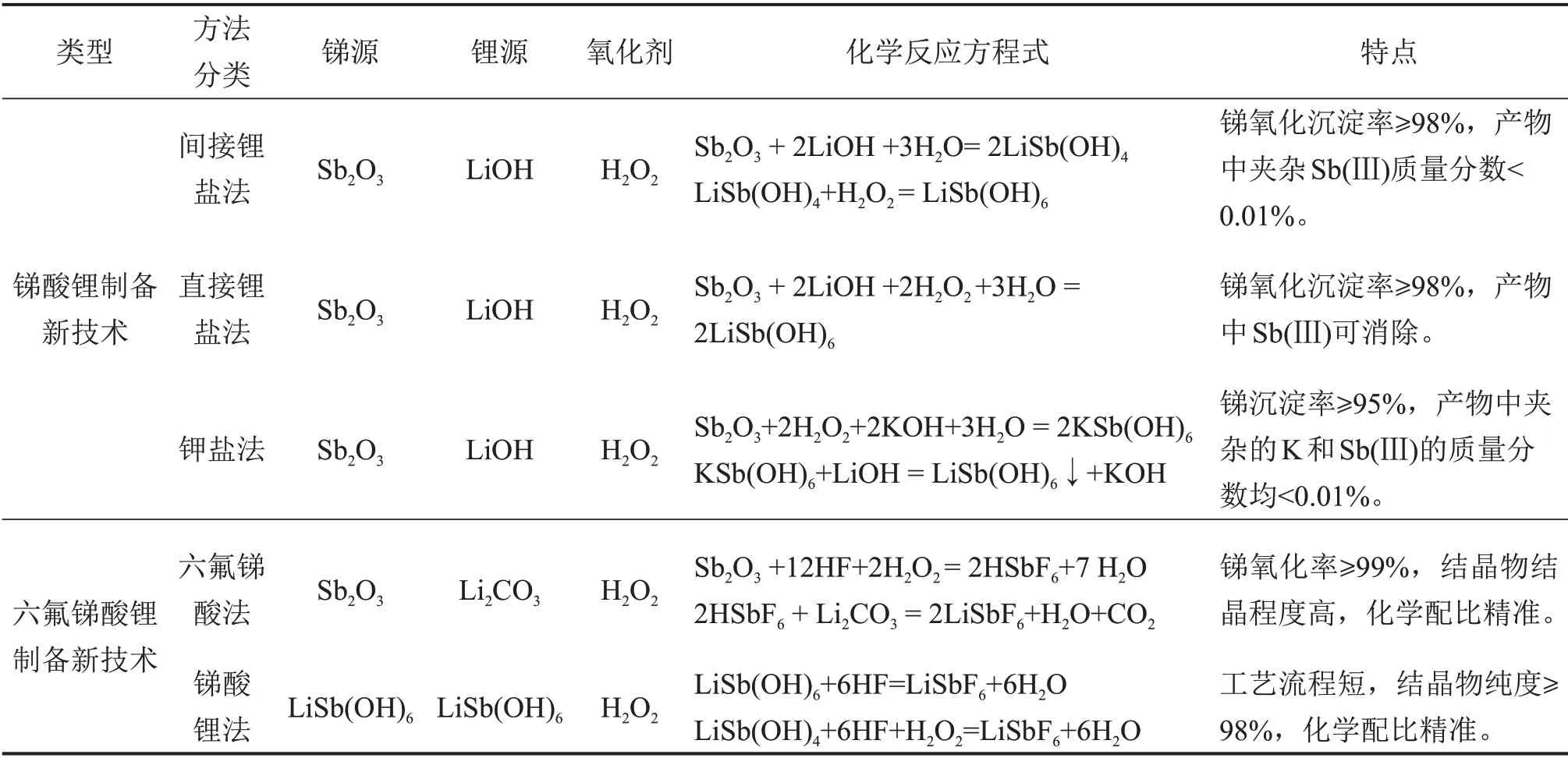
表4 銻酸鋰與六氟銻酸鋰制備新技術對比Table4 Comparison of novel technologies for preparation of LiSb(OH)6 and LiSbF6
4 結論
1)以Sb2O3為主要原料,分別通過間接鋰鹽法、直接鋰鹽法和鉀鹽法3種新技術制備LiSb(OH)6晶體,制備出的晶體化學配比精準、物相組成單一,Sb(Ⅲ)質量分數均低于0.01%且形貌為分布均勻的六邊形層狀和六方柱2種結構。
2)提出了以LiSb(OH)6和Sb2O3為原料,分別通過銻酸鋰法和六氟銻酸法制備六氟銻酸鋰的新技術,制備出的LiSbF6晶體的物相單一、產品純度高(≥98%),存在SbF6-的特征振動峰。
3)本文提出的3 種制備LiSb(OH)6的新技術實現了對傳統制備方法的改進,制備的LiSb(OH)6可作為合成LiSbO3和LiSbF6的前驅體;2種制備LiSbF6晶體的新技術也實現了對傳統制備工藝的技術提升,制備的LiSbF6晶體可作為具有良好應用前景的鋰離子電池電解質鋰鹽。

