唑來膦酸治療惡性腫瘤高鈣血癥的臨床效果及對不良反應發生的影響
何林莉


【摘要】 目的:探討唑來膦酸治療惡性腫瘤高鈣血癥的臨床效果及不良反應發生。方法:選取2016年5月-2017年7月在筆者所在醫院進行治療的惡性腫瘤高鈣血癥患者96例,隨機分為兩組,對照組采取帕米膦酸二納進行治療,研究組采取唑來膦酸進行治療。比較兩組血鈣值的變化、不良反應發生率和生命質量(QOL)評分。結果:對照組血鈣值的變化明顯差于研究組,研究組的不良反應發生率明顯低于對照組,研究組的生命質量評分明顯高于對照組,差異均有統計學意義(P<0.05)。結論:采取唑來膦酸對惡性腫瘤高鈣血癥進行治療,取得了理想的臨床治療效果,具有很高的安全性,不良反應較少,有利于疾病的康復,改善生活質量,值得進一步在各大醫院的臨床治療上進行推廣。
【關鍵詞】 唑來膦酸; 惡性腫瘤高鈣血癥; 不良反應; 生命質量
doi:10.14033/j.cnki.cfmr.2019.21.049 文獻標識碼 B 文章編號 1674-6805(2019)21-0-03
很多臨床研究表明,高鈣血癥是惡性腫瘤的常見代謝并發癥,臨床表現為腫瘤侵犯骨骼,增強了破骨細胞活性,誘導體內骨溶解、骨吸收,導致大量骨骼鈣在血內釋放[1]。隨著人們生活節奏的加快和飲食結構的改變,惡性腫瘤高鈣血癥發病率正在逐年上升,發病機制具有復雜性,大多數與患者體內維生素D3水平和前列腺素水平等有關系,該病對患者的身心健康造成一定的影響[2]。對惡性腫瘤高鈣血癥主要是采取藥物治療,高鈣血癥藥物主要選取抑制腎小管對鈣重吸收和減少骨吸收,帕米膦酸二納和唑來膦酸是惡性腫瘤高鈣血癥主要的治療藥物[3]。而唑來膦酸是第三代雙膦酸鹽類藥物的一種,藥效起效快,易于被患者所接受[4]。本研究中,選取在筆者所在醫院進行治療的惡性腫瘤高鈣血癥患者96例,對唑來膦酸治療惡性腫瘤高鈣血癥的臨床效果及對不良反應發生的影響進行探討,現具體報告如下。
1 資料與方法
1.1 一般資料
選取2016年5月-2017年7月在筆者所在醫院進行治療的惡性腫瘤高鈣血癥患者96例。納入標準:(1)均符合惡性腫瘤高鈣血癥診治標準[3];(2)凝血功能正常;(3)沒有認知功能障礙病史。排除標準:(1)存在精神疾病病史;(2)心肺功能出現障礙;(3)對本研究藥物有過敏現象。隨機分為兩組,對照組48例,男29例,女19例,年齡29~69歲,平均(47.5±0.4)歲。病程3~16個月,平均(9.7±0.4)個月。研究組48例,男31例,女17例,年齡31~68歲,平均(45.2±0.6)歲。病程1~13個月,平均(10.3±0.2)個月。兩組一般資料比較,差異無統計學意義(P>0.05),存在可比性。本研究在筆者所在醫院倫理委員會處經過了審核與批準。所有患者均知曉同意此次研究。
1.2 方法
1.2.1 對照組 采取帕米膦酸二納(仁怡,南京正大天晴公司,批號:0912141、0912143、1003103)進行治療,在住院期間對患者進行各項生命體征的監測,向患者及其家屬詳細的講解關于疾病的相關知識和注意事項,當體內的血鈣<3.0 mmol/L時,選取靜脈注射的方式,將30 mg的帕米磷酸二鈉與250 ml的5%葡萄糖靜脈相融合注入患者體內,注射2 h以上;當患者體內的血鈣3.0~3.5 mmol/L時,將60 mg的帕米磷酸二鈉與500 ml的5%葡萄糖靜脈相融合注入患者體內,注射4 h以上;當患者體內的血鈣大于3.5 mmol/L時,將90 mg的帕米磷酸二鈉與
750 ml的5%葡萄糖靜脈相融合注入患者體內,注射6 h以上。2次/d,兩周為1個療程。
1.2.2 研究組 采取唑來膦酸(擇泰,諾華公司,批號:S0024、S0142)進行治療,在住院期間對患者進行各項生命體征的監測,向患者及其家屬詳細的講解關于疾病的相關知識和注意事項,選擇靜脈注射的方式,將4 mg唑來膦酸與100 ml 0.9%氯化鈉注射液注入患者體內,注射時間為15 min,2次/d,兩周為1個療程。
在對兩組患者進行治療前2 d內,保證兩組患者擁有足夠的補液量。并且在使用過程中水化、利尿,并對鈣攝入進行限制。
1.3 觀察指標
統計并比較兩組血鈣值的變化及不良反應(骨痛、腎功能異常、發熱和嘔吐)。專業醫護人員對兩組QOL(生活質量)評分進行評定,包括身體狀況、行為、社會活動和自評生活質量,滿分100分,分數越高表示患者的QOL越高[5]。
1.4 統計學處理
數據應用SPSS 20.0進行分析,計量資料以(x±s)表示,采用t檢驗,計數資料以率(%)表示,采用字2檢驗,P<0.05為差異有統計學意義。
2 結果
2.1 兩組血鈣值變化對比
治療前兩組血鈣值對比差異無統計學意義(P>0.05),治療后1、4、7 d對照組的血鈣值變化明顯差于研究組(P<0.05),見表1。
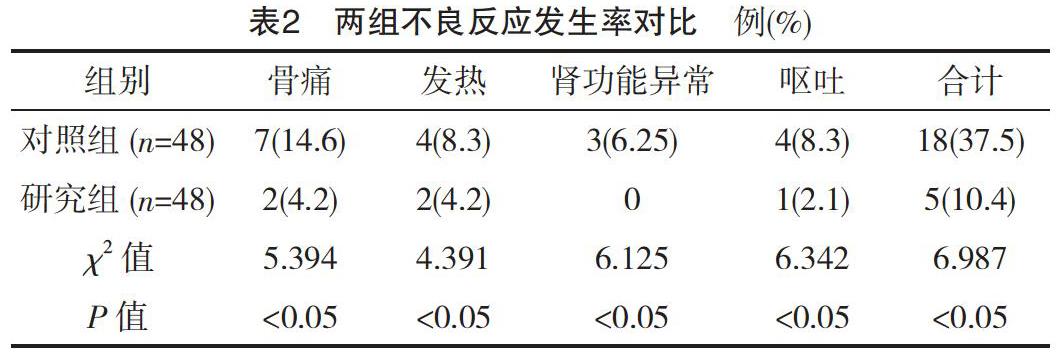
2.2 兩組不良反應發生率對比
研究組的不良反應發生率明顯低于對照組(P<0.05),見表2。
2.3 兩組QOL評分對比
對照組的QOL評分明顯低于研究組(P<0.05),見表3。
3 討論
很多臨床研究表明,惡性腫瘤并發的高鈣血癥與骨病變和骨轉移息息相關,該疾病是常見代謝性疾病的一種,嚴重威脅患者的生命健康[6]。治療該疾病的主要藥物中要含有內源性焦磷酸鹽類似物的雙磷酸鹽,主要是依附在骨骼羥磷灰石結晶上[7]。用來代替骨基質中的焦磷酸鹽含量,藥理上是抑制著破骨細胞的產生[8]。并且對破骨細胞對骨的吸收起到一定的阻礙作用,對破骨細胞起的抑制作用聯系著側鏈結構,對患有惡性腫瘤并發的高鈣血癥進行藥物治療取得理想的效果[9]。
唑來膦酸是一種新型的雙磷酸鹽類藥物,其主要的藥物機制包括:(1)對破骨細胞對骨的破壞具有直接性的阻礙;(2)不僅抑制了焦磷酸法尼基合成酶的活性,還對甲醛戊酸生物合成通路起到了一定的抑制作用[10-11]。進而將破骨細胞的活力進行抑制,間接地促進破骨細胞盡早地死亡[12-13]。(3)能夠阻止破骨細胞的前體細胞進行轉化,避免轉化為成熟的破骨細胞[14-15]。
(4)當破骨細胞合成并釋放一些疼痛和炎性介質時,能夠進行及時的抑制[16-17]。處于較低濃度的唑來膦酸不會影響成骨細胞增殖分化,反而可以利用成骨細胞護骨素對破骨細胞的骨吸收功能起到間接性的抑制作用,再則促進了軟骨的再吸收與骨骼結合阻滯礦物質骨結合下,起到了一系列的抑制作用,主要體現在對患者體內骨鈣的釋放和破骨細胞活性的異常增加的情況上,對患者體內磷和血清鈣水平起到了降低作用,促進患者度體內尿鈣和磷進行排泄[18-19]。本研究中,對照組血鈣值的變化明顯差于研究組(P<0.05),表明,采取唑來膦酸對惡性腫瘤高鈣血癥進行治療,取得了理想的臨床治療效果,有利于疾病的康復,改善生活質量。
但是少數患者在服用唑來膦酸藥物會存在不良反應,會出現骨痛、發熱、腎功能異常、嘔吐等一系列癥狀,還可能會影響患者的腎功能,但是與服用帕米膦酸二納藥物相比,出現腎功能虧損的情況較少,且不良反應發生率明顯低。本研究中,研究組的不良反應發生率明顯低于對照組(P<0.05)。表明,采取唑來膦酸對惡性腫瘤高鈣血癥進行治療,取得了理想的臨床治療效果,藥物的不良反應較少,具有很高的安全性。
綜上所述,采取唑來膦酸對惡性腫瘤高鈣血癥進行治療,取得了理想的臨床治療效果,具有很高的安全性,藥物的不良反應較少,有利于患者疾病的康復,改善生活質量,值得進一步在各大醫院的臨床治療上進行推廣。
參考文獻
[1]何斌,蔡雅霜,張志剛,等.雙膦酸鹽類藥物用于腫瘤輔助治療的臨床研究進展[J].中國新藥與臨床雜志,2018,37(4):185-192.
[2]李嘉,付婷婷,馬元琛,等.唑來膦酸聯合甲狀旁腺激素對椎體壓縮性骨折術后影響的臨床研究[J].中國骨質疏松雜志,2017,23(5):647-651.
[3] Billington E O,Horne A,Gamble G D,et al.Effect of single-dose dexamethasone on acute phase response following zoledronic acid:a randomized controlled trial[J].Osteoporosis International,2017,28(6):1867-1874.
[4]張鐸安,黨興,陳兆興.唑來膦酸結合鈣爾奇對老年腦梗死合并骨質疏松癥患者療效影響的臨床研究[J].中國骨質疏松雜志,2017,23(11):1468-1471.
[5] Aubry S,Dubut J,Nueffer J P,et al.Prospective 1-year follow-up pilot study of CT-guided microwave ablation in the treatment of bone and soft-tissue malignant tumours[J].European Radiology,2016,27(4):1477-1485.
[6]李鵬飛,賈楠,侯素平,等.伊班膦酸與唑來膦酸治療脊柱骨巨細胞瘤的療效及安全性[J].腫瘤,2016,36(3):334-339.
[7] Blanchette P S,Desautels D N,Pond G R,et al.Factors influencing survival among patients with HER2-positive metastatic breast cancer treated with trastuzumab[J].Breast Cancer Research & Treatment,2018,170(11):1-9.
[8]余德濤,王雷,邢貞武.唑來膦酸聯合經皮椎體成形術治療骨質疏松性椎體壓縮骨折的臨床研究[J].中國藥房,2017,28(29):4137-4139.
[9] Frazier A L,Stoneham S,Rodriguezgalindo C,et al.Comparison of carboplatin versus cisplatin in the treatment of paediatric extracranial malignant germ cell tumours:A report of the Malignant Germ Cell International Consortium[J].European Journal of Cancer,2018,24(11):30-37.
[10]關媛,高燕玲,李貴慶.唑來膦酸注射液治療高齡老年性骨質疏松的藥物不良反應發生情況研究[J].中國全科醫學,2017,20(28):77-81.
[11]劉智楠,鄭慧,郭向輝.西那卡塞片聯合骨化三醇膠丸治療血液透析伴高鈣血癥的臨床研究[J].中國臨床藥理學雜志,2017,33(23):2381-2383.
[12]袁志峰,劉會文.唑來膦酸、伊班膦酸鈉及阿倫膦酸鈉防治絕經后骨質疏松癥的療效對比研究[J].中國骨質疏松雜志,2018,24(2):23-25.
[13] Pinkawa M.Zoledronic Acid in first-line Treatment of prostate cancer[J].International Journal of Radiation Oncology Biology Physics,2017,97(1):6.
[14]張儒,吳鵬.唑來膦酸聯合瑞舒伐他汀輔助治療老年骨質疏松性椎體壓縮性骨折臨床觀察[J].中國骨質疏松雜志,2018,24(3):56-58.
[15] Davison M R,Lyardet L,Preliasco M,et al.Experimental model of osteonecrosis of the jaw associated to bisphosphonates(ONJBPs) in ewes chronically treated with high doses of zoledronic acid[J].Bone,2016,89(13):68.
[16]史光彩,崔麗,郝麗,等.骨化三醇治療維持性血液透析患者甲狀旁腺功能亢進的臨床療效[J].中國現代醫學雜志,2017,27(19):74-78.
[17] Abe T,Sato T,Kokabu S,et al.Zoledronic acid increases the circulating soluble RANKL level in mice,with a further increase in lymphocyte-derived soluble RANKL in zoledronic acid- and glucocorticoid-treated mice stimulated with bacterial lipopolysaccharide[J].Cytokine,2016,83(25):1-7.
[18] Majithia N,Atherton P J,Lafky J M,et al.Zoledronic acid for treatment of osteopenia and osteoporosis in women with primary breast cancer undergoing adjuvant aromatase inhibitor therapy:a 5-year follow-up[J].Supportive Care in Cancer,2016,24(3):1219-1226.
[19] Nagy D I,Grün A,Lévay K,et al.Efficient syntheses of zoledronic acid as an active ingredient of a drug against osteoporosis[J].Synthetic Communications,2018,48(6):1-9.
(收稿日期:2019-03-05) (本文編輯:何玉勤)

