長鏈非編碼RNA FGF14-IT1在人胃癌組織和細胞中的表達及臨床意義*
姚 林,譚 望,向萬平,唐翎翰,肖江衛
(1.川北醫學院附屬醫院胃腸外科/川北醫學院肝膽胰腸疾病研究所,四川南充 637000;2.成都醫學院第一附屬醫院胃腸外科,四川成都 610500)
胃癌是影響人類健康的一類重大疾病,是世界上第四大常見癌癥和第二大癌癥死因[1]。據統計,中國每年大約有679 100例新增胃癌患者,胃癌是中國人癌癥死亡的第二大原因,在中國由于超過80%的胃癌患者都是在晚期被確診,所以胃癌的5年生存率很低[2]。探明胃癌發生、發展及侵襲轉移的分子機制,對提高胃癌療效有著重要的意義,為胃癌患者個體化治療方案的制訂提供可能。在真核生物中,非編碼RNA的數量非常多,遠遠超過了編碼蛋白質的基因的數量。其中有很大比例的非編碼RNA在RNA轉錄過程中長度超過200個核苷酸,這類RNA往往缺乏明顯的開放閱讀框,并且目前沒有明顯的證據證明他們具有編碼蛋白質的功能,因此被定義為長鏈非編碼RNA(lncRNA)[3-5]。研究發現,在胃癌的發生、發展過程中存在許多異常表達的lncRNA,它們與腫瘤的增殖、凋亡、侵襲、轉移和不良的預后有著緊密的聯系[6-9]。本研究探討了課題組新發現的lnc RNA FGF14-IT1在胃癌組織和細胞中的表達差異,與臨床病理特征的關系及臨床價值。
1 資料與方法
1.1一般資料 收集2017年1月至2018年12月川北醫學院附屬醫院胃腸外科83例胃癌患者胃癌組織及其配對的距離癌組織5 cm外的癌旁胃黏膜組織標本,術后都經病理檢查證實。所有患者術前未進行放療、化療及其他抗腫瘤治療。83例患者中男68例、女15例,男女比例為4.53∶1.00;發病年齡40~79歲,中位年齡63歲;腫瘤直徑1~12 cm,平均直徑(4.3±2.05)cm。術后病理TNM分期中Ⅰ期患者9例,Ⅱ期患者16例,Ⅲ期患者55例,Ⅳ期患者3例。采集標本前均經患者同意并簽署知情同意書。組織標本取得后立即浸入液氮中迅速降溫,隨后放置于-80 ℃冰箱內保存。記錄患者的臨床及病理資料,包括性別、年齡、實驗室檢查、病史、臨床分期和病理類型,并隨訪。
1.2儀器與試劑 4種胃癌細胞株AGS、MGC-803、BGC-823、SGC-7901及正常胃黏膜細胞(GES-1)均購自上海中科院細胞庫。RNA提取試劑Trizol購自美國Invitrogen公司、cDNA合成試劑盒購自美國Promega公司、實時熒光定量聚合酶鏈反應(qPCR)試劑購自瑞士Roche公司。人FGF14-IT1引物及內參β-肌動蛋白(β-actin)引物均使用Primer Premier 6.0引物設計軟件設計。FGF14-IT1引物,上游:5′-TGG GAA TTG CAA AGG CTT AC-3′,下游:5′-TGG ACA TCA GCT TGT TCT GG-3′。β-actin引物,上游:5′-GCA AGC AGG AGT ATG ACG AG-3′,下游:5′-CAA ATA AAG CCA TGC CAA TC-3′。
1.3方法
1.3.1細胞培養 將4種胃癌細胞株和正常胃黏膜細胞復蘇在含有10%胎牛血清的培養基中,放于37 ℃、5%CO2、飽和濕度孵箱中培養,取對數生長期的細胞用于RNA的提取。
1.3.2RNA提取及qPCR 按Trizol說明書采用苯酚-氯仿抽提法,分別提取胃癌組織和細胞中總RNA,經紫外分光光度計檢測,A260/A280在1.9~2.1視為提取的RNA的純度很高。cDNA第一鏈合成:核糖核酸酶抑制劑 1 μL,5×反應緩沖液5 μL,四種脫氧核苷酸單體(dNTPs) 1.25 μL,反轉錄酶 1 μL,MgCl2 4 μL,Oligo(dT)15 Primer 1 μL,Random Primer 1 μL,無核酸酶的雙蒸水至總體積25 μL。其余步驟按照說明書進行。定量PCR實驗及結果分析:qPCR采用2×SYBR Green Master Mix,采用20 μL體系,其中cDNA1.5 μL,正向引物0.4 μL,反向引物0.4 μL,2×SYBR Green Master Mix 10 μL,無核酸酶的雙蒸水7.7 μL。PCR反應條件:95 ℃ 30 s,60 ℃ 30 s,70 ℃ 30 s擴增45個循環。以β-actin為內參照。結果分析采用經典的2-△△Ct法進行基因表達的相對定量[10]。目的基因Ct值用內參基因來進行統一標準化(△Ct=Ct目的-Ct內參)。
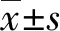
2 結果
2.1lncRNA FGF14-IT1在胃癌組織和細胞中的表達水平 36.14%(30/83)的胃癌組織FGF14-IT1表達水平高于癌旁組織,63.86%(53/83)的胃癌組織FGF14-IT1表達水平低于癌旁組織。在整體水平上,FGF14-IT1在癌組織中的相對表達量為1.630±1.896,明顯低于癌旁組織的2.257±2.599,差異有統計學意義(t=2.108,P=0.038)。胃癌細胞株AGS、MGC-803、SGC-7901中FGF14-IT1的相對表達量較正常胃黏膜細胞GES-1明顯降低(P<0.001),見圖1。

注:A為83例胃癌組織中lncRNA FGF14-IT1高表達與低表達情況;B 為lncRNA FGF14-IT1在胃癌組織及癌旁組織中的表達水平;C為各細胞株中FGF14-IT1的相對表達水平,此結果來自3次獨立實驗結果,*表示與GES-1比較,P<0.05
2.2lncRNA FGF14-IT1與臨床病理特征的關系 根據胃癌組織與其對應的癌旁組織中lncRNA FGF14-IT1的表達水平的高低,將癌組織中表達量高于對應癌旁組織的病例納入高表達組(30例),在癌組織中表達量低于對應癌旁組織的病例納入低表達組(53例)。用χ2檢驗分析發現,表達水平的高低與患者浸潤深度、淋巴結轉移、TNM分期顯著相關,而與性別、年齡、吸煙、飲酒、腫瘤直徑、分化程度、遠處轉移、脈管浸潤、神經浸潤、肝臟轉移、腹水、脂肪結節轉移無明顯相關性,見表1。

表1 FGF14-IT1表達水平與胃癌患者臨床資料的相關性分析(n)

續表1 FGF14-IT1表達水平與胃癌患者臨床資料的相關性分析(n)
2.3lncRNA FGF14-IT1與胃癌轉移的關系 將淋巴結轉移陽性患者定義為胃癌轉移陽性,沒有淋巴結轉移者定義為胃癌轉移陰性。單因素logistic回歸分析發現,FGF14-IT1、腫瘤大小、分化程度、浸潤深度與胃癌轉移有關聯;多因素分析發現,胃癌轉移與FGF14-IT1、浸潤深度有關聯,見表2。

表2 單因素和多因素分析影響胃癌患者腫瘤轉移的因素
注:OR為比值比;CI為置信區間;-表示該項無數據
3 討論
胃癌早期癥狀不明顯,多數人在確診時已經處于進展期,所以預后不良[11]。因此早期檢測胃癌,有效地預測治療前后的效果,開發新的治療方案是改善胃癌預后的有效策略,找到一個理想的特異性腫瘤標志物對于提高胃癌的早期診斷率至關重要。lncRNA具有豐富的生物學功能,它主要從表觀遺傳水平、轉錄水平、轉錄后水平這三個層面對基因表達進行調控,其中轉錄前水平主要通過DNA甲基化與去甲基化、組蛋白修飾等進行調控;轉錄水平的調控主要通過對啟動子、增強子的調節來影響基因的表達;轉錄后水平的調控主要是對mRNA剪接、編輯及降解等轉錄后加工修飾過程的調節[12-14]。近年來,隨著對lncRNA研究的深入,已經發現一些在胃癌中異常表達的lncRNA可以作為胃癌的腫瘤生物標志物,并且有助于胃癌預后的判斷。例如,ZHOU等[15]發現血漿中的H19可以作為生物標記物用于早期胃癌患者的篩查,并且可以作為胃癌患者術后的一個動態監測指標。SUN等[16]發現在胃癌組織中低表達的母系印記基因(MEG3)與腫瘤大小有關,下調MEG3的表達水平會促進胃癌細胞增殖,并能作為胃癌不良預后的生物標志物。SHAO等[17]發現lncRNA-RMRP可以吸附miR-206,調控細胞周期蛋白D2的表達,并且可以作為一個腫瘤標志物預示著不良的預后。
本研究前期通過基因芯片首次發現FGF14-IT1在胃癌組織中低表達,通過檢測83例胃癌及相應癌旁組織中FGF14-IT1的表達發現,與配對的癌旁組織比較,FGF14-IT1在53例胃癌組織中低表達,而在30例胃癌組織中高表達,在整體水平上, FGF14-IT1在胃癌組織中呈明顯低表達。筆者推測由于腫瘤的異質性,不同的胃癌細胞株具有不同的生物學特性及不同表型,所以在不同的胃癌患者及胃癌細胞株中,FGF14-IT1的調控機制可能存在差異,導致了一部分患者高表達,一部分患者低表達,但具體原因仍需進一步的探索。分析FGF14-IT1的表達與臨床病理特征之間的關系,發現FGF14-IT1與患者浸潤深度、淋巴結轉移、TNM分期顯著相關。因此推測FGF14-IT1可能參與了胃癌的發生發展過程,尤其是在侵襲轉移方面,為下一步的分子機制的探索提供了一個方向。此外通過回歸分析也發現異常表達的FGF14-IT1與胃癌轉移有關聯。雖然FGF14-IT1在胃癌中的調控機制目前尚不明確,但進一步的探索其機制,FGF14-IT1有望成為胃癌基因診斷和治療的重要靶點及用于評估胃癌患者預后的生物標志物。
4 結論
胃癌患者組織和細胞中FGF14-IT1的表達水平明顯降低,并且與患者發生淋巴結轉移、腫瘤浸潤、TNM高分期相關,可能是影響胃癌患者腫瘤轉移的獨立風險因素。本研究胃癌組織標本數量有限,組織中FGF14-IT1水平對胃癌是否具有診斷價值仍有很多工作需要完成,但隨著對FGF14-IT1在胃癌中的調控機制的進一步研究,FGF14-IT1在胃癌診斷方面可能展現出廣闊的臨床應用前景。

