石漠化地區野生多花木藍根瘤資源調查與分析
席 溢,趙麗麗,王小利,曾慶飛,陳 超*
石漠化地區野生多花木藍根瘤資源調查與分析
席 溢1,趙麗麗1,王小利2,曾慶飛2,陳 超1*
(1.貴州大學動物科學學院,貴州 貴陽 550025;2.貴州省草業研究所,貴州 貴陽 550006)
為充分發揮豆科植物在生態恢復與重建中的作用,調查了貴州省境內石漠化部分地區的野生多花木藍根瘤資源.結果表明:隸屬于干熱河谷南亞熱帶季雨林生態區的野生多花木藍根瘤菌及內生細菌資源較為豐富;野生多花木藍的共生結瘤率只達50%左右,根瘤全部著生于寄主的側根及須根上,大小可達0.5~3.0mm;12株根瘤菌分布在6個屬10個種,其中慢生根瘤菌屬()的分布頻率最高41.67%,慢生根瘤菌屬的和伯克霍爾德菌屬的發生頻率最高16.67%;16株根瘤內生細菌分布在4個屬11個種,其中芽孢桿菌屬()的分布頻率最高43.75%,芽孢桿菌屬的的發生頻率最高31.25%.
石漠化;多花木藍;根瘤菌;內生細菌;區系分析
喀斯特地區生境普遍土層淺薄、巖石裸露率高、保水性差,土壤養分易流失,生態系統脆弱,易遭破壞且難于恢復.再加上強烈的人為干擾,造成喀斯特地區土壤侵蝕嚴重,土地生產力嚴重下降,最終出現石漠化[1].石漠化治理的關鍵是提高植被覆蓋度,保持水土,增加土壤中碳、氮、磷含量等.相對化學手段,通過生物學手段促進土壤中氮積累,更環保[2].豆科植物()與根瘤菌()的共生固氮作用,是最重要的生物固氮形式[3].共生固氮量占生物固氮總量的80%左右[4].根瘤菌是與豆科植物共生,在其根部或莖部形成根瘤,并固定空氣中氮氣為植物提供營養的一類革蘭氏染色陰性需氧桿菌[1].因此,相對非豆科植物,豆科植物對土壤中全氮、速效氮和有機碳的改善作用更顯著[6-7].目前,常將豆科植物與非豆科植物進行輪作、套種,以改善土壤質量和提高農作物產量,并利用共生固氮進行生態修復[8].豆科植物被公認為逆境生態恢復和貧瘠退化土壤修復最有效的先鋒植物[9],能有效增加植被覆蓋度,減少徑流、泥沙及養分的流失[10].
某些豆科植物與根瘤菌形成固氮共生體的同時,其根瘤內還存在多種其他類群的內生細菌[11-12].此外,根瘤菌與豆科植物建立共生關系,不僅需要與寄主相互識別,還受地理環境的影響[13-14].寄主要適應所在環境,而與其結瘤的根瘤菌受到寄主和環境的選擇.
多花木藍()為豆科木藍屬灌木,耐貧瘠性和抗旱性較強,有水土保持作用;蛋白質含量高,有多種氨基酸成分,具有一定的飼用價值.研究表明,多花木藍也是結瘤植物之一[15],其根瘤菌具有豐富的遺傳多樣性[16].貴州是我國唯一沒有平原支撐的內陸山區省份,喀斯特環境獨特,針對該地區野生多花木藍根瘤資源系統研究工作缺乏[17-18].
本研究采集了貴州省境內石漠化部分地區的多花木藍根瘤資源,分離純化根瘤菌株,采用16S rDNA序列分析比對,鑒定菌株,并進行了區系分析.以期挖掘地區資源,為石漠化地區生態恢復與重建中充分發揮豆科植物與根瘤菌共生固氮技術提供理論支持.
1 材料與方法
1.1 資源調查區域及概況
根據云貴高原地形地貌和天然豆科牧草分布特點,于2016年7月~2017年6月,對貴州省境內野生多花木藍根瘤菌資源進行了調查.調查范圍涉及全省36個縣(市)(圖1).
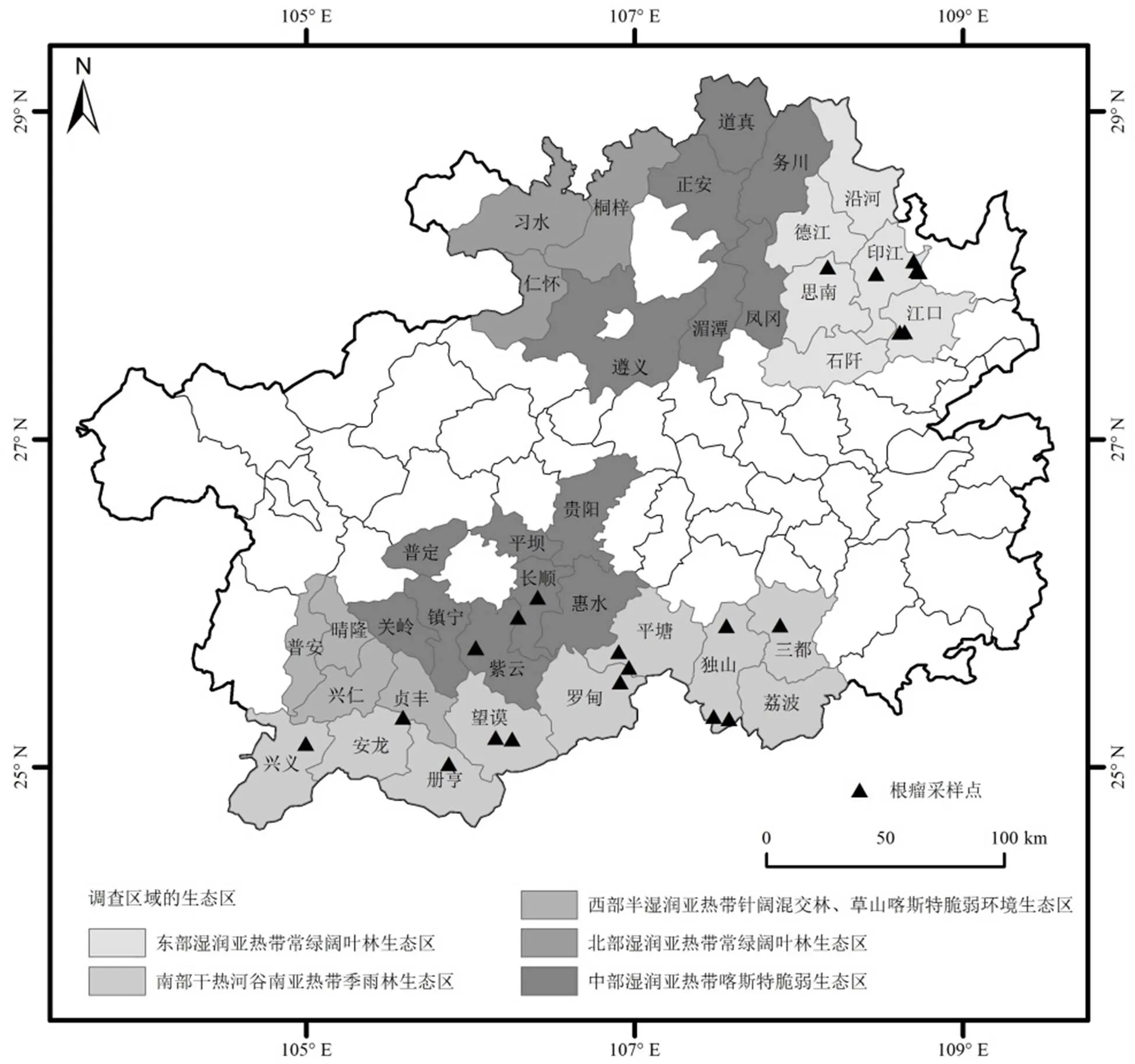
圖1 多花木藍根瘤資源調查區域的生態區及根瘤采集點
依據《貴州省生態功能區劃》[19],調查區域涉及了全省全部的生態區:(1)東部濕潤亞熱帶常綠闊葉林生態區.德江、沿河、印江、江口、思南、石阡,屬中亞熱帶季風濕潤氣候區,年均氣溫13.5~17.6℃,年均降水量1110~1410mm;(2)南部干熱河谷南亞熱帶季雨林生態區.興義、安龍、冊亨、望謨、羅甸、平塘、荔波、三都、獨山,屬典型的亞熱帶溫暖溫潤的季風氣候,年均氣溫13.6~19.6℃,年均降雨量1100~1400mm;(3)西部半濕潤亞熱帶針闊混交林、草山喀斯特脆弱環境生態區.普安、晴隆、興仁、貞豐,屬亞熱帶季風濕潤氣候,年均氣溫14.0~19.0℃,年降水量1100~1500mm;(4)北部濕潤亞熱帶常綠闊葉林生態區.仁懷、桐梓、習水,屬亞熱帶季風氣候,年均氣溫15.1℃,年均降水量1200mm;(5)中部濕潤亞熱帶喀斯特脆弱生態區.貴陽、遵義、湄潭、鳳岡、務川、正安、道真、惠水、長順、平壩、普定、鎮寧、關嶺、紫云,屬典型的高原型濕潤亞熱帶季風氣候,年均氣溫14℃,年均降雨量1360mm.
1.2 野生多花木藍根瘤標本的采集
相鄰采樣點要求路程距離大于15km,或海拔差大于50m.選擇生長狀況良好的植株,采集個大、飽滿根瘤.根瘤裝入離心管中密封、編號,并記錄采集點信息.
1.3 根瘤菌株與內生細菌的分離與純化
自來水沖凈樣品泥土,無菌水浸泡直至根瘤吸脹.每份樣品挑選10~20顆個大、飽滿的根瘤,95%酒精浸泡5min,0.1%HgCl2處理5min,無菌水沖洗數次,轉至無菌研缽.加無菌水1000mL,研磨成懸濁液,將懸濁液轉到YMA平板(加有剛果紅),均勻涂布,恒溫(28℃)倒置培養3~7d后,先后有菌落長出.及時挑取單菌落,進行革蘭氏染色,鏡檢.純化菌株接種到YMA液體培養基中,振蕩培養7d(28℃),30%甘油保種,-70℃保藏.
1.4 純化菌株16S rDNA的測定
菌株DNA利用試劑盒(UNIQ-10柱式)提取.引物為P1和P6.PCR反應條件:預變性94℃ 5min,變性94℃ 30s,退火54℃ 1min,延伸72℃ 2min;循環35次;延伸72℃ 10min.純化回收PCR產物,連接質粒載體PMD18-T,轉化大腸桿菌DH5α;篩選獲取轉化子,驗證提取的質粒DNA[20].產物送昆明碩擎生物公司測序.序列結果利用NCBI中Blast和GenBank數據庫中已知序列進行比對,確定分離菌株的分類地位.
1.5 根瘤菌株與內生細菌的區系分析
分析根瘤菌及內生細菌的種類組成、分布頻率以及優勢種類.
相對頻率計算分布頻率和發生頻率:分布頻率=有某菌種的樣品數/有菌種的總樣品數;發生頻率=有某菌種的菌株數/鑒定出的菌株總數.
2 結果與討論
2.1 野生多花木藍根瘤資源調查
在貴州省36個縣(市)不同生態環境的野生多花木藍根瘤資源調查中,共采集到根瘤樣品23份.所采樣品來自于印江、獨山、紫云等13個縣(市)(表1).在東部濕潤亞熱帶常綠闊葉林生態區、中部濕潤亞熱帶喀斯特脆弱生態區、南部干熱河谷南亞熱帶季雨林生態區中的部分縣(市)采集到了野生多花木藍根瘤資源,在北部濕潤亞熱帶常綠闊葉林生態區和西部半濕潤亞熱帶針闊混交林、草山喀斯特脆弱環境生態區未采集到.調查中發現,土壤疏松、水分條件正常的環境條件下,多花木藍長勢較好且根瘤較多,個體大;而土壤板結、干旱或低洼積水地帶,多花木藍長勢較差,根瘤較少,個體小(圖2).而海拔高度對多花木藍根瘤的數量與大小沒有直接的影響(表1).

a:根瘤較多根系;b:根瘤
本研究僅在部分區域采集到野生多花木藍根瘤資源.土壤疏松、水分條件正常的環境條件下,多花木藍長勢較好且根瘤較多,這應與多花木藍的生長習性有關.有研究也顯示,陰坡或常年陽光照射不足的區域,干旱氣候下很難采集到根瘤[21].未采集到根瘤資源的北部濕潤亞熱帶常綠闊葉林生態區和西部半濕潤亞熱帶針闊混交林、草山喀斯特脆弱環境生態區,可能是不適的水分條件造成形成的根瘤脫落,或是土壤條件不利于根瘤的形成,或是缺乏相應的根瘤菌[22-23].
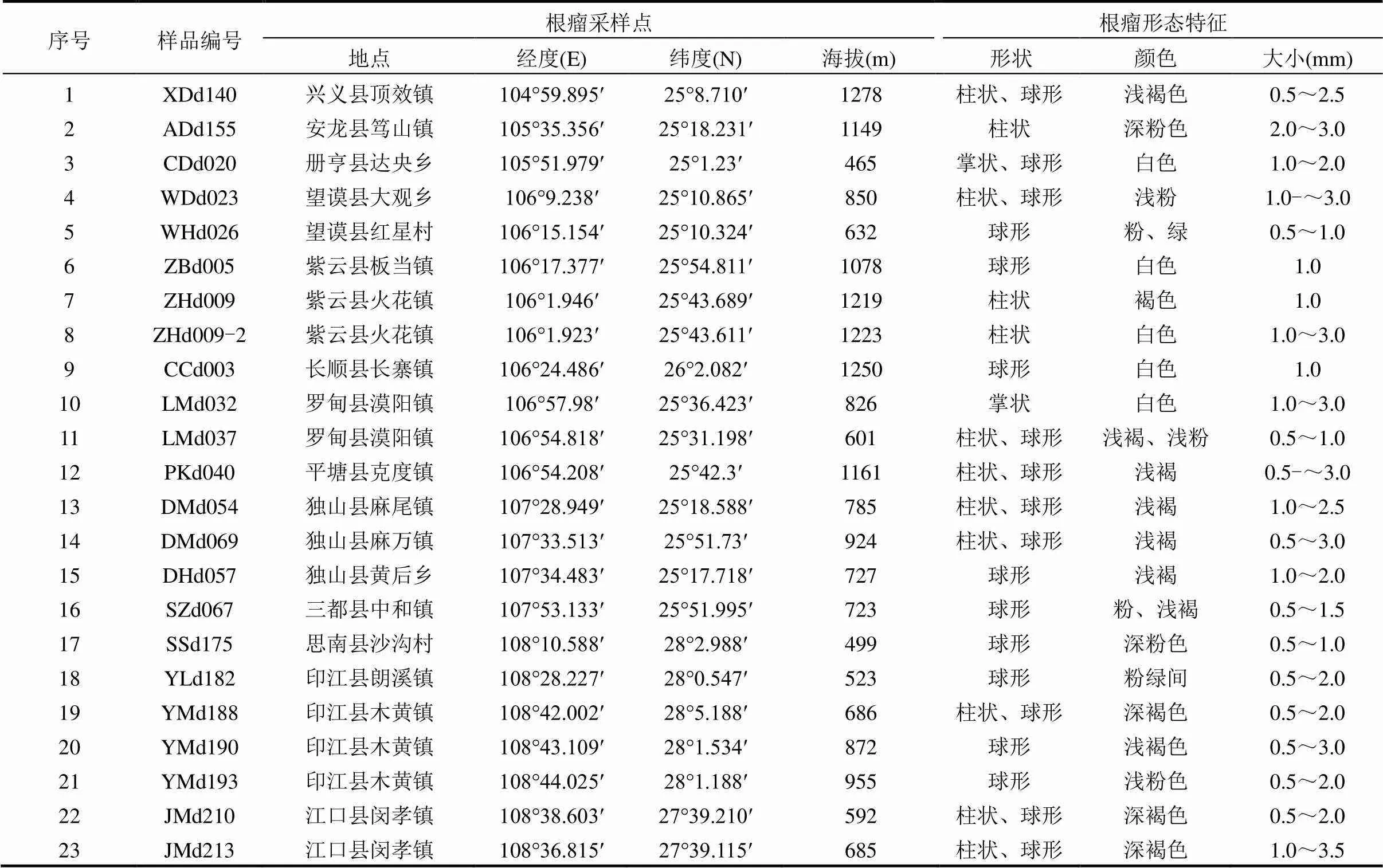
表1 野生多花木藍根瘤形態特征
2.2 野生多花木藍根瘤特征
本次所采集的多花木藍的共生結瘤率只達50%,且根瘤全部著生于寄主的側根及須根上,主根上無根瘤著生(圖2).根瘤多為球形和柱狀,少數為掌狀;顏色呈淺/深褐色、淺/深粉色、白色等;大小可達0.5~3.0mm(表1).
Andrews等[24]研究顯示,一年生豆科植物根瘤主要著生在主根及側根上部;多年生豆科植物根瘤一般著生在側根或須根,但少數種的粗壯主根上也會著生白色或粉紅色幼瘤.本研究中野生多花木藍為多年生植物,結果也顯示,根瘤都著生于側根及須根上.根瘤形狀與寄主植物有很大關系[15].本研究中根瘤多為球形和柱狀,少數為掌狀.可能因為野生多花木藍作為寄主缺乏永久分生組織,也就是缺乏感染線或感染線分布不廣.由于豆血紅蛋白的存在,具有固氮活性的有效根瘤斷切面呈粉紅色[16].本研究中的根瘤資源主要為淺/深褐色、淺/深粉色、白色.
2.3 根瘤菌株及內生細菌的分離純化
從采集的23份野生多花木藍的根瘤樣品中分離得到28個純化菌株.所得菌落表面光滑、濕潤,呈圓形、中間隆起(圖3).

圖3 分離純化的菌落
2.4 根瘤菌株及內生細菌的分子鑒定
通過PCR反應,所有待測菌株均擴增出了約1.5kb的序列片段(圖4).測定序列與NCBI中Blast和已知物種的16S rDNA序列比對得出, 28個菌株中,有根瘤菌12株(表2),內生細菌16株(表3).

12株根瘤菌來自于長順縣、冊亨縣、望謨縣、羅甸縣、獨山縣、三都縣(表2).除長順縣外,其他根瘤菌來源地均處于南部干熱河谷南亞熱帶季雨林生態區(圖1).
16株根瘤內生細菌來自于紫云縣、羅甸縣、平塘縣、獨山縣、三都縣、印江縣、江口縣(表3).大部分根瘤內生細菌來源地處于南部干熱河谷南亞熱帶季雨林生態區(圖1).
根瘤菌—豆科植物建立的共生關系有多重因子的復雜性,環境對根瘤菌能否結合共生有重要影響[25].每種植物都有一定的生態適應范圍,環境影響豆科植物—根瘤菌共生結瘤可能性和穩定性[26].本研究中分離鑒定出的根瘤菌和根瘤內生細菌也主要在分布在特定區域,也說明生態地理環境影響野生多花木蘭的結瘤能力.宿主植物要適應環境壓力,與其結瘤的根瘤菌要面臨宿主和環境的選擇,導致菌株呈現區域差異.
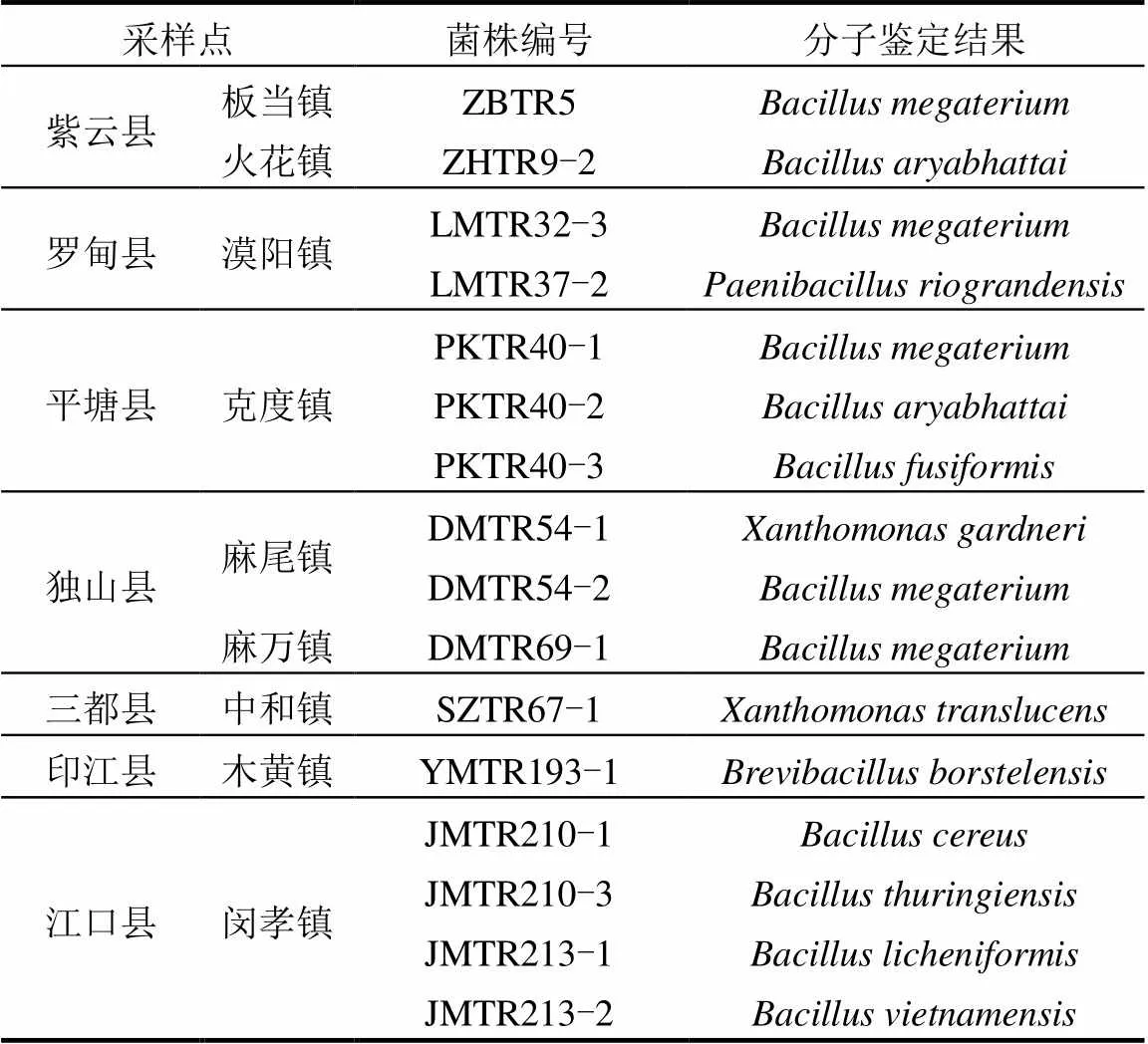
表2 野生多花木藍根瘤菌株分子鑒定結果
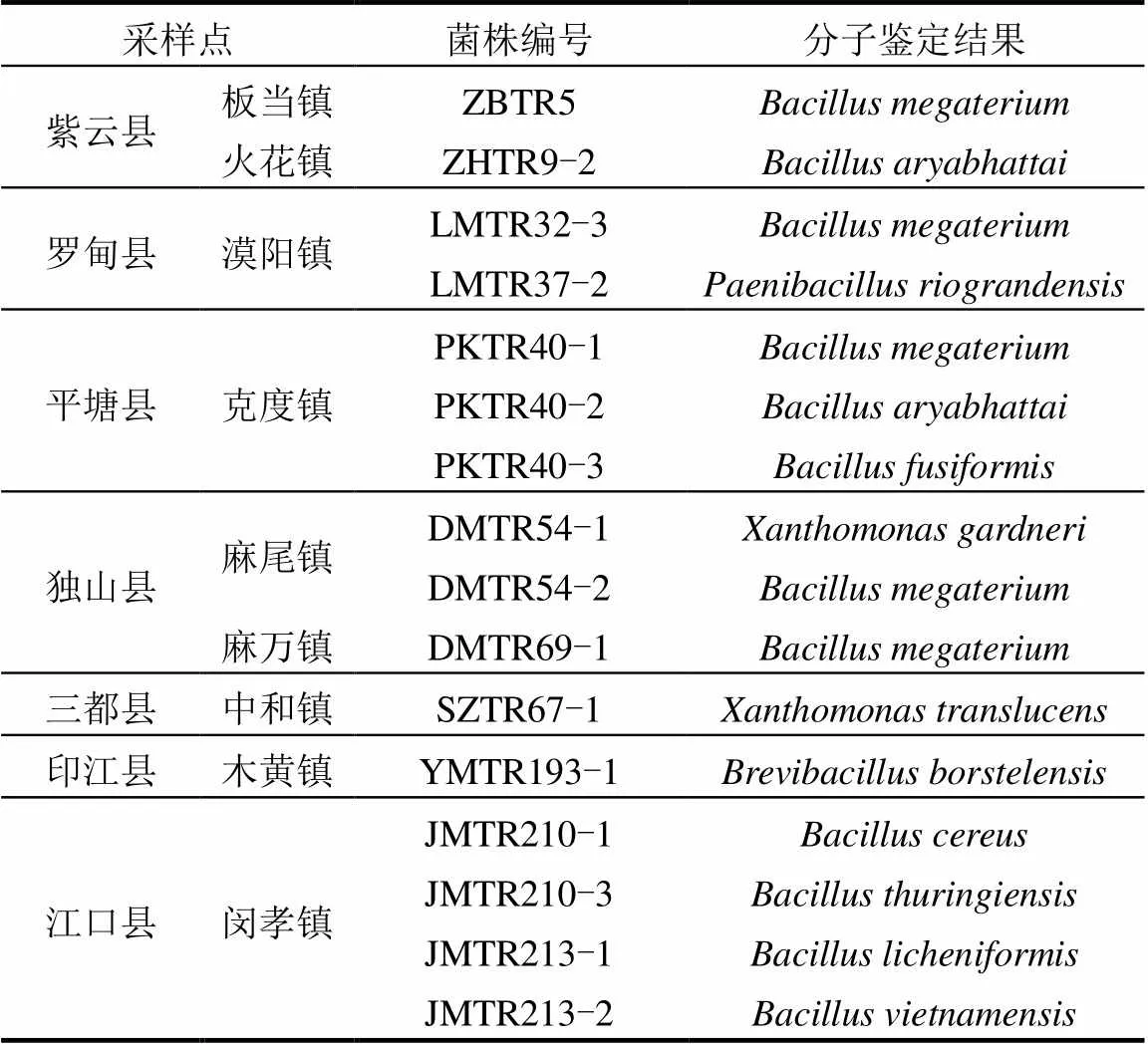
表3 野生多花木藍根瘤內生細菌分子鑒定結果
2.5 根瘤菌株及內生細菌的區系分析
12株根瘤菌分布在6個屬10個種(表4).慢生根瘤菌屬()4個、根瘤菌屬()2個、伯克霍爾德菌屬()1個、中慢生根瘤菌屬()1個、腸桿菌屬()1個、土壤桿菌屬()1個.慢生根瘤菌屬的分布頻率最高41.67%,其次是根瘤菌屬和伯克霍爾德菌屬為16.67%,其他的分布頻率都是8.33%.
與根瘤菌共生固氮是豆科植物的顯著特點.根瘤菌屬于細菌域變形桿菌門[27].本研究分離鑒定的根瘤菌分布在6個屬12個種,其中慢生根瘤菌屬、根瘤菌屬、中慢生根瘤菌屬屬于-變形桿菌綱,伯克霍爾德菌屬屬于-變形桿菌綱.慢生根瘤菌屬分布頻率最高,是優勢種群.

表4 野生多花木藍根瘤菌區系分析
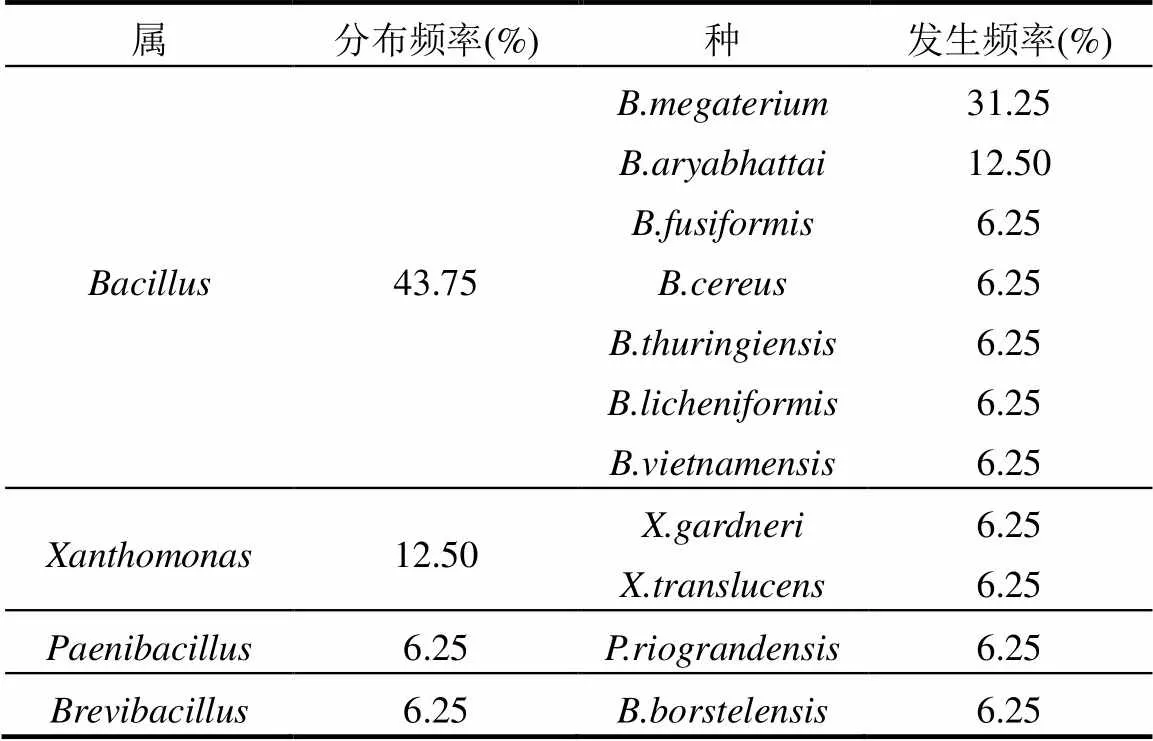
表5 多花木藍根瘤內生細菌區系分析
16株根瘤內生細菌分布在4個屬11個種(表5).芽孢桿菌屬()7個、黃單胞菌屬()1個、類芽胞桿菌屬()1個、短芽孢桿菌屬()1個.芽孢桿菌屬的分布頻率最高43.75%,黃單胞菌屬的次之為12.50%,其他的均為6.25%.其中芽孢桿菌屬的和的發生頻率分別為31.25%和12.50%,其他種的發生頻率均為6.25%.
除了與根瘤菌共生外,豆科植物還可以與其他微生物形成多種相互關系;在根瘤內,也存在其他類群的內生細菌[28-29].內生細菌可以促進植物生長,提高產出,擔當生物控制因子[30].內生細菌的形態、種類以及生物學作用也是豐富多樣[31].種類上占較大優勢的主要是假單胞菌屬、芽胞桿菌屬、腸桿菌屬和土壤桿菌屬[32].本研究分離鑒定的根瘤內生細菌分布在4個屬11個種,其中芽孢桿菌屬的分布頻率最高,芽孢桿菌屬的發生頻率最高.
3 結論
3.1 貴州境內隸屬于南部干熱河谷南亞熱帶季雨林生態區的野生多花木藍根瘤菌及內生細菌資源較為豐富.
3.2 從貴州石漠化地區野生多花木藍根分離鑒定的根瘤菌分布在6個屬(、、、、、)10個種(、、、、、、、、、).
3.2 從貴州石漠化地區野生多花木藍根分離鑒定的根瘤內生細菌分布在4個屬(、、、)11個種(、、、、、、、、、、).
[1] 劉濤澤,劉叢強,張 偉,等.喀斯特地區坡地土壤可溶性有機碳的分布特征[J]. 中國環境科學, 2009,29(3):248-253. Liu T Z, Liu C Q, Zhang W, et al. Concentrations and migration features of dissolved organic carbon in the soils of slope lands in Karst area [J]. China Environmental Science, 2009,29(3):248-253.
[2] 文克儉,羅天瓊,龍忠富,等.基于生態治理的豆科灌木品種篩選研究[J]. 草業與畜牧, 2017,(4):28-30. Wen K J, Luo T Q, Long Z F, et al. Study on the selection ofvarieties based on ecological management [J]. Prataculture & Animal Husbandry, 2017,(4):28-30.
[3] Werner G, Cornwell W, Cornelissen J, et al. Evolutionary signals of symbiotic persistence in the legume-rhizobia mutualism [J]. Proceedings of the National Academy of Sciences, 2015,112(33): 10262-10269.
[4] 陳利云,張海林,周志宇.生物與非生物因素對共生固氮的影響[J]. 草業科學, 2010,27(6):64-70.Chen L Y, Zhang H L, Zhou Z Y. Effect of biotic and abiotic factors on symbiotic nitrogen fixation [J]. Prataculture Science, 2010,27(6):64-70.
[5] Haichar F, Santaella C, Heulin T, et al. Root exudates mediated interactions belowground [J]. Soil Biology & Biochemistry, 2014, 77(7):69-80.
[6] Yan J, Han X Z, Ji Z J, et al. Abundance and diversity of soybean- nodulating rhizobia in black soil are impacted by land use and crop management [J]. Applied and Environmental Microbiology, 2014, 80(17):5394-5402.
[7] Mhamdi R, Nouairi I, Ben Hammouda T, et al. Growth capacity and biochemical mechanisms involved in rhizobia tolerance to salinity and water deficit [J]. Journal of basic Microbiology, 2015,55(4):51-61.
[8] 唐明燈,艾紹英,李盟軍,等.紫云英對污染土壤上葉菜生長及其鎘和鉛含量的影響[J]. 中國環境科學, 2011,31(3):461-465. Tang M D, Ai S Y, Li M J, et al. Effect of Astragalus sinicus on the growth, Cd and Pb concentration of leafy vegetables [J]. China Environmental Science, 2011,31(3):461-465.
[9] Chen J Y, Gu J, Wang E T, et al. Wild peanutare nodulated by diverse and novelspecies in acid soils [J]. Systematic and Applied Microbiology, 2014,37(7):525-532.
[10] Ferguson B J, Mathesius U. Phytohormone regulation of legume- rhizobia interactions [J]. Journal of Chemical Ecology, 2014,40(7): 770-790.
[11] Li J, Wang E, Chen W, et al. Genetic diversity and potential for promotion of plant growth detected in nodule endophytic bacteria of soybean grown in Heilongjiang province of China [J]. Soil Biology & Biochemistry, 2008,40(1):238-246.
[12] Trujillo M, Riesco R, Benito P, et al. Endophytic actinobacteria and the interaction of micromonospora and nitrogen fixing plants [J]. Frontiers in Microbiology, 2015,(6):1341.
[13] 李艷梅,鐘宇舟,譚 淵,等.四川地區結瘤大豆根際土壤中紫云英、苜蓿和三葉草根瘤菌的多樣性分析[J]. 應用與環境生物學報, 2015,21(2):234-241. Li Y M, Zhong Y Z, Tan Y, et al. Diversity of rhizobia nodulating,andin nodulated soybean rhizosphere soil in Sichuan [J]. Chinese Journal of Applied & Environmental Biology, 2015,21(2):234-241.
[14] Kimeklis A, Kuznetsova G, Sazanova A, et al. Divergent evolution of symbiotic bacteria: rhizobia of the relic legume vavilovia formosa form an isolated group within rhizobiumViciae [J]. Russian Journal of Genetics, 2018,54(7):866-870.
[15] 王衛衛,胡正海,關桂蘭.甘肅、寧夏部分地區根瘤菌資源及其共生固氮特性[J]. 自然資源學報, 2002,17(1):48-54.Wang W W, Hu Z H, Guan G L. The characteristics related to symbiotic nitrogen fixation and rhizobium resources in some areas of Gansu and Ningxia [J]. Journal of Natural Resources, 2002,17(1):48-54.
[16] 謝瑞美.陜西省木藍屬根瘤菌遺傳多樣性研究[D]. 楊凌:西北農林科技大學, 2009. Xie R M. Diversity of rhizobia isolated fromin Shaan Xi of China [D]. Yangling: Northwest A&F University, 2009.
[17] 劉 杰,汪恩濤,陳文新.豆科植物根瘤內生細菌的發現及其研究進展[J]. 微生物學報, 2011,51(8):1001-1006. Liu J, Wang E T, Chen W X. Discovery and research progress of endophytic bacteria in the root nodules of legumes——A review [J]. Acta Microbiologica Sinica, 2011,51(8):1001-1006.
[18] 邱并生.根瘤內生細菌[J]. 微生物學通報, 2013,40(3):544. Qiu B S. Nodule endophytic bacteria [J]. Microbiology China, 2013, 40(3):544.
[19] 貴州省人民政府.省人民政府關于貴州省生態功能區劃的批復[N]. 貴州省人民政府公報, 2005-05-10. Guizhou Provincial People's Government. Provincial People's Government's approval of ecological function regionalization in Guizhou province [N]. Official Gazette of Guizhou Provincial People's Government, 2005-05-10.
[20] 韋興迪,曾慶飛,譚玉蘭,等.貴州部分地區野生白三葉根瘤菌資源調查與區系分析[J]. 作物雜志, 2018,(2):35-43. Wei X D, Zeng Q F, Tan Y L, et al. Investigation and floristic analysis on rhizobial resources ofin some regions of Guizhou province [J]. Crops, 2018,(2):35-43.
[21] Afkhami M, Luke M, Burns J, et al. Symbioses with nitrogen-fixing bacteria: nodulation and phylogenetic data across legume genera [J]. Ecology, 2018,99(2):502.
[22] Allen O, Allen E. The Leguminosae: A source book of characteristics, uses and nodulation [J]. Economic Botany, 1982,36(2):224.
[23] Powell A, Doyle J. Enhanced rhizobial symbiotic capacity in an allopolyploid species of glycine (leguminosae) [J]. American Journal of Botany, 2016,103(10):1771.
[24] Andrews M, Andrews M. Specificity in legume-rhizobia symbioses [J]. International Journal of Molecular Sciences, 2017,18(4):1-39.
[25] 張敬宜,王金華,思 斯.根瘤菌對石漠化生態系統三葉草生長的影響研究[J]. 安徽農學通報, 2014,20(7):15-16. Zhang J Y, Wang J H, Si S. Effects of rhizobium on the growth of clover in rocky desertification ecosystem [J]. Anhui Agricultural Science Bulletin, 2014,20(7):15-16.
[26] 熊惠洋.蠶豆土著根瘤菌的生物地理分布及其形成機制[D]. 北京:中國農業大學, 2017. Xiong H Y. The biogeography of indigenous rhizobia associated with faba bean and its underlying formation mechanism [D]. Beijing: China Agricultural University, 2017.
[27] Huys G, Coopman R, Janssen P, et al. High-resolution genotypic analysis of the genus Aeromonas by AFLP fingerprinting [J]. International Journal of Systematic Bacteriology, 1996,46(2):572.
[28] Li L, Sinkko H, Montonen L, et al. Biogeography of symbiotic and other endophytic bacteria, isolated from medicinal glycyrrhiza species in china [J]. FEMS Microbiology Ecology, 2012,79(1):46-68.
[29] 鐘宇舟,余秀梅,陳 強,等.四川盆地大豆根瘤內生細菌的分離鑒定及促生效果[J]. 應用與環境生物學報, 2017,(1):46-53. Zhong Y Z, Yu X M, Cheng Q, et al. Isolation, identification and plant growth promotion ability evaluation of the endophytic bacteria isolated from soybean root nodule in Sichuan Basin [J]. Chinese Journal of Applied & Environmental Biology, 2017,(1):46-53.
[30] Forchetti G, Masciarelli O, Alemano S, et al. Endophytic bacteria in sunflower (L.): isolation, characterization, and production of jasmonates and abscisic acid in culture medium [J]. Applied Microbiology & Biotechnology, 2007,76(5):1145-1152.
[31] Rangeshwaran R, Raj J, Kumar P. Identification of endophytic bacteria in chickpea (L.) and their effect on plant growth [J]. Journal of Biological Control, 2008,22(1):13-23.
[32] Chen T, Chen Z, Ma G, et al. Diversity and potential application of endophytic bacteria in ginger [J]. Genetics & Molecular Research, 2014,13(3):4918-4931.
Investigation and analysis of root nodule resources of wildin rocky desertification areas.
XI Yi1, ZHAO Li-li1, WANG Xiao-li2, ZENG Qing-fei2, CHEN Chao1*
(1.College of Animal Science, Guizhou University, Guiyang 550025, China;2.Guizhou Institute of Pratacultural, Guiyang 550006, China)., 2019,39(10):4409~4415
In order to give full play to the role of leguminous plants in ecological restoration and reconstruction, the root nodule resources of wildin the rocky desertification region of Guizhou province were investigated. The results showed that the resources of rhizobia and endophytic bacteria of wildwere abundant in southern subtropical seasonal rain forest ecological zone in the dry and hot valley; the symbiotic nodulation rate of wildwas only about 50%, and all the nodules were on the lateral roots and fibrous roots of the host, 0.5~3.0mm in size; 12 rhizobia strains were distributed in 10 species of 6 genera, of which the distribution frequency ofwas the highest in frequency 41.67%, and the frequencies of occurrence ofofandofwere the highest in frequency 16.67%; 16 endophytic bacteria strains were distributed in 11 species of 4 genera, of which the distribution frequency ofwas the highest in frequency 43.75%, and the frequency of occurrence ofofwas the highest in frequency 31.25%.
rocky desertification;;rhizobia;endophytic bacteria;flora analysis
X176
A
1000-6923(2019)10-4409-07
席 溢(1987-),女,貴州安順人,副教授,博士,主要從事植物生理生態學研究.發表論文10余篇.
2019-03-19
貴州省科技重大專項計劃(黔科合重大專項字[2016]3002號);國家自然科學基金資助項目(31560664);貴州省科技合作計劃(黔科合LH字[2016]7450號)
* 責任作者, 教授, gzgyxgc3855218@163.com

