變化觀念與平衡思想中“博弈”意識的樹立
李旭林
(山西省臨汾第一中學校 041000)
發揮化學課程的整體育人功能,就必須立足于學生適應現代生活和未來發展的需要.而博弈論目前已經在經濟學、國際關系學、政治學、軍事戰略、生物學等很多學科廣泛地應用.所以“變化觀念與平衡思想”核心素養的構成要素中,不僅要有物質變化與能量變化、方向與限度、速率與平衡、守恒與定量關系的表征,還應該逐步滲透“博弈與平衡”思維意識.
化學平衡狀態存在于可逆反應,而可逆反應是在一定條件下,正反應和逆反應同時發生的反應.既然正、逆反應同時發生,它們之間就會存在相互的“博弈”,博弈的結果就是可逆反應在達到平衡狀態時存在一定的限度.本文就應用“博弈與平衡”思維意識解決酸堿反應、氧還反應以及電化學相關問題進行分析,闡述如下.
一、酸堿反應中的“博弈與平衡”意識


酸對應酸根電離方程式電離常數H2CO3HCO- 3H2CO3H+ + HCO-3Ka1HCO-3CO2-3HCO-3H++CO32-Ka2
因為較強的酸易電離出H+,即其對應的酸根難以與H+結合;同理較弱的酸難電離出H+,即其對應的酸根就易與H+結合.所以,當較強的酸遇到較弱酸對應的鹽溶液時,就存在“強酸與弱酸根反應”與“弱酸與強酸根反應”之間的博弈,其結果就是以“弱酸根與強酸電離出的H+結合生成弱酸”為主.可以表征為:強酸 + 弱酸鹽(弱酸根)= 弱酸 + 強酸鹽(強酸根).

例1(2015年課標Ⅰ卷26題節選)設計實驗證明:草酸的酸性比碳酸的強____.
例2(2015年福建卷23題節選)25℃,兩種酸的電離平衡常數如下表:

Ka1Ka2H2SO31.3×10-26.3×10-8H2CO34.2×10-75.6×10-11
H2SO3溶液和NaHCO3溶液反應的主要離子方程式為____.
二、原電池原理中的“博弈與平衡”意識
大多數學生在初學原電池原理時,總是想不通化學電源的“電動勢”從何而來.不需引入“雙電層”理論、電極電勢、能斯特方程等復雜知識,利用“博弈與平衡”意識來分析,便可以輕松理解.例如,對人教版選修4中鋅銅原電池(丹尼爾電池)裝置(如圖1所示)分析如下.


2.在未形成閉合回路時,上述兩平衡互不干涉.但是,用導線連接鋅棒和銅棒,并用鹽橋連接兩個燒杯中的溶液形成閉合回路后,兩個平衡就會開始“博弈”.由于Zn(s)失電子能力(還原性)比Cu(s)強,而Cu2+得電子能力(氧化性)比Zn2+強,而且導線的電阻幾乎為0,所以Zn失電子通過導線向Cu移動,Cu2+得電子生成Cu.


兩個平衡的博弈,就是產生“電動勢”的原因.
例3(2019年廣東七校高考沖刺11題)因存在濃度差而產生電動勢的電池稱為濃差電池.利用如圖所示裝置進行實驗,開始先閉合K2,斷開KL,一段時間后,再斷開K2,閉合KL,形成濃差電池,電流計指針偏轉(Ag+濃度越大,氧化性越強).下列說法不正確的是( ).

A. 閉合K2,斷開KL一段時間后,X電極質量增加
B. 閉合K2,斷開KL一段時間后,右池c(AgNO3)增大
C. 斷開K2,閉合K1,X電極發生氧化反應
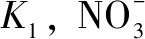

三、氧化還原反應中的“博弈與平衡”意識
與酸堿反應類似,氧還反應中同樣存在“強強成弱”的規律,也就是在一個氧還反應中氧化性:氧化劑>氧化產物,還原性:還原劑>還原產物.這條規律,在解題時經常用到,但一部分同學只是一般性套用規律,平時備考復習過程中沒有深刻體會其中的“博弈與平衡”的思維方式,所以在遇到2019年全國I卷28題,就會“深入山中”,不知所云.

(1)Shibata曾做過下列實驗:①使純H2緩慢地通過處于721 ℃下的過量氧化鈷CoO(s),氧化鈷部分被還原為金屬鈷(Co),平衡后氣體中H2的物質的量分數為0.0250.②在同一溫度下用CO還原CoO(s),平衡后氣體中CO的物質的量分數為0.0192.
根據上述實驗結果判斷,還原CoO(s)為Co(s)的傾向是CO____H2(填“大于”或“小于”).
(2)721℃時,在密閉容器中將等物質的量的CO(g)和H2O(g)混合,采用適當的催化劑進行反應,則平衡時體系中H2的物質的量分數為____(填標號).
A.<0.25 B.0.25 C.0.25~0.50
D.0.50 E.>0.50

(3)Shoichi研究了467℃、489℃時水煤氣變換中CO和H2分壓隨時間變化關系(如右圖所示),催化劑為氧化鐵,實驗初始時體系中的p(H2O)和p(CO)相等、p(CO2)和p(H2)相等.
467℃時p(H2)和p(CO)隨時間變化關系的曲線分別是____、____.489 ℃時p(H2)和p(CO)隨時間變化關系的曲線分別是____、____.



起始/mol 1 1 0 0
轉化/molxxxx
平衡/mol 1-x1-xxx
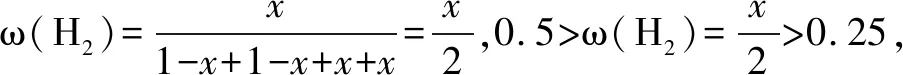
(3)該題綜合性較強,須同時從變化觀念與平衡思想的三個角度考慮得出結論:
①定量轉化:30~90 min的變化量b增0.34 kPa,c減0.34 kPa;a減0.28 kPa,d增0.28 kPa.可知,b、c為同一溫度下兩物質的變化曲線,a、d為另一溫度下兩物質的變化曲線.
②“博弈”意識:721℃下,CO的還原性強于H2,平衡時CO分壓小于H2分壓.且467℃、489℃均小于721℃,該反應為放熱反應,溫度降低平衡正向移動,CO的分壓會更小,H2分壓會更大.所以,A、B為H2的變化曲線;c、d為CO的變化曲線.
③勒夏特列原理:該反應為放熱反應,溫度降低平衡正向移動,467℃比489℃時H2的平衡分壓大,CO的平衡分壓小.所以,467℃時p(H2)和p(CO)隨時間變化關系的曲線分別是b、c.489 ℃時p(H2)和p(CO)隨時間變化關系的曲線分別是a、d.

