涼血通瘀方對腦出血大鼠氧化應激和炎癥反應的影響
顧恒,李建香,劉云芳,過偉峰
(南京中醫藥大學,江蘇 南京 210046)
腦出血在我國約占全部卒中的20%~30%,急性期病死率和致殘率高,存活患者也大多遺留后遺癥。受限于各地醫療水平,現代醫學認為降低腦出血負擔的最佳方法仍以預防高血壓為主[1]。國醫大師周仲瑛教授在中風痰熱腑實學說基礎上,創新性地提出瘀熱阻竅學說。認為本病系火熱毒邪壅于血分,瘀熱搏結,氣火上沖,迫血上涌,灼傷腦絡;同時因腦中蓄血,郁而化熱,絡熱血瘀,進一步損害腦元。據此,創制涼血通瘀方治療,功效涼血散瘀、通腑瀉熱。臨床觀察評價涼血通瘀方治療腦出血的臨床療效,經168例觀察,總有效率88.0%,優于對照組(169例)的77.5%(P<0.05)[2]。
腦出血后腦損傷主要在于原發性血腫引起的占位效應以及繼發性病理改變。血腫周圍的缺血水腫區形成后,腦組織急性氧化應激,生成的超氧陰離子自由基攻擊生物細胞膜大分子,同時引起一系列的炎癥反應。而中性粒細胞浸潤后會產生更多的活性氧,加重氧化損傷。氧化應激和炎癥反應貫穿本病各個階段,是導致神經功能缺損的關鍵機制。本實驗旨在從抗氧化和抗炎角度探討涼血通瘀方發揮神經功能保護的作用。
1 材料
1.1 實驗動物
SPF級雄性SD大鼠80只,體質量250~300 g,合格證號:SCXK(浙)2014-0001。于南京中醫藥大學動物實驗中心飼養,5只/籠,自由飲水攝食,7:00~19:00光暗交替,恒溫恒濕。
1.2 主要實驗藥物與試劑
涼血通瘀方:生大黃10 g,水牛角30 g,生地黃20 g,赤芍15 g,牡丹皮10 g,石菖蒲10 g。中藥材按常規方法水煎煮濃縮,每毫升含生藥1.2 g。
Takara SYBR Premix Ex Taq(日本Takara公司),Takara PrimeScript RT Master Mix(Perfect Real Time)(日本Takara公司),nNOS、TLR-4、IL-1β引物(上海生工生物工程有限公司),MDA檢測試劑盒(上海碧云天生物技術有限公司)。
1.3 主要實驗儀器
腦立體定位儀(成都泰盟軟件有限公司)、酶標儀(美國PerkinElmer公司)、注射泵控制器(保定蘭格恒流泵有限公司)、7500 Real Time PCR儀(美國ABI公司)。
2 方法
2.1 腦出血模型的建立
大鼠稱體質量編號,喂養一周后參照Xue M[3]自體尾動脈血注入法,制備大鼠腦出血模型,造模后評估神經功能缺損程度。選取Longa評分法中1~3分的大鼠作為模型動物。
2.2 動物分組及給藥
大鼠隨機分為以下4組,每組18只,分配至用藥后1 、3 、5 d三個時間點,各時間點6只。
正常組、模型組、假手術組(開顱后插入進樣器針頭但不注血):予用藥組等體積生理鹽水。
涼血通瘀組:造模后3 h開始灌胃用藥,給藥量均為1 mL/100 mg體質量,每日1次,共5 d。
2.3 行為學評分
采用Longa五級評分法[4]和平衡木測驗[5],于動物蘇醒后評估神經功能缺損癥狀。標準見表1。
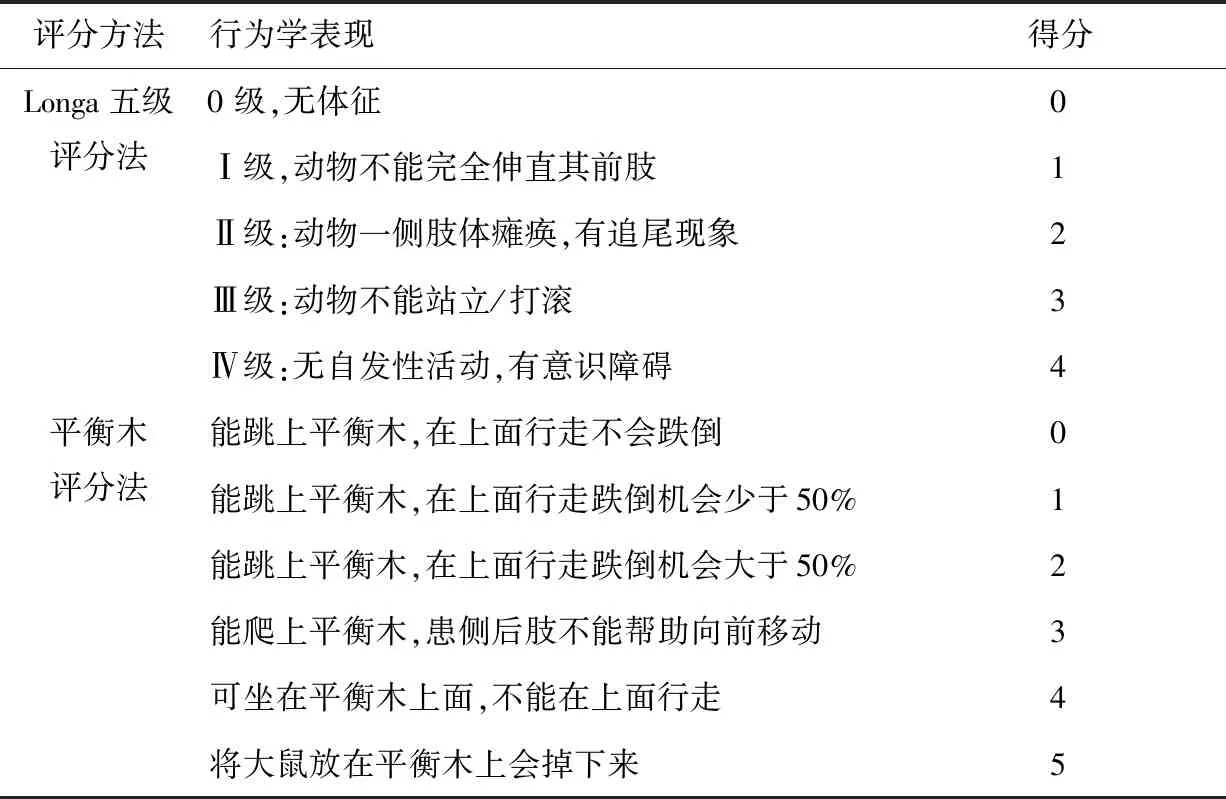
表1 腦出血大鼠行為學評分標準
2.4 硫代巴比妥酸反應法檢測腦組織中MDA含量
取腦組織處理后按照MDA試劑盒說明書步驟操作,依次加樣孵育進行顯色反應,將96孔板置入酶標儀檢測吸光值,制作標準曲線,計算腦組織MDA含量。
2.5 RT-PCR法檢測腦組織nNOS、CuZnSOD、TLR-4、IL-1β mRNA的表達
取體積約5×5×5 mm3大小的組織置于平頭管中,放入小鋼珠,按50~100 mg組織/mL Trizol加入Trizol使用球磨儀震蕩擊打裂解細胞,提取總RNA,使用分光光度計檢測RNA濃度及純度。按照Takara逆轉錄試劑說明書配制反應體系,進行逆轉錄。將逆轉錄后的產物處理后于PCR儀內進行擴增。引物設計如下:nNOS(sense primer:AATGGTGGAGGTGCTGGAGGAG;anti-sense primer: CTGGAGAGGAGCTGATGGAGTAGTAG);CuZnSOD(sense primer:GCCGTGTGCGTGCTGAAGG;anti-sense primer: TGTAATCTGTCCTGACACCACAACTG);TLR-4(sense primer:GCTGCCAACATCATCCAGGAAGG;anti-sense primer: TGATGCCAGAGCGGCTACTCAG);IL-1β(sense primer:CAGCAGCATCTCGACAAGAG;anti-sense primer: AAAGAAGGTGCTTGGGTCCT);GAPDH(sense primer:AAGGGCTCATGACCACAGTC;anti-sense primer: GGATGCAGGGATGATGTTCT)。PCR反應程序:Stage1(預變性):Reps:1;95℃ 30 s。Stage2(PCR反應):Reps:40;95℃ 5 s、60℃ 34 s。以GAPDH為內參,使用2公式計算目的基因相對表達量。
2.6 統計分析
3 結果
3.1 行為學評分結果
各時間點假手術組行為學評分均為0分。造模各組均出現不同程度的神經功能缺損,與假手術組比,P均<0.01。用藥3、5 d后,涼血通瘀組明顯低于模型組(P<0.05,P<0.01)。各造模組評分隨時間逐漸下降。見表2。
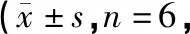
表2 各組大鼠行為學評分分)
注:與假手術組比較,*P<0.05,**P<0.01;與模型組比較,#P<0.05,##P<0.01
3.2 氧化應激指標CuZnSOD、nNOS mRNA表達和MDA含量的結果
各時間點模型組腦組織CuZnSOD mRNA表達量均明顯低于假手術組(P<0.01),涼血通瘀組明顯高于模型組(P<0.01)。見表3。
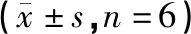
表3 各組大鼠腦組織CuZnSOD mRNA表達量
注:與正常組相比,$$P<0.01,$P<0.05;與假手術組比較,*P<0.05,**P<0.01;與模型組比較,##P<0.01
各時間點模型組腦組織nNOS mRNA表達均明顯高于假手術組(P<0.01),涼血通瘀組明顯低于模型組(P<0.01)。見表4。
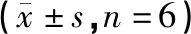
表4 各組大鼠腦組織nNOS mRNA表達量
注:與正常組相比,$$P<0.01;與假手術組比較,**P<0.01;與模型組比,##P<0.01
各時間點模型組腦組織MDA含量均明顯高于假手術組(P<0.05,P<0.01),涼血通瘀組明顯低于模型組(P<0.05)。見表5。
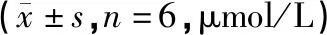
表5 各組大鼠腦組織MDA含量
注:與正常組相比,$P<0.05,$$P<0.01;與假手術組比較,*P<0.05,**P<0.01;與模型組比較,#P<0.05
3.3 炎性因子TLR-4、IL-1β mRNA表達結果
用藥1、5 d,模型組腦組織TLR-4 mRNA表達量明顯高于假手術組(P<0.05),涼血通瘀組明顯低于模型組(P<0.05)。
用藥1 d,模型組腦組織IL-1β mRNA表達量明顯高于假手術組(P<0.01),涼血通瘀組明顯低于模型組(P<0.01)。用藥5 d,模型組腦組織IL-1β mRNA表達量明顯高于假手術組(P<0.01)。見表6。
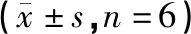
表6 各組大鼠腦組織TLR-4、IL-1β mRNA表達量
注:與正常組相比,$$P<0.01,$P<0.05;與假手術組比較,**P<0.01,*P<0.05;與模型組比較,##P<0.01,#P<0.05
4 討論
超氧化物歧化酶(SOD)能夠利用氧化還原金屬將超氧化物轉化成氧和過氧化氫,過氧化氫又被過氧化氫酶和過氧化物酶立即分解成無害的水,形成機體內天然存在的抗氧化機制[6]。脂質是氧化應激涉及最多的生物靶點,其氧化過程中會產生許多二級產物,這些產物主要是醛類如丙二醛(MDA)等,這些醛類持續存在且有高反應活性,易于產生高毒性分子,與核酸和蛋白質等生物大分子相互作用,誘導細胞凋亡[7]。神經系統調控神經型一氧化氮合酶(nNOS)的活化與去活化來調節一氧化氮(NO)的含量,從而調節腦部血流。腦出血后血腫周圍會出現不同程度的腦血流量改變,缺血缺氧后引發的氧化應激反應迅速產生大量NO,過量的NO會成為神經毒性物質。同時,NO作為信號分子,能夠啟動全身的炎癥反應,抑制nNOS活性是治療神經系統疾病的一個重要手段。TLR-4是各級炎性信號通路的初始開關,可激活下游NF-κB信號通路釋放大量炎癥因子,這些炎癥因子如IL-1β可直接或間接參與腦出血炎性反應[8]。IL-1β在繼發性腦損傷過程中大量分泌,可進一步激活巨噬細胞和星形膠質細胞,破壞血腦屏障通透性,誘導神經細胞凋亡,從而又加重腦水腫等繼發性腦損害,在惡性循環的腦損傷過程中炎性反應可級聯放大[9]。路夢茹[10]等研究發現抑制細胞內TLR-4表達后,可有效阻止TLR-4及下游炎癥因子IL-1β、IL-6等的信號傳遞和表達,從而減輕腦出血炎癥損傷。本實驗通過大鼠的腦出血模型來觀察神經功能修復水平,并測定可反映氧化應激和炎癥反應的指標,試從抗氧化和抗炎方面解釋涼血通瘀方對神經功能的保護作用。
實驗證明,經涼血通瘀方干預后的腦出血大鼠行為學評分明顯降低,神經功能缺損情況明顯改善。模型組在各時間點MDA含量和nNOS基因表達增高、CuZnSOD基因表達降低,表明腦出血后氧化應激反應活躍,超氧陰離子清除率降低,損傷血管和細胞功能。模型組造模后第1天和第5天TLR-4、IL-1β基因表達均明顯升高,表明炎癥反應與腦出血息息相關,腦出血后腦損傷激活TLR-4大量表達后激活下游的IL-1β大量表達,損害腦功能。涼血通瘀方對比模型組,在不同時間點明顯降低MDA含量和nNOS、TLR-4、IL-1β基因表達,提高CuZnSOD基因表達,發揮了抗氧化和抗炎作用。
綜上所述,涼血通瘀方能夠減輕氧化應激和炎癥反應,有效清除氧自由基,抑制炎癥的級聯放大效應,從而保護腦出血后的神經功能。本實驗為名老中醫的有效驗方的使用提供了現代科學依據。

