HPLC測定鹽酸法舒地爾注射液中異構體的含量
高宏濤 楊建玲 朱澤 陳云建
(昆藥集團股份有限公司 云南 昆明 650106)
鹽酸法舒地爾是由日本旭化成株式會社研制開發,是一種異喹啉磺胺衍生物[1],也是一種蛋白激酶抑制劑。鹽酸法舒地爾不僅對蛛網膜下腔出血后腦血管痙攣有較強的抗痙攣作用,對缺血腦組織也有一定的保護作用,所以鹽酸法舒地爾現已成為改善及預防蛛網膜下腔出血術后的腦血管痙攣及隨之引起的腦缺血癥狀的首選藥物。
根據處方、生產工藝及質量研究的相關文獻資料顯示[2-8],鹽酸法舒地爾的有關物質來源主要為工藝雜質、副產物和降解雜質。目前主要對異喹啉-5-磺酸、異喹啉、法舒地爾二聚體、N-氧化物、高哌嗪等已知雜質進行了相關質量研究和控制。
鹽酸法舒地爾的起始物料為5-異喹啉磺酸[1],該起始物料中可能含有磺化異喹啉雜質;導致在合成鹽酸法舒地爾的過程中,產生磺化異構體的衍生物,即法舒地爾的異構體雜質。
目前鹽酸法舒地爾注射劑的質量標準中未收錄異構體雜質的質控方法,而國內僅研究了鹽酸法舒地爾原料中一種異構體的檢測方法[9]。
本研究通過建立一種有效可行的HPLC法對鹽酸法舒地爾注射液中的2種異構體雜質(1位異構體衍生物和8位異構體衍生物)的含量進行測定,為更好地控制鹽酸法舒地爾注射液的質量提供依據。
鹽酸法舒地爾及其異構體雜質的化合物結果見圖1。
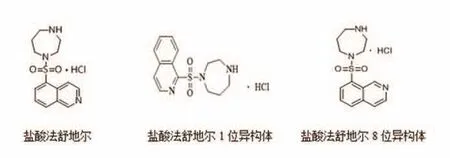
圖1 化合物結構式
1.儀器及試藥
SHIMAZDU LC20AD高效液相色譜儀(日本島津公司);XPE26電子天平(瑞士梅特勒-托利多公司);FE20型pH計(瑞士梅特勒-托利多公司)鹽酸法舒地爾注射液(昆藥集團股份有限公司);鹽酸法舒地爾1位異構體對照品(深圳博爾特公司,含量97.81%);鹽酸法舒地爾8位異構體對照品(深圳博爾特公司,含量97.61%);乙腈和三乙胺為色譜純;磷酸為分析純;水為自制雙蒸水。
2.方法與結果
2.1 色譜條件
采用十八烷基鍵合硅膠為填充劑的YMC-Pack Pro C18色譜柱(4.6×250mm,5μm),以1.5%三乙胺pH5.4:乙腈=87∶13為流動相A,乙腈為流動相B,流速:1.0ml/min,柱溫:30℃
檢測波長:275nm,進樣量:20μl,稀釋劑:1.5%三乙胺pH5.4:乙腈=85∶15,按下表1進行梯度洗脫。

表1 梯度洗脫表
2.2 溶液配制
2.2.1 1.5%三乙胺pH5.4:精密移取15ml三乙胺至985ml水中,用磷酸調pH至5.4,用0.22μm的水膜抽濾。
2.2.2 1.5%TEA (pH5.4)/乙腈(87/13,V/V):量取1.5%三乙胺(pH5.4)溶液870ml與乙腈130ml,混勻。
2.2.3 稀釋劑(空白溶劑):量取850ml 1.5%三乙胺(pH5.4)與150ml乙腈,混勻。
2.2.4 空白輔料溶液:取氯化鈉15mg,精密稱定,置50ml量瓶中,用稀釋劑溶解稀釋至刻度,搖勻,作為空白輔料溶液。
2.2.5 異構體雜質儲備液(5μg/ml):分別取異構體雜質1與異構體雜質2對照品各5mg,精密稱定,置100ml量瓶中,用稀釋劑溶解稀釋至刻度,搖勻;精密移取5ml,置50ml量瓶中,用稀釋劑稀釋至刻度,搖勻,作為雜質儲備液。
2.2.6 對照品溶液(0.005mg/ml):取鹽酸法舒地爾對照品5mg,精密稱定,置10ml量瓶中,用稀釋劑溶解稀釋至刻度,搖勻;精密移取1.0ml,置100ml量瓶中,用稀釋劑稀釋至刻度,搖勻,作為對照品溶液。
2.2.7 供試品溶液(0.48mg/ml):取鹽酸法舒地爾注射液10支并混勻,精密移取10ml置25ml量瓶中,用稀釋劑稀釋至刻度,搖勻;精密移取2ml置25ml量瓶中,用稀釋劑稀釋至刻度,搖勻,作為供試品溶液。
2.3 專屬性試驗
取空白溶劑、空白輔料溶液、異構體雜質儲備液和對照品溶液各20μl,照上述色譜條件進樣,記錄色譜圖(見圖2),鹽酸法舒地爾峰與相鄰雜質峰,各雜質峰間均能良好分離,空白溶劑色譜圖在各雜質以及主峰保留時間處無干擾,專屬性溶液中主峰與相鄰雜質以及各雜質之間分離度符合要求。本方法的專屬性良好。
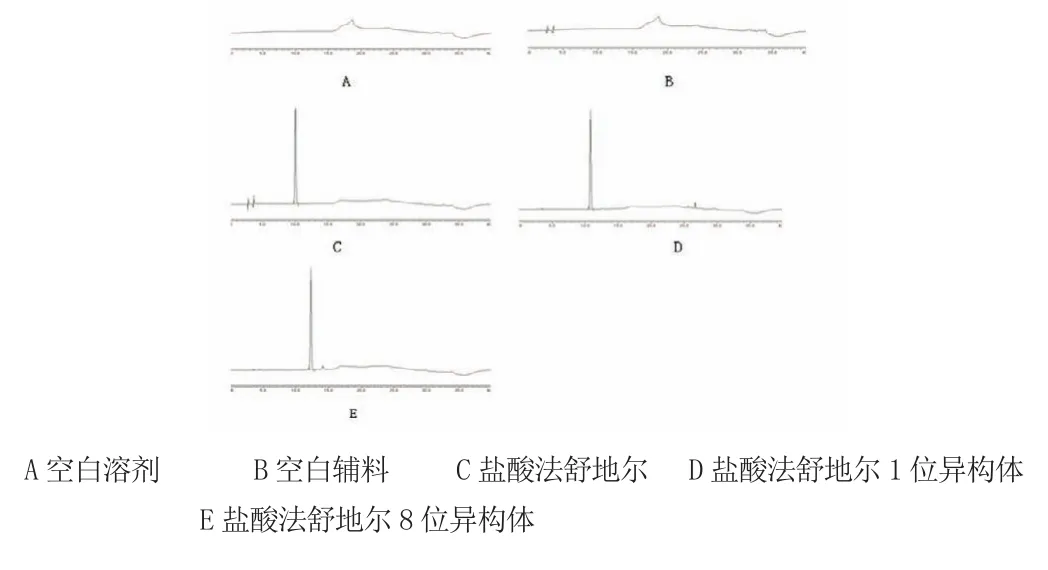
圖2 專屬性HPLC色譜圖
2.4 線性和范圍
分別取鹽酸法舒地爾1位異構體雜質和鹽酸法舒地爾8位異構體雜質對照品各5mg,加稀釋劑溶解稀釋成各雜質濃度為0.25、0.41、0.51、0.76、1.01和1.521的異構體雜質系列溶液,分別精密量取上述溶液20μl注入液相色譜儀,記錄色譜圖;以相應對照品的濃度(C)為橫坐標,對應的峰面積(A)為縱坐標,進行線性回歸。
結果顯示:鹽酸法舒地爾1位異構體在0.2539μg/ml~5.0780μg/ml濃度范圍內的線性關系良好,線性方程為y=0.1583 x+0.0044,相關系數r為0.9998;鹽酸法舒地爾8位異構體在0.2227μg/ml~1.3360μg/ml濃度范圍內關系良好,線性的線性方程為y=14669.9311x- 63.7465,相關系數r為0.9999。
2.5 定量限與檢測限
在選定的色譜條件下,分別取鹽酸法舒地爾1位異構體和鹽酸法舒地爾8位異構體的對照品溶液逐級稀釋,按信噪比3∶1和10∶1分別確定檢出限和定量限。
結果顯示:鹽酸法舒地爾1位異構體的定量限濃度為0.4062μg/ml,相對應的百分比含量為0.081%,檢測限濃度為0.1270μg/ml,相對應的百分比含量為0.025%;鹽酸法舒地爾8位異構體的定量限濃度為0.2227μg/ml,相對應的百分比含量為0.045%,檢測限濃度為0.1114μg/ml,相對應的百分比含量為0.022%。
2.6 準確度
精密移取8.0ml鹽酸法舒地爾注射液,置25ml量瓶中,用稀釋劑溶解稀釋至刻度,搖勻,作為供試品儲備液。按2.2.5項下雜質儲備液配制方法配制雜質儲備液,精密移取5.0ml,置50ml容量瓶中,用稀釋劑稀釋至刻度,搖勻,作為準確度雜質儲備液。照限度水平為0.05%、0.2%以及0.3%的各準確度溶液,每個濃度水平配制3份,精密量取空白供試品溶液以及各準確度溶液20μl,按要求注入高效液相色譜儀,記錄色譜圖,并計算回收率。
結果顯示:鹽酸法舒地爾1位異構體的單個回收率在93.21%~102.13%;9份溶液的平均回收率為98.30%,RSD為3.29%。鹽酸法舒地爾8位異構體的單個回收率在93.5%~102.6%;9份溶液的平均回收率為99.5%,RSD為4.0%。表明本方法準確度良好。
2.7 精密度
2.7.1 重復性 照2.2.5項下配制方法配制0.2%濃度水平加標溶液,平行配制6份。取空白供試品溶液以及各加標溶液20μl按要求分別注入高校液相色譜儀,記錄色譜圖,并計算每份溶液的回收率以及RSD。結果顯示:鹽酸法舒地爾1位異構體的回收率的RSD為3.0%;鹽酸法舒地爾8位異構體的回收率的RSD為2.1%。
2.7.2 中間精密度 在不同天、不同的分析人員、不同的液相系統,按重復性試驗項下的方法制備空白供試品溶液以及0.2%濃度水平加標溶液進行測定,計算每份溶液的回收率及RSD。
結果顯示:鹽酸法舒地爾1位異構體的回收率的RSD為3.63%。鹽酸法舒地爾8位異構體的回收率的RSD為2.4%。表明本方法具有較好的精密度。
2.8 溶液穩定性
取“重復性”下0.2%濃度水平的加標溶液分別置于室溫和冰箱(約5℃)中,精密量取上述溶液各20μl,分別于不同時間注入液相色譜儀,記錄色譜圖。
結果顯示:與0小時相比,加標樣品溶液在室溫條件下放置9小時,鹽酸法舒地爾1位異構體的最大絕對差值為0.01%,鹽酸法舒地爾8位異構體的絕對差值為0.01%;與0小時比較,加標樣品溶液在5℃條件下放置2天,鹽酸法舒地爾1位異構體的最大絕對差值為0.02%,鹽酸法舒地爾8位異構體的絕對差值為0.00%。加標樣品溶液在5℃條件下2天內穩定,加標樣品溶液在室溫條件下24小時內穩定。
2.9 耐用性
取“重復性”項下方法配制加標供試品溶液。改變色譜條件,測定供試品有關物質的量,見表2。
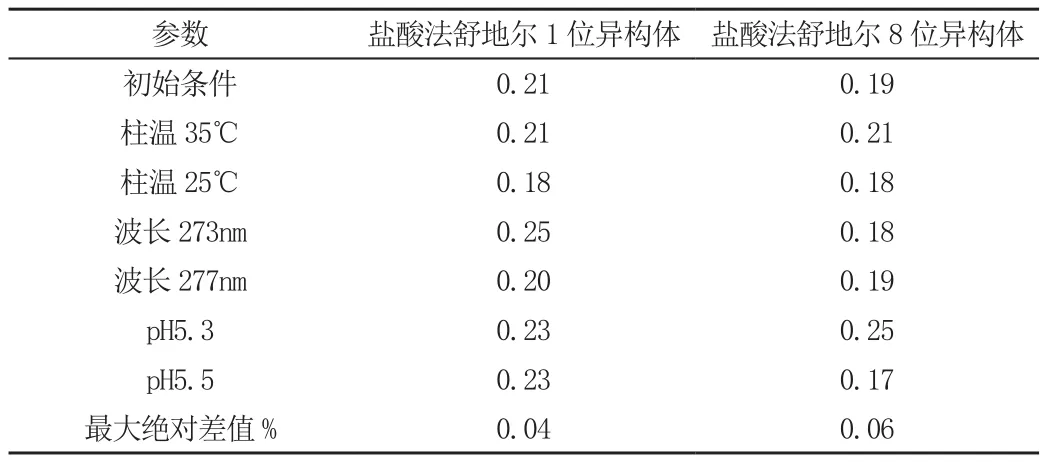
表2 方法耐用性試驗結果
結論:異構體雜質的絕對差值均小于0.1%,該方法在檢測波長273nm~277nm范圍內,柱溫在30℃~35℃范圍內,流動相pH在5.3~5.5范圍內,方法耐用性良好。
2.10 樣品的檢測
按“2.2”配制雜質對照溶液與3批供試品溶液,按“2.1”項下色譜條件進樣測定,按外標法計算鹽酸法舒地爾原料中異構體的含量。結果3個批號(批號:17EC01、17EC02、17EC03)注射劑樣品的異構體含量均未檢出。
3.討論
本試驗研究的鹽酸法舒異構體為原料起始原料中引入的異構體衍生物,為鹽酸法舒地爾的非對映異構體。由于該異構體雜質毒性數據未知,且本制劑為注射劑,必須嚴格控制原料中該雜質的含量,從而保證臨床用藥的安全性。
通過對方法的專屬性、線性與范圍、檢測限與定量限、準確度,精密度、耐用性、溶液穩定性的方法學研究,表明方法可用于鹽酸法舒地爾注射液中異構體雜質含量的檢測。

