電廠脫硫石膏制水泥緩凝劑二水石膏的研究
尤彩霞 ,李 軍 ,孫 娜 ,邸 青 ,胡俊要
(1.河北化工醫藥職業技術學院化學與環境工程系,河北石家莊050026;2.四川大學化工學院)
煙氣脫硫技術可分為干法脫硫、半干法脫硫以及濕法脫硫[1]。中國電廠以火力發電為主,目前大型燃煤電廠普遍采用濕法脫硫技術,脫硫效率達到90%以上[2]。中小型燃煤電廠普遍采用干法、半干法煙氣脫硫技術,以克服濕法脫硫技術的不足。干法、半干法脫硫多采用石灰/石灰石作為吸收劑,產生的脫硫渣由于含有亞硫酸鈣、碳酸鈣、氧化鈣、氯化鈣等使其利用十分困難,人們對亞硫酸鈣的氧化過程研究得最多[3-6],同時對廢渣制備石膏晶須以及石膏晶須對水泥基復合材料的影響也有研究[7-8]。在中國脫硫石膏的利用主要有兩大塊,即制作石膏板、用作水泥緩凝劑,尤其是在天然石膏資源缺乏的地區,其中用作水泥緩凝劑約占石膏利用總量的80%。在水泥熟料中加入一定量石膏,其摻入量一般不超過3.5%[9],可解決水泥的快凝問題[10],延長水泥使用過程中操作的時間和提高水泥的強度,降低水泥制品的干縮率,但是用作水泥緩凝劑的脫硫石膏有一定的技術規格。
目前干法脫硫石膏由于亞硫酸鈣含量較高,且容易被空氣中的O2氧化成硫酸鈣,用作混凝土摻合料時容易造成體積膨脹、產生裂紋,導致混凝土強度下降,使得干法脫硫石膏很難利用。筆者以電廠干法脫硫石膏為原料,采用催化氧化-重結晶技術,研究把亞硫酸鈣(CaSO3)氧化并重結晶形成晶形良好、便于過濾的二水石膏的工藝條件,以求尋找出一條經濟、易于操作、能耗低、成本低、無二次污染的制備水泥緩凝劑二水石膏的工藝路線。
1 實驗部分
1.1 原料、試劑和儀器
原料:某火力發電廠提供的干法脫硫石膏,亞硫酸鈣質量分數為35%±10%。
試劑:硫酸、氫氧化鈉、硫酸亞鐵、硫酸錳、碘、硫代硫酸鈉、可溶性淀粉,均為分析純。
儀器:DZKW-4型電子恒溫水浴鍋;S312型電子恒速攪拌器;DFG-6T型氣體流量計;ACO-002型氧氣泵;DHG-9070A電熱恒溫鼓風干燥箱;TGA/DSC2 1600熱重分析儀;XDS-1B型倒置攝影生物顯微鏡。
1.2 實驗方法和實驗裝置(見圖1)
1)取一定量干法脫硫石膏與一定量水置于1 000 mL燒杯中,攪拌均勻,同時加入一定量催化劑(硫酸亞鐵與硫酸錳)。
2)將制備的料漿倒入三口圓底燒瓶中,用一定濃度的硫酸及氫氧化鈉溶液調節料漿pH,用鼓風機向漿液中通入空氣,并且用流量計測量氣速,亞硫酸根與空氣中的氧氣進行催化氧化反應:

3)待反應一定時間后,過濾,所得濾餅即為產品,母液用于循環利用。
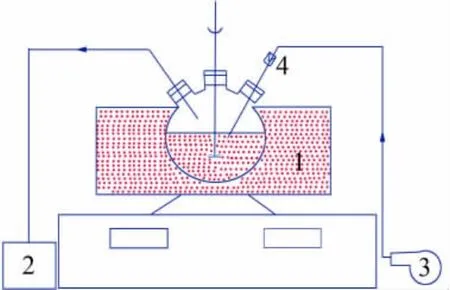
圖1 亞硫酸鈣催化氧化制備二水硫酸鈣裝置圖
1.3 測定方法
1.3.1 亞硫酸鈣含量的測定[11]
稱取2.000g經過預處理的反應產物(m),將其放入三角瓶中,同時取50mL蒸餾水、5mL稀硫酸(1+1)、1~2 mL 淀粉溶液于三角瓶中,用碘液(0.05 mol/L)滴加至過量,記下碘液消耗的體積V1(mL)。用硫代硫酸鈉標準溶液(0.1 mol/L)滴定過量碘液,溶液由藍色變為無色即為滴定終點,硫代硫酸鈉標準溶液消耗的體積記為V2(mL)。
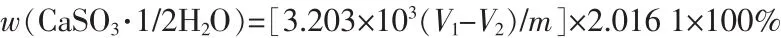
式中:1 mL 碘液相當于 64.063 8c(I2)×10-3g SO2;2.016 1為SO2換算成CaSO3·1/2H2O的系數。
1.3.2 結晶水含量的測定
稱取反應后的濾餅1.000 g置于稱量瓶(烘干至質量恒定,m0)中,在45~60℃真空條件下烘干至質量恒定,在干燥器中冷卻至室溫稱其質量(m1);繼續將樣品在230℃以上烘干至質量恒定,在干燥器中冷卻至室溫稱其質量(m2)。 結晶水含量=(m1-m2)/m1×100%。
2 實驗結果與討論
2.1 各因素對亞硫酸鈣轉化率的影響
2.1.1 溶液pH的影響
固定條件:反應時間為 1.5 h,空氣流速為0.25 m3/h,液固比為5∶1,催化劑用量為7.5。 改變溶液pH進行實驗,考察pH對亞硫酸鈣轉化率的影響,實驗結果見圖2。由圖2可知,在pH較低條件下(pH<5),亞硫酸鈣轉化率較高且變化不大;之后隨著pH繼續增大,亞硫酸鈣轉化率隨之減小。這是由于,隨著pH降低亞硫酸鈣溶解度會隨之增加,有利于催化氧化反應的進行;隨著pH升高,亞硫酸鈣溶解度會隨之減小,同時復合催化劑中Fe2+等容易發生價態變化,進而以沉淀形式析出,降低催化劑有效質量。但是,亞硫酸鈣催化氧化體系pH不宜過低,隨著pH降低更容易對工業設備造成腐蝕。因此,適宜pH 為 4~5。
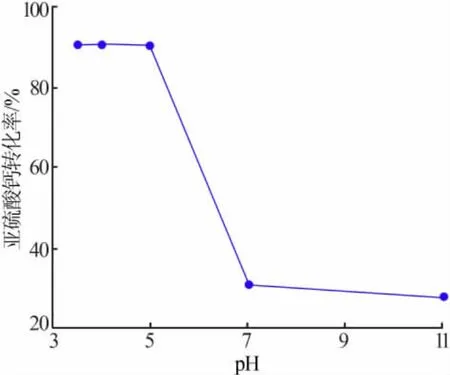
圖2 不同pH條件下亞硫酸鈣轉化率
2.1.2 液固比的影響
固定條件:反應體系pH=4~5,反應時間為1.5 h,空氣流速為0.25 m3/h,催化劑用量為7.5。改變液固比進行實驗,考察液固比對亞硫酸鈣轉化率的影響,實驗結果見圖3。圖3表明,隨著液固比增加,亞硫酸鈣轉化率隨之增大。亞硫酸根的氧化實質是氣、液、固三相反應,在此反應過程中氧通過氣液膜擴散至液相中,SO32-和HSO3-通過固液膜擴散至液相中并與氧反應。當溶液中亞硫酸根濃度增大到一定值后,催化氧化反應速率與CaSO3漿液濃度及催化劑濃度無關,與氧氣的擴散速率有關。隨著料漿中液固比越大,空氣中的氧擴散速率將會增大,有利于料液中亞硫酸鈣的轉化。但是同時液固比增大,耗能會隨之增加。因此,液固比也不能太大。適宜的液固比為10∶1。
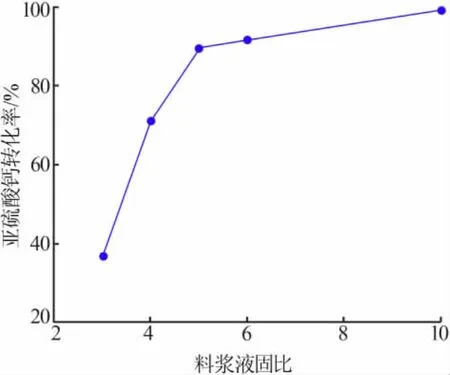
圖3 不同液固比條件下亞硫酸鈣轉化率
2.1.3 空氣流速的影響
固定條件:反應體系pH=4~5,反應時間為1.5 h,液固比為10∶1,催化劑用量為7.5。改變空氣流速進行實驗,考察空氣流速對亞硫酸鈣轉化率的影響,實驗結果見圖4。圖4表明,隨著空氣流速增加,亞硫酸鈣轉化率呈上升趨勢。隨著料漿中通入空氣的速度變大,料漿的湍動程度增強,有利于氧氣在料液中的擴散。同時空氣流速增大,會增加料漿與空氣的接觸面積以及接觸時間。但是,空氣流速過大,若在連續化生產中石膏料漿中夾帶液體會隨之增加,給后續石膏晶體和母液分離造成困難。因此,適宜的空氣流速為0.15 m3/h。
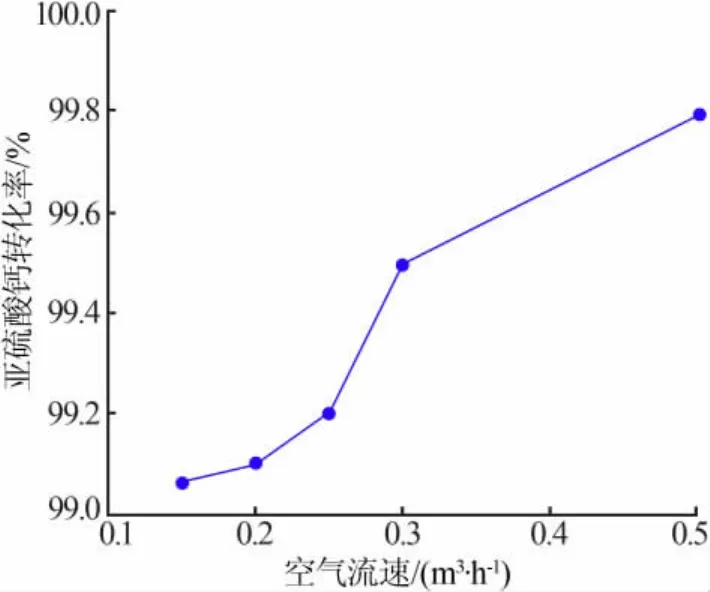
圖4 不同空氣流速條件下亞硫酸鈣轉化率
2.1.4 催化劑用量的影響
固定條件:反應體系pH=4~5,反應時間為1.5 h,空氣流速為0.15 m3/h,液固比為10∶1。改變催化劑用量進行實驗,考察催化劑用量(亞硫酸鈣與催化劑的質量比)對亞硫酸鈣轉化率的影響,實驗結果見圖5。圖5表明,隨著催化劑用量增加,亞硫酸鈣轉化率增加。亞硫酸鈣的催化氧化反應是氣、液、固三相反應,當溶液中亞硫酸鈣濃度到達一定值后,反應主要受氧氣擴散到溶液主體中的氣液膜控制,隨著催化劑用量增加氧化速度加快,亞硫酸鈣轉化率增加。當催化劑用量為7.5時,亞硫酸鈣轉化率接近100%。因此,適宜的催化劑用量為7.5。
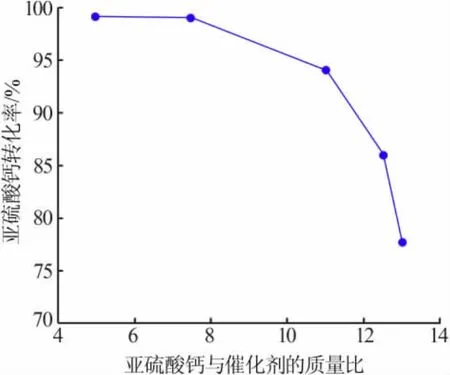
圖5 不同催化劑用量條件下亞硫酸鈣轉化率
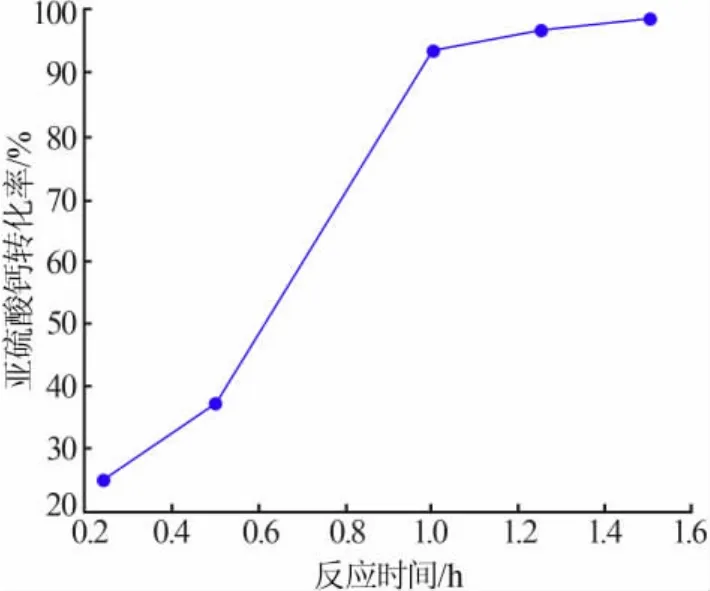
圖6 不同反應時間條件下亞硫酸鈣轉化率
2.1.5 反應時間的影響
固定條件:反應體系pH=4~5,催化劑用量為7.5,空氣流速為 0.15 m3/h,液固比為 10∶1。改變反應時間進行實驗,考察反應時間對亞硫酸鈣轉化率的影響,實驗結果見圖6。圖6表明,隨著反應時間增加,亞硫酸鈣轉化率隨之增加。但是,當反應時間增加到一定值時,亞硫酸鈣轉化率增長趨勢趨于平緩。當反應時間達到1.5 h時,亞硫酸鈣轉化率接近100%。因此,適宜的反應時間為1.5 h。
2.2 CaSO4·2H2O產品形貌及熱重-差熱分析
以燃煤電廠干法脫硫石膏為原料,采用上述優化催化氧化工藝條件,即:反應體系pH=4~5、催化劑用量為7.5、空氣流速為0.15 m3/h、液固比為10∶1,反應時間為1.5 h,制得二水硫酸鈣產品顆粒形貌以及熱重-差熱(TG-DTA)曲線見圖7、圖8。從圖7看出,二水硫酸鈣結晶粗大、粒徑均勻。結晶產品顆粒粗大,可縮短過濾時間,降低能耗。從圖8看出,DTA曲線在100~180℃發生了吸熱變化,TG曲線顯示產品質量損失約為20%。由圖7和圖8可知,制得的產品為二水硫酸鈣。

圖7 二水硫酸鈣產品晶體形貌圖
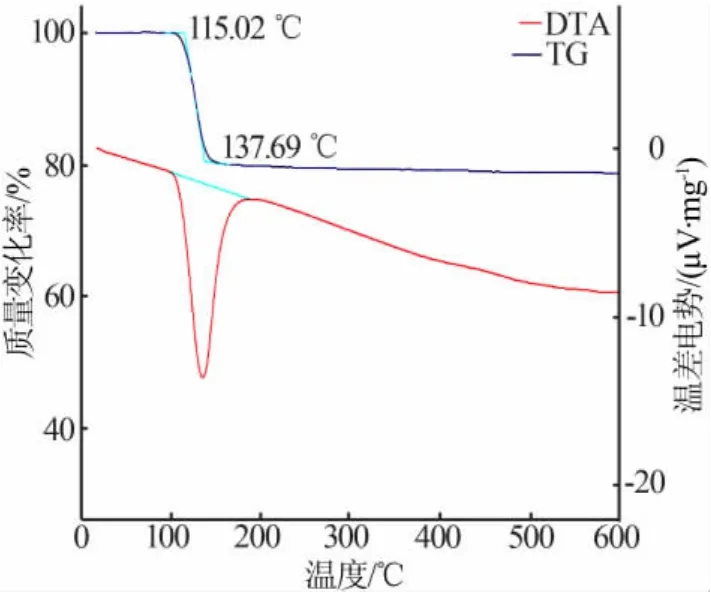
圖8 二水硫酸鈣產品TG-DTA曲線
3 結論
以電廠干法脫硫石膏為原料,采用催化氧化-重結晶技術把亞硫酸鈣氧化并重結晶,制成晶形良好便于過濾的石膏(CaSO4·2H2O)。該工藝流程簡單、設備簡單、能耗低(反應溫度為50℃左右)、無二次污染、經濟可行,適合小型電廠解決干法脫硫石膏的回收利用問題。優化條件:反應體系pH=4~5,催化劑用量為7.5,空氣流速為0.15 m3/h,液固比為10∶1,反應時間為1.5 h。在此條件下亞硫酸鈣轉化率將近100%。制得的CaSO4·2H2O產品粒徑均勻、顆粒粗大,便于過濾,為工業化放大奠定了基礎。

