龍眼類受體蛋白激酶CRK家族全基因組鑒定及表達調控分析
孫瑩 林藝靈 趙鵬程 徐小萍 陳曉慧 申序 林玉玲 賴鐘雄


摘 ?要??為了解龍眼富含半胱氨酸的類受體蛋白激酶(cysteine-rich receptor-like kinase,CRK)家族的基本特征與功能,本研究采用生物信息學分析方法對篩選出的98個龍眼CRK基因家族的成員進行分析鑒定,包括分子進化樹的構建和對蛋白結構域及其特性、啟動子及其順式作用元件、體胚發(fā)生的過程以及組織器官特異性表達的分析。結果顯示:通過對龍眼和擬南芥CRK基因做進化樹分析,可根據親緣關系的遠近將其分為7個亞家族;不同亞家族成員的蛋白質特性(氨基酸數量、相對分子質量、等電點、信號肽及糖基化位點)有所不同;各成員基因結構特性,啟動子順式作用元件,蛋白結構域特性等與進化樹中家族成員親緣關系的遠近相關;98個CRK家族成員在體胚發(fā)生過程(NEC、EC、ICpEC、GE)以及生長發(fā)育過程中組織器官特異性表達情況有所不同,其中在非胚性愈傷組織以及幼果中表達量較高,在種子和果實中幾乎未表達。此外,富含半胱氨酸的類受體蛋白激酶在生物脅迫、非生物脅迫(抗病蟲害、抗旱、抗寒、抗鹽脅迫等)以及在植物生長發(fā)育過程中起著重要作用。
關鍵詞 ?龍眼;CRK;基因家族;鑒定;表達調控中圖分類號??S667.2??????文獻標識碼??A
Genome-wide Identification and Regulation of Expression Analysis of Cysteine-rich Receptor-like Kinase in Longan
SUN?Ying, LIN Yiling,?ZHAO Pengcheng, XU?Xiaoping, CHEN Xiaohui, SHEN Xu, LIN Yuling,LAI Zhongxiong*
Institute of Horticultural Biotechnology, Fujian Agriculture and Forestry University, Fuzhou, Fujian?350002, China
Abstract ?In order to understand the basic characteristics and functions of cysteine-rich receptor-like kinase (CRK) family in longan, a series of bioinformatics methods were used to analyze and identify 98 members ofCRKgene family?members, including constructing the molecular evolutionary tree, analyzing protein domains and characteristics, promoters, homeopathic elements, somatic embryogenesis and tissue-organ specific expression. Results showed?that the?CRK gene of longan andArabidopsiscould be divided into seven subfamilies according to the distance of the relationship by evolutionary tree analysis, and the protein characteristics (the quantity?of amino acids, the relative molecular weight, the isoelectric point, the signal peptide and sites?of glycosylation) of different subfamilies were?different. Structural characteristics of the genes?of each member, promoter homeopathic elements and protein domain characteristics were?closely related to family members in the evolutionary tree.?The specific expression of 98?CRK family members during somatic embryogenesis (NEC, EC, ICpEC, GE) and growth were different, particularly higher in non-embryogenic callus and young fruits, but they were?almost not expressed in seeds and matured?fruits. In addition, cysteine-rich receptor-like protein kinases?played?important roles?in biological stress, abiotic stress (insect-induce diseases, drought resistance, cold resistance, salt resistance, etc.) and it played?important roles?in plant growth and development as well.
Keywords ?longan;CRK;?gene family; identification; regulation of expression
DOI10.3969/j.issn.1000-2561.2019.10.005
富含半胱氨酸類受體蛋白激酶(cysteinerich receptor-like kinase, CRK)在植物類受體蛋白激酶(receptor-like kinase, RLK)家族中具有重要地位,在植物生長發(fā)育、激素信號傳導、生物和非生物脅迫以及植物抗病性細胞過敏性死亡中發(fā)揮著至關重要的作用[1-2]。
國內外研究發(fā)現CRK家族基因可調控植物生長發(fā)育及抵抗逆境。在對擬南芥的CRK基因研究中:CRK45通過調控ABA的生物合成而調控著對非生物逆境脅迫,如干旱、高鹽以及ABA的響應,對植物耐藥性有正向調控作用,即與抗病性相關,參與了水楊酸介導的抗病信號途徑[3];CRK5是參與調節(jié)基本生理過程的生化機制的重要組成部分,CRKs突變體的功能特性表現出氣孔導度降低和衰老加速,與活性氧種類的積累有關,CRK5可以在紫外線照射下表現出細胞死亡和氧化損傷的增強[4],轉基因擬南芥對紫外線強度的適應性可通過過表達CRK5來增強[4];CRK17受水楊酸誘導表達參與植物的抗病防御反應[5];用誘導型啟動子過量表達CRK4、CRK5、CRK19、CRK20能引起過敏反應導致細胞程序化死亡[4-6];CRK13可通過依賴水楊酸抑制病原菌[7]。從番茄分離的CRK1基因在花粉中可以特異性表達[8];菜豆中CRK基因PvPK20-1可調控病原菌、共生菌與腫瘤因子[9];水稻中OsCRK1基因沉默后嚴重影響水稻對白葉枯病的抗性,可證明其與葉枯病抗性密切相關[10];在甜瓜中,大多數CRK基因在白粉病和ABA脅迫后下調表達,在鹽和低溫處理后上調表達,并對冷害脅迫表現較強烈[11]。
龍眼(Dimocarpus longanLour.)是我國重要的亞熱帶果樹,種植面積及產量均居世界首位[12]。但高溫、干旱、鹽堿、寒冷等非生物脅迫以及生物脅迫均會對龍眼的生長發(fā)育造成不良影響,且現今對龍眼生物和非生物脅迫耐受的分子調控機制了解較為匱乏。因此,通過對CRK基因家族的分析,在龍眼生長發(fā)育以及抗逆性研究中具有重大意義。本文通過對龍眼CRK家族成員進行分析鑒定以及表達調控研究(進化樹分析、基因結構分析、啟動子順式作用元件分析、蛋白保守結構域分析以及在不同體胚發(fā)生過程中和生長發(fā)育階段不同組織器官特異性表達的FPKM值分析),了解了CRK家族基因及其在龍眼中的表達情況,可為CRK家族在龍眼生長發(fā)育及對其他植物調控的研究中提供理論基礎。
1??材料與方法
1.1材料
1.1.1 ?實驗材料??實驗材料為福建農林大學園藝植物生物工程研究所提供的‘紅核子品種龍眼體胚發(fā)生早期胚性愈傷組織(embryonic callus, EC)、非胚性愈傷組織(non-embryoniccallus, NEC)、不完全胚性緊實結構(incomplete embryonic compact structure, ICpEC)、球形胚(globular embryo, GE)[13]。
1.1.2 ?數據來源??實驗室構建的龍眼基因組數據庫(NCBI登錄號:BioProject PRJNA305337);龍眼轉錄組數據庫(SRA050205);擬南芥(Arabidopsis thaliana)CRK基因家族成員序列下載于https://phytozome.jgi.doe.gov/pz/portal.?html。
1.2方法
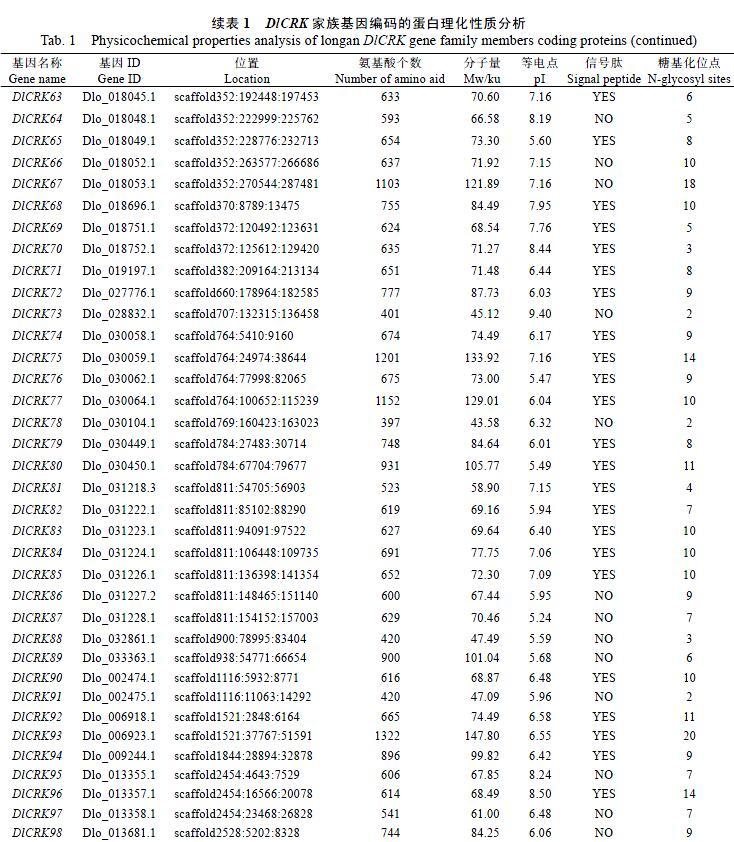
1.2.1 ?龍眼CRK基因家族成員的鑒定及其基本理化性質分析??對龍眼CRK基因家族成員進行鑒定,經龍眼基因組數據庫同源對比,篩選獲得98條具有完整Open Reading Frame(ORF)的龍眼CRK候選序列。根據基因注釋,采用DNAMAN 6.0軟件對CRK的gDNA、CDS以及啟動子序列進行比對分析,結合NCBI Blast同源比對分析,初步確定龍眼CRK家族成員。其次,根據其基因座位置[14],將龍眼CRK家族成員命名為CRK1-CRK98(表1)。此外,從ExPASy(www.expasy.org)中獲取CRK家族的基本理化性質,并對其分子量(Mw)、氨基酸個數(aa)、等電點(pI)、信號肽(signal peptide)及其糖基化位點(N-glycosyl sites)進行系統(tǒng)的分析。
1.2.2CRK基因家族進化樹構建??采用MEGA 6.06軟件中的鄰近法Neighbor-joining method對龍眼98個基因進行進化樹分析,且將龍眼、擬南芥2個物種共141條CRK家族氨基酸序列構建系統(tǒng)進化樹,手動刪除同源差異較大的序列后進行Bootstrap分析,設置參數為1000次重復性檢驗。最后使用iTOL(itol.embl.de)對進化樹進行修飾編輯。
1.2.3??龍眼CRK基因家族啟動子順式作用元件及蛋白結構域分析??本研究利用PlantCARE對龍眼CRK家族基因各成員ATG上游2000 bp序列進行分析以及利用TBtools結合龍眼CRK家族基因本身進化樹進行啟動子順式作用元件分析。為了進一步了解不同龍眼CRK蛋白間motif組成的相似性和多樣性,可利用MEME(http://meme)對龍眼CRK蛋白序列中的motif進行預測,其中參數為:保守基序最小寬度≥6,最大寬度為50,保守基序數目設置為25,其他參數為默認值,最后利用TBtools結合龍眼CRK家族自身進化樹繪制分析圖,對蛋白結構域進行預測分析。
1.2.4??龍眼CRK基因家族不同成員的不同組織器官特異性表達分析??為了解各成員在龍眼不同組織器官或在胚胎中可能發(fā)揮的功能特點,通過結合龍眼基因組數據庫提取的CRK家族基因在不同體胚發(fā)生階段NEC、EC、ICpEC、GE以及不同組織器官(種子、根、莖、葉、花、花蕾、果肉、幼果、果皮)中特異表達的FPKM值,分析龍眼CRK基因家族各成員在不同組織器官中特異性表達情況。
2??結果與分析
2.1龍眼CRK基因家族成員的鑒定及其基本理化性質分析
根據CRK家族基因成員基因座的位置將98個成員命名為DlCRK1~DlCRK98。為進一步分析龍眼CRK基因家族的基因結構特征,了解其生物學功能,因此對龍眼98條基因的基因結構進行內含子、外顯子數目及位置進行分析。結果顯示,龍眼CRK基因長度介于2~39 kb,其中大部分CRK基因長度小于5 kb;外顯子數目5~14個,其中大多數外顯子個數為6~8個。
對龍眼DlCRK家族氨基酸序列的基本理化性質進行分析,結果如表1所示,龍眼CRK家族成員的蛋白質分子量為26.09 ku(DlCRK53)~147.8 ku(DlCRK93),其中大部分基因蛋白分子量分布在60~90 ku之間,平均值為79.34 ku;等電點在5.01(DlCRK41)~9.49(DlCRK5)之間,平均值為6.74,其中pI值大于7的有80條,即大部分為酸性;DlCRK5、DlCRK21、DlCRK35、DlCRK43、DlCRK51、DlCRK66等39個成員不含有信號肽,剩余59個成員均含信號肽,可以引導蛋白質在細胞內運輸;糖基化位點有1個(CRK53)~20個(CRK93),大部分分布6~14個,糖基化是一種蛋白轉錄翻譯后的修飾方式,在生命活動中起重要作用,糖基化位點的多少可能嚴重影響細胞的生命活動[15]。
2.2 CRK基因家族進化樹構建
采用龍眼CRK氨基酸序列進行進化樹構建時手動刪除一個同源差異較大的基因Dlo-?011283.1(DlCRK53),將該基因的長度、蛋白質分子量以及糖基化位點與其他基因相對比,其數值明顯較低,且與其他基因的同源差異大,龍眼CRK家族基因與其他模式作物的CRK家族基因親緣關系較遠。利用龍眼和擬南芥2個物種共141條基因在手動刪除3條同源差異較大的基因(Dlo-011283.1?DlCRK53、Dlo-032861.1?CRK88、AT4G23170)后構建進化樹,可將龍眼和擬南芥2個物種的CRK蛋白家族分為7類(圖1):Group1中只含有龍眼CRK家族基因,這部分基因與擬南芥CRK基因同源差異較大,Group4中含有大部分ATCRK基因家族成員與DlCRK46、DlCRK63等聚類相對較近,其余各組中ATCRK基因相對較少且同物種間同源性高。
2.3龍眼CRK基因家族啟動子順式作用元件分析
通過對龍眼CRK基因家族的啟動子預測結果分析表明,龍眼CRK家族的啟動子區(qū)域富含光響應、逆境脅迫響應以及植物激素響應的順式作用元件。逆境脅迫中包括低溫脅迫、干旱脅迫、創(chuàng)傷修復等非生物脅迫。龍眼CRK家族98個成員中可將97個進行聚類,繪制進化樹與其啟動子順式作用元件結合,其中DlCRK53同源差異較大,對其單獨作圖(圖2)。其中所有CRK基因啟動子均包含至少1個光響應元件;92%的基因響應脫落酸、赤霉素、茉莉酸甲酯、生長素等激素應答;此外,86%的基因序列包含厭氧誘導所必需的元件,其中DlCRK44、DlCRK51、DlCRK97、DlCRK12這4個基因還參與缺氧特異性誘導。含有MBY轉錄因子是龍眼CRK基因的另一個值得注意的特點,其中72%的龍眼CRK基因包含MYB光響應以及干旱誘導的結合位點,DlCRK98、DlCRK69、DlCRK23、DlCRK31、DlCRK34中包含黃酮類化合物生物合成相關基因調控的MYB轉錄因子結合位點;還有部分基因(DlCRK41、DlCRK7、DlCRK67、DlCRK68、DlCRK15、DlCRK81、DlCRK31、DlCRK40)包含與細胞周期相關的順式作用元件。總之,龍眼CRK基因家族含有多個順式作用元件可推測其在功能上的多樣性。
2.4龍眼CRK基因家族蛋白結構域分析
為解龍眼CRK家族基因在龍眼中的蛋白保守結構域特點以及分布情況,使用MEME搜索出25個motif。大部分序列(圖3)包含motif10(81)、motif6(74)、motif8(82)、motif17(73),說明這4個基序在龍眼CRK基因家族中比較保守。龍眼CRK基因具有相對保守的蛋白功能結構域(圖4),功能結構域分析顯示68條基因具有STKc_IRAK結構域,只有DlCRK80和DlCRK86具有B_lecyin結構域。而不能與其他成員進行聚類的CRK53其長度較短,相應的蛋白結構域也僅有一個,其功能特性有缺失。通過對龍眼CRK蛋白家族系統(tǒng)發(fā)育樹的分析結果可知,位于進化樹同一個分支的同源基因有相似的功能結構域,進一步推測這些基因具有相似的生物學功能。
2.5龍眼CRK基因家族不同成員在體胚發(fā)生早期不同階段和不同組織器官特異性表達分析
為了解龍眼CRK基因家族成員們在龍眼體胚發(fā)生的不同時期,生長發(fā)育過程中不同組織器官中所起到的作用,利用龍眼全基因組數據庫中獲得DlCRK基因家族成員在體胚發(fā)生早期不同階段,以及生長發(fā)育階段不同組織器官的FPKM值,制作熱圖對其進行分析(圖5)。除了DlCRK36、DlCRK97、DlCRK80、DlCRK88、DlCRK67這5個DlCRK成員在整個體胚發(fā)生過程以及生長發(fā)育階段的不同器官中都不表達,其余93個DlCRK成員在體胚發(fā)生早期不同階段或不同組織器官中都有所表達;在不同體胚發(fā)生階段,98個成員中有22個成員在體胚發(fā)生階段完全不表達,其余76個成員大部分在非胚性階段(NEC)顯著表達,少量成員在CE、ICPEC、GE階段顯著表達;另外,龍眼CRK家族成員在不同組織器官形態(tài)建成方面(幼果、種子、花、花蕾、葉子、果皮、莖)也發(fā)揮著重要作用,但在種子和果實階段幾乎未表達。
在不同體胚發(fā)生過程有11種表達模式:DlCRK31、DlCRK7、DlCRK46、DlCRK29、DlCRK56、DlCRK18、DlCRK22、DlCRK19、DlCRK34、DlCRK37、DlCRK35、DlCRK21、DlCRK11、DlCRK98、DlCRK79、DlCRK6、DlCRK53這17個基因在體胚發(fā)生早期的4個階段(NEC、EC、ICpEC、GE)均未表達,不同組織器官中少量表達;在NEC階段上調表達而其他階段都下調表達(DlCRK25、71、76、64、1、50、2、43、85、83、55、44、66、20、89、17、40、32、8、59、77、12、61、49、74、60、45、48、5、68、93、3、96);在EC階段上調表達其他階段都下調表達(DlCRK58、41、72);在ICpEC階段上調表達在其他階段都下調表達(DlCRK30、47、65、9);在NEC和EC階段上調表達其他階段都下調表達(DlCRK14且在EC階段上調表達不明顯);在NEC和ICPEC階段中表達其他階段下調表達(DlCRK24、91、92、69、4、26、84、95、73、63);在NEC和GE階段上調表達其他階段下調表達(DlCRK10、39、13);在EC和ICPEC階段上調表達其他階段下調表達(DlCRK94、42、33、16、78、62、51、96、92);在EC和GE階段上調表達其他階段下調表達(DlCRK28);在ICpEC和GE階段上調表達其他階段下調表達(DlCRK38、54、57、27、90、75、87、73);DlCRK81、94、15在EC、ICpEC、GE階段均上調。總體來看龍眼CRK家族成員在體胚發(fā)生過程中主要呈下調趨勢。
在研究中發(fā)現番茄的SlCRK1基因在花這一器官中表達具有組織特異性(具有花粉特異性的順式作用元件)[8]。根據龍眼CRK基因家族成員在不同組織器官中特異性表達分析結果來看,部分基因在花中顯著表達,所以很可能龍眼CRK家族成員在花這一器官中也具有組織特異性的表達。在DlCRK64、90、74、81中含有種子特異性的順式作用元件,但DlCRK家族成員在龍眼種子中并未表達,表明雖含有與某種功能相關的順式作用元件,但最終并不一定會在組織器官中表達出來。擬南芥CRK5可以通過控制植物光和作用來控制植物的生長發(fā)育[4],在龍眼CRK家族成員中有與光響應相關的順式作用元件。對于龍眼來說與光合作用相關性最大的組織器官為葉子,與之相對應有一部分DlCRK基因在葉子中顯著表達,所以龍眼CRK家族成員可能通過對植物色素合成、葉片上氣孔數量[26]等因素的調控來影響植物光合作用以及抵抗光脅迫[18-20]。龍眼CRK基因家族成員在幼果中表達量呈上調趨勢,說明龍眼CRK基因家族成員在花粉的特異性以及在幼果的形成過程中起著重要作用。龍眼CRK家族成員在胚胎與組織表達特性具有多樣性與特異性,對整個龍眼生長發(fā)育過程有著重要影響。
3.3大多數基因受植物激素和逆境調控
龍眼CRK家族成員中,大部分具有抵抗各種逆境以及受不同激素調控的順式作用元件,其中包含低溫脅迫、干旱脅迫、創(chuàng)傷修復等非生物脅迫;響應脫落酸、赤霉素、茉莉酸甲酯、生長素等激素應答。脫落酸在種子和芽休眠的起始和維持過程中起著重要作用[27],脫落酸可能通過調控龍眼CRK家族基因的表達來影響種子與芽的休眠過程;赤霉素能調節(jié)種子中淀粉酶的合成,來打破種子休眠,進而促進莖尖分生組織的細胞分裂,增強頂端優(yōu)勢,也可使果實增大[28],所以龍眼CRK家族基因可能與淀粉酶的合成相關,以此影響種子休眠以及植物生長發(fā)育。植物激素在整個植物生長發(fā)育過程中起著重要作用,而龍眼CRK家族成員大多數受多種植物激素調控,進一步說明了龍眼CRK基因家族對龍眼生長發(fā)育過程中起重要作用。
在龍眼中已發(fā)現多個基因家族中含有抵抗逆境相關的功能:龍眼漆酶家族基因可以通過影響細胞壁組成來響應非生物脅[29];DlUGD6參與龍眼中細胞壁多糖合成,可影響植物對逆境的抵抗[30];龍眼Hsf可能通過DNA甲基化來影響植物對逆境的抵抗[13];龍眼ERF家族基因與乙烯之間存在負調控[31]。那么龍眼中CRK基因家族成員抵抗逆境的機理是什么呢?蛋白激酶主要是通過激活不同磷酸化途徑來介導外界環(huán)境信號的感知與傳遞,調控下游抗逆基因的轉錄表達來啟動相應的生理生化等適應性的反應來降低或者消除危害[22]。有研究發(fā)現擬南芥中CRK45在植物應答非生物脅迫(干旱、高鹽以及ABA脅迫)中發(fā)揮著重要作用[3],參與水楊酸介導的抗病信號途徑的轉變[3];AtCRK45和AtCRK36在植物細胞內共同作用,并且參與應答脫落酸和滲透脅迫信號的負調控反應[3,10]。以上可說明龍眼CRK家族基因可能通過感知和傳遞信號來調控抗逆基因的表達,來啟動適應逆境的能力。另外,植物激素可以對擬南芥CRK基因家族成員進行轉錄調控[32];而龍眼CRK家族成員中有許多響應激素應答的順式作用元件,其必然與植物抗逆性有直接或間接相關。在植物的生長發(fā)育過程中植物激素起著重要作用,而植物抵抗逆境的能力直接決定了植物能否正常的生長發(fā)育,因此龍眼CRK家族成員對植物激素的響應與抵抗逆境的能力息息相關。
參考文獻
[1]張中起, 王 ?嬌, 靳 ?煒, 等. 陸地棉CRK基因家族的鑒定及其表達分析[J]. 中國農業(yè)科學, 2018, 51(13): 2442-2461.
[2]Elsa-Herminia?Q, Gabriel-Xicoténcatl?G, Manoj-Kumar?A,?et al.Cysteine-rich receptor-like kinasegene family identification in the phaseolus genome and comparative analysis of their expression profiles specific to mycorrhizal and rhizobial symbiosis[J]. Genes, 2019, 10(1): 59.
[3]Zhang X?J, Han X?M, Shi R,et al.Arabidopsiscysteine-rich receptor-like kinase 45positively regulates disease resistance to pseudomonas syringae[J]. Plant Physiology and Biochemistry: PPB/Société Fran?aise de Physiologie Végétale, 2013, 73: 383-391.
[4]Pawe??B, Anna?R, Damian?W,et al.Cysteine-rich receptor-like kinase CRK5 as a regulator of growth development and ultraviolet radiation responses inArabidopsisthaliana[J]. Journal of Experimental Botany, 2015, 66(11): 3325-3337.
[5]Ohtake Y, Takahashi T, Komeda Y. Salicylic acid induces the expression of a number ofreceptor-like kinasegenes inArabidopsis thaliana[J]. Plant and Cell Physiology, 2000, 41(9): 1038-1044.
[6]Chen K, Fan B, Du L,et al. Activation of hypersensitive cell death by pathogen-inducedreceptor-like protein kinasesfromArabidopsis[J]. Plant Molecular Biology, 2004, 56(2): 271-283.
[7]Acharya B R, Surabhi?R, Maqbool S B,et al. Overexpression ofCRK13, anArabidopsis cysteine-rich receptor-like kinase, results in enhanced resistance toPseudomonas syringae[J]. The Plant Journal, 2007, 50(3): 488-499.
[8]Woong B, So Y, Sang K,et al. Identification of a pollen-specificgene,SlCRK1(RFK2)in tomato[J]. Genes & Genomics, 2014, 36(3): 303-311.
[9]Lange J, Xie Z, Broughton W J,et al. A gene encoding areceptor-like protein kinase in the roots of common bean is differentially regulated in response to pathogens symbionts and nodulation factors[J]. Plant Science, 1999, 142(2): 133-145.
[10]張明偉. 水稻抗白葉枯病相關基因OsCRK1的鑒定和克隆[D]. 北京:?中國農業(yè)科學院, 2015.
[11]?張海斐. 甜瓜CDPK和CRK基因家族的鑒定及表達分析[D]. 楊凌:?西北農林科技大學, 2017.
[12]?羅 ?軍, 周燦芳, 付丹文, 等. 2011年廣東龍眼產業(yè)發(fā)展現狀分析[J]. 廣東農業(yè)科學, 2012, 39(5): 6-8.
[13]?王 ?云, 彭麗云, 孫雪麗, 等. 龍眼Hsf基因家族全基因組鑒定及體胚發(fā)生過程中的表達分析[J]. 應用與環(huán)境生物學報, 2019, 25(2): 420-431.
[14]?Jue D?W, Sang X?L, Liu L?Q,et al. Identification ofWRKY gene family fromDimocarpus longanand its expression analysis during flower induction and abiotic stress responses[J]. International Journal of Molecular Sciences, 2018, 19(8): 2169.
[15]?張小倩, 張騰騰, 閆 ?攀, 等. 蛋白N-糖基化分析方法研究進展[J]. 生物技術進展, 2019, 9(3): 246-252.
[16]?朱巍巍, 馬天意, 張梅娟, 等. 類受體蛋白激酶在植物中的研究進展[J]. 基因組學與應用生物學, 2018, 37(1): 451-458.
[17]?鄭 ?超, 李登高, 白 ?薇. 植物富含半胱氨酸的類受體激酶的研究進展[J]. 生物技術通報, 2016, 32(11): 10-17.
[18]?王文泉, 鄭永戰(zhàn), 梅鴻獻, 等. 厭氧誘導木葡聚糖轉葡糖苷酶(XET)基因在芝麻和小麥根中的表達[J]. 農業(yè)生物技術學報, 2004(3): 258-263.
[19]?Li J?L, Han G?L, Sun C?F,et al. Research advances ofMYB transcription factors in plant stress resistance and breeding[J]. Plant Signaling & Behavior, 2019, 14(8): 1613-1631.
[20]?楊 ?雪, 雒 ?軍, 王引權. 調控植物黃酮類化合物生物合成的MYB轉錄因子研究進展[J]. 甘肅中醫(yī)藥大學學報, 2018, 35(6): 77-81.
[21]?王軍妮, 黃艷紅, 牟志美, 等. 植物次生代謝物黃酮類化合物的研究進展[J]. 蠶業(yè)科學, 2007(3): 499-505.
[22]?王岸娜, 向 ?琳, 吳立根, 等. 果蔬中黃酮類物質的研究進展[J]. 河南工業(yè)大學學報(自然科學版), 2019, 40(3): 118-125.
[23]?賴瑞聯, 林玉玲, 賴鐘雄. 龍眼不同愈傷組織培養(yǎng)方法的探討及細胞觀察[J]. 龍巖學院學報, 2014, 32(2): 70-75.
[24]?賴鐘雄, 潘良鎮(zhèn), 陳振光. 龍眼胚性細胞系的建立與保持[J]. 福建農業(yè)大學學報, 1997(2): 33-40.
[25]?陳義挺. 龍眼體胚發(fā)生過程中的CDC48和GPX基因克隆與表達[D]. 福州: 福建農林大學, 2009.
[26]?Yeh Y H, Chang Y H, Huang P Y,et al. EnhancedArabidopsispatterntriggered immunity by over?expression of?cysteine-rich receptor-like kinases[J]. Frontiers in Plant Science, 2015, 6: 322.
[27]?傅梅萍. 植物激素ABA/GA代謝與響應通路基因表達在秋茄(Kandelia obovata)顯胎生過程中的調控作用[D]. 廈門:?廈門大學, 2018.
[28]?倪德祥, 鄧志龍. 植物激素對基因表達的調控[J]. 植物生理學通訊, 1992(6): 461-466.
[29]?徐小萍, 陳曉慧, 呂科良, 等. 龍眼漆酶家族成員全基因組結構與功能分析[J]. 應用與環(huán)境生物學報, 2018, 24(4): 833-844.
[30]?徐小萍, 賴瑞聯, 林玉玲, 等. 龍眼UGD6基因克隆及其表達特性分析[J]. 西北植物學報, 2017, 37(4): 636-645.
[31]?陳 ?燕, 呂科良, 厲 ?雪, 等. 龍眼ERF家族成員鑒定及其在體胚發(fā)生早期的表達[J]. 西北植物學報, 2018, 38(11): 1986-1999.
[32]?Wrzaczek M, Brosché M, Saloj?rvi J,et al. Transcriptional regulation of theCRK/DUF26 group ofreceptor-like protein kinasesby ozone and plant hormones inArabidopsis[J]. BMC?Plant Biology, 2010, 10(1): 95.

