Sakaguchia cladiensis對磺胺甲嘧啶/銅復合污染中抗生素的降解
曾潔儀,曾蘇杭,紀夢鈿,檀 笑,韓偉江,,陳爍娜*
Sakaguchia cladiensis對磺胺甲嘧啶/銅復合污染中抗生素的降解
曾潔儀1,曾蘇杭1,紀夢鈿1,檀 笑2,韓偉江1,2,陳爍娜1*
(1.華南農業大學資源環境學院,廣東 廣州 510642;2.生態環境部華南環境科學研究所,廣東 廣州 510655)
以某畜禽養殖場土壤篩選分離到的一株對磺胺甲嘧啶(Sulfamethazine,SMZ)具有耐受性的酵母菌(,A5)為研究對象,開展生長特性及其對SMZ-Cu2+復合污染中SMZ降解特性研究.結果表明,SMZ和Cu2+脅迫下,菌A5也能較好生長.降解性能研究顯示,菌A5在復合污染體系中反應3d,SMZ去除率達37.3%,共存的Cu2+對SMZ降解具有促進作用.當投菌量為1g/L,溶液pH值為中性,菌A5對1mg/L SMZ的降解效果最佳.透射電鏡分析表明,SMZ和Cu2+共存時,菌A5的細胞壁膜破損嚴重,導致細胞質外流.
磺胺甲嘧啶;銅;復合污染;;微生物降解
磺胺類抗生素和重金屬銅常被用作飼料添加劑,用于畜禽疾病防治和促生長,但是大部分抗生素卻不能被機體完全吸收,約超過85%會以藥物原形或代謝物經排泄物進入環境[1-2],重金屬也不能被降解[3-5],從而在畜禽養殖區及周邊形成典型的抗生素/重金屬復合污染[6].長期脅迫下,勢必會誘導多重抗性微生物出現,進而破壞微生物生態系統多樣性平衡,對生態環境造成更大危害.因此,開展環境中殘留抗生素/重金屬去除的研究至關重要.微生物是環境中污染物分解轉化的主要參與者,關系到污染物在環境中的歸趨.據報道,已有學者從環境中篩選到多種抗生素降解菌[7-11],主要包括有節桿菌屬[7]、細桿菌屬[8]、無色桿菌屬[9]、不動桿菌屬[10]、假單胞菌屬[11]和紅球菌屬[12]等,大部分都屬于細菌[13].研究顯示,這些細菌可將SAs作為唯一碳源或共代謝基質進行分解,環境條件的改變,包括溫度[14]、酸堿度[14]、鹽度[15]、濁度[16]以及營養物質[17]等都會影響SAs的去除.Zhang等[18]研究發現,外加維生素和氨基酸可以促進降解磺胺甲噁唑(SMX),抗生素濃度影響其抑菌效果,因此SAs初始濃度越高,其降解率越低[19],但是也有相矛盾的研究報道[20-21].微生物和抗生素的類別也是影響降解的主要因素,例如紅球菌可以共代謝降解磺胺甲噁唑(SMX)和磺胺甲噻二唑(SMT),但是卻不能以單一SAs為碳源生長[12].另外一種紅球菌,可以降解SMX,但是當有其它微生物共存時,卻失去降解能力[22].由此可見,抗生素降解是一個復雜的過程,盡管已經取得一些研究進展,但是還很不足,而且關于抗生素/重金屬復合污染條件下微生物降解的研究還鮮有報道.
鑒于此,本研究選取磺胺甲嘧啶(Sulfamethazine, SMZ)和銅(Cu2+)為研究對象,開展水體SMZ-Cu2+復合污染中SMZ微生物降解特性研究,以期為微生物技術在環境抗生素/重金屬復合污染治理中的應用提供參考.
1 材料與方法
1.1 材料
1.1.1 培養基 營養培養基(NB):蛋白胨10g, NaCl 5g,牛肉膏 3g,水1000mL, pH=7.2~7.4.LB培養基:NaCl 10g,酵母提取物5g,胰蛋白胨 10g,水 1000mL, pH=7.0~7.2.無機鹽培養基(MSM):NaCl 0.5g,MgCl·6H2O 0.1g,KH2PO40.3g,K2HPO4·3H2O 0.3g,水1000mL, pH=7.0~7.2.上述培養基使用前均置于高壓蒸汽滅菌鍋,121℃,滅菌30min.固體培養基是在液體培養基中加入質量分數為1.5%~2.0%的瓊脂粉,充分混合,滅菌后冷卻凝固而制成.
1.1.2 實驗試劑 SMZ儲備液:稱取一定量SMZ (Ehrenstorfer GmbH,德國)于棕色容量瓶中,用色譜純甲醇溶解定容,配制成100mg/L的SMZ標準儲備液,置于4℃冰箱,避光保存備用.Cu2+標液:稱取一定量的Cu(NO3)2,用去離子水溶解定容,配制成Cu2+濃度為1000mg/L的溶液,用0.22μm微孔過濾器過濾后,置于4℃冰箱保存待用.磷酸鹽緩沖液(PBS, pH=7):NaCl 8.5g,NaHPO4·2H2O 2.2g, NaH2PO4·2H2O 0.4g,水1000mL, 121℃,滅菌30min, 4℃冰箱保存待 用.
1.2 實驗方法
1.2.1 SMZ耐受菌的篩選和分離 從珠三角某畜禽養殖場采集土樣.稱取1g土樣,加入含10mg/L SMZ的營養培養基,置于恒溫振蕩培養箱中150r/ min,30℃避光培養3d后,取10mL培養液轉接到含20mg/L SMZ的新鮮營養培養基中,相同條件下繼續培養3d.然后同樣操作進行轉接,每次接種新培養體系中SMZ的濃度增加10mg/L.當接種4次后,即SMZ濃度增至50mg/L時,連續培養7d后,取培養液涂布在固體營養培養基平板上,于30℃恒溫培養箱,倒置避光培養1~2d.挑取單一菌落在新平板上劃線分離培養,進一步純化.最后,選取純化的單菌落進行擴大培養,分別考察其對SMZ的降解效果.
1.2.2 菌體擴大培養和菌懸液的制備 刮取一環目標菌株接種到LB液體培養基中,置于振蕩培養箱,25℃,150r/min恒溫培養24~36h.取活化至對數期的菌培養液離心(6000r/min,25℃,6min),收集菌體,用無菌水洗滌2次(6000r/min,離心5min).最后用無菌水重懸,配成0.02g/mL的菌懸液待用.
1.2.3 菌A5生長曲線的測定 將活化的目標菌株接種到LB液體培養基中(接種量1%),于25℃, 150r/min恒溫振蕩培養.總共設置3個不同培養體系,分別為(1)純營養培養;(2)含20mg/L SMZ;(3)含有20mg/L SMZ和20mg/L Cu2+,分別于0.5,1,2,3,4,6, 8,10,12,24,36,48,72,96,120,144,168,192,216,240h取樣,用分光光度計測定培養液在600nm的吸光值(OD600),繪制菌A5的生長曲線.
1.2.4 復合污染中SMZ的微生物降解性能 在含有SMZ和Cu2+(10mg/L)的MSM體系中接種菌A5,以SMZ為唯一碳源,分別考察時間,投菌量,溶液pH值以及污染物初始濃度對菌A5降解SMZ的影響,設計條件如下:
(1)時間:設置單一SMZ和SMZ-Cu2+復合污染降解體系,分別于0.5,1,2,3,5,7,9d取樣,分析SMZ殘余濃度;
(2)投菌量:于復合污染降解體系,分別設置投菌量為0.5,1,1.5,2g/L;
(3)溶液pH值:于復合污染降解體系,分別調節溶液初始pH值為1~3(酸性),5~6(弱酸),7(中性),9~10(弱堿)和12~14(堿性)的復合污染降解體系;
(4)SMZ初始濃度:于復合污染降解體系,分別設置SMZ初始濃度為0.5,1,3,5mg/L;
除特殊說明,所有反應體系溶液pH值為中性,SMZ濃度為1mg/L,Cu2+濃度為10mg/L,投菌量為1g/L,反應條件為150r/min,25℃,作用48h.以不加菌體系作為空白對照,每組試樣做3個平行樣.
1.2.5 溶液中SMZ的分析 將樣品離心(6000r/ min,8min,25℃),取0.5mL上清液置于1.5mL離心管中,加入等體積的萃取液(0.1%甲酸:乙腈:甲醇=10:3: 1,//),旋渦振蕩至完全混合,之后10000r/min離心5min,上清液用0.22μm微孔過濾器過濾到棕色進樣瓶,置于4℃保存,待測.
溶液中SMZ用高效液相色譜儀(HPLC, LC- 20A,Shimadzu Japan)進行分析.分析條件: C18反相柱(4.6×250mm,5μm,Thermo Fisher Scientific),柱溫30℃,流動相為含0.1%甲酸的高純水:乙腈=30%: 70%(/),流速為1.000mL/min,進樣量為20μL,紫外檢測波長為270nm.
1.2.6 菌A5細胞微觀結構檢測 設置4組實驗條件:①不含污染物的MSM,作為空白對照;②含3mg/L SMZ的MSM;③含10mg/L Cu2+的MSM; ④含3mg/L SMZ和10mg/L Cu2+的MSM.所有培養體系接種菌A5,于25 ℃,150r/min恒溫振蕩培養72h,收集菌體,依次進行固定,脫水,包埋處理,然后將其超薄切片染色后,用透射電鏡(TEM,TECNAI G212,FEI Holland)對菌A5的細胞微觀結構進行觀察.
2 結果與討論
2.1 SMZ降解菌的篩選與鑒定
經過多次富集培養和篩選,從采集的畜禽養殖場土樣中分離得到4株對SMZ具有較好耐受性的菌株,分別命名為A4,A5,A13和A14.對這4株耐受菌降解SMZ的能力進行考察,結果如圖1所示.其中菌A5表現出較好的降解能力,反應3d,其對SMZ的去除率最高,達38.2%,而菌A4的降解效果最不理想,在第3d時其對SMZ的降解率只有17.2%.另外,菌A13和A14的降解能力相近,作用3d對SMZ的去除率在25%~28%之間.因此選取降解效果較好的菌A5作為進一步研究的目標菌株,并委托廣東省微生物所對其進行鑒定.經過DNA提取,PCR擴增,26S rDNA序列測序及序列對比,鑒定菌A5與酵母菌同源性最高,達99.02%.
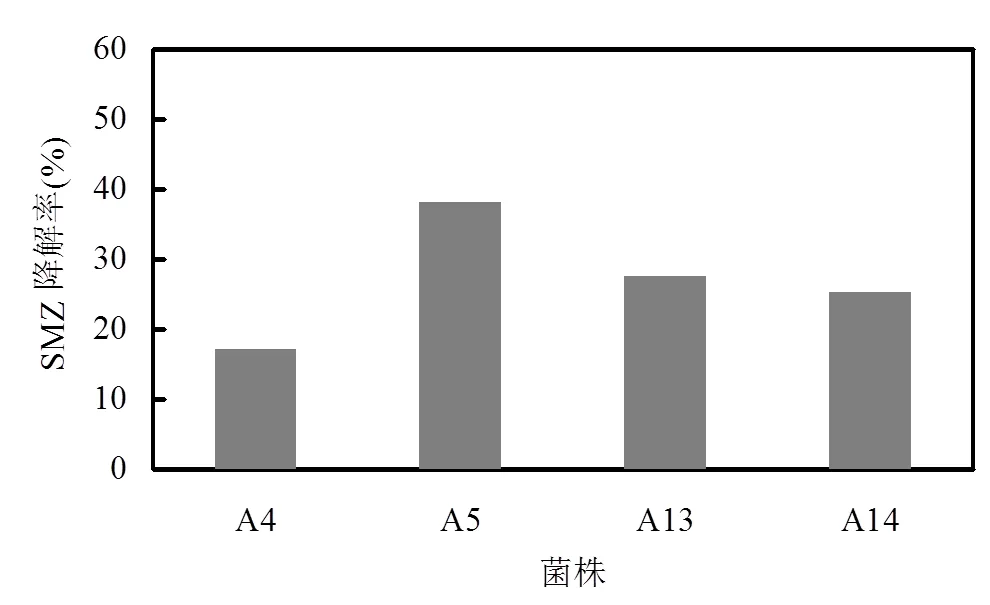
圖1 耐受菌降解SMZ能力對比
2.2 菌A5的生長特性
分別在營養體系(對照),單一SMZ和SMZ-Cu2+復合污染體系中,考察菌A5的生長特性.如圖2所示,純營養培養時,菌A5經過12h的生長延遲期,之后開始快速生長,進入對數生長期,直到第36h,菌A5生長和死亡速率處于平衡,進入較長的生長穩定期,最后,隨著體系中營養物質的消耗,菌體死亡速率超過生長速率,在第168h之后,菌A5逐漸進入衰亡期.此外,從圖上可以看出,在單一SMZ和SMZ-Cu2+復合污染的培養體系中,菌A5仍正常生長.但是當培養液中含有單一SMZ時,到達穩定期,菌A5生物量(即OD600)明顯較少,而同時含有SMZ和Cu2+的培養體系,菌A5的生物量卻跟對照組基本一致.這說明SMZ對菌A5的生長是有一定抑制作用,但當有Cu2+共存時,兩者產生交叉抗性,Cu2+增強了菌A5對SMZ的抗性,進而影響SMZ的抑菌效果[23-24].
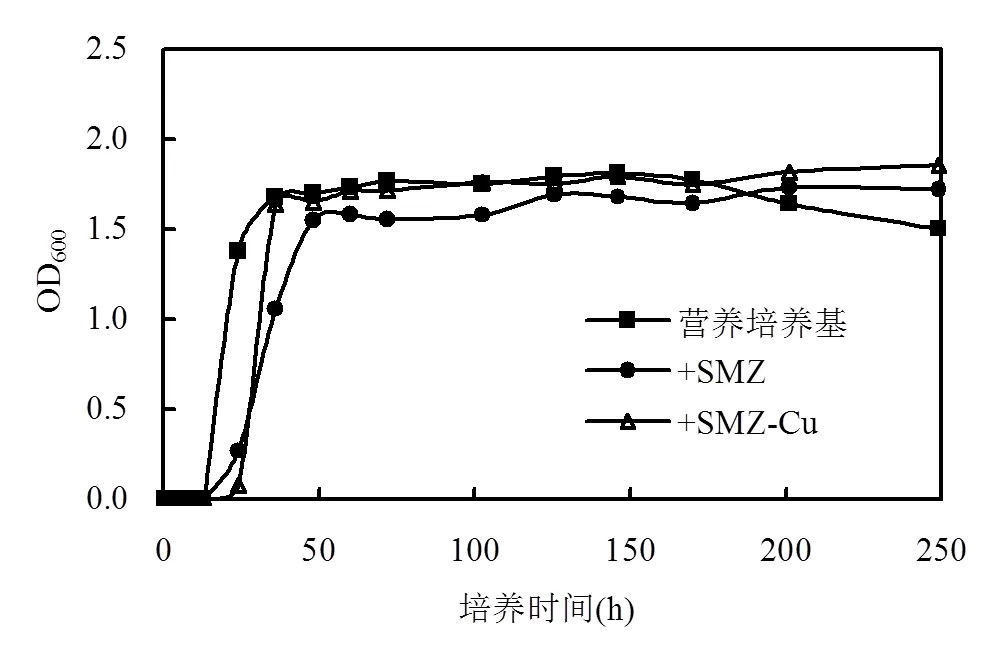
圖2 不同培養體系中菌A5的生長曲線
該實驗結果表明,雖然SMZ和Cu2+存在對菌A5生長影響不顯著,但是延遲了菌體進入對數期的時間,從12h延緩至24h.這說明菌A5對體系中存在的污染物具有生長適應期,需要通過延遲期對自身代謝調整來重新適應和響應外環境不利條件的脅迫.除此,研究還發現,在含有SMZ和Cu2+的培養體系中,菌A5直到第250h仍沒有進入衰亡期,而是一直保持穩定的持續生長.這是因為一旦菌A5適應了新環境,并且在生長過程中受著污染物的持續馴化,到生長后期,即使體系中營養物質消耗殆盡,但是被馴化的菌A5仍可以利用污染物SMZ作為碳源和能源物質來維持生長[25],因此,跟無添加污染物的培養體系相比,其衰亡期推遲. Chen等[26]在研究苯并[a]芘(BaP)的微生物降解時也發現,在BaP存在的培養體系中,可以二次生長,同樣推遲進入衰亡期.另一方面,Cu2+作為多種細胞酶激活劑,可以誘導菌A5分泌和激活更多細胞酶,促使體系中有害物質的代謝分解,從而提高菌體適應性[27-28].由于對數生長期的菌體生命力旺盛,代謝活躍,因此在之后的實驗中,選取培養12~24h的菌A5開展一系列SMZ降解性能研究.
2.3 SMZ降解隨時間變化
分別考察菌A5在單一和復合污染體系中對SMZ降解隨時間的變化,結果如圖3所示.隨時間推移,菌A5對SMZ的降解率逐漸增大,但是由于污染物不同,SMZ降解率增長的情況也不一樣.當體系中只含有SMZ時,菌A5在前3d對SMZ的去除率只有10%左右,之后隨時間快速增長,到第5d基本穩定,保持在37.0%.而在SMZ-Cu2+復合污染體系中,菌A5對SMZ的去除率從第12h開始就隨時間持續上升,到第3d達到最大值,為37.3%,之后基本保持穩定.
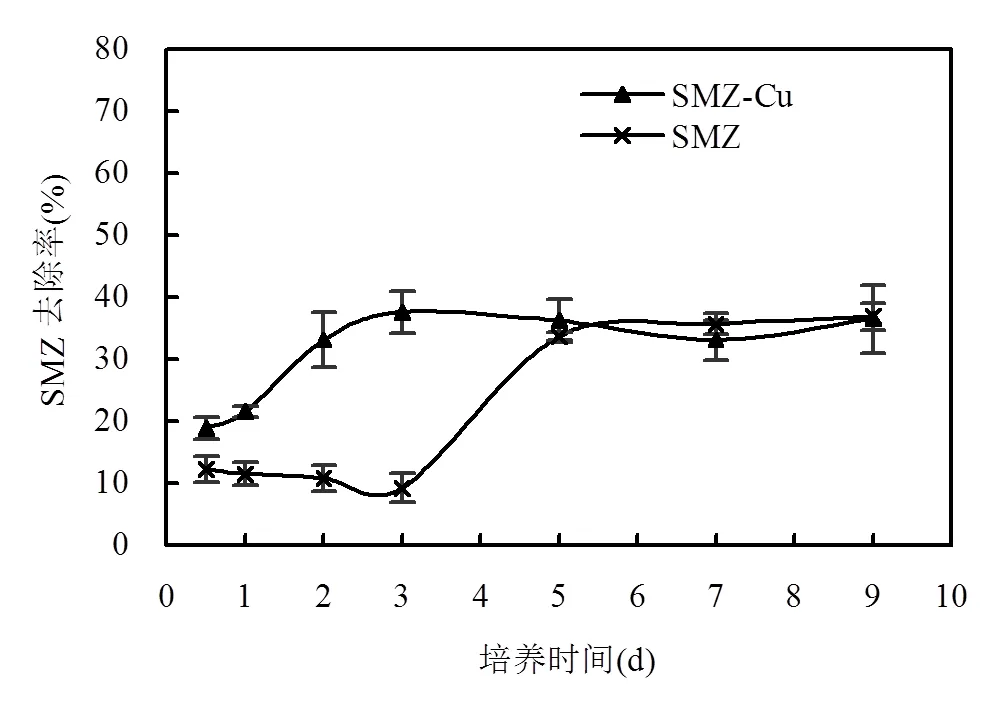
圖3 SMZ去除率隨時間變化
從結果顯示,菌A5降解SMZ經歷了遲緩期,再到快速降解,之后趨于穩定,可見菌體在反應初始對外源污染物需要一個適應過程,在這階段SMZ去除率較低.之后,在SMZ不斷誘導應激下,而且體系速效碳源和氮源的缺乏,致使菌A5分泌細胞酶將SMZ作為碳源和氮源分解利用,因此SMZ去除率快速增長,但是隨著時間延長,菌體代謝物不斷積累,此時菌A5會優先利用更容易分解的代謝物以及SMZ分解產生的小分子物質作為能源,所以SMZ的去除被停滯.大部分金屬離子是微生物生長代謝的重要輔助因子,是多種酶的重要激活劑,可協助催化細胞代謝中的氧化等反應.佟瑤等[29]就研究證實,部分金屬離子在適當濃度范圍內可以作為酶激活劑促進三苯基錫的酶促降解.因此,當體系同時含有Cu2+時,菌A5對SMZ的降解幾乎不需經歷遲緩期,那是因為銅離子作為多種細胞酶激酶,可以有效激活菌A5各種細胞降解酶,進而將SMZ快速分解利用.
2.4 投菌量對SMZ降解的影響
改變投菌量,考察復合污染情況下,不同生物量對菌A5降解SMZ的影響,結果如圖4所示.當投菌量為1g/L時,菌A5對SMZ的降解效果最佳,作用48h, SMZ的去除率可達33.3%,而當投菌量分別為0.5,1.5,2g/L時,菌A5對SMZ的去除率差別不顯著,在15.7%~17.1%之間.
從結果顯示,投菌量并非越大越好.當投菌量由0.5g/L增加到1.0g/L時,菌A5對SMZ的去除率顯著增大,但當投菌量繼續增加(>1.0g/L)時,菌A5對SMZ的降解效果反而下降.這是因為SMZ具有一定的抑菌毒性,當生物量較小時,單位質量菌體承受的毒害作用大,菌體的生長受到抑制,進而影響其對SMZ的降解.而如果投菌量持續增大,雖然菌體抵抗SMZ脅迫的能力增強,可以正常生長,但是由于MSM體系中SMZ是唯一的碳源和氮源,隨著生物量增大,有限的營養物質勢必會成為菌體生長的制約因素,隨著一些菌體的死亡,其細胞分解并作為存活下來菌A5利用的能源物質,因此抑制了菌A5對SMZ的分解利用.通過本實驗證實,當投菌量為1g/L時,菌A5對SMZ的降解效果最好,所以在后續實驗中設定投菌量為1g/L.
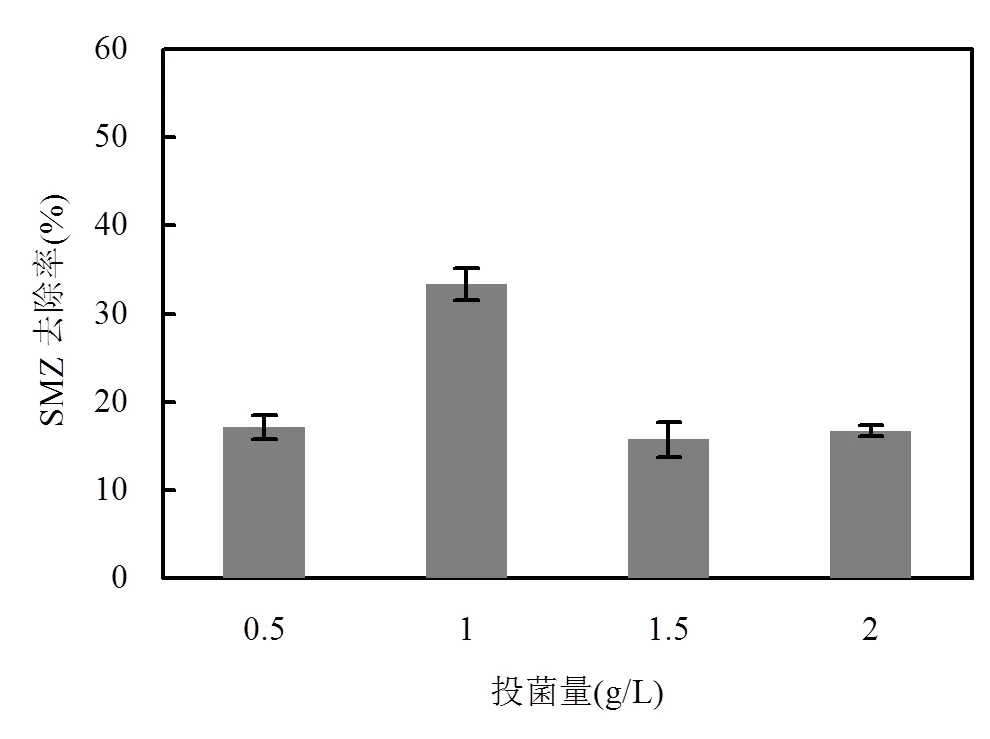
圖4 投菌量對SMZ降解的影響
2.5 溶液pH值對SMZ降解的影響
環境pH值是微生物活性的敏感因子,微生物的生命活動和物質代謝都與環境pH值密切相關[30-31].同時,環境pH值的改變也會影響某些污染物的化學形態和性質[32].本實驗通過改變溶液的初始pH值,研究不同酸堿度對菌A5降解SMZ的影響,結果如圖5所示.菌A5對溶液pH值的變化表現出較好的適應性,均能在一定程度去除SMZ,但是不同酸堿度對菌A5降解SMZ的影響還是較顯著,中性條件(pH =7)下更有利于菌A5對SMZ的去除,作用48h去除率達39.9%.
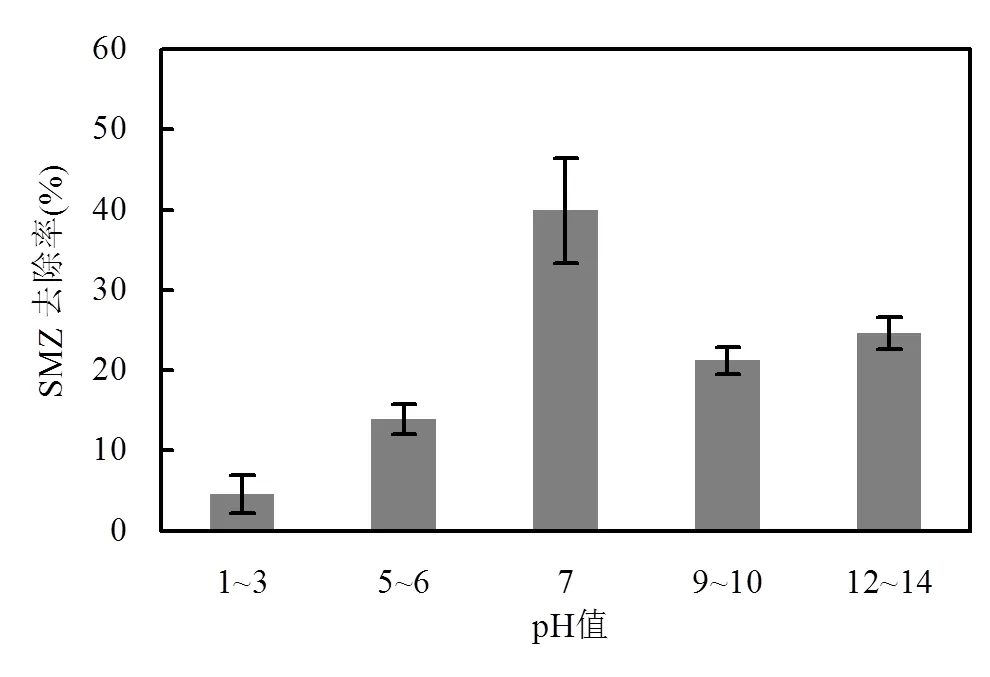
圖5 不同溶液pH值對SMZ去除的影響
溶液pH值對SMZ降解的影響主要表現在兩方面:一是影響SMZ的水解途徑;二是影響微生物生長代謝以及相關酶的合成及活性[26].磺胺類抗生素在中性條件下水解較慢,活性較低[33],但結果顯示中性條件SMZ的去除率最佳,可見此時溶液中SMZ以微生物去除為主.從圖5還可以看出,堿性條件下,菌A5對SMZ仍有較好去除效果,這是因為菌A5生長過程中會分泌大量的有機酸代謝產物,調節了溶液的pH值,使反應體系趨向中性或弱堿性,從而有利于菌A5對SMZ的去除.而當溶液過酸時(pH£3),會導致H+濃度超過酶的適應范圍,引起細胞膜電荷變化,進而影響菌的代謝活性.張珈瑜等[34]研究J2對磺胺二甲基嘧啶降解特性時發現,初始pH=6.0~8.0時,較適宜磺胺二甲基嘧啶的微生物降解,這與本研究結果相似.另外,也有研究表明,溶液酸堿度不同會影響SMZ的化學形態.當溶液為酸性或堿性時,SMZ主要以陽離子或陰離子形態存在,只有當溶液為中性時,SMZ則以非解離狀態存在,而不同形態的SMZ會影響其與微生物之間的相互作用[35-36].
2.6 初始濃度對SMZ微生物降解的影響
圖6顯示的是 SMZ 初始濃度分別為0.5,1.0, 3.0,5.0mg/L 時,菌A5作用48h, 復合污染中SMZ的去除情況.結果表明,菌A5對不同濃度的SMZ均有一定的降解效果.當SMZ的初始濃度為1mg/L時,菌A5對SMZ去除率最好,達38.2%.而隨著SMZ濃度的增加,菌A5對其去除率呈下降趨勢,這是因為SMZ濃度越大,其對微生物的抑菌毒性越強,不利于微生物生長,抑制菌體的代謝活性[19].另一方面,如果SMZ濃度過低,菌體與SMZ接觸的量以及SMZ的傳質會受到限制,這在一定程度會阻礙SMZ的微生物降解.
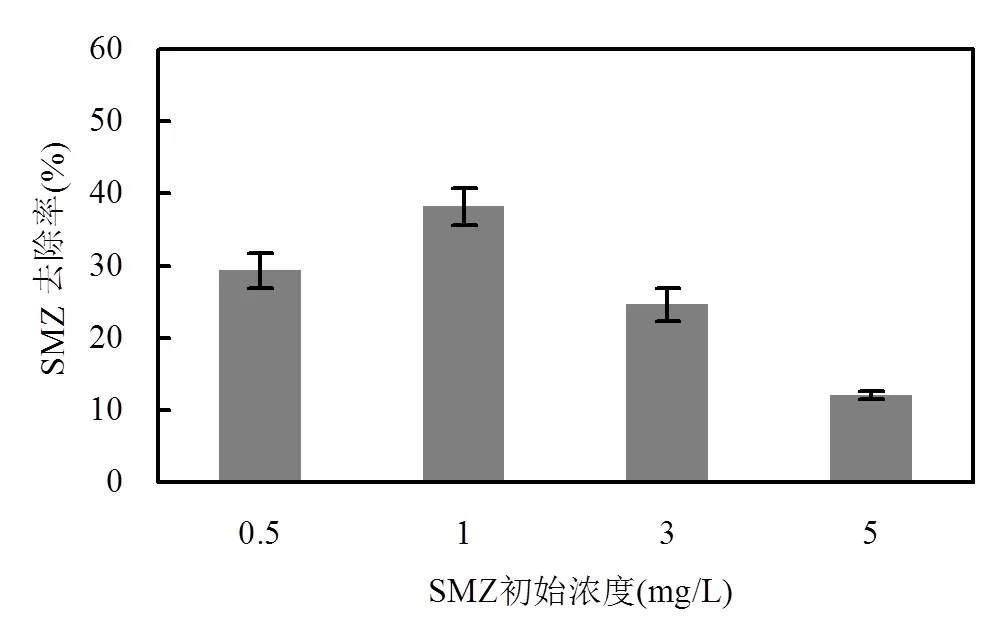
圖6 菌A5對不同濃度SMZ的降解
2.7 SMZ/Cu2+脅迫下菌A5細胞微觀結構變化
分別收集單一SMZ,單一Cu2+,以及SMZ-Cu2+復合污染處理了3d的菌A5細胞,并以營養培養的菌體為對照,利用TEM觀察在不同污染物脅迫下,菌A5細胞微觀結構的變化.
從圖7(A)可以看出,對照組的菌A5生長狀態良好,細胞呈橢圓形,菌體內充盈原生質體,液泡和核區清晰可見,甚至觀察到細胞出芽生殖.圖7(B)是單一SMZ處理的菌A5細胞,可見少數細胞仍可進行出芽生殖,但有的細胞結構受到破壞,細胞內陷甚至破裂.相比SMZ的影響,單一Cu2+處理的菌A5細胞形態正常(見圖7(C)),保持較好的橢圓形,但細胞邊緣有一圈明顯的白色亮部,可推測在Cu2+影響下,菌A5細胞發生質壁分離;而且在細胞壁表面黏附了很多細微顆粒物,可能是溶液中Cu2+被吸附到細胞表面.圖7(D)顯示的是SMZ-Cu2+復合污染處理的菌A5,可見細胞破損嚴重,細胞形狀扭曲變形,部分細胞原生質大量流失.由此可見,抗生素SMZ對菌體細胞的影響較明顯,尤其是復合污染.但是即使菌體細胞發生變形破損,仍可以對SMZ進行降解,這是因為細胞中發揮作用的降解酶仍沒有全部流失,從而保證了細胞的代謝活性;也有可能雖然胞內酶隨著細胞破裂流出,但是仍能保持活性,對溶液中的SMZ發揮降解作用.
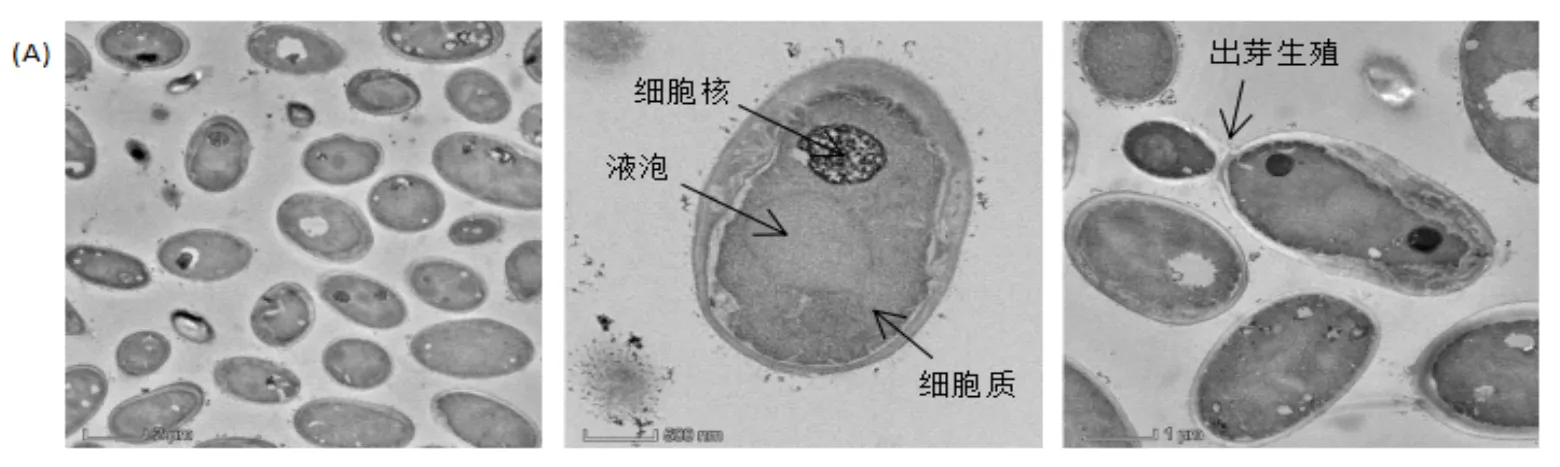
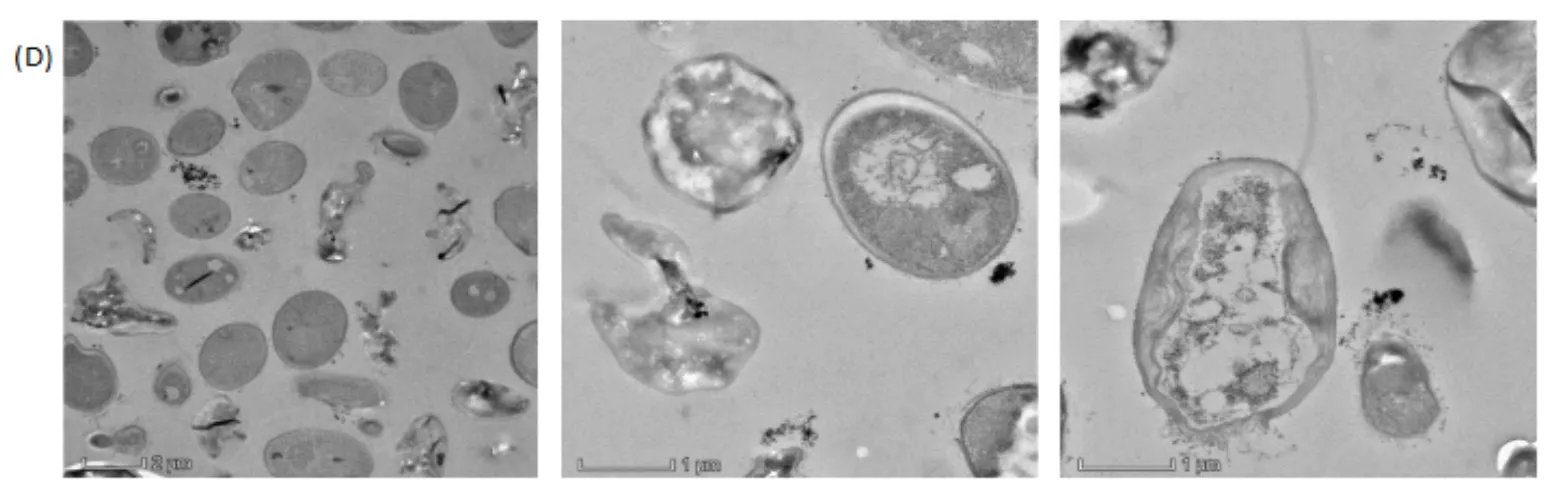
圖7 不同處理條件下的菌A5細胞TEM圖
(A)對照組;(B)單一SMZ處理;(C)單一Cu2+處理;(D) SMZ-Cu2+復合污染處理
3 結論
3.1 從某畜禽養殖場土壤篩選分離到1株SMZ降解菌,經鑒定為酵母菌,命名為A5.污染物SMZ和SMZ-Cu2+復合污染的存在,菌A5仍能保持正常生長,但是其對數生長期延遲,同時也推遲進入衰亡期.
3.2 SMZ-Cu2+復合污染中,菌A5作用3d,對SMZ的去除率達37.3%,Cu2+的存在可以促進菌A5對SMZ的降解.投菌量,溶液pH值,SMZ初始濃度均會對菌A5降解SMZ產生影響.當投菌量為1g/L, pH值為中性,SMZ初始濃度為1mg/L時,菌A5對SMZ降解效果最佳.
3.3 TEM分析表明,相比Cu2+,SMZ對菌體細胞的影響更顯著,尤其在SMZ-Cu2+復合污染脅迫下,菌A5細胞破損嚴重,細胞形狀扭曲變形,部分細胞質流失.
[1] Liu J L, Wong M H. Pharmaceuticals and personal care products (PPCPs): A review on environmental contamination in China [J]. Environment International, 2013,59:208-224.
[2] Radke M, Lauwigi C, Heinkele G, et al. Fate of the antibiotic sulfamethoxazole and its two major human metabolites in a water sediment test [J]. Environmental Science & Technology, 2009,43(9): 3135-3141.
[3] 張家泉,田 倩,許大毛,等.大冶湖表層水和沉積物中重金屬污染特征與風險評價 [J]. 環境科學, 2017,38(6):2355-2363. Zhang J Q, Tian Q, Xu D M, et al. Pollution characteristics and risk assessment of heavy metals in water and sediment from daye lake [J].Environmental Science, 2017,38(6):2355-2363.
[4] 張博文,趙甲亭,吳二威,等.滏陽河河流水體中重金屬污染特征及其對青海弧菌和斜生柵藻的毒性效應 [J].生態毒理學報,2018,13(1): 179-189.Zhang B W, Zhao J T, Wu E W, et al. Water pollution characteristics of heavy metals in Fuyang River system and their toxicity tosp. Q67and[J]. Asian Journal of Ecotoxicology, 2018,13(1):179-189.
[5] Chen C Q, Zheng L, Zhou J L, et al. Persistence and risk of antibiotic residues and antibiotic resistance genes in major mariculture sites in Southeast China [J]. Science of Total Environment, 2017,580:1175– 1184.
[6] Hu Y A, Cheng H F, Tao S. Environmental and human health challenges of industrial livestock and poultry farming in China and their mitigation [J]. Environment International, 2017,107:111-130.
[7] Deng Y, Mao Y P, Li B, et al. Aerobic degradation of sulfadiazine byspp.: kinetics, pathways, and genomic characterization [J]. Environmental Science & Technology, 2016,50(17):9566-9575.
[8] Topp E, Chapman R, Devers-Lamrani M, et al. Accelerated biodegradation of veterinary antibiotics in agricultural soil following long-term exposure, and isolation of a sulfamethazine-degradingsp. [J]. Journal of Environmental Quality, 2013,42(1): 173-178.
[9] Reis P J M, Reis A C, Ricken B, et al. Biodegradation of sulfamethoxazole and other sulfonamides byPR1 [J]. Journal of Hazardous Materials, 2014,280: 741-749.
[10] Yang C W, Hsiao W C, Chang B V. Biodegradation of sulfonamide antibiotics in sludge [J]. Chemosphere, 2016,150:559-565.
[11] Jiang B C, Li A, Cui D, et al. Biodegradation and metabolic pathway of sulfamethoxazole byHA-4, a newly isolated cold-adapted sulfamethoxazole-degrading bacterium [J]. Applied Microbiology and Biotechnology, 2014,98(10):4671-4681.
[12] Gauthier H, Yargeau V, Cooper D G. Biodegradation of pharmaceuticals byandby co-metabolism [J]. Science of the Total Environment, 2010,408: 1701-1706.
[13] Chen J F, Xie S G. Overview of sulfonamide biodegradation and the relevant pathways and microorganisms [J]. Science of the Total Environment, 2018,640-641:1465-1477.
[14] Zheng T, Cai L, Xu B T, et al. Sulfadiazine biodegradation by: Mechanism and degradation product identi?cation [J]. Chemosphere, 2019,237:124418.
[15] Yang C C, Huang C L, Cheng T C, et al. Inhibitory effect of salinity on the photocatalytic degradation of three sulfonamide antibiotics [J]. International Biodeterioration & Biodegradation, 2015,102:116-125.
[16] Nguyen P Y, Carvalho G, Reis A C, et al. Impact of biogenic substrates on sulfamethoxazole biodegradation kinetics bystrain PR1 [J]. Biodegradation, 2017,28:205-217.
[17] Liang D H, Hu Y Y. Simultaneous sulfamethoxazole biodegradation and nitrogen conversion bysp. JL9 using with di?erent carbon and nitrogen sources [J]. Bioresource Technology, 2019,293:122061.
[18] Zhang Y B, Zhou J, Xu Q M, et al. Exogenous cofactors for the improvement of bioremoval and biotransformation of sulfamethoxazole by[J]. Science of the Total Environment, 2016,565:547-556.
[19] Mao F, Liu X H, Wu K, et al. Biodegradation of sulfonamides byMR-1 andsp. strain MR-4 [J]. Biodegradation, 2018,29:129-140.
[20] Lin B, Lyu J L, Lyu X J, et al. Characterization of cefalexin degradation capabilities of twostrains isolated from activated sludge [J]. Journal of Hazardous Materials, 2015,282:158- 164.
[21] Selvi A, Salam J A, Das N. Biodegradation of cefdinir by a novel yeast strain,sp. SMN03isolated from pharmaceutical wastewater [J]. World Journal of Microbiology and Biotechnology, 2014,30: 2839-2850.
[22] Larcher S, Yargeau V. Biodegradation of sulfamethoxazole by individual and mixed bacteria [J]. Applied Microbiology and Biotechnology, 2011,91:211-218.
[23] 劉愛菊,劉 敏,李夢紅,等.Cu,抗生素協同污染對土壤微生物活性的影響 [J]. 生態環境學報, 2013,22(11):1825-1829. Liu A J, Liu M, Li M H, et al. Collaborative effects of Cu and antibiotic on soil microbial activities [J]. Ecology and Environmental Sciences, 2013,22(11):1825-1829.
[24] 傅海霞,劉 怡,董志英,等.抗生素與重金屬復合污染的生態毒理效應研究進展[J]. 環境工程, 2016,34(4):60-63+104. Fu H X, Liu Y, Dong Z Y, et al.Progress in research on ecological toxicity of combined pollution of antibiotics and heavy metals [J]. Environmental Engineering, 2016,34(4):60-63+104.
[25] Ni B J, Zeng R J, Fang F,et al. Fractionating soluble microbial products in the activated sludge process [J]. Water Research, 2010, 44(7):2292-2302.
[26] Chen S N, Yin H, Ye J S, et al. Effect of copper(II) on biodegradation of benzo[a]pyrene by[J]. Chemosphere, 2013,90(6):1811-1820.
[27] 王 瑞,魏源送.畜禽糞便中殘留四環素類抗生素和重金屬的污染特征及其控制[J]. 農業環境科學學報, 2013,32(9):1705-1719. Wang R, Wei Y S. Pollution and control of tetracyclines and heavy metals residues in animal manure [J]. Journal of Agro-Environment Science, 2013,32(9):1705-1719.
[28] Steffen K T, Hatakka A, Hofrichter M. Degradation of benzo[a]pyrene by the litter-decomposing basidiomycete: role of manganese peroxidase [J]. Applied and Environmental Microbiology, 2003,69(7):3957-3964.
[29] 佟 瑤,葉錦韶,尹 華,等.金屬離子對三苯基錫酶促降解的影響[J]. 環境科學, 2011,32(3):779-783. Tong Y, Ye J S, Yin H, et al.Effect of heavy metal ions on triphenyltin enzymatic degradation [J]. Environmental Science, 2011, 32(3):779-783.
[30] 鄭 蕾,田 禹,孫德智.pH值對活性污泥胞外聚合物分子結構和表面特征影響研究[J]. 環境科學, 2007,28(7):1507-1511. Zheng L, Tian Y, Sun D Z. Effects of pH on the surface characteristics and molecular structure of extracellular polymeric substances from activated sludge [J]. Environmental Science, 2007,28(7):1507-1511.
[31] 劉春光,金相燦,孫 凌,等.pH值對淡水藻類生長和種類變化的影響[J]. 農業環境科學學報, 2005,24(2):294-298. Liu C G, Jin X C, Sun L, et al. Effects of pH on growth and species changes of algae in freshwater [J]. Journal of Agro-Environment Science, 2005,24(2):294-298.
[32] 廖 敏,黃昌勇,謝正苗.pH值對鎘在土水系統中的遷移和形態的影響[J]. 環境科學學報, 1999,19(1):83-88. Liao M, Huang C Y, Xie Z M. Effect of pH on transport and transformation of cadmium in soil-water system [J]. Acta Scientiae Circumstantiae, 1999,19(1):83-88.
[33] 王 冉,劉鐵錚,王 恬.抗生素在環境中的轉歸及其生態毒性[J]. 生態學報, 2006,26(1):265-270. Wang Y, Liu T Z, Wang T.The fate of antibiotics in environment and its ecotoxicology: A review [J]. Acta Ecologica Sinica, 2006,26(1): 265-270.
[34] 張珈瑜,彭星星,賈曉珊.磺胺二甲基嘧啶(SM2)高效降解菌J2的分離篩選及降解特性研究[J].環境科學學報, 2019,39(9):2919-2927. Zhang J Y, Peng X X, Jia X S. Isolation and characterization of high efficiency sulfamethazine-degrading bacterium strain J2 [J]. Acta Scientiae Circumstantiae, 2019,39(9):2919-2927.
[35] Gao J, Pedersen J A. Adsorption of sulfonamide antimicrobial agents to clay minerals [J]. Environmental Science and Technology, 2005, 39(24):9509-9516.
[36] Pan L J, Tang X D, Li C X, et al. Biodegradation of sulfamethazine by an isolated thermophile-sp. S-07 [J]. World Journal of Microbiology & Biotechnology, 2017,33(5):85.
Biodegradation of Sulfamethazine in Sulfamethazine/Copper combined pollution by.
ZENG Jie-yi1, ZENG Su-hang1, JI Meng-tian1, TAN Xiao2, HAN Wei-jiang1,2, CHEN Shuo-na1*
(1.College of Natural Resources and Environment, South China Agricultural University, Guangzhou 510642, China;2.South China Institute of Environmental Science, Ministry of Ecology and Environment, Guangzhou 510655, China)., 2019,39(12):5293~5300
To understand the characteristics of sulfamethazine (SMZ) biodegradation in the polluted environment where SMZ and Cu2+co-existed, this study focused on the bio-treatment of SMZ-Cu2+in different conditions by(named A5), a strain resistant to sulfamethazine, which was screened and isolated from the soil of a livestock and poultry farm (Guangzhou, China). The results showed that, with the presence of single SMZ or SMZ-Cu2+combined pollution in the culture medium, strain A5 still maintained a good growth trend.was an effective strain to remove SMZ from pollution system. The presence of Cu2+was beneficial for A5 to decompose SMZ. The degradation rates of SMZ reached 37.3% in 3d. Under the condition of 1g/L of inoculum, 1mg/L initial concentration of SMZ, and neutral pH, the removal effect of strain A5 on SMZ was the best. The transmission electron microscope (TEM) analysis showed that the cells of strain A5 were severely damaged when SMZ and Cu2+co-existed in solution, leading to the outflow of cytoplasm.
sulfamethazine;copper ions;combined pollution;;biodegradation
X172
A
1000-6923(2019)12-5293-08
曾潔儀(1997-),女,廣東茂名人,華南農業大學本科生,主要從事環境污染微生物修復研究.發表論文2篇.
2019-05-10
廣東省自然科學基金項目(2017A030313062,2018A030310203);廣州市科學計劃項目(201804010208)
* 責任作者, 講師,chenshuona@scau.edu.cn

